文档内容
氮及其化合物(2)
重难点 题型 分值
1. 氨的物理性质、化学性质
+
重点 2. 铵盐及NH4的检验
3. 硝酸的性质
4. 氮的化合物之间的转化
选 择 和
6-8分
填空
1. 氨气的化学性质和实验室制法
+
难点
2. NH4的检验
3. 硝酸的强氧化性
核心知识点一:
一、氨
1. 氨的物理性质
颜色 状态 气味 密度 溶解性 熔沸点
无色 气体 刺激性气味 比空气小 极 易 溶 于 水 ( 体 积 比 较高,易液
1∶700) 化
【注意】由于氨气易液化,所以常用作制冷剂。
2. 喷泉实验
(1)喷泉实验的原理
第1页使烧瓶内外在短时间内产生较大的压强差,利用大气压将烧瓶下面烧杯中的液体压入
烧瓶内,在尖嘴导管口形成喷泉。
(2)形成喷泉的类型
①极易溶于水的气体(如NH 、HCl等)与水可形成喷泉。
3
②能与NaOH溶液反应的气体能形成喷泉。
③常见的能形成喷泉的气体和液体组合。
CO、Cl、 NO、O、 NO 、O
气体 HCl NH 2 2 NO 2 2 2
3 SO 、HS 2 (4∶3) (4∶1)
2 2
水、
NaOH
吸收剂 NaOH 水 水 水 水
溶液
溶液
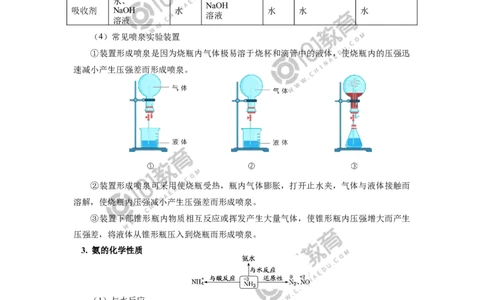
(4)常见喷泉实验装置
①装置形成喷泉是因为烧瓶内气体极易溶于烧杯和滴管中的液体,使烧瓶内的压强迅
速减小产生压强差而形成喷泉。
②装置形成喷泉可采用使烧瓶受热,瓶内气体膨胀,打开止水夹,气体与液体接触而
溶解,使烧瓶内压强减小产生压强差而形成喷泉。
③装置下部锥形瓶内物质相互反应或挥发产生大量气体,使锥形瓶内压强增大而产生
压强差,将液体从锥形瓶压入到烧瓶而形成喷泉。
3. 氨的化学性质
(1)与水反应
NH +HO NH ·H O(一水合氨)
3 2 3 2
+
①氨气溶于水得氨水,氨水中含有的粒子有:NH ·H O、HO、NH 、NH4、OH-、H
3 2 2 3
+。②NH ·H O为可溶性一元弱碱,不稳定,易分解,化学方程式为 NH ·H O NH ↑+
3 2 3 2 3
HO。
2
③氨气溶于水的溶液能使酚酞溶液变红,使石蕊溶液变蓝。氨水呈弱碱性,原因是:
+
NH ·H O NH4+OH-
3 2
【注意】①NH 是中学化学中唯一的碱性气体,能使湿润的红色石蕊试纸变蓝,可在
3
第2页推断题中作为解题突破口。
②氨水呈碱性,NH ·H O属于一元弱碱,计算氨水的浓度时,溶质按NH 进行计算。
3 2 3
(2)氨气的还原性
性质 方程式
催化氧化
4NH +5O 4NO+6HO
3 2 2
被CuO氧化 2NH +3CuO 3Cu+N+3HO
3 2 2
2NH +3Cl===N +6HCl
3 2 2
被氯气氧化
或8NH +3Cl===N +6NH Cl
3 2 2 4
被氮氧化物 6NO+4NH ===5N +6HO
3 2 2
氧化 6NO +8NH ===7N +12HO
2 3 2 2
(3)与酸的反应
蘸有浓盐酸(或浓硝酸)的玻璃棒与蘸有浓氨水的玻璃棒靠近,其现象为有白烟生成。
化学方程式分别为HCl+NH ===NHCl、HNO+NH ===NHNO 。
3 4 3 3 4 3
注意:浓硝酸、浓盐酸等挥发性酸遇氨会产生白烟,利用这点可以检验浓氨水或氨的
存在。硫酸、磷酸等难挥发性酸虽然能与氨反应生成铵盐,但不会产生白烟。
二、铵盐
1. 物理性质
铵盐都是白色固体,均易溶于水。
2. 化学性质
(1)①受热分解. 固态铵盐受热都易分解。根据组成铵盐的酸根阴离子对应的酸的性
质的不同,铵盐分解时有以下三种情况:
a. 组成铵盐的酸根阴离子对应的酸是非氧化性的挥发性酸时,则加热时酸与氨气同时
挥发,冷却时又重新化合生成铵盐。
例如: ; (试管上端又有白色固体附
着 ) ; 又 如 : ;
。
b. 组成铵盐的酸根阴离子对应的酸是难挥发性酸,加热时则只有氨气逸出,酸或酸式
盐仍残留在容器中。
第3页如: ;
c. 组成铵盐的酸根阴离子对应的酸是氧化性酸,加热时则发生氧化还原反应,无氨气
逸出。
例如:
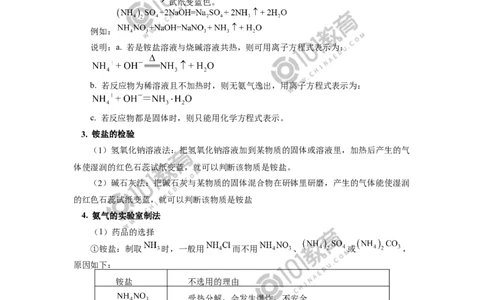
②跟碱反应——铵盐的通性。
、 有 刺 激 性 气 味 的 气 体
湿润的红色石蕊试纸
试纸变蓝色。
例如:
说明:a. 若是铵盐溶液与烧碱溶液共热,则可用离子方程式表示为:
b. 若反应物为稀溶液且不加热时,则无氨气逸出,用离子方程式表示为:
c. 若反应物都是固体时,则只能用化学方程式表示。
3. 铵盐的检验
(1)氢氧化钠溶液法:把氢氧化钠溶液加到某物质的固体或溶液里,加热后产生的气
体使湿润的红色石蕊试纸变蓝,就可以判断该物质是铵盐。
(2)碱石灰法:把碱石灰与某物质的固体混合物在研钵里研磨,产生的气体能使湿润
的红色石蕊试纸变蓝,就可以判断该物质是铵盐
4. 氨气的实验室制法
(1)药品的选择
①铵盐:制取 时,一般用 而不用 、 或 ,
原因如下:
铵盐 不选用的理由
受热分解,会发生爆炸,不安全
与 反应时生成 ,反应物呈块状,不
利于NH 逸出,且反应后试管难清洗
3
受热分解会产生 ,使收集到的 不纯
②碱:一般用熟石灰,不用 ,因为 易吸水结块,而且对玻
璃腐蚀性较强。
(2)反应装置
固+固 气
第4页与实验室用 制取 的装置相同。
(3)操作时的注意事项
①收集装置和反应装置的试管和导管必须是干燥的;
②发生装置的试管口略向下倾斜;
③由于氨气的密度比空气小,因此收集氨气时,导管应插入试管的底部。
④加热温度不宜过高,并用酒精灯外焰由前向后逐渐加热。
(4)氨气的干燥
通常使用碱石灰,不能使用 或浓 ,也不能用无水 。
(5)验满
①用湿润的红色石蕊试纸放置在试管口附近,若变蓝,说明已经收集满。
②用蘸取浓盐酸的玻璃棒靠近试管口,若有白烟生成,说明已经收集满。
(6)尾气处理
多余的氨要吸收掉(可在导管口放一团用水或稀硫酸浸湿的棉花球)以避免污染空气。
但多余气体在尾气吸收时要防止倒吸,常采用的装置有:
(7)氨气的其他制法
方法 化学方程式(或原理) 气体发生装置
加热浓氨水 注:① 不稳定,受热
易分解;②加热温度不宜过高
浓氨水+固 溶于水放热,促使一水合氨分解,且 浓度的增
体
大有利于 放出
, 的作用:①
浓氨水+固
体
吸水;②吸水后放热促进NH
3
放出;③增大溶液中的
浓度,减少 的溶解
第5页核心知识点二:
三、硝酸
1. 工业制硝酸
①NH 在催化剂作用下与O 反应生成NO:
3 2
4NH +5O 4NO+6HO。
3 2 2
②NO进一步氧化生成NO :2NO+O===2NO。
2 2 2
③用水吸收NO 生成HNO:
2 3
3NO +HO===2HNO +NO。
2 2 3
2. 物理性质
硝酸是无色易挥发的液体,有刺激性气味。
王水是浓硝酸和浓盐酸按1:3的体积比配制成的混合溶液
3. 化学性质
(1)不稳定性
反应的化学方程式:4HNO 2HO+4NO ↑+O↑。
3 2 2 2
【注意】硝酸的保存
①保存硝酸:棕色瓶(避光)、玻璃塞(橡胶塞易被氧化)、阴凉处(防热)。
②存放的浓硝酸中,因分解产生的NO 溶于HNO 而使其呈黄色。与工业盐酸中因含
2 3
Fe3+而呈黄色易混。
(2)强氧化性
浓、稀硝酸均具有强氧化性,浓度越大,氧化性越强,其还原产物的价态越高。还原
产物一般为HNO(浓)―→NO ,HNO(稀)―→NO。
3 2 3
稀硝酸与铜反应的化学方程式:
与金属反应 3Cu+8HNO(稀)===3Cu(NO )+2NO↑+4HO
3 3 2 2
浓硝酸与铜反应的化学方程式:
第6页Cu+4HNO(浓)===Cu(NO )+2NO ↑+2HO
3 3 2 2 2
浓硝酸与C反应的化学方程式:
与非金属反应
C+4HNO(浓) CO↑+4NO ↑+2HO
3 2 2 2
硝酸可氧化Fe2+、HS、SO 、NaSO 、HI等还原性物质。
2 2 2 3
与还原性化合物反应 如稀硝酸与FeSO 溶液反应的离子方程式: 3Fe2++4H++NO
4
−
3 ===3Fe3++NO↑+2HO
2
【注意】①硝酸浓度越大,其还原产物的价态越高。还原产物一般为 HNO (浓)
3
→NO ,HNO(稀)→NO。
2 3
②浓硝酸能使紫色石蕊溶液先变红,后褪色,该反应过程中浓硝酸表现出强酸性和强
氧化性。
③常温下,铁、铝遇浓硝酸能发生“钝化”,并非不反应,故浓硝酸可以用铁桶盛放。
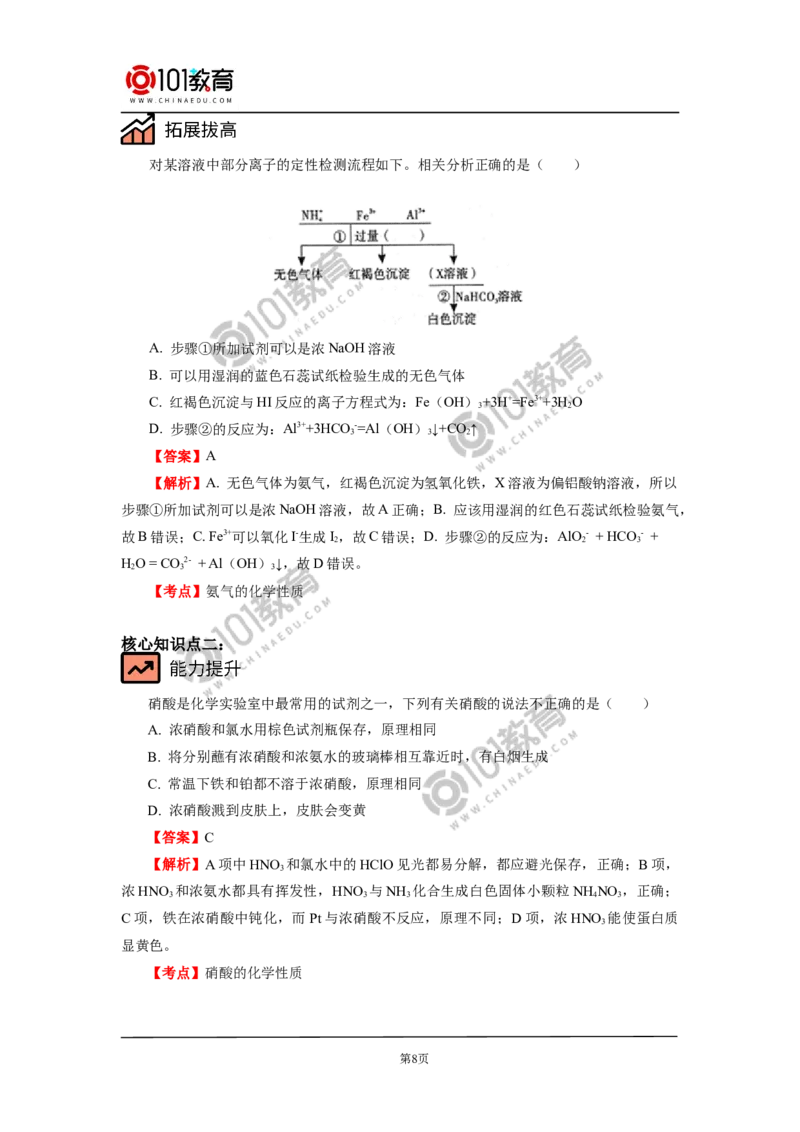
④浓硝酸和稀硝酸的性质比较
核心知识点一:
有关氨气的实验较多,下面对这些实验的实验原理的分析正确的是( )
A. 氨气极易溶于水的性质可以解释氨气的喷泉实验
B. 氨气的还原性可以解释氨气与氯化氢的反应实验
C. 铵盐的水溶性大是实验室中用NH Cl和Ca(OH) 固体混合物制取氨气的原因
4 2
D. NH·H O的热不稳定性可以解释液氨用作制冷剂
3 2
【答案】A
【解析】B项氨气与氯化氢的反应不是氧化还原反应;C项铵盐的水溶性与制氨气无
关;D项液氨用作制冷剂是利用氨的易液化的性质,故B、C、D选项均错误,A项正确。
【考点】氨气的化学性质
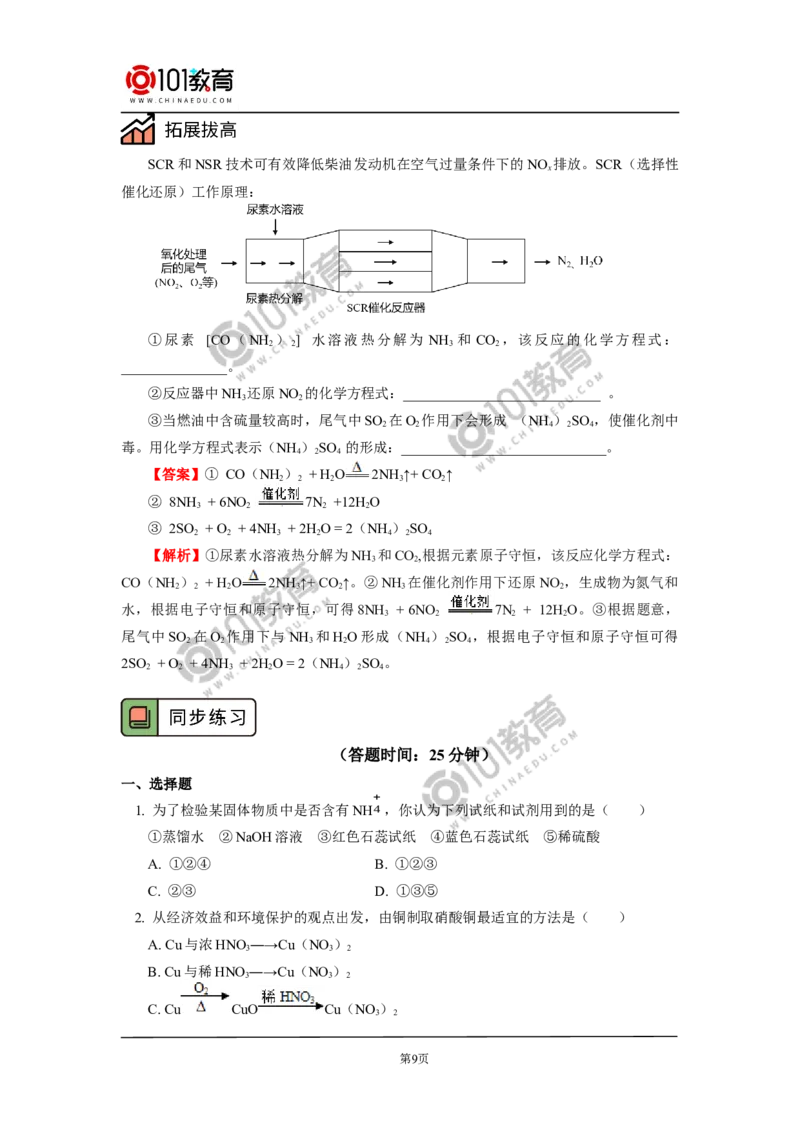
第7页对某溶液中部分离子的定性检测流程如下。相关分析正确的是( )
A. 步骤①所加试剂可以是浓NaOH溶液
B. 可以用湿润的蓝色石蕊试纸检验生成的无色气体
C. 红褐色沉淀与HI反应的离子方程式为:Fe(OH)+3H+=Fe3++3H O
3 2
D. 步骤②的反应为:Al3++3HCO-=Al(OH)↓+CO ↑
3 3 2
【答案】A
【解析】A. 无色气体为氨气,红褐色沉淀为氢氧化铁,X溶液为偏铝酸钠溶液,所以
步骤①所加试剂可以是浓NaOH溶液,故A正确;B. 应该用湿润的红色石蕊试纸检验氨气,
故B错误;C. Fe3+可以氧化I-生成I,故C错误;D. 步骤②的反应为:AlO- + HCO - +
2 2 3
HO = CO 2- + Al(OH)↓,故D错误。
2 3 3
【考点】氨气的化学性质
核心知识点二:
硝酸是化学实验室中最常用的试剂之一,下列有关硝酸的说法不正确的是( )
A. 浓硝酸和氯水用棕色试剂瓶保存,原理相同
B. 将分别蘸有浓硝酸和浓氨水的玻璃棒相互靠近时,有白烟生成
C. 常温下铁和铂都不溶于浓硝酸,原理相同
D. 浓硝酸溅到皮肤上,皮肤会变黄
【答案】C
【解析】A项中HNO 和氯水中的HClO见光都易分解,都应避光保存,正确;B项,
3
浓HNO 和浓氨水都具有挥发性,HNO 与NH 化合生成白色固体小颗粒NH NO ,正确;
3 3 3 4 3
C项,铁在浓硝酸中钝化,而Pt与浓硝酸不反应,原理不同;D项,浓HNO 能使蛋白质
3
显黄色。
【考点】硝酸的化学性质
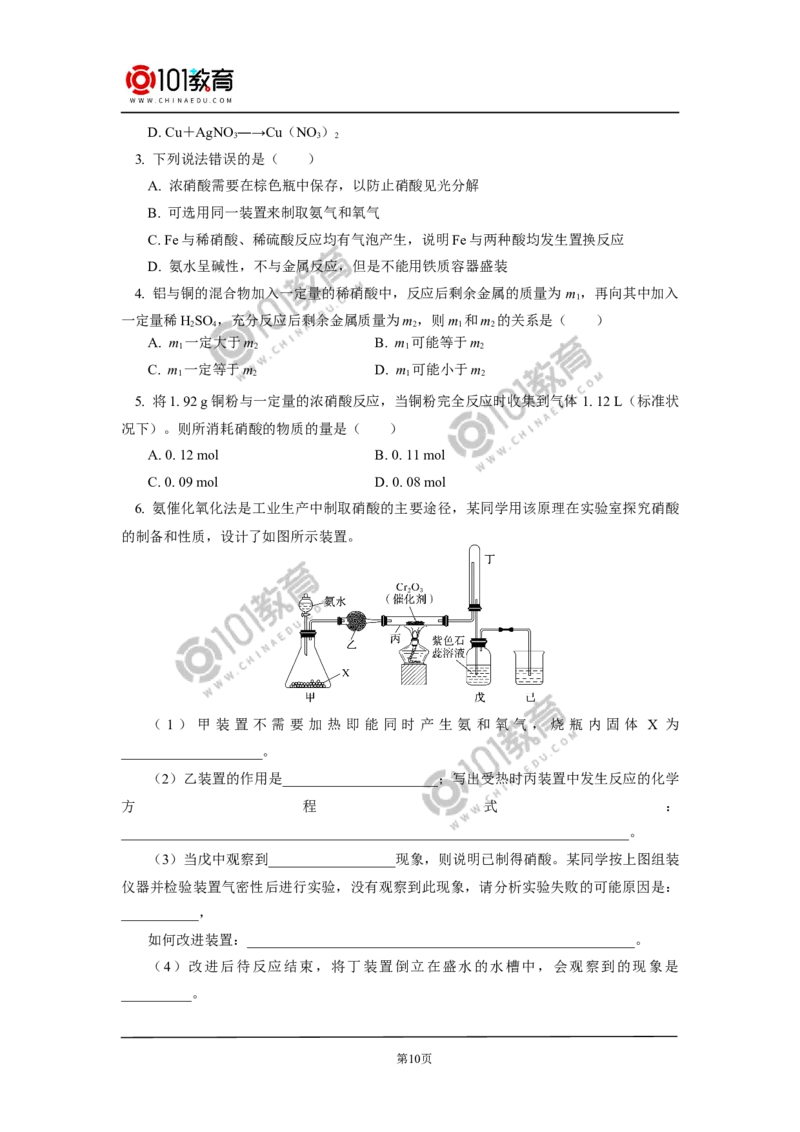
第8页SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NO 排放。SCR(选择性
x
催化还原)工作原理:
①尿素 [CO(NH ) ] 水溶液热分解为 NH 和 CO ,该反应的化学方程式:
2 2 3 2
_______________。
②反应器中NH 还原NO 的化学方程式:____________________________ 。
3 2
③当燃油中含硫量较高时,尾气中SO 在O 作用下会形成 (NH ) SO ,使催化剂中
2 2 4 2 4
毒。用化学方程式表示(NH )SO 的形成:_____________________________。
4 2 4
【答案】① CO(NH ) + H O 2NH ↑+ CO↑
2 2 2 3 2
② 8NH + 6NO 7N +12H O
3 2 2 2
③ 2SO + O + 4NH + 2H O = 2(NH )SO
2 2 3 2 4 2 4
【解析】①尿素水溶液热分解为NH 和CO,根据元素原子守恒,该反应化学方程式:
3 2
CO(NH ) + H O 2NH ↑+ CO ↑。②NH 在催化剂作用下还原NO ,生成物为氮气和
2 2 2 3 2 3 2
水,根据电子守恒和原子守恒,可得8NH + 6NO 7N + 12HO。③根据题意,
3 2 2 2
尾气中SO 在O 作用下与NH 和HO形成(NH ) SO ,根据电子守恒和原子守恒可得
2 2 3 2 4 2 4
2SO + O + 4NH + 2H O = 2(NH )SO 。
2 2 3 2 4 2 4
(答题时间:25分钟)
一、选择题
+
1. 为了检验某固体物质中是否含有NH4,你认为下列试纸和试剂用到的是( )
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸
A. ①②④ B. ①②③
C. ②③ D. ①③⑤
2. 从经济效益和环境保护的观点出发,由铜制取硝酸铜最适宜的方法是( )
A. Cu与浓HNO―→Cu(NO )
3 3 2
B. Cu与稀HNO―→Cu(NO )
3 3 2
C. Cu CuO Cu(NO )
3 2
第9页D. Cu+AgNO―→Cu(NO )
3 3 2
3. 下列说法错误的是( )
A. 浓硝酸需要在棕色瓶中保存,以防止硝酸见光分解
B. 可选用同一装置来制取氨气和氧气
C. Fe与稀硝酸、稀硫酸反应均有气泡产生,说明Fe与两种酸均发生置换反应
D. 氨水呈碱性,不与金属反应,但是不能用铁质容器盛装
4. 铝与铜的混合物加入一定量的稀硝酸中,反应后剩余金属的质量为 m,再向其中加入
1
一定量稀HSO ,充分反应后剩余金属质量为m,则m 和m 的关系是( )
2 4 2 1 2
A. m 一定大于m B. m 可能等于m
1 2 1 2
C. m 一定等于m D. m 可能小于m
1 2 1 2
5. 将1. 92 g铜粉与一定量的浓硝酸反应,当铜粉完全反应时收集到气体 1. 12 L(标准状
况下)。则所消耗硝酸的物质的量是( )
A. 0. 12 mol B. 0. 11 mol
C. 0. 09 mol D. 0. 08 mol
6. 氨催化氧化法是工业生产中制取硝酸的主要途径,某同学用该原理在实验室探究硝酸
的制备和性质,设计了如图所示装置。
( 1 ) 甲 装 置 不 需 要 加 热 即 能 同 时 产 生 氨 和 氧 气 , 烧 瓶 内 固 体 X 为
____________________。
(2)乙装置的作用是______________________;写出受热时丙装置中发生反应的化学
方 程 式 :
________________________________________________________________________。
(3)当戊中观察到__________________现象,则说明已制得硝酸。某同学按上图组装
仪器并检验装置气密性后进行实验,没有观察到此现象,请分析实验失败的可能原因是:
___________,
如何改进装置:_______________________________________________________。
(4)改进后待反应结束,将丁装置倒立在盛水的水槽中,会观察到的现象是
__________。
第10页第11页1.【答案】B
+ +
【解析】固体溶于NaOH溶液后,加热,若含有NH4,则发生NH4+OH- NH ↑
3
+HO,NH 能使湿润(用到蒸馏水)的红色石蕊试纸变蓝。
2 3
2.【答案】C
【解析】A项,生成的NO 会造成大气污染,不正确;B项,生成的NO也会造成大
2
气污染,不正确;C项,生成等量的硝酸铜所用的原料少比较经济,又不会对环境造成污
染,正确;D项,硝酸银成本较高,同时硝酸银会对环境造成一定的污染,主要是重金属
污染,不正确。
3.【答案】C
【解析】受热或见光易分解的试剂均需要保存在棕色试剂瓶中,A项正确;加热氯化
铵和碱石灰的混合物制取氨气与加热氯酸钾和二氧化锰的混合物制取氧气的装置一样,B
项正确;Fe与稀硝酸的反应不属于置换反应,C项错误。
4.【答案】A
− −
【解析】原溶液中存在NO3 ,再加入一定量的稀硫酸时,NO3 在酸性条件下能够继
续和金属反应,故质量为m 的固体无论是Al与Cu的混合物还是Cu,质量都会减少,故
1
m 一定大于m。故正确答案为A。
1 2
5.【答案】B
【解析】铜与HNO 反应时,消耗的HNO 转变为Cu(NO ) 和氮的氧化物(NO 或
3 3 3 2 2
1.92g 1.12L
NO)。n(Cu)=
64g⋅mol−1
=0. 03 mol;n(气体)=
22.4L⋅mol−1
=0. 05 mol;所以
共耗HNO 的物质的量n(HNO)=0. 03 mol×2+0. 05 mol=0. 11 mol。
3 3
6.【答案】(1)过氧化钠
(2)干燥氧气和氨的混合气体 4NH +5O 4NO+6HO
3 2 2
(3)紫色石蕊溶液变红 过量的氨致使戊中溶液不一定呈酸性 在丙和丁之间连接盛
有无水氯化钙的干燥管或盛有浓硫酸的洗气瓶
(4)试管丁内水面慢慢上升,上升到一定高度不再变化,试管内气体颜色由红棕色逐
渐变淡至无色
【解析】(1)甲中不需要加热即能同时产生NH 和O ,说明固体X溶于氨水既产生
3 2
O 又放出大量热,则该固体为NaO 。(2)乙装置可干燥NH 和O ;NH 和O 在加热和
2 2 2 3 2 3 2
Cr O 的催化作用下,发生催化氧化反应。(3)HNO 能使石蕊溶液变红;由于NH 过量,
2 3 3 3
可能会与HNO 反应,致使观察不到溶液变红的现象;可在丙和丁之间连接一个能除去
3
NH 的装置。(4)丁装置中为NO ,NO 会与HO反应生成无色的NO。
3 2 2 2
第12页