文档内容
第二章 化学反应速率与化学平衡
课
第二节 化学平衡
题
课时2
知识与技能 理解化学平衡的概念,使学生理解浓度、压强对化学平衡的影响
教 1、通过浓度实验,逐步探究平衡移动的原理及其探究的方法,引起
学 学生在学习过程中主动探索化学实验方法,
过程与方法
目 2、通过讨论、分析、对比的方法,培养学生的观察能力和实验探究
能力
标
情感态度 激发学生的学习兴趣,培养学生尊重科学、严谨求学、勤于思考的态
与价值观 度,树立透过现象看本质的唯物主义观点
教学
浓度、压强、温度、催化剂对化学平衡的影响
重点
教学
平衡移动的原理分析及应用
难点
教
学
设
教
化学平衡是中学化学的重要理论之一,也是每年高考的热点内容之一。
材
本节是在前两节关于反应速率的基础进行的教学。学习化学平衡,不仅能加深
分
析 对化学反应速率的理解,还能为今后学习电离、水解等离子平衡的知识奠定理
论基础。
所以本节内容作为高考热点,同时在本章教材体系中起着承上启下的作用,是
本章教学、乃至高中化学教学的重点。
学 我们的学生基础较差,特别是对实验现象的概括叙述不规范,需要老师规范
情
学生的用语,本节学生掌握化学反应速率的概念以及计算应该没问题,让学生自
分
析 己总结影响化学反应速率的因素会有一些困难。
想
以培养学生自主获取新知识的能力为目的来设计教学,采用发现,探究的教学
教
法 模式,其设计的教学指导思想,是由浅入深,从学生日常生活中的化学现象和实
设 验中抽象出有关的概念和原理。形成一个由宏观到微观、由感性到理性、由简单
计
到复杂的科学探究过程。
教学 教 学 内 容 设计
环节 意图
教师活动 学生活动[问]1、平衡状态的特征及实质?2、影响速率的外界因素有哪
些? 引入新课
[投影] 逆:可逆反应(或可逆过程) 学生讨论 明确要学
等:V =V (不同的平衡对应不同的速率) 思 考 问 习的内容
正 逆
动:动态平衡。达平衡后,正逆反应仍在进行(V =V ≠0) 题。
正 逆
定:平衡时,各组分浓度、含量保持不变(恒定)
变:条件改变,平衡发生改变平衡状态各成分含量保持不变,
正逆反应速率相等
浓度、温度、压强、催化剂等
改变影响速率的条件,来打破原有平衡,建立新平衡
[板书]第三节 化学平衡(二)
一、浓度对化学平衡的影响
[科学探究]实验 2-5 已知 K Cr O 的溶液中存在着如下平
2 2 7
衡:Cr O 2- +H O 2CrO 2-+2H+ 。K Cr O 为橙色,K CrO
2 7 2 4 2 2 7 2 4
为黄色。 学生讨论 引导发现
取两支试管各加入5 mL 0.1 mol/L K Cr O 溶液,然后按下表步 后回答:
2 2 7
骤操作,观察并记录溶液颜色的变化。
滴加 3~ 滴加10~20滴
10 滴 浓 6 mol/LNaOH
硫酸
引
K Cr O 橙色 黄色
入 2 2 7
新 溶液 学生掌握
课
[投影]
[科学探究]实验2-6 向盛有5 mL 0.005 mol/L FeCl 溶液的试
3
管中加入5 mL 0.01 mol/L KSCN溶液,溶液呈红色。在这个反
应体系中存在下述平衡:Fe3++3SCN- Fe(SCN)
3
(1) 将上述溶液均分置两支试管中,向其中一支试管中加入饱
和FeCl 溶液4滴,充分振荡,观察溶液颜色变化,向另一支
3
试管中滴加4滴1 mol/L KSCN溶液,观察溶液颜色变化
运用迁移
(2) 向上述两支试管中各滴加0.01 mol/L NaOH溶液 3-5滴,观察现象,
方法
填写下表。
编号 1 2 学生思考
步 骤 滴加饱和 FeCl 滴加浓的KSCN溶液
3
(1) 溶液
现象 颜色加深 颜色加深
C 增大 增大
生
步 骤 滴加NaOH溶液 滴加NaOH溶液
(2)
现象 试管都有红褐色沉淀,且溶液颜色变浅
C 都减小
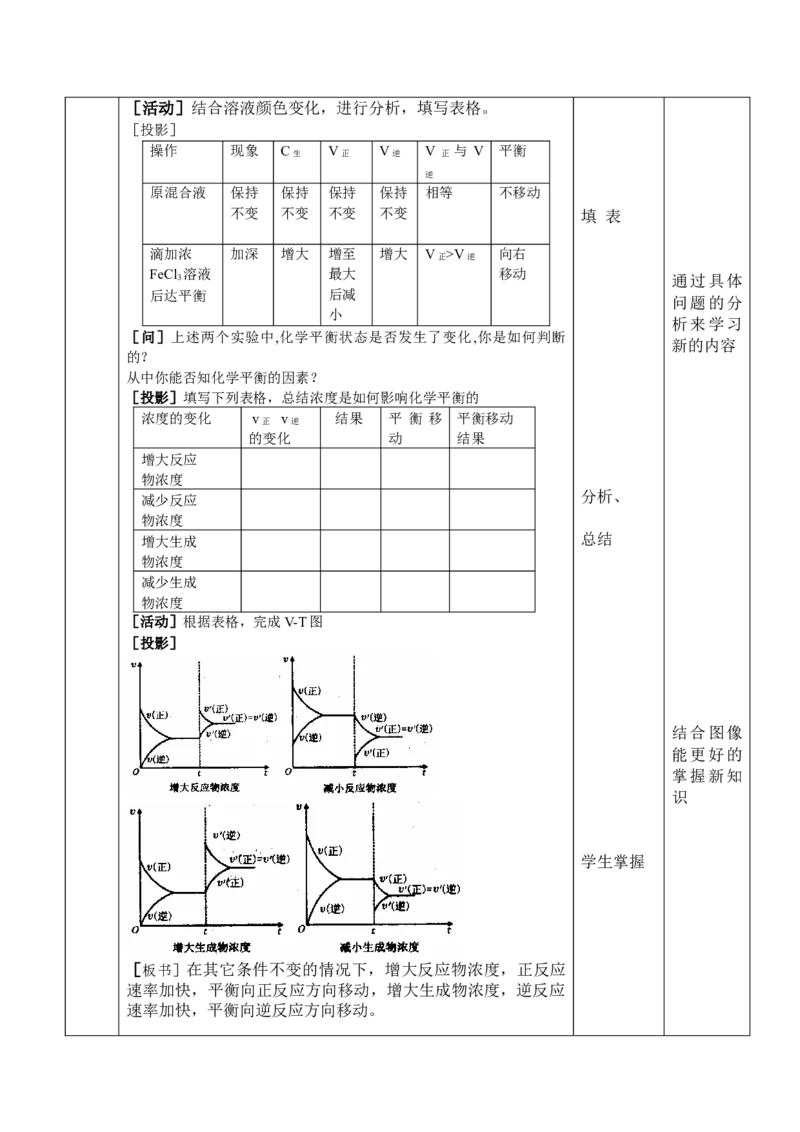
生[活动]结合溶液颜色变化,进行分析,填写表格。
[投影]
操作 现象 C V V V 与 V 平衡
生 正 逆 正
逆
原混合液 保持 保持 保持 保持 相等 不移动
不变 不变 不变 不变 填 表
滴加浓 加深 增大 增至 增大 V >V 向右
正 逆
FeCl 溶液 最大 移动
3 通过具体
后达平衡 后减
问题的分
小
析来学习
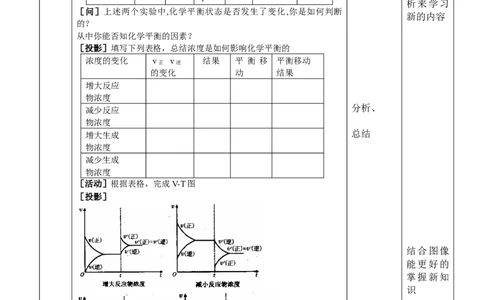
[问]上述两个实验中,化学平衡状态是否发生了变化,你是如何判断
新的内容
的?
从中你能否知化学平衡的因素?
[投影]填写下列表格,总结浓度是如何影响化学平衡的
浓度的变化 v v 结果 平 衡 移 平衡移动
正 逆
的变化 动 结果
增大反应
物浓度
分析、
减少反应
物浓度
增大生成 总结
物浓度
减少生成
物浓度
[活动]根据表格,完成V-T图
[投影]
结合图像
能更好的
掌握新知
识
学生掌握
[板书]在其它条件不变的情况下,增大反应物浓度,正反应
速率加快,平衡向正反应方向移动,增大生成物浓度,逆反应
速率加快,平衡向逆反应方向移动。[过渡] 哪些状态物质受压强影响比较大?如何影响的?压强也
能够影响化学反应速率,那究竟如何改变呢?
[讲] 压强对化学平衡的影响:固态、液态物质的体积受压强影
响很小,压强不使平衡移动。反应中有气体参加:压强减小→
浓度减小→平衡向体积减小的方向移动,反之亦然。
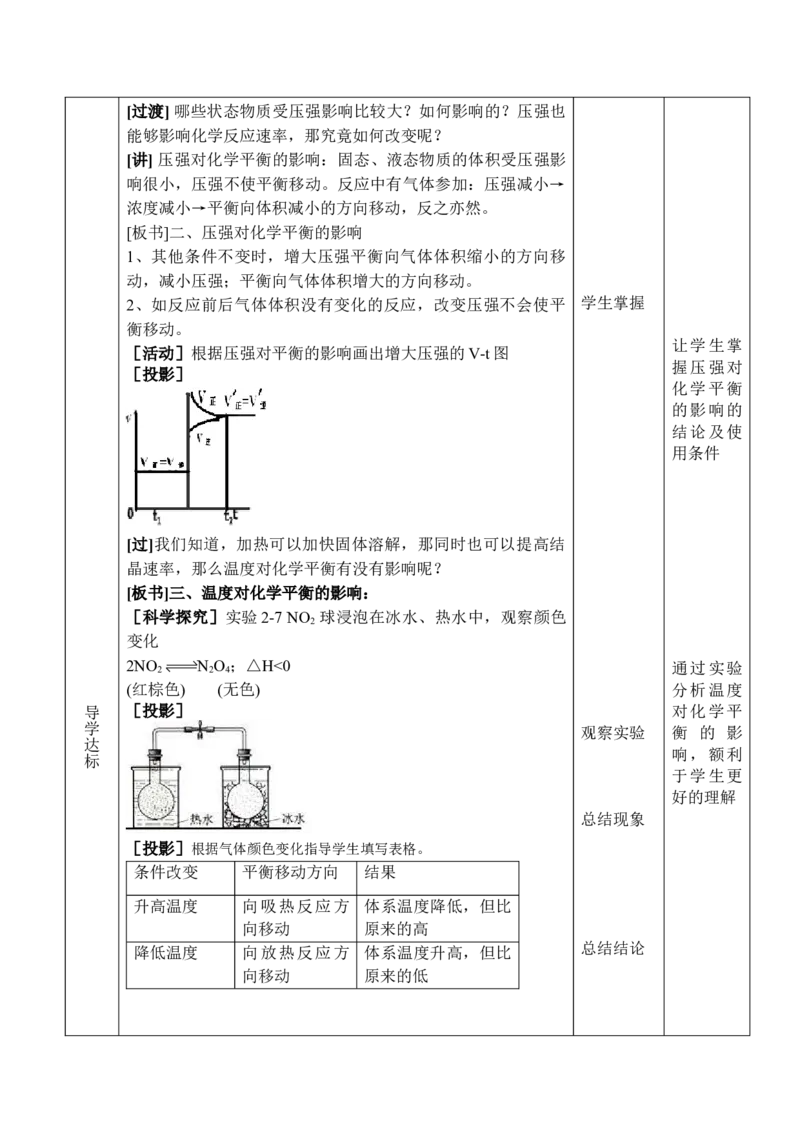
[板书]二、压强对化学平衡的影响
1、其他条件不变时,增大压强平衡向气体体积缩小的方向移
动,减小压强;平衡向气体体积增大的方向移动。
2、如反应前后气体体积没有变化的反应,改变压强不会使平 学生掌握
衡移动。
让学生掌
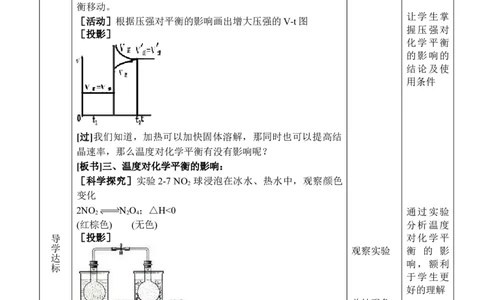
[活动]根据压强对平衡的影响画出增大压强的V-t图
握压强对
[投影]
化学平衡
的影响的
结论及使
用条件
[过]我们知道,加热可以加快固体溶解,那同时也可以提高结
晶速率,那么温度对化学平衡有没有影响呢?
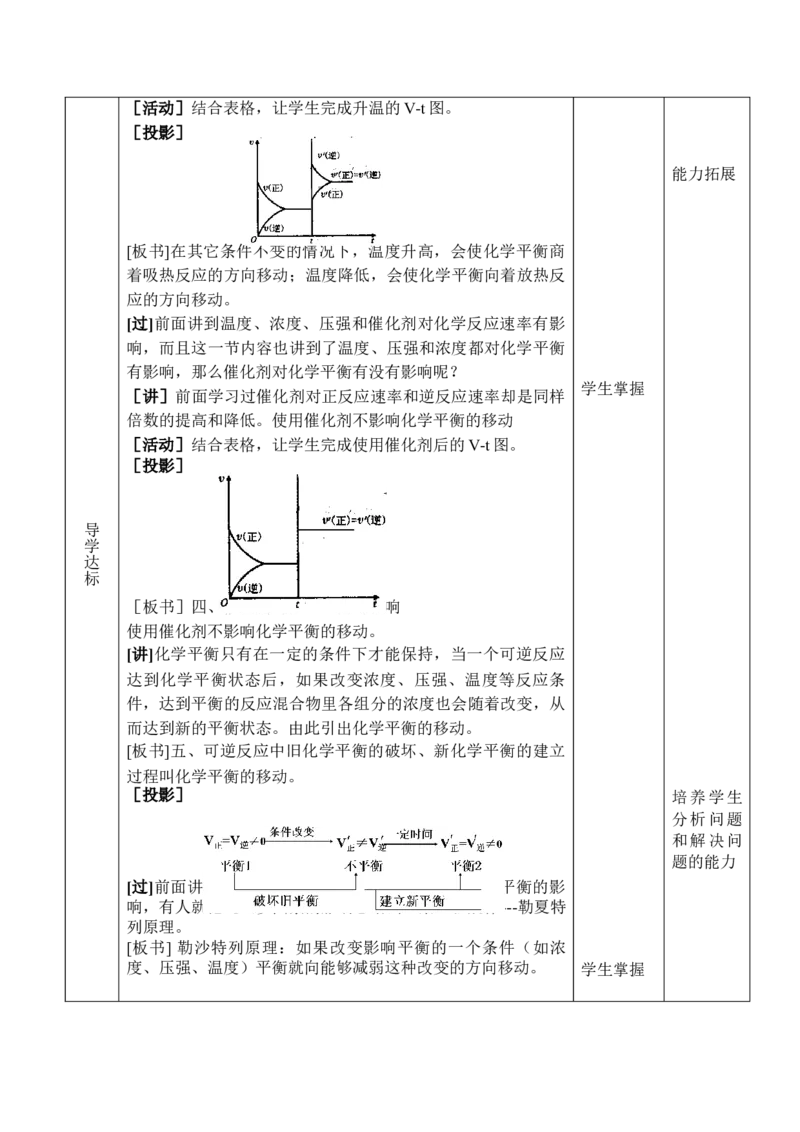
[板书]三、温度对化学平衡的影响:
[科学探究]实验2-7 NO 球浸泡在冰水、热水中,观察颜色
2
变化
2NO N O ;△H<0 通过实验
2 2 4
(红棕色) (无色) 分析温度
导 [投影] 对化学平
学
观察实验 衡 的 影
达
响,额利
标
于学生更
好的理解
总结现象
[投影]根据气体颜色变化指导学生填写表格。
条件改变 平衡移动方向 结果
升高温度 向吸热反应方 体系温度降低,但比
向移动 原来的高
总结结论
降低温度 向放热反应方 体系温度升高,但比
向移动 原来的低[活动]结合表格,让学生完成升温的V-t图。
[投影]
能力拓展
[板书]在其它条件不变的情况下,温度升高,会使化学平衡商
着吸热反应的方向移动;温度降低,会使化学平衡向着放热反
应的方向移动。
[过]前面讲到温度、浓度、压强和催化剂对化学反应速率有影
响,而且这一节内容也讲到了温度、压强和浓度都对化学平衡
有影响,那么催化剂对化学平衡有没有影响呢?
学生掌握
[讲]前面学习过催化剂对正反应速率和逆反应速率却是同样
倍数的提高和降低。使用催化剂不影响化学平衡的移动
[活动]结合表格,让学生完成使用催化剂后的V-t图。
[投影]
导
学
达
标
[板书]四、催化剂对化学平衡的影响
使用催化剂不影响化学平衡的移动。
[讲]化学平衡只有在一定的条件下才能保持,当一个可逆反应
达到化学平衡状态后,如果改变浓度、压强、温度等反应条
件,达到平衡的反应混合物里各组分的浓度也会随着改变,从
而达到新的平衡状态。由此引出化学平衡的移动。
[板书]五、可逆反应中旧化学平衡的破坏、新化学平衡的建立
过程叫化学平衡的移动。
[投影] 培养学生
分析问题
和解决问
题的能力
[过]前面讲述了浓度、压强和温度等多种因素对化学平衡的影
响,有人就把这么多因素的影响总结出一条经验规律---勒夏特
列原理。
[板书] 勒沙特列原理:如果改变影响平衡的一个条件(如浓
度、压强、温度)平衡就向能够减弱这种改变的方向移动。 学生掌握[讲]需要我们注意的是,勒夏特列原理中的“减弱”这种改
变,不是“消除”。勒夏特列原理只考虑有单个条件改变。勒
沙特列原理适用于任何动态平衡体系
[小结]本节课以实验和讨论的方法主要学习温度和催化剂对
化学平衡的影响以及归纳了勒夏特列原理,加深了影响化学平
衡因素的理解,重点温度和催化剂对化学平衡的影响,难点是
勒夏特列原理的理解。
作
业
设
计
第三节 化学平衡
一、浓度对化学平衡的影响
在其它条件不变的情况下,增大反应物浓度,正反应速率加快,平衡向正反应方向移
动,增大生成物浓度,逆反应速率加快,平衡向逆反应方向移动。
二、压强对化学平衡的影响
1、其他条件不变时,增大压强平衡向气体体积缩小的方向移动,减小压强;平衡向气
体体积增大的方向移动。
2、如反应前后气体体积没有变化的反应,改变压强不会使平衡移动。
板 三、温度对化学平衡的影响:
书 在其它条件不变的情况下,温度升高,会使化学平衡商着吸热反应的方向移动;温度降
设
计 低,会使化学平衡向着放热反应的方向移动。
在其它条件不变的情况下,温度升高,会使化学平衡商着吸热反应的方向移动;温度降
低,会使化学平衡向着放热反应的方向移动。
四、催化剂对化学平衡的影响
使用催化剂不影响化学平衡的移动。
五、可逆反应中旧化学平衡的破坏、新化学平衡的建立过程叫化学平衡的移动
勒沙特列原理:如果改变影响平衡的一个条件(如浓度、压强、温度)平衡就向能够减
弱这种改变的方向移动