文档内容
2.2.1 氯气的性质及制取
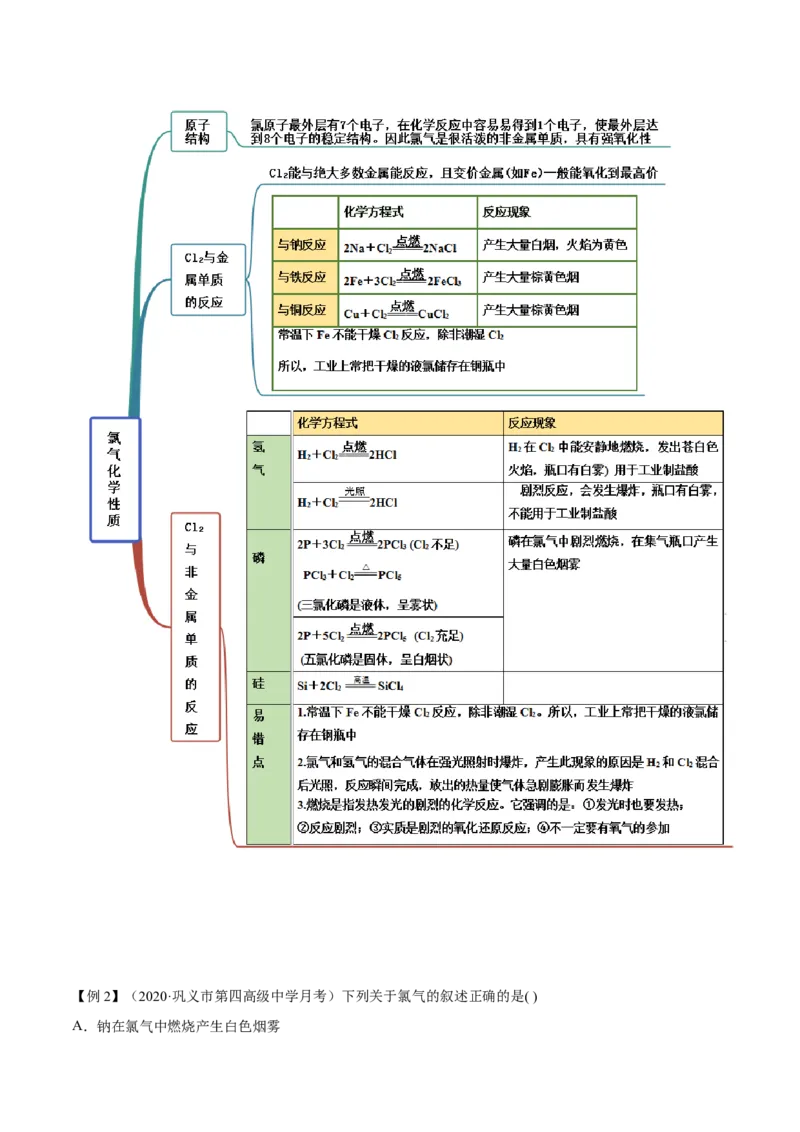
知识点一 氯气的物理性质
【例1】(2020·全国高一课时练习)下列有关氯气的叙述中,不正确的是( )
A.氯气是一种黄绿色、有刺激性气味的气体
B.氯气、液氯是同一种物质
C.氯气不能溶于水
D.氯气是一种有毒的气体
【答案】C
【解析】A.氯气是一种黄绿色、有刺激性气味的气体,故A正确;
B.氯气、液氯是不同状态的同一种物质,故B正确;
C.氯气能溶于水,常温常压下,1体积的水可溶解约2体积的Cl,故C错误;
2
D.氯气是密度大于空气的有毒的气体,故D正确。综上所述,答案为C。
【一隅三反】
1.(2020·全国课时练习)下列关于氯气的叙述正确的是( )
A.若氯气发生泄漏,应立即向下风地区转移
B.用管子把氯气通入老鼠洞中可以灭鼠
C.氯气不能溶于水,所以可用排水法收集
D. 、 均呈黄绿色且均有毒
【答案】B
【解析】A.氯气有毒且密度比空气的大,因此若氯气发生泄漏,应立即用湿毛巾捂住口鼻,并向上风地
区转移,A错误;
B.氯气有毒,可以杀灭老鼠,因此可用于灭鼠,B正确;
C.氯气可溶于水,常温下1体积水约溶解2体积的氯气,因此不能用排水法收集,可用排饱和食盐水法收集,C错误;
D.Cl-无色、无毒,D错误;
故答案为B。
2.(2019·江苏省上冈高级中学高一期中)氯气是一种有毒气体,在运输与储存过程中必须防止泄漏.一
旦储存液氯的钢瓶发生泄漏,必须立即采取措施.下列各种措施不合理的是( )
A.将人群向高处疏散
B.将人群逆风向疏散
C.用浸有烧碱溶液的毛巾捂住口鼻
D.向泄漏地点撒一些石灰
【答案】C
【解析】A.氯气的密度大于空气密度,所以氯气泄漏时,要人群向高处疏散,A正确;
B.氯气有毒,所以如果发生氯气泄漏,氯气向顺风方向扩散较快,所以应将人群逆风向疏散,B正确;
C.氯气能和碱反应生成盐,但氢氧化钠有强腐蚀性,如果用浸有烧碱溶液的毛巾捂住口鼻,虽然能减弱
氯气的毒性,但人易被氢氧化钠腐蚀,C错误;
D.石灰一般是指生石灰(CaO)或熟石灰[Ca(OH) ],生石灰与水反应后得熟石灰,氯气可以与熟石灰反
2
应生成氯化钙和次氯酸钙,故可将氯气吸收,D正确;
故选C。
3.(2020·宝山·上海交大附中高一月考)生活中难免会遇到一些突发事件,我们要善于利用学过的知识,
采取科学、有效的方法保护自己。如果发生了氯气泄漏,以下自救方法得当的是( )
A.只要在室内放一盆水
B.向地势低的地方撤离
C.观察风向,顺风撤离
D.用湿毛巾或蘸有纯碱水的毛巾捂住口鼻撤离
【答案】D
【解析】A.氯气与水反应,其速度慢且反应不充分,A错误;
B.氯气的密度大于空气,故应向地势高的地方跑,B错误;
C.逆风跑,才可以脱离氯气的笼罩,C错误;
D.因纯碱水为弱碱性,则可以吸收氯气,以减少对口鼻的刺激,D正确;故答案为:D。
知识点二 氯气与金属、非金属的反应【例2】(2020·巩义市第四高级中学月考)下列关于氯气的叙述正确的是( )
A.钠在氯气中燃烧产生白色烟雾B.红热的铜丝在氯气中燃烧生成CuCl
C.纯净的氢气可以在氯气中安静地燃烧,发出黄色火焰
D.向田鼠洞里通入氯气杀灭田鼠,利用了氯气有毒和密度较大的性质
【答案】D
【解析】A.钠在氯气中燃烧,生成NaCl固体小颗粒,形成白烟,没有雾出现(雾为小液滴),A错误;
B.红热的铜丝在氯气中燃烧生成CuCl ,B错误;
2
C.氢气在氯气中燃烧发出苍白色火焰,C错误;
D.氯气有毒,密度比空气的大,可杀灭田鼠,D正确;答案选D。
【一隅三反】
1.(2020·全国高一单元测试) 、 、 三种气体之间的转化关系如图所示。下列说法正确的是(
)
A. 为
B. 为
C. 、 、 分别为 、 、
D. 与NaOH溶液反应的化学方程式为
【答案】C
【解析】A.由分析可知,X 为O,A错误;
2 2
B.由分析可知,XY为HO,B错误;
2 2
C.由分析可知: 、 、 分别为 、 、 ,C正确;
D. 与NaOH溶液反应的化学方程式为 ,项错误;
故答案为:C。2.(2019·全国高一课时练习)下列关于氯气的叙述正确的是( )
A.钠在氯气中燃烧产生白色烟雾B.红热的铜丝在氯气中燃烧生成
C.纯净的氢气可以在氯气中安静地燃烧,发出黄色火焰D.氯气有毒且密度比空气大
【答案】D
【解析】A.钠在氯气中燃烧,生成NaCl固体小颗粒,形成白烟,没有雾出现(雾为小液滴),故A错误;
B.红热的铜丝在氯气中燃烧生成 ,故B错误;
C.氢气在氯气中燃烧发出苍白色火焰,故C错误;
D.氯气有毒且密度比空气大,故D正确。
答案选D。
3.(2019·全国高一课时练习)下列现象不属于氢气在氯气中燃烧现象的是( )
A.苍白色火焰 B.瓶口有白雾
C.集气瓶内气体颜色变浅 D.爆炸
【答案】D
【解析】A.H 在Cl 中燃烧,发出苍白色火焰,故A正确;
2 2
B.瓶口因生成的HCl吸收空气中的HO形成盐酸小液滴而出现白雾,故B正确;
2
C.瓶内气体的颜色因Cl 的消耗而变浅,故C正确;
2
D.不发生爆炸,故D错误;故答案为D。
4.(2019·全国高一课时练习)关于氯气的叙述中,下列说法正确的是
A .氯气是一种黄绿色、有毒的气体
B.氯气可以与铁反应生成FeCl
2
C.氯气不能溶于水,所以可用排水法收集氯气
D.氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物
【答案】A
【解析】A.氯气是一种黄绿色、有毒的气体,故A正确;
B.氯气的强氧化性将铁氧化为氯化铁,故B错误;
C.氯气能溶解于水,所以不能用排水法收集氯气,应用排饱和食盐水的方法收集,故C错误;
D.氯气、液氯是同一种物质,只是状态不同,都属于纯净物,氯水是氯气的水溶液属于混合物,故D错误。
故选A。
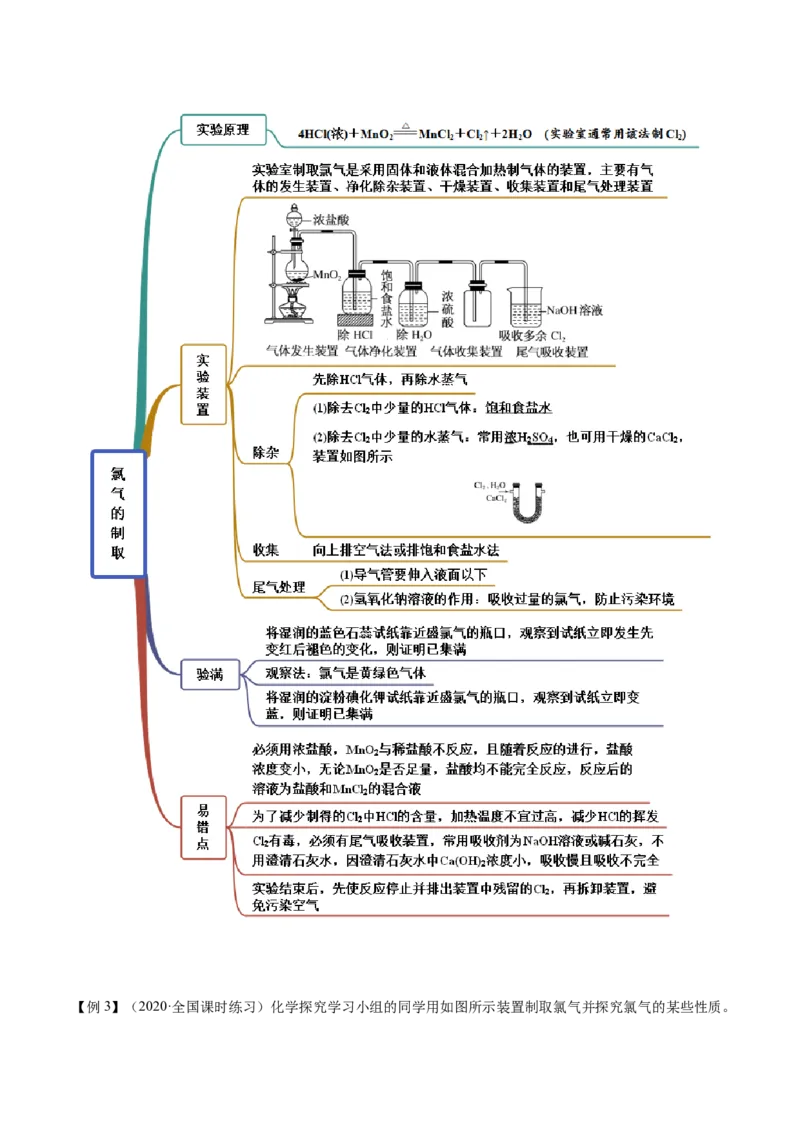
知识点三 氯气实验室制取【例3】(2020·全国课时练习)化学探究学习小组的同学用如图所示装置制取氯气并探究氯气的某些性质。回答下列问题:
(1)装置A中制取 的离子方程式为_________,该反应中体现了HCl的________性。
(2)装置C中发生反应的离子方程式为__________,反应后溶液中含有的具有氧化性的含Cl元素的粒子有
________。
(3)实验结束后,测得装置D的溶液中存在大量 ,则Cl 通过装置D时发生反应的离子方程式为
2
__________。
(4)装置F的作用是_________,该装置中发生反应的离子方程式为_________。
【答案】(1)MnO +4H++2Cl- Mn2++Cl↑+2H O 还原性和酸
2 2 2
(2)Cl+HO H++Cl-+HClO HClO、Cl、ClO-
2 2 2
(3)
(4) 吸收未反应完的Cl Cl +2OH-=Cl-+ClO-+HO
2 2 2
【解析】(1)装置A中制取Cl 的离子方程式为:MnO +4H++2Cl- Mn2++Cl↑+2H O,从离子方程式可看
2 2 2 2
出,Cl元素的化合价由-1升高到0,HCl作还原剂,表现出还原性;HCl中的部分Cl-未参与反应,其中的
全部参与反应,所以HCl同时表现出酸性;
(2)装置C中的Cl 与HO反应产生HCl、HClO,该反应是可逆反应,产生的HCl是强酸,完全电离,而
2 2
HClO是弱酸,部分电离存在电离平衡,主要以电解质分子存在,故该反应的离子方程式为Cl+HO
2 2
H++Cl-+HClO,反应后溶液中含有的具有氧化性的含Cl元素的粒子有Cl、HClO、ClO-。
2
(3)在装置D中Cl、NaSO 、HO发生氧化还原反应产生NaSO 、HCl,发生反应的离子方程式为
2 2 3 2 2 4
。(4)装置F的作用是吸收未反应完的Cl,Cl 与 NaOH反应产生NaCl、NaClO、HO,发生反应的离子方程
2 2 2
式为:Cl+2OH-=Cl-+ClO-+HO。
2 2
1.次氯酸的三大性质
①弱酸性:次氯酸是易溶于水的弱酸,比碳酸酸性弱,写离子方程式时不能拆成离子形式
如:NaClO溶液中通入少量CO,化学方程式为:NaClO+CO+HO===NaHCO+HClO
2 2 2 3
②不稳定性:2HClO=====2HCl+O↑ (氯水须现用现配,保存在棕色试剂瓶中,置于冷暗处)
2
③强氧化性:次氯酸具有强氧化性,其氧化性比Cl 强,可用于自来水的杀菌、消毒,还可以用作漂白剂
2
2.次氯酸的漂白作用
①原理:将有色物质氧化为稳定的无色物质
②特点:被HClO漂白的物质,久置后不再恢复原色
【一隅三反】
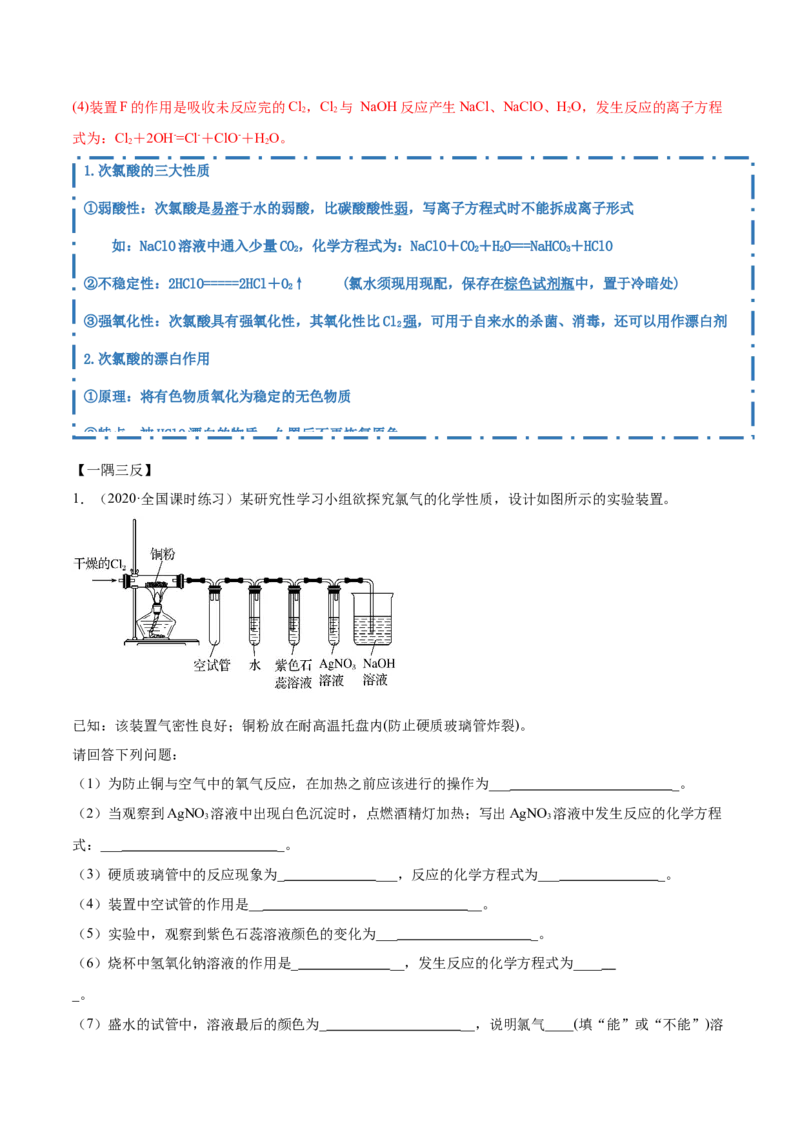
1.(2020·全国课时练习)某研究性学习小组欲探究氯气的化学性质,设计如图所示的实验装置。
已知:该装置气密性良好;铜粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为___ _。
(2)当观察到AgNO 溶液中出现白色沉淀时,点燃酒精灯加热;写出AgNO 溶液中发生反应的化学方程
3 3
式:___ _。
(3)硬质玻璃管中的反应现象为_ ___,反应的化学方程式为___ _。
(4)装置中空试管的作用是__ __。
(5)实验中,观察到紫色石蕊溶液颜色的变化为___ _。
(6)烧杯中氢氧化钠溶液的作用是_ __,发生反应的化学方程式为____
_。
(7)盛水的试管中,溶液最后的颜色为_ __,说明氯气____(填“能”或“不能”)溶于水。
【答案】(1)通入氯气排尽装置中的空气
(2)Cl+HO=HCl+HClO、HCl+AgNO=AgCl↓+HNO
2 2 3 3
(3)剧烈反应,产生棕黄色的烟 Cu+Cl CuCl
2 2
(4)防止右侧试管中的水倒吸入硬质玻璃管中,使硬质玻璃管炸裂
(5)先变红后褪色
(6) 吸收尾气中的氯气,防止污染空气 Cl+2NaOH=NaCl+NaClO+HO
2 2
(7)浅黄绿色 能
【解析】(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为通入氯气排尽装置中的空气。
(2)氯气与水反应生成盐酸和次氯酸,当观察到AgNO 溶液中出现白色沉淀时,点燃酒精灯加热;
3
AgNO 溶液中发生反应的化学方程式:Cl+HO=HCl+HClO、HCl+AgNO=AgCl↓+HNO 。
3 2 2 3 3
(3)铜和氯气加热后发生反应生成氯化铜,硬质玻璃管中的反应现象为剧烈反应,产生棕黄色的烟,反
应的化学方程式为Cu+Cl CuCl 。
2 2
(4)装置中空试管的作用是防止右侧试管中的水倒吸入硬质玻璃管中,使硬质玻璃管炸裂。
(5)氯水既有酸性又有漂白性,实验中,观察到紫色石蕊溶液颜色的变化为先变红后褪色。
(6)氯气有毒,烧杯中氢氧化钠溶液的作用是吸收尾气中的氯气,防止污染空气,发生反应的化学方程
式为Cl+2NaOH=NaCl+NaClO+HO。
2 2
(7)盛水的试管中,溶液最后的颜色为浅黄绿色,说明氯气能溶于水。
2.(2018·厦门市湖滨中学高二期中)为了探究和验证氯气的性质,某研究性学习小组以MnO 和浓盐酸
2
为主要原料,设计了如图所示装置(其中a是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行了
研究。
(资料:氯气与铁反应制取氯化铁要在无水条件下进行)
试回答下列问题:
(l)装置A中发生反应的化学方程式为_____________________(2)装置B中的试剂为_________,装置D里的药品是________
(3)装置C中发生反应的离子方程式为_____________________________
(4)反应开始后,装置E中玻璃管内的现象为_______________________________;可以检验生成物中有
Fe3+的试剂是__________.
(5)装置F中发生反应的化学方程式为________________________
(6)利用氯气可以制得漂白粉,漂白粉的有效成份是_______________(写化学式)。
【答案】(1)MnO + 4HCl (浓) CaCl + Cl ↑+ H O
2 2 2 2
(2)饱和食盐水 浓硫酸
(3)2I- + Cl == 2Cl- + I
2 2
(4)生成红棕色的烟 KSCN(硫氰化钾)
(5)2NaOH + Cl == NaCl + NaClO + 2H O
2 2
(6)Ca(ClO)
2
【解析】(1)装置A为MnO 和浓盐酸反应制备氯气的装置,其化学方程式为:MnO + 4HCl (浓) CaCl
2 2 2
+ Cl ↑+ H O;
2 2
(2)装置A中产生的氯气中混有HCl气体,需要除去,故装置B中的试剂为饱和食盐水;氯气一部分在
装置C中发生反应,验证Cl 的氧化性,因氯气与铁反应制取氯化铁要在无水条件下进行,因此氯气进入
2
装置E时必须为干燥气体,故装置D的目的是干燥氯气,故装置D中的试剂为浓硫酸;
(3)装置C中含有KI溶液,氯气通入后发生氧化还原反应,其反应的离子方程式为:2I- + Cl == 2Cl- +
2
I;
2
(4)装置E中氯气通入并加热时,发生反应2Fe+3Cl 2FeCl ,其反应现象为生成红棕色的烟;检验
2 3
Fe3+常用试剂为KSCN(硫氰化钾)溶液;
(5)氯气为有毒气体,不能直接排放于空气中,需进行尾气处理,常选用NaOH溶液,NaOH与Cl 的化
2
学反应方程式为:2NaOH + Cl == NaCl + NaClO + 2H O;
2 2
(6)氯气制备漂白粉的方程式为:2Ca(OH) +2Cl===CaCl +Ca(ClO) +2HO,其漂白有效成分为
2 2 2 2 2
Ca(ClO) 。
2
3.(2020·渭南市铁路自立中学高一月考)下图为实验室制取纯净、干燥的Cl,并进行检验Cl 性质的实
2 2
验装置。其中D瓶中放有干燥的红色布条;E中为铜网,E右端出气管口附近为棉球。试回答:(1)A中发生反应的化学方程式为_________________________。
(2)为得到干燥纯净的氯气,一般在B瓶中加入________________,其作用是_______。
(3)C中盛放的试剂为___________________________________。
(4)F中加入物质是_________________。
【答案】(1)MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
(2)饱和食盐水 吸收HCl气体
(3)浓HSO
2 4
(4)NaOH溶液
【解析】(1)实验室是利用二氧化锰和浓盐酸加热反应生成氯气,A中是浓盐酸,B中是二氧化锰固体,反
应的化学方程式为MnO +4HCl(浓) MnCl +Cl↑+2H O,故答案为:MnO +4HCl(浓)
2 2 2 2 2
MnCl +Cl↑+2H O;
2 2 2
(2)生成的氯气中含有氯化氢,用饱和食盐水除去氯气中的氯化氢,故答案为:饱和食盐水;吸收HCl气体;
(3)用浓硫酸除去氯气中的水蒸气得到干燥纯净的氯气,故答案为:浓HSO ;
2 4
(4)氯气有毒,不能排放到空气中,需要用氢氧化钠溶液吸收,氯气和氢氧化钠溶液反应生成氯化钠、次氯
酸钠和水反应的化学方程式为:Cl+2NaOH=NaCl+NaClO+H O,故答案为:氢氧化钠溶液。
2 2