文档内容
第二章 烷
第二节 烯烃、炔烃
第一课时 烯烃
课题: 2.2.1 烯烃 课时 2 授课年级 高二
《普通高中化学课程标准(2017年版)》对本节课作出了明确的【内容要求】:烯烃和
炔烃是有机化学中的重要内容。对于烯烃,学生需要理解其作为不饱和烃的特性,并通过官
能团的结构与性质来分析掌握烯烃的化学性质。此外,通过乙烯结构为例,深入理解碳碳双
键的特性以及“结构与性质”的关系。
在炔烃的学习上,学生需了解其在日常生活、有机合成和化工生产中的重要作用。特别
课标要 是对乙炔这一最简单的炔烃的学习,可让学生进一步理解官能团对物质性质的重要作用,并
求 学会从分类及官能团角度认识有机物的性质。同时,要掌握乙炔的主要物理性质并能描述和
分析乙炔的重要反应。
要注意的是,烯烃与炔烃的化学性质是一个重要的考察点,学生需要理解并能分析它们
性质相似的原因。例如,它们都能燃烧,但燃烧时的现象可能不同;乙炔还能与酸性
KMnO4溶液反应等。总的来说,通过对烯烃和炔烃的学习,学生应深化“结构决定性质”
的化学基本观念,培养宏观辨识与微观探析的学科核心素养。
烯烃和炔烃是两类重要的不饱和烃。本节内容主要包括烯烃的结构、性质和立体异构,
以下以乙炔为代表物的炔烃的结构和性质。
本节在编排上先帮助学生回忆乙烯的结构和性质,通过“思考与讨论”帮助学生复习乙
烯的加成反应和加聚反应规律,再向丙烯和异丁烯等烯烃进行迁移应用。由此帮助学生建立
“结构决定性质”的化学基本观念。
教材 烯烃的命名在烷烃系统命名的基础上,标注了碳碳双键官能团的位置。可以结合烯烃的
碳架异构、官能团位置异构和立体异构进行讨论学习,帮助学生进一步认识有机化合物分子
分析
结构的复杂性和多样性。
在必修阶段,学生只是简单地认识了乙炔,有关乙炔的结构和性质的学习是本节的另一
个重点。教材在编排上先通过实验探究结合交流讨论帮助学生认识乙炔有哪些化学性质,这
些化学性质与其分子结构有什么关系,并将其与乙烯的结构和性质进行对比。再通过化学方
程式帮助学生认识有关反应规律,了解乙炔在有机合成中的应用。最后,在炔烃类别的层面
帮助学生认识炔烃的结构特点和性质。
1.复习乙烯的结构和性质,进而掌握烯烃的结构和性质。
教学目
2.列举二烯烃的结构和性质。
标
3.烯烃的命名以及烯烃的顺反异构现象。
教学 重点:烯烃的结构和性质
重、难 难点:烯烃的立体异构以及加聚产物的书写
点
证据推理与模型认知:通过学习烯烃、炔烃的结构与化学性质的知识及乙炔的实验室制
核心素 法,提高学生分析解释、辨识记忆、简单设计等能力,发展学生宏观辨识与微观探析、证据推
养 理与模型认知的学科核心素养。
宏观辨识与微观探析:运用辨识记忆能力、推论预测能力及复杂推理能力,深入理解烯烃、炔烃的化学性质与分子结构之间的关系,领悟“结构--性质--用途”之间的对应关系,对炔
烃的结构与化学性质建立联系,设计合理的实验验证假设并得出结论,发展证据推理与模型认
知的学科核心素养。
概括关联与推论预测:在考查“烯烃的组成和结构特点”“烯烃化学性质与结构的关
系”“乙炔的实验室制法”的试题情境中,运用创新思维、推论预测、概括关联等综合能力解
决问题,发展宏观辨识与微观探析、证据推理与模型认知、科学探究与创新意识的学科核心素
养。
1.学生已有的知识水平和能力基础
(1)学生在必修二学习了乙烯的结构和性质,简单认识了乙炔。
(2)学生在选择性必修3第一章学习了有机化合物中碳原子的杂化方式以及成键方式。
学情分
2.学生在本节课上可能存在的困难
析
(1)将烯烃、炔烃的结构特点与烯烃、炔烃的性质进行关联。
(2)对烯烃的立体异构进行分析与判断。
(3)对乙炔的实验室制备及性质实验的理解。
教学过程
教学环
教学活动 设计意图
节
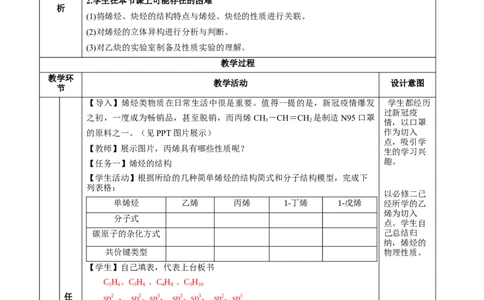
【导入】烯烃类物质在日常生活中很是重要。值得一提的是,新冠疫情爆发 学生都经历
过新冠疫
之初,一度成为畅销品,甚至脱销,而丙烯CH -CH=CH 是制造N95口罩
3 2 情,以口罩
的原料之一。(见PPT图片展示) 作为切入
点,吸引学
【教师】展示图片,丙烯具有哪些性质呢?
生的学习兴
【任务一】烯烃的结构 趣。
【学生活动】根据所给的几种简单烯烃的结构简式和分子结构模型,完成下
列表格:
以必修二已
单烯烃 乙烯 丙烯 1-丁烯 1-戊烯 经所学的乙
烯为切入
分子式
点。学生自
碳原子的杂化方式 己总结归
纳,烯烃的
共价键类型 物理性质。
【学生】自己填表,代表上台板书
C H、C H 、C H 、C H
2 4 3 6 4 8 5 10
任 sp2 , sp2、sp3, sp2、sp3, sp2、sp3
务
一
σ和π,σ和π,σ和π,σ和π
、
【教师】评价、总结。
教师知识讲
烯
【总结】1.定义:分子中含有碳碳双键的烃,属于不饱和烃。
解,学生认
烃
的 2.官能团:碳碳双键 真听讲并记
忆,培养学
结
3.结构特点:碳原子均采取sp2杂化,以碳碳双键为中心的6个
生总结归纳
构
原子一定在同一平面。
能力。
4.通式:链状单烯烃C H (n≥2)
n 2n
5.分类:单烯烃(CH=CH )、二烯烃(CH=CH-
2 2 2活 CH=CH)、多烯烃
2
动
6.共价键---分子中的碳原子均采取sp2杂化,碳原子与氢原子
一
间形成σ键,两个碳原子之间形成双键(1个σ键和1个π键)。
、
烯 7.空间结构---乙烯中的所有原子都位于同一平面,相邻两个键
烃 之间的夹角约为120°
的
【典型例题】
结
构 例1.下列关于乙烯(CH 2 CH 2 )的说法正确的是( )。
A.乙烯分子中有1个σ键、1个π键
B.乙烯分子中2个碳原子都是sp2杂化
C.乙烯分子中不存在非极性键
D.乙烯分子中6个原子在同一直线上
【答案要点】 B
解析 共价单键是σ 键,共价双键中一个是σ 键一个是π键,所以乙烯分
子中有5个σ 键、1个π 键,A项错误;乙烯分子中2个碳原子的价层电子对数
为3,所以碳碳双键中的碳原子采用sp2杂化,B项正确;同种非金属元素之间存
在非极性共价键,不同非金属元素之间存在极性共价键,所以乙烯分子中存在非
极性键,C项错误;乙烯分子中的6个原子在同一平面上,D项错误。
典型例题检
例2.下列关于乙烯和乙烷的说法中,不正确的是( )。
测学生知识
A.乙烯属于不饱和链烃,乙烷属于饱和链烃 点的掌握情
况,实时调
B.乙烯分子中所有原子处于同一平面上,乙烷分子则为立体结构,所有原子 整课程进
不在同一平面上 度。
C.乙烯分子中的碳碳双键和乙烷分子中的碳碳单键相比较,双键的键能更
大,键长更长
D.乙烯能使酸性KMnO 溶液褪色,乙烷不能
4
【答案要点】 C
解析 碳碳双键比碳碳单键短,C项错误。
【任务一】烯烃的物理性质
【学生活动】根据所给表格,总结烯烃的物理性质:
任 通过小组讨
活 务 论得出结
动 一 论,加深学
二 、 生对知识的
、 理解,培养
烯
烯 学生总结归
烃
烃 纳的能力。
的
的
物
性
理
质
性
【学生】分组讨论,总结规律
氧质
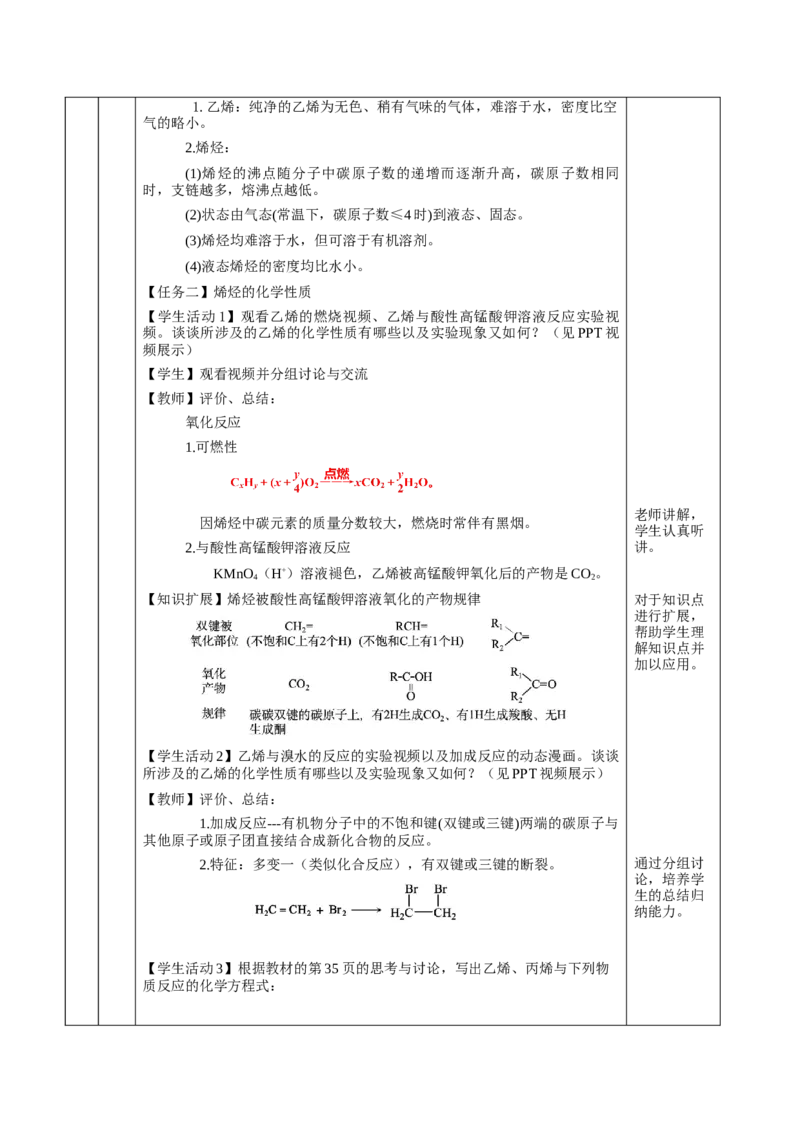
【教师】鼓励、评价1.乙烯:纯净的乙烯为无色、稍有气味的气体,难溶于水,密度比空
气的略小。
2.烯烃:
(1)烯烃的沸点随分子中碳原子数的递增而逐渐升高,碳原子数相同
时,支链越多,熔沸点越低。
(2)状态由气态(常温下,碳原子数≤4时)到液态、固态。
(3)烯烃均难溶于水,但可溶于有机溶剂。
(4)液态烯烃的密度均比水小。
【任务二】烯烃的化学性质
【学生活动1】观看乙烯的燃烧视频、乙烯与酸性高锰酸钾溶液反应实验视
频。谈谈所涉及的乙烯的化学性质有哪些以及实验现象又如何?(见PPT视
频展示)
【学生】观看视频并分组讨论与交流
【教师】评价、总结:
氧化反应
1.可燃性
老师讲解,
因烯烃中碳元素的质量分数较大,燃烧时常伴有黑烟。
学生认真听
2.与酸性高锰酸钾溶液反应 讲。
KMnO (H+)溶液褪色,乙烯被高锰酸钾氧化后的产物是CO。
4 2
【知识扩展】烯烃被酸性高锰酸钾溶液氧化的产物规律 对于知识点
进行扩展,
帮助学生理
解知识点并
加以应用。
【学生活动2】乙烯与溴水的反应的实验视频以及加成反应的动态漫画。谈谈
所涉及的乙烯的化学性质有哪些以及实验现象又如何?(见PPT视频展示)
【教师】评价、总结:
1.加成反应---有机物分子中的不饱和键(双键或三键)两端的碳原子与
其他原子或原子团直接结合成新化合物的反应。
2.特征:多变一(类似化合反应),有双键或三键的断裂。 通过分组讨
论,培养学
生的总结归
纳能力。
【学生活动3】根据教材的第35页的思考与讨论,写出乙烯、丙烯与下列物
质反应的化学方程式:试剂 乙烯 丙烯
Br
2
HCl
HO
2
【学生】学生自己默写,学生代表上台板书。
【教师】鼓励、点评、强调
【学生活动4】如何用实验证明,乙烯与溴水发生的是加成反应而不是取代反
应?
【学生】分组讨论,组内代表回答。
【教师】点评、强调
总结:将足量的乙烯通入溴水中,充分反应后,加入足量的稀硝酸酸
化,再加硝酸银溶液,无沉淀产生,说明乙烯与溴水发生的是加成反
应。
【典型例题】
例3.丙烯在一定条件下能发生如图所示的转化:
典型例题检
测学生知识
点的掌握情
况,实时调
整课程进
度。
有机物A的结构简式为_______________;
生成B的化学方程式为:_________________________________。
【答案要点】
CH=CHCHBr
2 2
CHCH=CH+Br →CHCHBrCH Br
3 2 2 3 2
【学生活动5】阅读教材第36页的资料卡片,尝试总结共轭二烯烃的性质?
【学生】分组讨论,组内代表回答。
【教师】点评、强调
总结:1.二烯烃定义---分子含有两个碳碳双键的烯烃。
2.链状二烯烃的通式:C H (n ≥ 4)
n 2n-2
1,3-丁二烯:CH=CH-CH=CH
2 2
3.共轭二烯烃的加成反应(1,3-丁二烯为例)1,2-加成;1,4-加成;完
全加成
1,2-加成和1,4-加成是竞争反应,到底哪一种加成占优势,取决于反应条
件。在温度较高的条件下大多发生1,4-加成,在温度较低的条件下大多发生
1,2-加成。
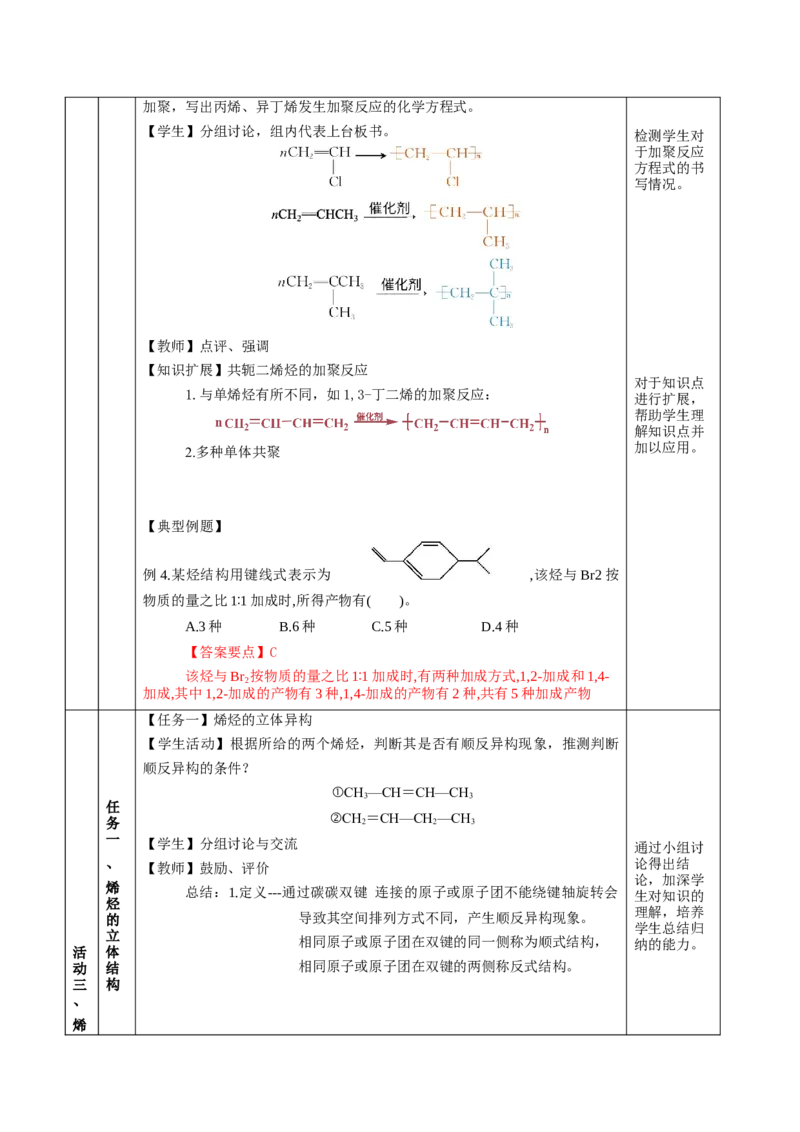
【学生活动6】阅读教材第35页的思考与讨论,请根据乙烯、氯乙烯发生的加聚,写出丙烯、异丁烯发生加聚反应的化学方程式。
【学生】分组讨论,组内代表上台板书。
检测学生对
于加聚反应
方程式的书
写情况。
【教师】点评、强调
【知识扩展】共轭二烯烃的加聚反应
对于知识点
1.与单烯烃有所不同,如1,3-丁二烯的加聚反应:
进行扩展,
帮助学生理
解知识点并
加以应用。
2.多种单体共聚
【典型例题】
例4.某烃结构用键线式表示为 ,该烃与Br2按
物质的量之比1∶1加成时,所得产物有( )。
A.3种 B.6种 C.5种 D.4种
【答案要点】C
该烃与Br 按物质的量之比1∶1加成时,有两种加成方式,1,2-加成和1,4-
2
加成,其中1,2-加成的产物有3种,1,4-加成的产物有2种,共有5种加成产物
【任务一】烯烃的立体异构
【学生活动】根据所给的两个烯烃,判断其是否有顺反异构现象,推测判断
顺反异构的条件?
①CH—CH=CH—CH
3 3
任
务 ②CH 2 =CH—CH 2 —CH 3
一
【学生】分组讨论与交流 通过小组讨
、 论得出结
【教师】鼓励、评价
论,加深学
烯
总结:1.定义---通过碳碳双键 连接的原子或原子团不能绕键轴旋转会 生对知识的
烃
理解,培养
的 导致其空间排列方式不同,产生顺反异构现象。
学生总结归
立
相同原子或原子团在双键的同一侧称为顺式结构, 纳的能力。
活 体
动 结 相同原子或原子团在双键的两侧称反式结构。
三 构
、
烯烃
的
立
体
结
构
2.判断条件
(1)有碳碳双键
(2)双键的每个碳原子必须连接两个不同的原子或原子团。
3.性质
顺反异构体的化学性质基本相同,物理性质有一定的差异。
【典型例题】
例5、下列哪种物质存在顺反异构( )
【答案要点】A、D
课堂总
结
2.2.1烯烃
一、烯烃的结构
二、烯烃的性质
板书
1.物理性质
设计
2.烯烃的化学性质
(1)氧化反应
a.可燃性
b.与酸性高锰酸钾溶液反应
(2)加成反应(3)加聚反应
三、烯烃的立体异构
1.定义
2.判断立体异构的条件
本节在复习乙烯的结构和性质的基础上,运用类比迁移的方法学习烯烃的结构与性质,并
对二烯烃的性质及烯烃的立体异构作了简单的介绍,要求学生重点掌握烯烃的化学性质。这里
特别要强调的是烯烃的不对称加成和二烯烃的1,2-加成和1,4-加成,难用度较大,且学生也不
容易理解。在实际的教学实践中,要根据本校实际情况,多引导学生进行类比迁移,突破这一教
教学
学重点。
反思