文档内容
2.2.2 影响化学平衡的因素(学案)
1.掌握浓度、温度、压强等条件对化学平衡移动的影响。
2.能够画出简单的化学反应速率和平衡移动的图形、图表。
3.理解勒夏特列原理的涵义。
1.浓度、温度、压强等条件对化学平衡移动的影响
对正逆反应速率影响不同的因素是___________、___________、___________。
一、化学平衡的移动
1、定义
在一定条件下,可逆反应达到化学平衡状态,如果改变影响平衡的条件(如___________、
___________、___________等),化学平衡状态被破坏,直至正、逆反应速率___________,在
新的条件下达到新的化学平衡状态。这种现象称作平衡状态的移动,简称平衡移动。
2、平衡移动的原因
化学平衡的根本特征为___________,因此化学平衡移动的根本原因为V(正)≠V(逆),平衡移
动的方向根据V(正)、V(逆)的相对大小来决定。
当V(正)>V(逆)时则向___________方向移动
V(正)<V(逆)时则向___________方向移动
V(正)=V(逆)时则___________
平衡移动的结果是Vˋ(正)______Vˋ(逆),达到新的化学平衡。
二、浓度、压强对化学平衡移动的影响
1、浓度变化对化学平衡移动的影响规律
(1)增大反应物浓度或减小生成物浓度,平衡向___________方向移动。
(2)减小反应物浓度或增大生成物浓度,平衡向___________方向移动。
若其他条件不变,一次性改变浓度对化学平衡的影响如下表所示:
化学
aA+bB⇌cC+dD(A、B、C、D为非固体)
平衡
体系浓 增大反应物浓 增大生成物浓
减小反应物浓度 减小生成物浓度
度改变 度 度平衡移
正向移动 逆向移动 逆向移动 正向移动
动方向
v 先增大,v v 先增大,v v 先减小,v v 先减小,v
正 逆 逆 正 逆 逆 正
速率
随后增大,且v′ 随后增大, 随后减小,且v′ 随后减小,且v′
正
变化
>v′ 且v′ >v′ >v′ >v′
正 逆 逆 正 逆 正 正 逆
图像
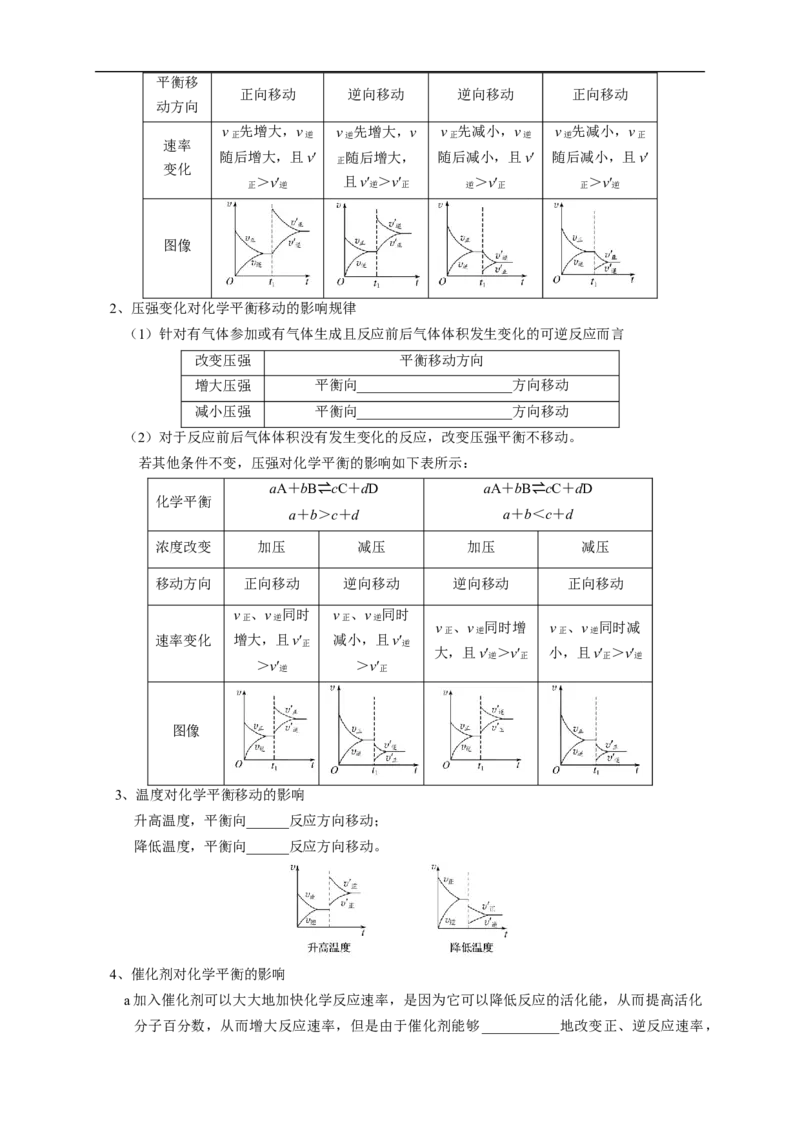
2、压强变化对化学平衡移动的影响规律
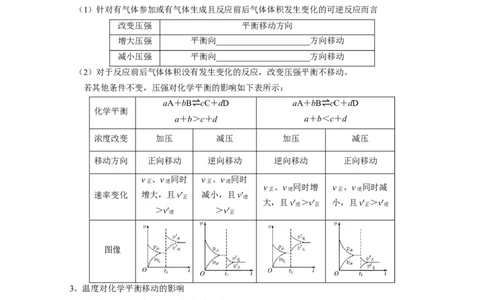
(1)针对有气体参加或有气体生成且反应前后气体体积发生变化的可逆反应而言
改变压强 平衡移动方向
增大压强 平衡向______________________方向移动
减小压强 平衡向______________________方向移动
(2)对于反应前后气体体积没有发生变化的反应,改变压强平衡不移动。
若其他条件不变,压强对化学平衡的影响如下表所示:
aA+bB⇌ cC+dD aA+bB⇌cC+dD
化学平衡
a+b>c+d a+b<c+d
浓度改变 加压 减压 加压 减压
移动方向 正向移动 逆向移动 逆向移动 正向移动
v 、v 同时 v 、v 同时
正 逆 正 逆
v 、v 同时增 v 、v 同时减
正 逆 正 逆
速率变化 增大,且v′ 减小,且v′
正 逆
大,且v′ >v′ 小,且v′ >v′
逆 正 正 逆
>v′ >v′
逆 正
图像
3、温度对化学平衡移动的影响
升高温度,平衡向______反应方向移动;
降低温度,平衡向______反应方向移动。
4、催化剂对化学平衡的影响
a加入催化剂可以大大地加快化学反应速率,是因为它可以降低反应的活化能,从而提高活化
分子百分数,从而增大反应速率,但是由于催化剂能够___________地改变正、逆反应速率,因此它对化学平衡移动___________。
b催化剂不能改变达到化学平衡状态时的反应混合物中的组成含量,但是使用催化剂能改变反
应达到平衡所需的时间。
三、勒夏特列原理
1、原理
如果改变影响平衡的一个条件(如___________、___________或___________),则平衡将向
着能够___________这种改变的方向移动。
2、注意事项
(1)研究对象一定是处于平衡状态的___________反应。
(2)勒夏特列原理只适用于判断“___________影响平衡的一个条件”时的平衡移动方向。
(3)平衡移动的结果只能是“_______”外界条件的改变,但不能完全“_____”这种改变。
四、转换率
对于反应mA(g)+nB(g)⇌pC(g)+qD(g)
平衡转化率可以表示为:_________________________________
1
【练习】在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g) N (g)+CO
2 2 2
(g)ΔH=﹣373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正
确措施是( )
A.加催化剂同时升高温度
B.加催化剂同时增大压强
C.升高温度同时充入N
2
D.降低温度同时增大压强
【练习】化合物在水溶液中因存在以下电离平衡:HIn(红色) H++In﹣(黄色),故可用作酸
碱指示剂。浓度为0.4mol·L-1的下列各溶液:①盐酸②石灰水③NaCl溶液④NaHSO 溶
4
液⑤硝酸钾溶液⑥氨水,其中能使指示剂显红色的是( )
A.①④ B.②⑤⑥ C.①④⑤ D.②③⑥
【练习】在体积一定的恒温密闭容器中加入等物质的量的X、Y,进行如下可逆反应:X(g)+Y(g)
Z(g)+W(s)ΔH>0。下列叙述正确的是( )
A.若继续充入X,平衡向正反应方向移动,Y的转化率增大
B.若继续充入Z,平衡逆向移动,Z的体积分数减小
C.若移走部分W,平衡正向移动
D.平衡后移走X,上述反应的ΔH减小【练习】α 和α ,c 和c 分别为两个恒容容器中平衡体系NO (g) 2NO (g)和3O (g)
1 2 1 2 2 4 2 2
2O (g)的反应物转化率及反应物的平衡浓度,在温度不变的情况下,均增加反应
3
物的物质的量,下列判断正确的是( )
A.α、α 均减小,c、c 均增大
1 2 1 2
B.α、α 均增大,c、c 均减小
1 2 1 2
C.α 减小,α 增大,c、c 均增大
1 2 1 2
D.α 减小,α 增大,c 增大,c 减小
1 2 1 2
【练习】在一个恒温恒容的密闭容器中充入1molHI,建立如下平衡:2HI(g) H (g)+I
2 2
(g),测得HI的转化率为a%。保持恒温恒容,在上述平衡体系中再充入2molHI,待新
平衡建立后HI的转化率为b%,则a与b的关系是( )
A.a>b B.a<b C.a=b D.无法确定
【练习】在下列平衡体系中,保持温度一定时,改变某物质的浓度,混合气体的颜色会改变;改变
压强时,颜色也会改变,但平衡并不移动,这个反应是( )
A.2NO(g)+O(g) 2NO (g)
2 2
B.NO(g) 2NO (g)
2 4 2
C.Br (g)+H(g) 2HBr(g)
2 2
D.6NO(g)+4NH (g) 5N(g)+3HO(g)
3 2 2
【练习】某对于平衡体系xA(g)+yB(g) mC(g)+nD(g),其他条件不变增大压强,C的百分含量
减少,则下列关系中正确的是( )
A.x+mx D.m+n0
3 2 2
D.4NH (g)+5O(g) 4NO(g)+6HO(g)ΔH<0
3 2 2
3.可逆反应:3A(g) 3B(?)+C(?)ΔH>0,随着温度升高,气体平均相对分子质量有减小趋势,
则下列判断正确的是( )
A.B和C可能都是固体
B.B和C一定都是气体
C.若C为固体,则B一定是气体
D.B和C一定都不是气体
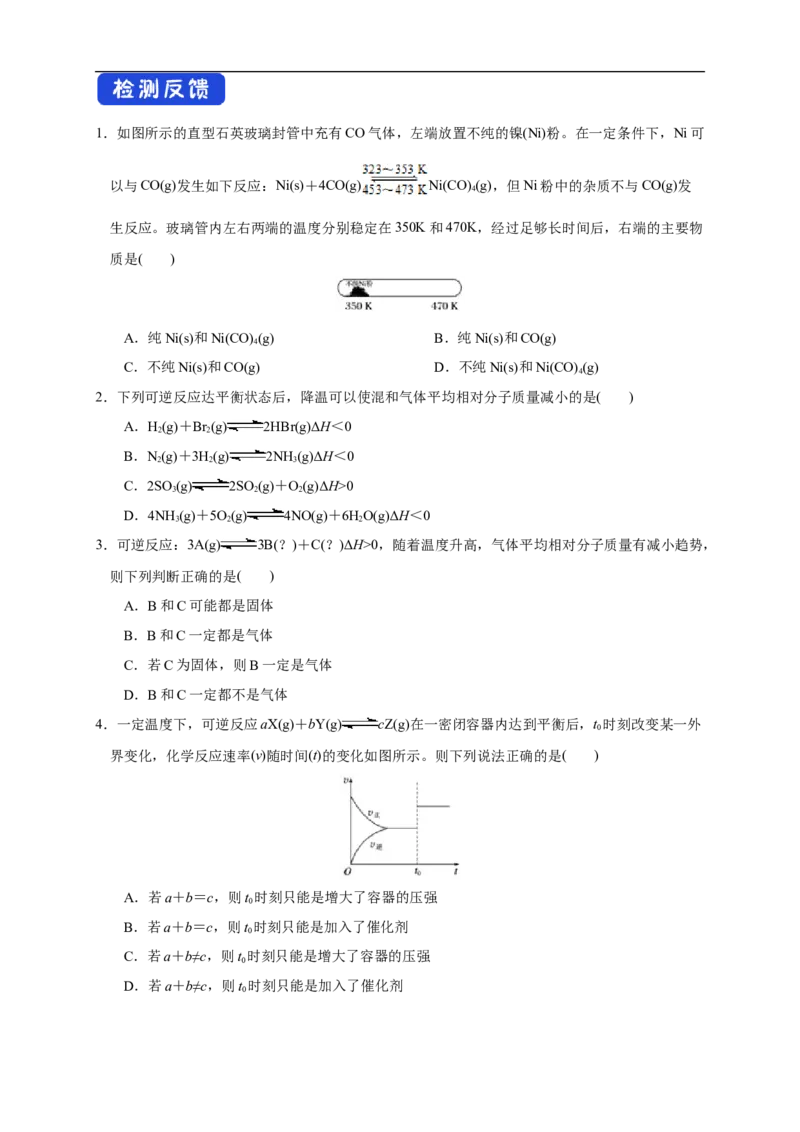
4.一定温度下,可逆反应aX(g)+bY(g) cZ(g)在一密闭容器内达到平衡后,t 时刻改变某一外
0
界变化,化学反应速率(v)随时间(t)的变化如图所示。则下列说法正确的是( )
A.若a+b=c,则t 时刻只能是增大了容器的压强
0
B.若a+b=c,则t 时刻只能是加入了催化剂
0
C.若a+b≠c,则t 时刻只能是增大了容器的压强
0
D.若a+b≠c,则t 时刻只能是加入了催化剂
05.已知某可逆反应在密闭容器中进行:A(g)+2B(g) 3C(g)ΔH>0,如图中曲线a代表一定条
件下该反应的过程,若使a曲线变为b曲线,可采取的措施是( )
A.恒温恒容条件下将A、B的浓度增加一倍
B.恒温条件下加压(缩小容器体积)
C.使用合适的催化剂
D.升高温度
6.下列变化不能用勒夏特列原理解释的是( )
A.合成氨是放热反应,采用在较高温度下进行反应
B.氯化镁溶液加热蒸干最终得不到氯化镁固体
C.工业生产硫酸的过程中使用过量的空气,以提高二氧化硫的转化率
D.实验室用排饱和食盐水的方法收集氯气
7.下列事实中,不能用勒夏特列原理解释的是( )
A.合成NH 反应,为提高NH 的产率,理论上应采取相对较低的温度
3 3
B.实验室中常用排饱和食盐水的方式收集氯气
C.对于CO(g)+NO(g) CO(g)+NO(g)的平衡体系,增大压强可使颜色变深
2 2
D.对熟石灰的悬浊液加热,悬浊液中固体质量增加
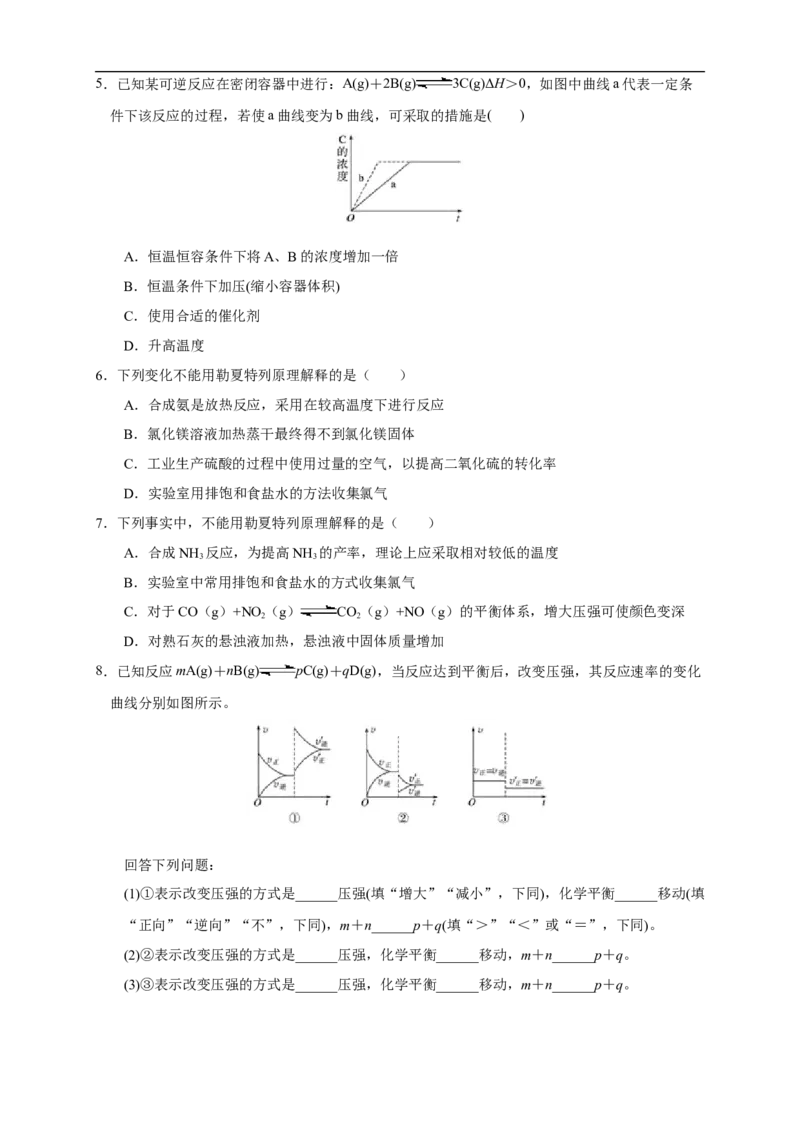
8.已知反应mA(g)+nB(g) pC(g)+qD(g),当反应达到平衡后,改变压强,其反应速率的变化
曲线分别如图所示。
回答下列问题:
(1)①表示改变压强的方式是______压强(填“增大”“减小”,下同),化学平衡______移动(填
“正向”“逆向”“不”,下同),m+n______p+q(填“>”“<”或“=”,下同)。
(2)②表示改变压强的方式是______压强,化学平衡______移动,m+n______p+q。
(3)③表示改变压强的方式是______压强,化学平衡______移动,m+n______p+q。9.将5mL0.005mol·L-1的FeCl 溶液与5mL0.01mol·L-1的KSCN溶液混合,建立平衡:FeCl +
3 3
3KSCN 3KCl+Fe(SCN) (红色)
3
(1)若滴加饱和FeCl 溶液4滴,平衡向________方向移动,溶液红色________。
3
(2)若滴加1mol·L-1KSCN溶液4滴,平衡向________方向移动,溶液红色________。
(3)若滴加0.01mol·L-1NaOH溶液4滴,则产生______(填颜色)沉淀,c(Fe3+)________,平衡向
________方向移动,溶液红色________。
(4)若加入少量KCl固体,则平衡________移动,原因
__________________________________________________。
【知识点填空答案】浓度;压强;温度
【知识点填空答案】
浓度;压强;温度;再次相等;V(正)=V(逆);正方向;逆方向;;不移动;=;正反应;逆反应;
气体体积缩小;气体体积增大;吸热;放热;同等程度地;无影响;浓度;压强;温度;减弱;可
n(消耗) n (A)-n (A)
a(A)= ×100%= 0 平 ×100%
n(总) n (A)
逆;改变;减弱;消除; 0
【练习答案】BAACCCBAC
【检测反馈答案】1-8:BDCDCAC
8.(1)增大逆向<(2)减小正向<(3)减小不=
9.(1)正反应加深(2)正反应加深(3)红褐色减小逆反应变浅(4)不KCl不参与反应