文档内容
第二章 分子结构与性质
第二节 分子的空间结构
2.2.2 杂化轨道理论简介
本节从分子结构的测定、三原子、四原子、五原子分子的立体构型为例,介绍典型分子立体构
型;然后从价层电子对互斥理论和杂化轨道理论解释分子结构的多样性和复杂性,并根据上述理论
判断简单分子和离子的构型。
课程目标 学科素养
1.了解杂化轨道理论的基本内容。 1.微观探析:通过杂化轨道理论的学习,能从
微观角度理解中心原子的杂化类型对分子空
2.在理解杂化轨道理论的基础上,对分子的空间构
间结构的影响。
型进行解释和预测。
2.模型认知:通过杂化轨道理论的学习,掌握
中心原子杂化轨道类型判断的方法,建立分子
空间结构分析的思维模型。
教学重点:杂化轨道理论
教学难点:杂化轨道理论
多媒体调试、讲义分发
【创设情境】
甲烷呈正四面体形,它的4个C—H键的键能、键长相同,H—C—H的键角109°28′,按照我
们已经学过的价键理论,甲烷的4个C- H单键都应该是σ键,然而,碳原子的4个价层原子轨道是
3个相互垂直的2p轨道和1个球形的2s轨道,用它们跟4个氢原子的1s原子轨道重叠,不可能得
到正四面体形的甲烷分子。请解释原因。
【讲解】
当碳原子与4个氢原子形成甲烷分子时,碳原子的2s轨道和3个2p轨道会发生混杂,混杂时
保持轨道总数不变,却得到4个新的能量相同、方向不同的轨道,各指向正四面体的4个顶角,夹
角109°28',称为sp3杂化轨道,表示这4个轨道是由1个s轨道和3个p轨道杂化形成的。当碳原子跟4个氢原子结合时,碳原子以4个sp杂化轨道分别与4个氢原子的1s轨道重叠,形成4个C-H σ
键,因此呈正四面体形的空间结构。
【过渡】
了解了CH 的杂化方式,接下来我们就来具体学习杂化轨道理论。
4
【讲解】
1.杂化轨道理论
(1)杂化轨道理论是一种价键理论,是鲍林为了解释分子的空间结构提出的。
①轨道的杂化:在外界条件影响下,原子内部能量相近的原子轨道发生混杂,重新组合成一
组新的轨道的过程。
②杂化轨道:原子轨道杂化后形成的一组新的原子轨道,叫做杂化原子轨道,简称杂化轨
道。
③轨道杂化的过程:激发→杂化→轨道重叠。
(2)杂化轨道理论要点:
①原子在成键时,同一原子中能量相近的原子轨道可重新组合成杂化轨道。
②参与杂化的原子轨道数等于形成的杂化轨道数。
③杂化改变了原子轨道的形状、方向。杂化使原子的成键能力增加。
④杂化前后原子轨道数目不变(参加杂化的轨道数目等于形成的杂化轨道数目),且杂化轨道
的能量相同。
⑤原子轨道的杂化只有在形成分子的过程中才会发生,孤立的原子不可能发生杂化。
⑥杂化轨道用于形成σ键或者用来容纳未参与成键的孤电子对。未参与杂化的p轨道可用于形
成π键。分子的空间结构主要取决于原子轨道的杂化类型。
⑦杂化轨道数=中心原子上的孤电子对数+与中心原子结合的原子数。
(3)杂化轨道的形成及其特点
【讲解】
2.杂化类型
CH 是由1个s轨道和3个p轨道杂化形成的,sp3杂化轨道的夹角为109°28′,呈空间正四面体
4
形这种杂化方式我们称为sp3杂化。
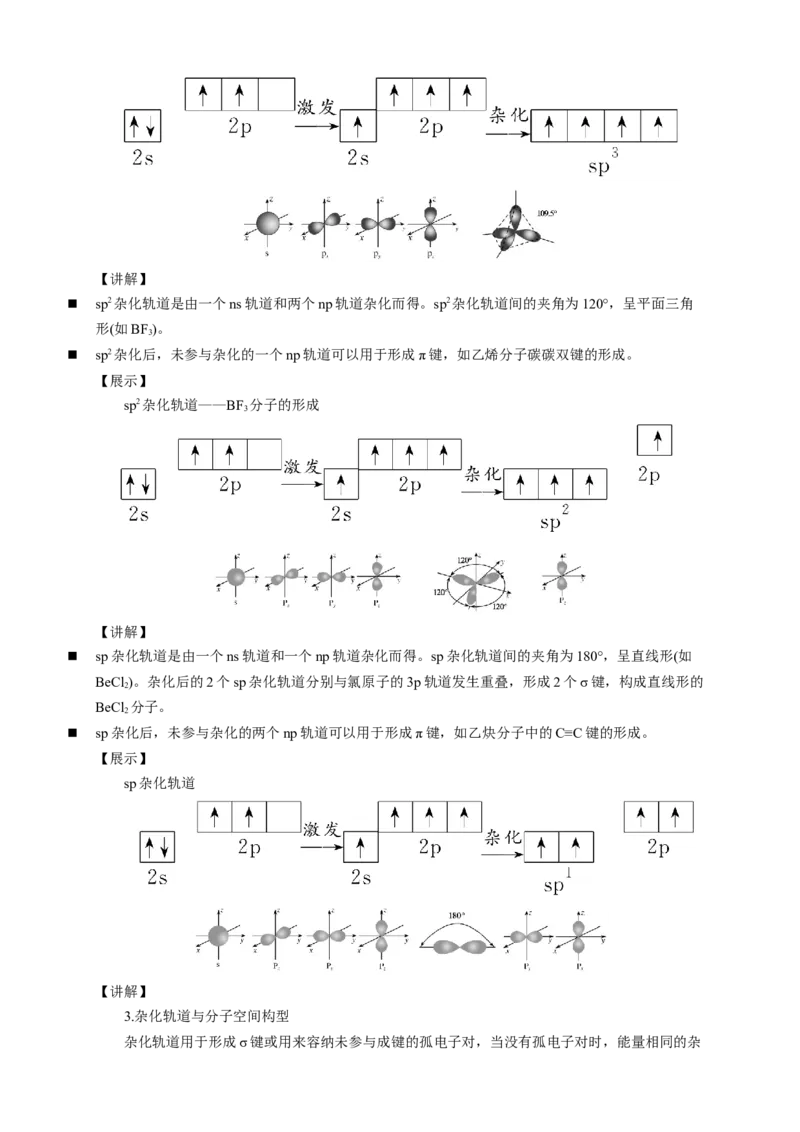
【展示】 sp3杂化轨道的形成。【讲解】
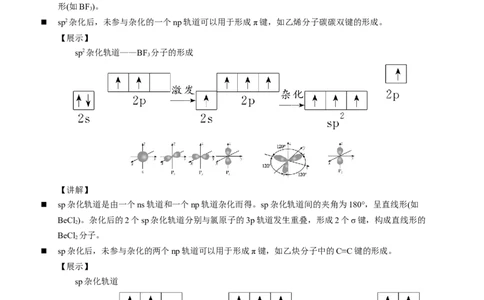
sp2杂化轨道是由一个ns轨道和两个np轨道杂化而得。sp2杂化轨道间的夹角为120°,呈平面三角
形(如BF)。
3
sp2杂化后,未参与杂化的一个np轨道可以用于形成π键,如乙烯分子碳碳双键的形成。
【展示】
sp2杂化轨道——BF 分子的形成
3
【讲解】
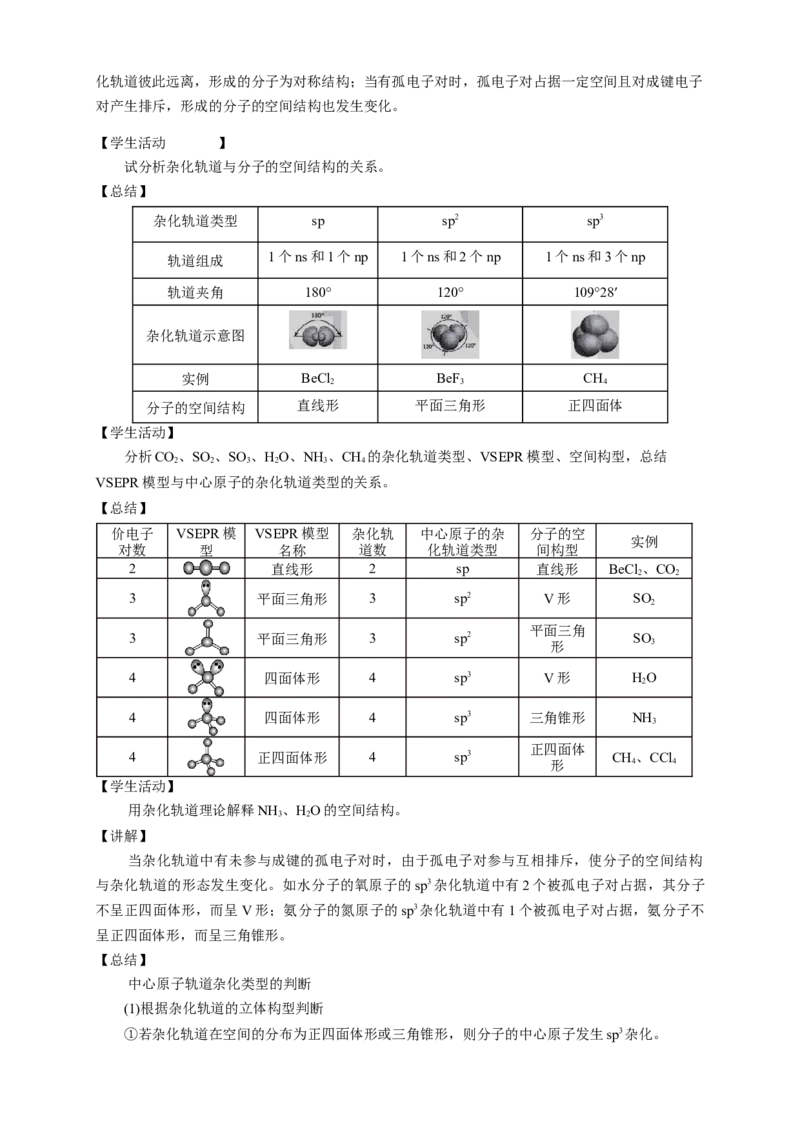
sp杂化轨道是由一个ns轨道和一个np轨道杂化而得。sp杂化轨道间的夹角为180°,呈直线形(如
BeCl )。杂化后的2个sp杂化轨道分别与氯原子的3p轨道发生重叠,形成2个σ键,构成直线形的
2
BeCl 分子。
2
sp杂化后,未参与杂化的两个np轨道可以用于形成π键,如乙炔分子中的C≡C键的形成。
【展示】
sp杂化轨道
【讲解】
3.杂化轨道与分子空间构型
杂化轨道用于形成σ键或用来容纳未参与成键的孤电子对,当没有孤电子对时,能量相同的杂化轨道彼此远离,形成的分子为对称结构;当有孤电子对时,孤电子对占据一定空间且对成键电子
对产生排斥,形成的分子的空间结构也发生变化。
【学生活动 】
试分析杂化轨道与分子的空间结构的关系。
【总结】
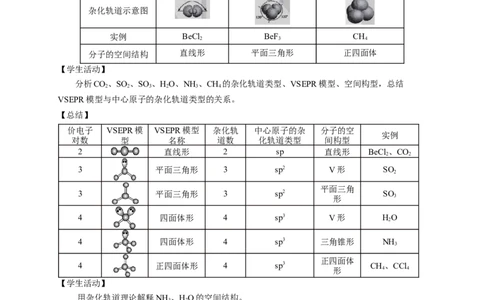
杂化轨道类型 sp sp2 sp3
轨道组成
1个ns和1个np 1个ns和2个np 1个ns和3个np
轨道夹角 180° 120° 109°28′
杂化轨道示意图
实例 BeCl BeF CH
2 3 4
分子的空间结构 直线形 平面三角形 正四面体
【学生活动】
分析CO、SO 、SO 、HO、NH 、CH 的杂化轨道类型、VSEPR模型、空间构型,总结
2 2 3 2 3 4
VSEPR模型与中心原子的杂化轨道类型的关系。
【总结】
价电子 VSEPR模 VSEPR模型 杂化轨 中心原子的杂 分子的空
实例
对数 型 名称 道数 化轨道类型 间构型
2 直线形 2 sp 直线形 BeCl 、CO
2 2
3 平面三角形 3 sp2 V形 SO
2
平面三角
3 平面三角形 3 sp2 SO
形 3
4 四面体形 4 sp3 V形 HO
2
4 四面体形 4 sp3 三角锥形 NH
3
正四面体
4 正四面体形 4 sp3 CH、CCl
形 4 4
【学生活动】
用杂化轨道理论解释NH 、HO的空间结构。
3 2
【讲解】
当杂化轨道中有未参与成键的孤电子对时,由于孤电子对参与互相排斥,使分子的空间结构
与杂化轨道的形态发生变化。如水分子的氧原子的sp3杂化轨道中有2个被孤电子对占据,其分子
不呈正四面体形,而呈V形;氨分子的氮原子的sp3杂化轨道中有1个被孤电子对占据,氨分子不
呈正四面体形,而呈三角锥形。
【总结】
中心原子轨道杂化类型的判断
(1)根据杂化轨道的立体构型判断
①若杂化轨道在空间的分布为正四面体形或三角锥形,则分子的中心原子发生sp3杂化。②若杂化轨道在空间的分布呈平面三角形,则分子的中心原子发生sp2杂化。
③若杂化轨道在空间的分布呈直线形,则分子的中心原子发生sp杂化。
(2)根据杂化轨道之间的夹角判断
若杂化轨道之间的夹角为109°28′,则分子的中心原子发生sp3杂化;若杂化轨道之间的夹角为
120°,则分子的中心原子发生sp2杂化;若杂化轨道之间的夹角为180°,则分子的中心原子发生sp
杂化。
(3)根据等电子原理进行判断
如CO 是直形线分子,CNS-、N与CO 互为等电子体,所以分子构型均为直线形,中心原子
2 2
均采用sp杂化。
(4)根据中心原子的价电子对数判断
如中心原子的价电子对数为4,是sp3杂化,为3是sp2杂化,为2是sp杂化。
(5)根据分子或离子中有无π键及π键数目判断
如没有π键为sp3杂化,含1个π键为sp2杂化,含2个π键为sp杂化。
【学生活动】
CH 、NH 、HO中心原子的杂化类型都为sp3,键角为什么依次减小?从杂化轨道理论的角度
4 3 2
比较键角大小时有什么方法?
【提示】
CH、NH 、HO中心原子都采取sp3杂化,中心原子的孤电子对数依次为0个、1个、2个。由
4 3 2
于孤电子对对共用电子对的排斥作用使键角变小,孤电子对数越多排斥作用越大,键角越小。比较
键角时,先看中心原子杂化类型,杂化类型不同时:一般键角按sp、sp2、sp3顺序依次减小;杂化
类型相同时,中心原子孤电子对数越多,键角越小。
【课堂小结】
回顾本节课的内容,本节课需要掌握判断杂化类型。先确定分子的价层电子对数,就可以知
道杂化的轨道数,再由VSEPR模型确定杂化类型,即可得出杂化轨道构型。
1. 根据杂化轨道理论和价层电子对互斥模型判断,下列分子或者离子的中心原子杂化方式及空间
构型正确的是
选 价层电子对互斥模
分子或离子中心原子杂化方式 分子或离子的立体构型
项 型
A sp 直线形 直线形
B HCHO 平面三角形 三角锥形
C 四面体形 平面三角形
D 正四面体形 正四面体形
【答案】D
【解析】分子或离 中心原子杂 价层电子对互 分子或离子的立
选项
子 化方式 斥模型 体构型
A 平面三角形 V形
B HCHO 平面三角形 平面三角形
C 四面体形 三角锥形
D 正四面体形 正四面体形
2. 下列说法中正确的是( )
A. 和 都是正四面体形分子,且键角都为
B. 乙烯分子中,碳原子的 杂化轨道形成 键,未杂化的2p轨道形成 键
C. 键长 ,因此稳定性
D. 分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用弱
【答案】B
【解析】
A. 的键角为 ,故A错误;
B.乙烯分子中,碳原子的价层电子对数为3,碳原子的 杂化轨道形成 键, 之间未参加
杂化的2p轨道“肩并肩”形成 键,故B正确;
C.键长越长,键能越小,分子的稳定性越差,则稳定性 ,故C错误;
D. 分子中孤电子对与成键电子对的排斥作用比成键电子对之间的排斥作用大,所以 分子
为三角锥形,键角小于 ,故D错误。
3. 已知如图所示反应中的四种物质由三种元素组成,其中a的分子空间构型为正四面体形,组成
a物质的两种元素的原子序数之和小于10,组成b物质的元素为第三周期元素。下列判断正确
的是
A. 四种分子中的化学键均是极性键
B. a、c分子中中心原子均采用 杂化C. 四种分子中既有 键,又有 键
D. b、d分子中共价键的键能:
【答案】B
【解析】
由题意可知,a的分子空间构型为正四面体.组成a分子的两种元素的原子序数和小于10,所以a
是甲烷分子,组成b分子的元素为第三周期的元素,形成双原子分子是氯气分子,所以反应是a甲
烷与b氯气反应生成c一氯甲烷和d氯化氢。
A.四种分子中氯气分子所含的化学键为非极性键,A错误;
B.甲烷、一氯甲烷分子中,中心原子C原子均采用 杂化,B正确;
C.四种分子中均只存在 键而没有 键,C错误;
D. 键的键能小于 键的键能,D错误。
故选B。
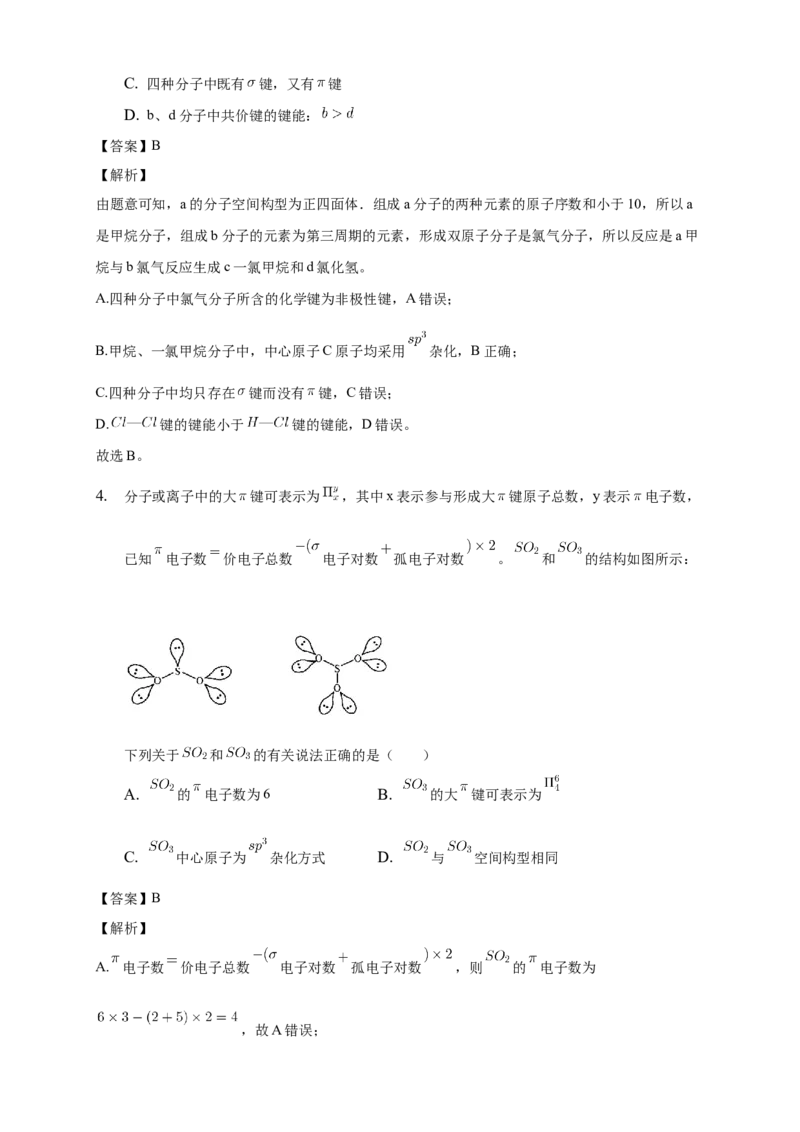
4. 分子或离子中的大 键可表示为 ,其中x表示参与形成大 键原子总数,y表示 电子数,
已知 电子数 价电子总数 电子对数 孤电子对数 。 和 的结构如图所示:
下列关于 和 的有关说法正确的是( )
A. 的 电子数为6 B. 的大 键可表示为
C. 中心原子为 杂化方式 D. 与 空间构型相同
【答案】B
【解析】
A. 电子数 价电子总数 电子对数 孤电子对数 ,则 的 电子数为
,故A错误;B. 的 电子数为 ,则 的大 键可表示为 ,故B正确;
C. 中心原子价层电子对数为 ,则杂化方式为 杂化,故C错误;
D. 中心原子价层电子对数为 ,有一对孤电子对,则空间构型为V形, 中
心原子价层电子对数为 ,没有孤电子对,则空间构型为平面三角形,故D错误。
5. 下列中心原子的杂化轨道类型和分子几何构型均不正确的是
A. 中C原子 杂化,为正四面体形
B. 中B原子 杂化,为平面三角形
C. 中C原子sp杂化,为直线形
D. 分子中,S为sp杂化,为直线形
【答案】D
【解析】
A. 中C原子形成4个 键,孤电子对数为0,则为 杂化,为正四面体形,故A正确;
B. 中B原子形成3个 键,孤电子对数为 ,则为 杂化,为平面三角形,故B
正确;
C. 中C原子形成2个 键,孤电子对数为 ,则为sp杂化,为直线形,故C正
确;
D. 分子中,S原子形成2个 键,孤电子对数为 ,则为 杂化,为V形,故D
错误。
故选D。
本节课能从价层电子对互斥理论和杂化轨道理论解释分子结构的多样性和复杂性,并根据上述
理论判断简单分子和离子的构型。通过杂化轨道理论的学习,能从微观角度理解中心原子的杂化类
型对分子空间结构的影响,培养学生宏观辨识与微观探析的可续素养,通过杂化轨道理论的学习,
掌握中心原子杂化轨道类型判断的方法,建立分子空间结构分析的思维模型。培养学生证据推理与
模型认知的科学素养。