文档内容
2.2.2 氯水与氯离子检验
【题组一 氯水】
1.(2020·全国课时练习)下列有色溶液褪色原理相同的是( )
① 使品红溶液褪色 ② 使品红溶液褪色 ③将 加入含酚酞的水溶液中,溶液先变红后褪色
④ 使酸性 溶液褪色
A.④② B.②④ C.②③ D.①④
【答案】C
【解析】① 与品红反应生成无色物质,体现其漂白性;
②氯气和水反应生成的HClO具有强氧化性,能使品红溶液褪色;
③ 和水反应生成的NaOH显碱性,故溶液先变红, 与水反应的过程中可生成 ,
具有强氧化性从而使溶液褪色;
④ 使酸性 溶液褪色,是因为发生了氧化还原反应
,与 的还原性有关。
综合以上分析,有色溶液褪色原理相同的是②③;故选C。
2.(2020·全国课时练习)下列关于氯水的叙述,正确的是
A.新制氯水中只含C1 和HO分子
2 2
B.新制氯水可使蓝色石蕊试纸变红但不褪色
C.光照氯水有气泡逸出,该气体是Cl
2
D.氯水放置数天后酸性增强
【答案】D
【解析】A.氯水中存在Cl+H O=HClO+HCl反应,HClO为弱酸,溶液中存在Cl、HClO、HO分子,A
2 2 2 2
错误;
B.氯水中含有HCl,具有酸性,可使蓝色石蕊试纸先变红,HClO具有强氧化性、漂白性,可使蓝色石蕊
试纸褪色,B错误;
C.在光照条件下次氯酸分解生成氯化氢和氧气,气体是氧气,C错误;
D.光照下生成HCl,溶液酸性变强,pH减小,D正确,答案选D。3.(2019·渭南高级中学月考)在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的
是( )
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl
2
B.向氯水中滴加硝酸酸化的AgNO 溶液,产生白色沉淀,说明氯水含有Cl-
3
C.向氯水中加入NaHCO 粉末,有气泡产生,说明氯水中含有H+
3
D.新制的氯水能使红色布条褪色,说明氯气有漂白性
【答案】D
【解析】A.氯水中只有氯气有颜色,为黄绿色,氯水呈浅黄绿色是由于含有氯气,A正确;
B.溶液与硝酸银反应产生白色沉淀,只能是氯离子与银离子反应得到AgCl白色沉淀,说明氯水中含有
Cl-,B正确;
C.氯水中含有盐酸和次氯酸,溶液呈酸性,能与碳酸氢钠反应生成二氧化碳,C正确;
D.新制的氯水能使有色布条褪色,说明氯水中存在次氯酸,次氯酸具有漂白性,氯气没有漂白性,D错
误;
答案选D。
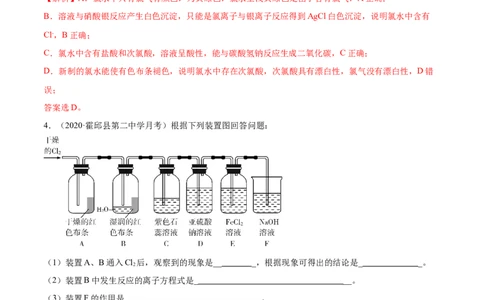
4.(2020·霍邱县第二中学月考)根据下列装置图回答问题:
(1)装置A、B通入Cl 后,观察到的现象是__ _,根据现象可得出的结论是_ _。
2
(2)装置B中发生反应的离子方程式是_ __。
(3)装置F的作用是_ __。
(4)实验开始后,观察到装置C中的现象是__ _。
(5)装置E中发生反应的离子方程式是__ __。
(6)通入Cl 时装置D中发生反应的离子方程式是_ __。
2
【答案】(1)干燥的红色(或A中)布条不褪色,湿润的红色(或B中)布条褪色
(2)Cl 无漂白性,Cl 与水反应生成的HClO有漂白性
2 2
(3)Cl+H O H++Cl-+HClO
2 2
(4)吸收氯气,防止污染环境 溶液先变红色,后褪色(5)2Fe2++Cl=2Fe3++2Cl-
2
(6)HO+SO +Cl=2H++SO +2Cl-
2 2
【解析】(1)干燥氯气遇到干燥的红色(或A中)布条不褪色,湿润的红色(或B中)布条褪色,说明Cl 无
2
漂白性,Cl 与水反应生成的HClO有漂白性;
2
(2)氯气和水反应生成盐酸和次氯酸,盐酸是强酸,能拆成离子形式,离子方程式为:Cl+H O H+
2 2
+Cl-+HClO;
(3)装置F中盛有氢氧化钠,能吸收氯气,防止污染环境;
(4)氯气和水反应生成盐酸和次氯酸,能使紫色石蕊溶液先变红色,后褪色;
(5)氯气和氯化亚铁反应生成氯化铁,离子方程式为:2Fe2++Cl=2Fe3++2Cl-;
2
(6)氯气氧化亚硫酸根离子生成硫酸根,本身被还原为氯离子,离子方程式为HO+SO +Cl=2H++SO
2 2
+2Cl-。
5.(2020·天津武清·)某课外小组同学用下图所示装置在实验室制氯气并探究其相关性质(夹持设备已
略)。
(1)制备氯气选用的药品为:漂白粉固体和浓盐酸,相关的化学反应方程式为_______________。
(2)装置B的作用之一是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象
________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中①、②、③依次放入_____(选填表中字
母)。
① ② ③
a 干燥的有色布条 碱石灰 湿润的有色布条
b 干燥的有色布条 硅胶 湿润的有色布条
c 湿润的有色布条 浓硫酸 干燥的有色布条
d 湿润的有色布条 无水氯化钙 干燥的有色布条(4)设计装置D、E的目的是比较氯、溴、碘的非金属性强弱。当向D中缓缓通入一定量氯气时,可以看
到无色溶液逐渐变为________色,说明氯的非金属性大于溴;之后打开活塞,将装置D中少量溶液加入装
置E中,振荡;观察到的现象是___________________,则说明溴的非金属性大于碘。
(5)有同学提出该实验方案仍有不足,请说明其中的不足及后果。
①_________________________;②______________________。
【答案】(1)Ca(ClO) +2HCl=Cl ↑+H O+CaCl
2 2 2 2
(2)长颈漏斗中液面明显上升,形成水柱
(3) d
(4)黄(或橙) 溶液变蓝色
(5)E处未能排除D中过量Cl 的干扰,而置换出I Cl 通入NaHSO 溶液中会产生SO ,污染空气
2 2 2 3 2
【解析】(1)漂白粉的主要成分有次氯酸钙和氯化钙,次氯酸钙与浓盐酸反应生成氯气,反应方程式为:
Ca(ClO) +4HCl(浓)=CaCl +2Cl↑+2H O,故答案为Ca(ClO) +4HCl(浓)=CaCl +2Cl↑+2H O;
2 2 2 2 2 2 2 2
(2)装置B的作用之一是安全瓶,监测实验进行时C中是否发生堵塞,若堵塞,装置AB中气体压强增大,
会把B中的液体压入长颈漏斗中形成水柱;故答案为长颈漏斗中液面明显上升,形成水柱;
(3)氯气无漂白作用,氯气和水反应生成次氯酸具有漂白性。a、氯气从食盐水中出来会含有水蒸气,干燥
有色布条会褪色,通过碱石灰后,氯气会被吸收,后续试验无法验氯气是否具有漂白性,故a错误;b、氯
气从食盐水中出来会含有水蒸气,干燥有色布条会褪色,通过硅胶后,水蒸气会被吸收,但遇到湿润的有
色布条会褪色,不能证明其漂白作用的物质,故b错误;c、氯气从食盐水中出来会含有水蒸气,湿润有色
布条会褪色,U形管中加入浓硫酸,气体不能进入后面装置,不能证明氯气是否有漂白性,故c错误;d、
氯气从食盐水中出来会含有水蒸气,湿润有色布条会褪色,通过固体干燥剂氯化钙吸收水后,遇干燥的有
色布条不褪色证明氯气无漂白性,故d正确;故答案为d;
(4)D中是溴化钠,当向D中缓缓通入少量氯气时,氯气和溴化钠反应生成溴单质,可以看到无色溶液逐渐
变为黄,所以现象为:溶液从无色变化为黄色:氧化还原反应中氧化剂的氧化性大于氧化产物,说明氯气
的氧化性强于溴;打开活塞,将装置D中含溴单质的少量溶液加入含碘化钾淀粉溶液的装置E中,溴单质
和碘化钾反应生成碘单质,碘单质遇淀粉变蓝,故答案为黄(或橙); 溶液变蓝色;
(5)装置中在验证溴单质氧化性大于碘单质的实验验证方法中 不能排除氯气氧化碘离子的干扰作用;最后
装置F氯气通入会和水反应生成盐酸,盐酸和亚硫酸氢钠反应生成二氧化硫污染气,不能被吸收,故答案
为①E处未能排除D中过量Cl 的干扰,而置换出I;
2 2
②Cl 通入NaHSO 溶液中会产生SO ,污染空气。
2 3 2【题组二 氯水与碱反应】
1.(2020·巩义市第四高级中学月考)工业上生产漂白粉时应采用 ( )
A.石灰水与氯气反应
B.纯净的熟石灰粉末与氯气反应
C.含适量水分的熟石灰粉末与氯气反应
D.石灰乳与氯气反应
【答案】D
【解析】A.石灰水是氢氧化钙的水溶液,与氯气能反应,但难以获得漂白粉,A不合题意;
B.没有水的帮助,纯净的熟石灰粉末与氯气反应难以进行,B不合题意;
C.含适量水分的熟石灰粉末与氯气接触面积小,反应进行缓慢,不利于漂白粉的大量生产,C不合题意;
D.石灰乳是氢氧化钙的悬浊液,与氯气反应速率快,生产漂白粉的产率高,D符合题意;
故选D。
2.(2020·全国课时练习)为了增强漂粉精的漂白能力,常在漂粉精溶液中加入少量的
A.NaOH B.NaCl C.HCl D.CaCl
2
【答案】C
【解析】漂白粉是混合物,主要成分是Ca(ClO) 和CaCl ,有效成分是Ca(ClO) ,次氯酸钙可与酸反应生
2 2 2
成具有漂白性的次氯酸,则增强漂白能力,应加入酸,题给物质中只有盐酸符合,发生反应
Ca(ClO) +2HCl=CaCl +2HClO,答案选C。
2 2
3.(2020·全国课时练习)下列叙述不正确的是( )
A.84消毒液的有效成分是NaClO
B.漂白粉在空气中不稳定,可用于漂白纸张
C.向氯水中滴加硝酸酸化的 溶液,产生白色沉淀,说明氯水中含有
D.向 溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
【答案】D
【解析】A.84消毒液的有效成分是NaClO,A项正确;
B.漂白粉的有效成分是 ,因为在空气中发生反应
, 而失效,B项正确;
C.氯水中的 与 溶液反应产生白色沉淀,C项正确;D.氯水中的 、HClO均能与 反应生成 ,从而使溶液变成棕黄色,D项错误;
故选D。
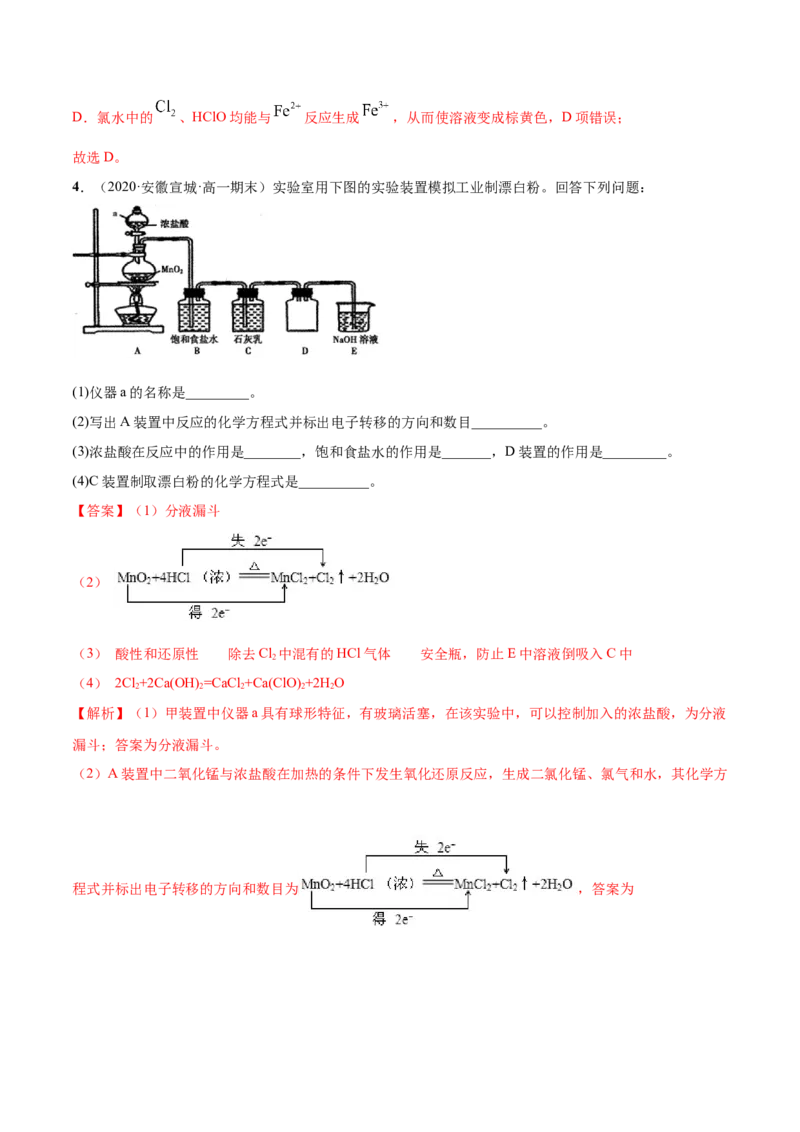
4.(2020·安徽宣城·高一期末)实验室用下图的实验装置模拟工业制漂白粉。回答下列问题:
(1)仪器a的名称是_________。
(2)写出A装置中反应的化学方程式并标出电子转移的方向和数目__________。
(3)浓盐酸在反应中的作用是________,饱和食盐水的作用是_______,D装置的作用是_________。
(4)C装置制取漂白粉的化学方程式是__________。
【答案】(1)分液漏斗
(2)
(3) 酸性和还原性 除去Cl 中混有的HCl气体 安全瓶,防止E中溶液倒吸入C中
2
(4) 2Cl+2Ca(OH) =CaCl +Ca(ClO) +2H O
2 2 2 2 2
【解析】(1)甲装置中仪器a具有球形特征,有玻璃活塞,在该实验中,可以控制加入的浓盐酸,为分液
漏斗;答案为分液漏斗。
(2)A装置中二氧化锰与浓盐酸在加热的条件下发生氧化还原反应,生成二氯化锰、氯气和水,其化学方
程式并标出电子转移的方向和数目为 ,答案为。
(3)由 可知,浓盐酸中4个Cl-,有2个Cl-化合价没有改变,
形成MnCl ,起酸的作用,有2个Cl-化合价升高,失电子,起还原剂的作用,浓盐酸和二氧化锰反应过程
2
中会挥发出氯化氢气体,氯化氢在氯化钠饱和溶液中易溶,而氯气的溶解度小,通过饱和食盐水的作用是
除去Cl 中混有有的HC气体,D装置的作用是安全瓶,防止E中溶液倒吸入C中;答案为酸性和还原性,
2
除去Cl 中混有有的HC气体,安全瓶,防止E中溶液倒吸入C中。
2
(4)制取漂白粉是氢氧化钙与氯气反应生成氯化钙、次氯酸钙和水,制取漂白粉的化学方程式是
2Cl+2Ca(OH) =CaCl +Ca(ClO) +2H O,故答案为2Cl+2Ca(OH) =CaCl +Ca(ClO) +2H O。
2 2 2 2 2 2 2 2 2 2
5.(2020·辽宁高一月考)I.某化学实验小组为了探究在实验室制备Cl 的过程中有水蒸气和HCl挥发出
2
来,同时证明氯气的某些性质,某同学设计了如图所示的实验装置(氯气易溶于CCl ,HCl不溶于CCl )。
4 4
请回答下列问题:
(1)装置A中连接橡皮管的目的是_____________________________________。
(2)装置A中发生反应的离子方程式为_________________________________,装置B中盛放的试剂是
___________。
(3)装置D与E中出现的不同现象说明的问题是_________________________。
(4)有同学基于实验的严谨性考虑,认为可在F、G两个装置之间再加一个装有湿润的淀粉KI试纸的装置,
其目的是___________________________________。
Ⅱ.某研究性学习小组欲制备漂白粉,设计在上述装置A后连接如右图所示的组合装置:(5)装置②中发生反应的化学方程为___________________________________。
(6)制漂白粉的反应是放热反应,反应温度较高时有副反应发生,改进该实验装置以减少副反应发生的方法
是___________________________________。
【答案】(1)使内外压强相等,有利于分液漏斗中的浓盐酸顺利流下
(2)MnO +4H++2Cl- Mn2++Cl↑+2HO 无水硫酸铜
2 2 2
(3)氯气无漂白性,次氯酸有漂白性
(4)验证HCl中的Cl 已经完全除去(或验证是否还含有Cl)等同类合理答案均可
2 2
(5)2Ca(OH) +2Cl=CaCl +Ca(ClO) +2HO
2 2 2 2 2
(6)将装置②放于冷水浴中进行实验
【解析】(1)装置A中连接橡皮管,可使分液漏斗与圆底烧瓶压强相等,有利于有利于分液漏斗中的浓盐酸
顺利流下;
(2)装置A中利用浓盐酸和MnO 混合加热制氯气,发生反应的离子方程式为:MnO +4H++2Cl- Mn2+
2 2
+Cl↑+2HO;无水硫酸铜遇到水发生反应生成蓝色硫酸铜晶体,因此装置B的目的是检验水的存在,装
2 2
置内盛放的试剂是:无水硫酸铜;
(3)干燥的氯气没有漂白性,D中有色布条不褪色,氯气与水反应生成的HClO具有漂白性,E中湿润的有
色布条褪色;
(4)氯气易溶于有机溶剂四氯化碳,而氯化氢不溶,因此装置F的作用为吸收Cl,G的作用为检验HCl,为
2
避免氯气与水反应生成的盐酸,对氯化氢气体的检验带来的影响,应该在F、G两个装置之间再加一个装
有湿润的淀粉KI试纸的装置,可用于检验Cl 是否被除尽;
2
(5)装置②中发生Cl 与Ca(OH) 制Ca(ClO) 的反应,方程式为:2Ca(OH) +2Cl═CaCl +Ca(ClO) +2H O;
2 2 2 2 2 2 2 2
(6)制漂白粉的反应是放热反应,反应温度较高时有副反应发生,为了减少副反应发生,可将装置②放于冷
水浴中降低温度来达到目的。
6.(2020·湖北荆州· 高一期末)某学生设计如下图所示的实验装置,利用氯气与潮湿的消石灰反
应制取少量漂白粉(这是一个放热反应),回答下列问题:(1)在A装置中用固体二氧化锰与浓盐酸,在加热条件下制取氯气,写出反应的化学方程式____;
(2)C装置的作用是____。
(3)此实验所得漂白粉的有效成分偏低,该学生经分析并查阅资料发现,主要原因是在U形管中还存在
两个副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO ),为避免此副反应的发生,可采取的措施是____。
3 2
②另一个副反应是2HCl+Ca(OH)=CaCl +2HO,为避免此副反应的发生,可将装置如何改进____。
2 2 2
【答案】(1)MnO +4HCl(浓) MnCl +Cl↑+2H O
2 2 2 2
(2) 吸收未反应的Cl,防止污染空气
2
(3) ①将B装置冷却(或将B装置放入冷水液中)
②A、B之间接一个盛饱和NaCl溶液的洗气瓶
【解析】(1)A装置中用固体二氧化锰与浓盐酸,在加热条件下制取氯气,反应的化学方程式为:
MnO +4HCl(浓) MnCl +Cl↑+2H O,故答案为:MnO +4HCl(浓) MnCl +Cl↑+2H O;
2 2 2 2 2 2 2 2
(2)氯气是有毒气体,要进行尾气处理,则装置C中的氢氧化钠溶液用于吸收未反应完的氯气,防止污染空
气,故答案为:吸收未反应完的氯气,防止污染空气;
(3)①温度较高时发生副反应生成Ca(ClO ),为避免此副反应的发生,则可将B装置冷却来避免该副反应的
3 2
发生,故答案为:将B装置冷却(或将B装置放在冷水浴中);
②因浓盐酸易挥发,则另一个副反应为HCl与消石灰反应,2HCl+Ca(OH) =CaCl +2HO,所以应除去氯
2 2 2
气中的HCl,可以在A、B之间接一个盛有饱和的NaCl溶液的洗气瓶,除去HCl,故答案为:在A、B之
间接一个饱和的NaCl溶液的洗气瓶。
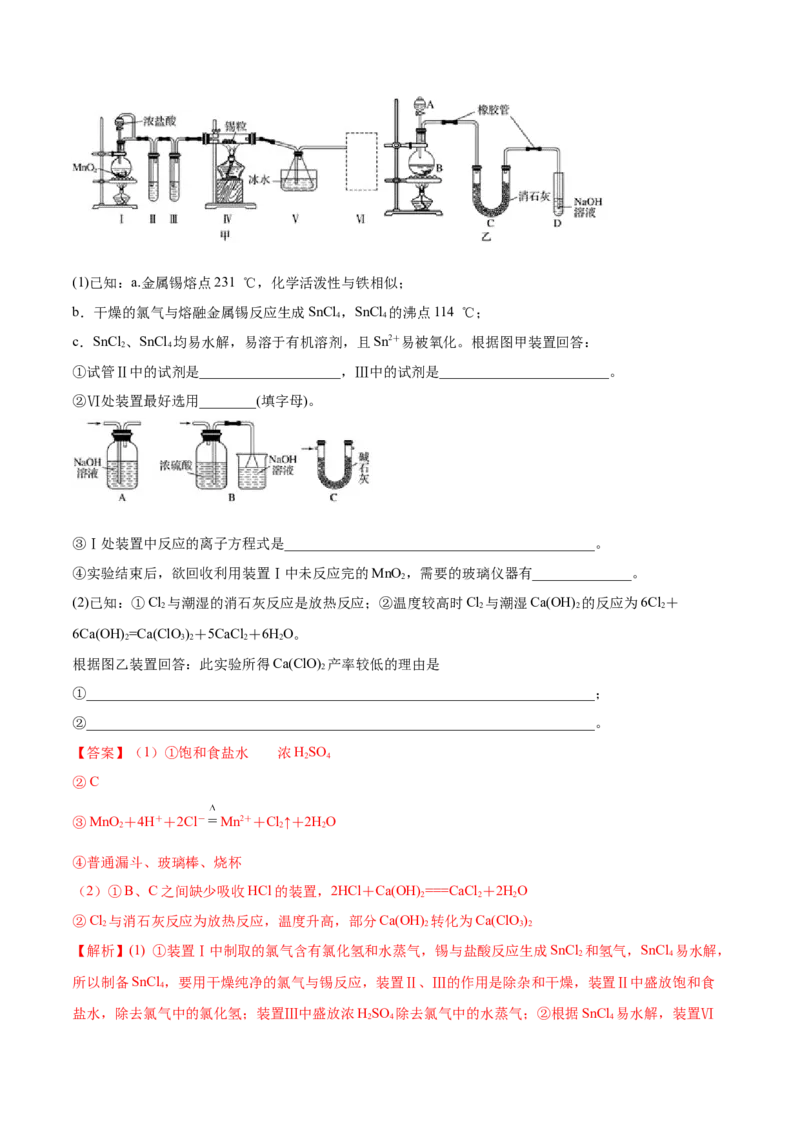
7.(2020·贵州省晴隆县第二中学高一期末)甲、乙实验小组设计如下实验装置分别制备SnCl 和漂白粉。
4(1)已知:a.金属锡熔点231 ℃,化学活泼性与铁相似;
b.干燥的氯气与熔融金属锡反应生成SnCl ,SnCl 的沸点114 ℃;
4 4
c.SnCl 、SnCl 均易水解,易溶于有机溶剂,且Sn2+易被氧化。根据图甲装置回答:
2 4
①试管Ⅱ中的试剂是____________________,Ⅲ中的试剂是________________________。
②Ⅵ处装置最好选用________(填字母)。
③Ⅰ处装置中反应的离子方程式是____________________________________________。
④实验结束后,欲回收利用装置Ⅰ中未反应完的MnO ,需要的玻璃仪器有______________。
2
(2)已知:①Cl 与潮湿的消石灰反应是放热反应;②温度较高时Cl 与潮湿Ca(OH) 的反应为6Cl+
2 2 2 2
6Ca(OH) =Ca(ClO)+5CaCl +6HO。
2 3 2 2 2
根据图乙装置回答:此实验所得Ca(ClO) 产率较低的理由是
2
①________________________________________________________________________;
②________________________________________________________________________。
【答案】(1)①饱和食盐水 浓HSO
2 4
②C
③MnO +4H++2Cl- Mn2++Cl↑+2HO
2 2 2
④普通漏斗、玻璃棒、烧杯
(2)①B、C之间缺少吸收HCl的装置,2HCl+Ca(OH) ===CaCl +2HO
2 2 2
②Cl 与消石灰反应为放热反应,温度升高,部分Ca(OH) 转化为Ca(ClO )
2 2 3 2
【解析】(1) ①装置Ⅰ中制取的氯气含有氯化氢和水蒸气,锡与盐酸反应生成SnCl 和氢气,SnCl 易水解,
2 4
所以制备SnCl ,要用干燥纯净的氯气与锡反应,装置Ⅱ、Ⅲ的作用是除杂和干燥,装置Ⅱ中盛放饱和食
4
盐水,除去氯气中的氯化氢;装置Ⅲ中盛放浓HSO 除去氯气中的水蒸气;②根据SnCl 易水解,装置Ⅵ
2 4 4处连接的装置应具有干燥和吸收氯气的作用,故选C。③Ⅰ处装置中二氧化锰与浓盐酸加热生成氯化锰、
氯气、水,反应的离子方程式是MnO +4H++2Cl- Mn2++Cl↑+2HO;④MnO 难溶于水,实验结束后,
2 2 2 2
用过滤法回收装置Ⅰ中未反应完的MnO ,需要的玻璃仪器是普通漏斗、玻璃棒、烧杯;(2) 氯气中含有杂
2
质氯化氢,B、C之间缺少吸收HCl的装置,2HCl+Ca(OH) ===CaCl +2HO ; Cl 与消石灰反应为放热
2 2 2 2
反应,温度升高,Cl 与潮湿Ca(OH) 的反应为6Cl+6Ca(OH) =Ca(ClO)+5CaCl +6HO,部分Ca(OH)
2 2 2 2 3 2 2 2 2
转化为Ca(ClO )。
3 2
8.(2020·北京朝阳·高一期末)用Cl 和Ca(OH) 制备少量漂粉精(一种含氯消毒剂)的装置如下。
2 2
(1)A为氯气发生装置。A中反应方程式是________。
(2)B的作用是吸收挥发出的HCl。HCl可能对制备漂粉精造成的影响是________。
(3)用Cl 和Ca(OH) 制备的漂粉精,其有效成分是_________。
2 2
(4)漂粉精常用于游泳池的消毒,起消毒作用的是HClO。漂粉精在水中释放HClO的途径如下:
途径一:Ca(ClO) + 2H O Ca(OH) + 2HClO
2 2 2
途径二:Ca(ClO)
2
+ H
2
O + ⇌CO
2
=________+ _______(把反应补充完整)
(5)池水的酸碱性对漂粉精的消毒效果影响明显。
①池水碱性过强,杀毒作用会________(填“增强”或“减弱”)。
②池水酸性过强,会刺激眼睛和皮肤。通常加入NaCO、NaHCO 以降低酸性,起到降低酸性作用的离子
2 3 3
分别是________(填离子符号)。
(6)某届奥运会期间,发生了室外游泳池水变绿的事件,成为当时的一大新闻。有关负
责人说,池水变绿是藻类生长造成的。该游泳池每隔一段时间就要投放含氯消毒剂,当再次投放时,误投
了过氧化氢(HO)消毒剂。消毒剂为什么不起作用了?_______。
2 2【答案】(1)MnO +4HCl(浓) MnCl +Cl↑+2HO
2 2 2 2
(2)HCl能与Ca(OH) 发生反应生成CaCl 和HO,使Ca(ClO) 浓度降低
2 2 2 2
(3) Ca(ClO)
2
(4) HClO CaCO
3
(5) 减弱 CO2-、HCO -
3 3
(6) HClO具有强氧化性,能将HO 氧化,HClO+HO=HCl+O↑+HO
2 2 2 2 2 2
【解析】(1)装置A为氯气发生装置,其中反应方程式为MnO +4HCl(浓) MnCl +Cl↑+2HO;
2 2 2 2
答案:MnO +4HCl(浓) MnCl +Cl↑+2HO;
2 2 2 2
(2)制取漂粉精的有效成分是Ca(ClO) ,HCl能与Ca(OH) 发生反应生成CaCl 和HO,使Ca(ClO) 浓度降低;
2 2 2 2 2
答案:HCl能与Ca(OH) 发生反应生成CaCl 和HO,使Ca(ClO) 浓度降低;
2 2 2 2
(3)Cl 与Ca(OH) 发生2Cl+2Ca(OH) =CaCl +Ca(ClO) +2HO,其有效成分是Ca(ClO) ;
2 2 2 2 2 2 2 2
答案:Ca(ClO) ;
2
(4)利用碳酸的酸性强于次氯酸,即途径二:Ca(ClO) +CO+HO=HClO+CaCO ;
2 2 2 3
答案:HClO、CaCO ;
3
(5)①ClO-在酸性条件下生成HClO,HClO具有强氧化性,即ClO-在碱性过强时,ClO-氧化性减弱,消
毒作用减弱;
答案:减弱;
②酸性过强,说明溶液中有大量的H+,CO2-、HCO -能与H+反应生成CO 和HO,降低c(H+);
3 3 2 2
答案:CO2-、HCO -;
3 3
(6)根据题意,再次投放时,误投过氧化氢,HClO具有强氧化性,能将HO 氧化,即发生反应的是HClO
2 2
+HO=HCl+O↑+HO,造成藻类生长;
2 2 2 2
答案:HClO具有强氧化性,能将HO 氧化,HClO+HO=HCl+O↑+HO。
2 2 2 2 2 2
9.(2020·全国高一单元测试)含氯消毒剂是指溶于水产生具有杀死微生物活性的次氯酸的消毒剂,无机
含氯消毒剂包括液氯、次氯酸钠、次氯酸钙等。
(1)下列叙述正确的是____________(填字母)。
A.液氯和新制氯水都是游离态氯,都能作杀菌消毒剂
B.因为Cl 能与水反应,所以自来水中不存在游离态氯
2
C.溶液中H+的浓度越大,次氯酸钠的消毒效果越好
D.含氯消毒剂应密封保存
(2)漂白粉是一种优良高效、价格低廉的常用杀菌消毒剂。实验室中有一瓶密封不严的漂白粉,其中肯定存
在CaCl ,设计实验,探究该漂白粉中可能存在的其他物质。
2[提出合理假设]
假设1:该漂白粉未变质,只含有__________;
假设2:该漂白粉全部变质,只含有__________;
假设3:该漂白粉部分变质,既含有Ca(ClO) 又含有CaCO 。
2 3
[设计实验方案]
限选用的仪器和药品:试管、胶头滴管、带导管的单孔塞、蒸馏水、自来水、1 mol·L-1稀盐酸、品红溶液、
新制澄清石灰水(提示:不必检验Ca2+和Cl-,表格可以不填满)。
实验步骤 预期现象和结论
取少量上述漂白粉与试管中,
① _________________________。
_________________________。
② _________________________。 _________________________。
【答案】(1)CD
(2)Ca(ClO) CaCO
2 3
加入适量1mol/L稀盐酸,将产生的气体通入到新制备的澄清石灰水中
若新制备的澄清石灰水变浑浊,则该漂白粉中不含CaCO ,若新制备的澄清石灰水不变浑浊,则该漂白粉
3
中含CaCO
3
向步骤①反应后的试管中滴加1~2滴品红溶液,震荡
若品红溶液褪色,则该漂白粉中含有Ca(ClO) ,若品红溶液不褪色,则该漂白粉中不含有Ca(ClO)
2 2
【解析】(1)A.液氯是游离态氯,新制氯水是混合物,故A错误;
B.Cl 能与水反应,该反应并不能完全进行到底,溶液中还存在部分Cl,故B错误;
2 2
C.根据题给信息,含氯消毒剂是因为含有HClO而具有杀菌作用,HClO是弱酸,NaClO溶于水电离出
ClO-,ClO-与H+结合生成HClO,所以溶液中H+的浓度越大,ClO-与H+结合生成的HClO的浓度也越
大,其消毒效果越好,故C正确;
D.HClO易分解,所以含氯消毒剂需密封保存,故D正确;
(2) 合理假设:漂白粉的主要成分是CaCl 、Ca(ClO) ,除CaCl 外,如果漂白粉没有变质,则一定含有
2 2 2
Ca(Cl0) ,由于在空气中发生:Ca(Cl0) +CO +H O=CaCO +2HClO,如漂白粉全部变质,则含有CaCO ,如
2 2 2 2 3 3
漂白粉部分变质,则既含有Ca(ClO) 又含有CaCO ;
2 3
设计实验方案:
取少量上述漂白粉于试管中,加入适量1mol/L盐酸溶解后,再将产生的气体导入到足量的澄清石灰水中,
①若澄清石灰水未见浑浊,则假设1成立;
②若澄清石灰水变浑浊,则假设2或3成立;向步骤①反应后的试管滴入1~2滴品红溶液,振荡,若品红褪色,固体中存在 Ca(ClO) ;若品红不褪色,则固体中不存在 Ca(ClO) 。
2 2
【题组三 氯离子的检验】
1.(2020·全国高一课时练习)已知两瓶气体,分别是HCl和Cl。可以区别它们的方法或试剂是
2
①观察颜色 ②打开瓶盖看有无白雾 ③湿润的淀粉试纸
④湿润的红色石蕊试纸 ⑤湿润的蓝色石蕊试纸 ⑥硝酸银溶液
A.①②③④ B.①②⑤⑥ C.①②④⑤ D.①②④⑥
【答案】C
【解析】①Cl 为黄绿色气体,而氯化氢无色,可以通过观察气体颜色鉴别二者,故①正确;
2
②氯化氢极易溶于水,打开瓶盖后有白雾,而Cl 不具有此性质,据此可鉴别二者,故②正确;
2
③HCl和Cl 都不与淀粉反应,无法用湿润的淀粉试纸检验,故③错误;
2
④HCl不能使红色石蕊试纸变色,而Cl 能够使湿润的红色石蕊试纸褪色,可以据此鉴别二者,故⑤正确;
2
⑤湿润的蓝色石蕊试纸遇Cl 先变红后褪色,湿润的蓝色石蕊试纸遇HCl只变红,故可以用湿润的蓝色石
2
蕊试纸来区别Cl 和HCl,故⑤正确;
2
⑥HCl和Cl 都能够与硝酸银溶液反应生成氯化银沉淀,无法用硝酸银溶液鉴别二者,故⑥错误;
2
故答案为C。
2.(2020·全国课时练习)现有久置氯水、氯化钠溶液、氢氧化钠溶液和新制氯水,可用来鉴别它们的试
剂是( )
A.AgNO 溶液 B.酚酞溶液 C.紫色石蕊溶液 D.饱和食盐水
3
【答案】C
【解析】A.久置氯水的溶质为HCl,AgNO 溶液与久置氯水、氯化钠溶液、新制氯水反应均生成白色沉
3
淀,无法鉴别,A不合题意;
A.酚酞溶液只能鉴别出氢氧化钠溶液,B不合题意;
A.紫色石蕊溶液遇久置氯水显红色,遇氯化钠溶液不变色,遇氢氧化钠溶液显蓝色,遇新制氯水先变红
后褪色,故可以鉴别题给四种溶液,C符合题意;
A.饱和食盐水与题给四种溶液均无明显现象,无法鉴别,D不合题意;
故选C。
3.(2020·大庆市第十中学高三开学考试)氯仿可作为麻醉剂,但在光照下容易被氧化成剧毒的光气:
2CHCl +O =2COCl +2HCl。为防止事故发生,使用前要检验其是否变质,你认为检验使用的最佳试剂是(
3 2 2
)
A.溴水 B.烧碱溶液
C.硝酸银溶液 D.淀粉碘化钾试纸【答案】C
【解析】A.溴水与氯化氢不反应,不能用来检验,选项A错误;
B.加入NaOH溶液,没有明显的现象,不能用来检验,选项B错误;
C.氯仿被氧化时生成HCl,加入硝酸酸化的硝酸银溶液生成AgCl白色沉淀,可检验,选项C正确;
D.淀粉KI试剂与氯化氢不反应,不能用来检验,选项D错误;
答案选C。
4.(2019·全国高一课时练习)现有盐酸、NaCl溶液、NaOH溶液和新制氯水,可用来区别它们的一种试
剂是( )
A.AgNO 溶液 B.酚酞溶液
3
C.紫色石蕊溶液 D.饱和食盐水
【答案】C
【解析】A.盐酸、氯化钠、氢氧化钠和氯水四种溶液与AgNO 溶液混合,均生成白色沉淀,不能鉴别,
3
故A错误;
B.盐酸、氯化钠、和氯水遇酚酞均为无色,不能鉴别,故B错误;
C.盐酸、氯化钠、氢氧化钠和氯水四种溶液与紫色石蕊混合的现象分别为:显红色、显紫色、显蓝色,
先变红后褪色,现象不同,能鉴别,故C正确;
D.盐酸、氯化钠、氢氧化钠和氯水四种溶液与饱和食盐水均不反应,现象相同,不能鉴别,故D错误;
故答案为C。