文档内容
单元素养评价(七)(第七章)
(90分钟 100分)
【合格性考试】(60分钟 70分)
一、选择题(本题包括12小题,每小题2分,共24分)
1.书法离不开文房四宝(笔、墨、纸、砚),制作笔用的狼毫、研墨用的墨条、宣纸
(即白纸)和制作砚台用的砚石的主要成分依次是 ( )
A.多糖、石墨、蛋白质、无机盐
B.塑料、石墨、多糖、无机盐
C.蛋白质、炭黑、多糖、无机盐
D.蛋白质、煤炭、多糖、有机玻璃
【解析】选C。狼毫为动物的毛,属于蛋白质;墨条由炭黑制成;宣纸的主要成分为
纤维素,属于多糖;砚石的主要成分为无机盐。
2.下列各组物质中不符合“物理性质不同,化学性质相似”的是
( )
A.互为同位素的14C、12C
B.互为同系物的丁烷和庚烷
C.互为同素异形体的金刚石和石墨D.互为同分异构体的丙烯和环丙烷
【解析】选D。A项,同位素原子因为核外电子排布相同,所以物理性质不同,化学
性质相似;同系物结构相似,化学性质相似,但物理性质不同;金刚石和石墨物理
性质不同,但组成均为C,故化学性质相似;D项,丙烯和环丙烷不是同类物质,化
学性质不相同。
3.“化学是五颜六色的”是指在化学实验中有着丰富多彩的颜色变化。下列有
关反应获得的颜色不正确的是 ( )
①红 ②橙 ③黄 ④绿 ⑤青 ⑥蓝 ⑦紫
A.乙烯气体通入酸性高锰酸钾溶液中:⑦
B.淀粉遇碘:⑥
C.蛋白质遇浓硝酸:③
D.热的氧化铜遇酒精:①
【解析】选A。乙烯通入酸性高锰酸钾溶液中发生氧化反应,溶液紫红色褪去,A项
错误。
4.下列营养物质在人体内发生的变化及其对人的生命活动所起的作用叙述不正
确的是 ( )
A.淀粉 葡萄糖 CO 和H O(释放能量维持生命活动)
2 2B.纤维素 葡萄糖 CO 和H O(释放能量维持生命活动)
2 2
C.油脂 甘油和高级脂肪酸 CO 和H O(释放能量维持生命活动)
2 2
D.蛋白质 氨基酸 人体所需的蛋白质(人体生长发育)
【解析】选B。人体中没有水解纤维素的酶,纤维素在人体内不消化。
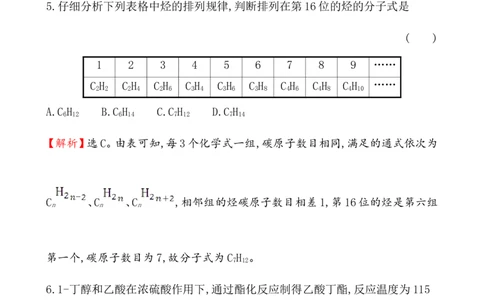
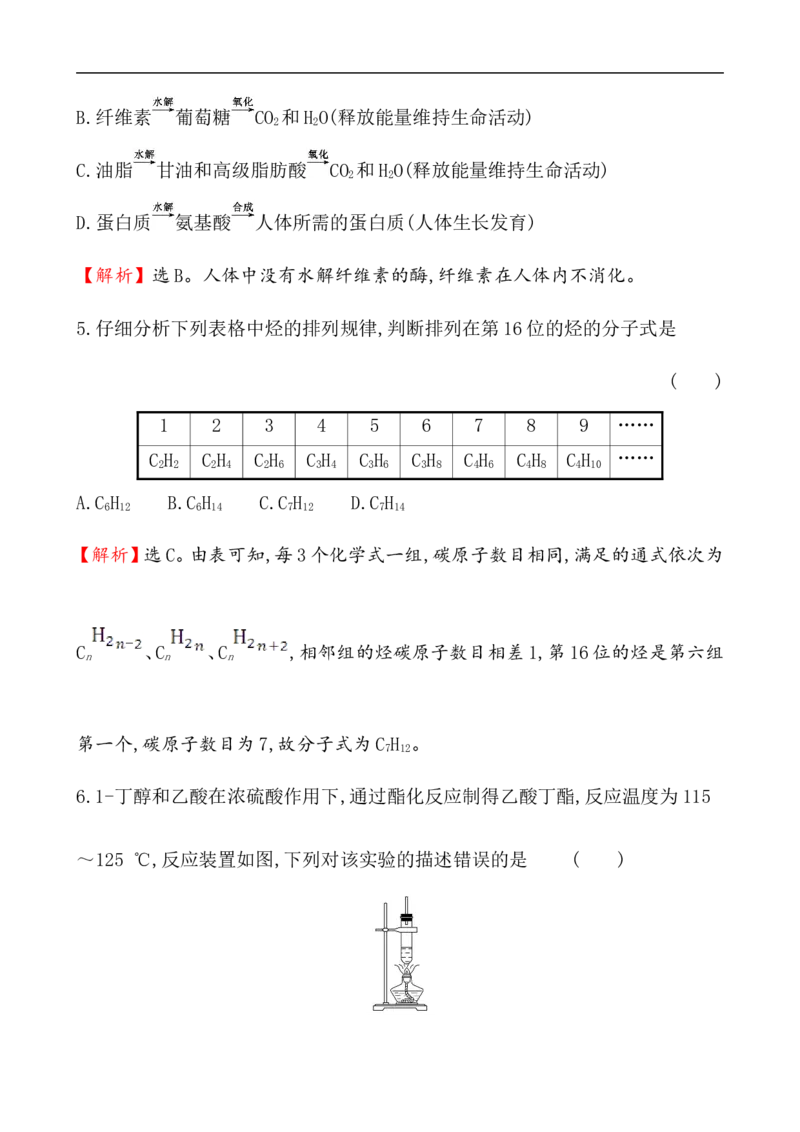
5.仔细分析下列表格中烃的排列规律,判断排列在第16位的烃的分子式是
( )
1 2 3 4 5 6 7 8 9 ……
C H C H C H C H C H C H C H C H C H ……
2 2 2 4 2 6 3 4 3 6 3 8 4 6 4 8 4 10
A.C H B.C H C.C H D.C H
6 12 6 14 7 12 7 14
【解析】选C。由表可知,每3个化学式一组,碳原子数目相同,满足的通式依次为
C 、C 、C ,相邻组的烃碳原子数目相差1,第16位的烃是第六组
n n n
第一个,碳原子数目为7,故分子式为C H 。
7 12
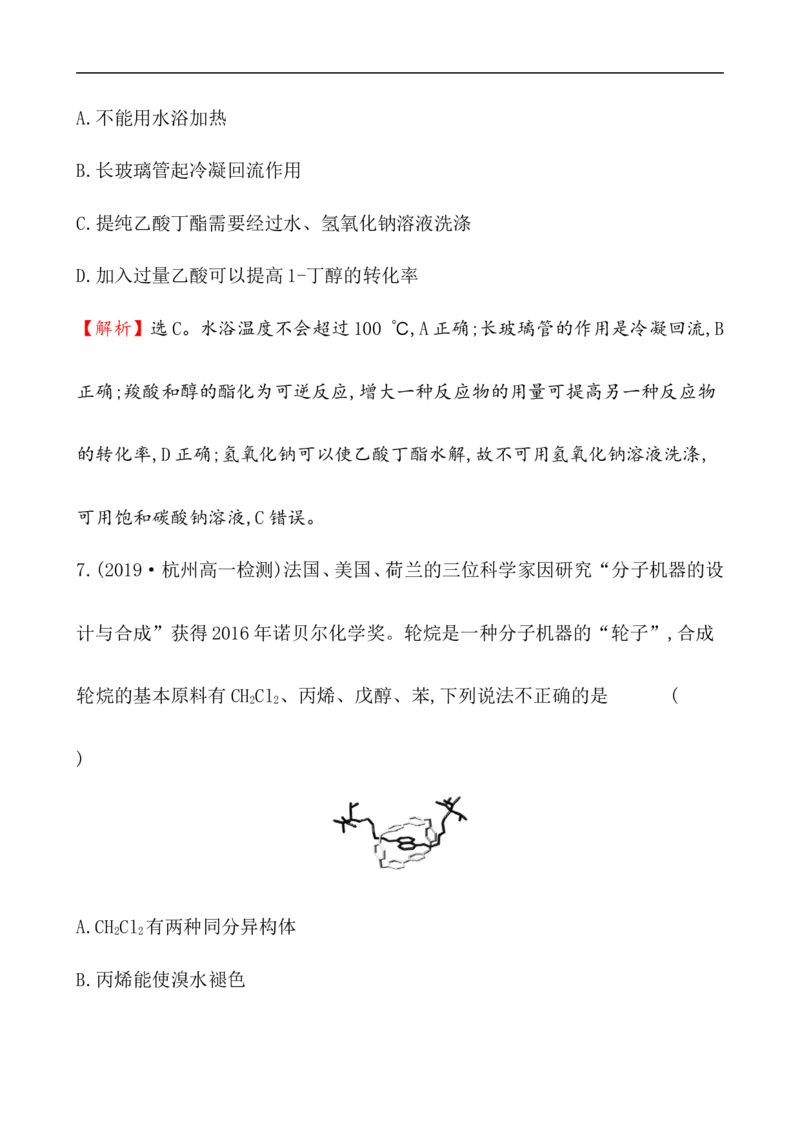
6.1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115
~125 ℃,反应装置如图,下列对该实验的描述错误的是 ( )A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、氢氧化钠溶液洗涤
D.加入过量乙酸可以提高1-丁醇的转化率
【解析】选C。水浴温度不会超过100 ℃,A正确;长玻璃管的作用是冷凝回流,B
正确;羧酸和醇的酯化为可逆反应,增大一种反应物的用量可提高另一种反应物
的转化率,D正确;氢氧化钠可以使乙酸丁酯水解,故不可用氢氧化钠溶液洗涤,
可用饱和碳酸钠溶液,C错误。
7.(2019·杭州高一检测)法国、美国、荷兰的三位科学家因研究“分子机器的设
计与合成”获得2016年诺贝尔化学奖。轮烷是一种分子机器的“轮子”,合成
轮烷的基本原料有CH Cl 、丙烯、戊醇、苯,下列说法不正确的是 (
2 2
)
A.CH Cl 有两种同分异构体
2 2
B.丙烯能使溴水褪色C.戊醇与乙醇都含有羟基
D.戊醇与金属钠反应会生成氢气
【解析】选A。CH 是正四面体结构,CH Cl 没有同分异构体,故A错误;丙烯含有碳
4 2 2
碳双键,能使溴水褪色发生加成反应,故B正确;戊醇与乙醇都含有羟基,故C正
确;戊醇中含有羟基,能与金属钠反应生成氢气,故D正确。
8.用括号中的试剂和方法除去各物质中的杂质,正确的是 ( )
A.甲烷中的乙烯(酸性高锰酸钾溶液,洗气)
B.乙醇中的乙酸(NaOH溶液,分液)
C.乙醇中的水(CaO,蒸馏)
D.乙酸乙酯中的乙酸(加入浓硫酸和过量乙醇并加热)
【解析】选C。乙烯可被氧化为二氧化碳,会引入新杂质,A错误;乙酸与氢氧化钠
反应生成乙酸钠,溶于水,乙醇与之不分层,B错误;乙酸与乙醇的酯化反应是可
逆反应,即使乙醇过量,也不能将乙酸除尽,且引入新杂质,D错误。
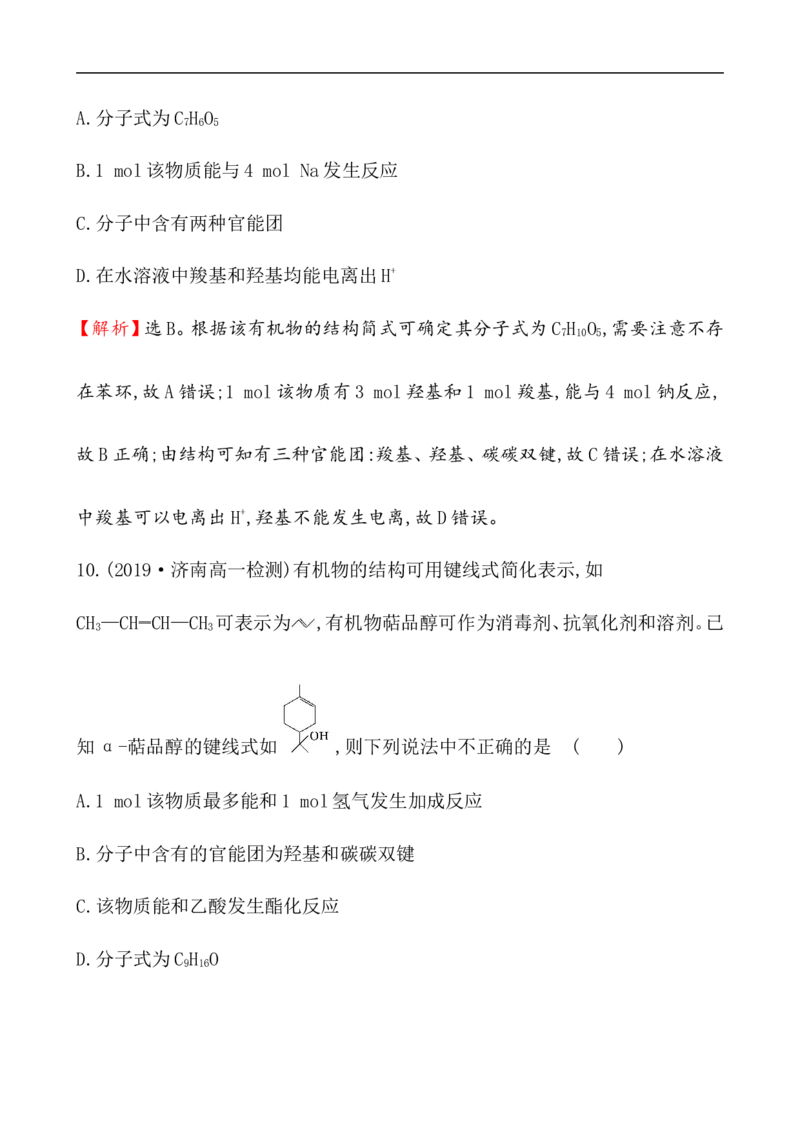
9.(2019成都高一检测)某有机物的结构简式如图,下列关于该有机物的说法正
确的是 ( )A.分子式为C H O
7 6 5
B.1 mol该物质能与4 mol Na发生反应
C.分子中含有两种官能团
D.在水溶液中羧基和羟基均能电离出H+
【解析】选B。根据该有机物的结构简式可确定其分子式为C H O ,需要注意不存
7 10 5
在苯环,故A错误;1 mol该物质有3 mol羟基和1 mol羧基,能与4 mol钠反应,
故B正确;由结构可知有三种官能团:羧基、羟基、碳碳双键,故C错误;在水溶液
中羧基可以电离出H+,羟基不能发生电离,故D错误。
10.(2019·济南高一检测)有机物的结构可用键线式简化表示,如
CH —CH CH—CH 可表示为 ,有机物萜品醇可作为消毒剂、抗氧化剂和溶剂。已
3 3
知α-萜品醇的键线式如 ,则下列说法中不正确的是 ( )
A.1 mol该物质最多能和1 mol氢气发生加成反应
B.分子中含有的官能团为羟基和碳碳双键
C.该物质能和乙酸发生酯化反应
D.分子式为C H O
9 16【解析】选D。含有1个碳碳双键,则1 mol该物质最多能和1 mol氢气发生加成
反应,故A正确;由结构简式可知分子中含有的官能团为羟基和碳碳双键,故B正
确;含有羟基,则可与乙酸发生酯化反应,故C正确;由结构简式可知分子式为
C H O,故D错误。
10 18
11.下列实验操作及结论正确的是 ( )
A.钠和乙醇反应的现象与钠和水反应的现象相同
B.在淀粉溶液中加入20%的稀硫酸,水解后,立即加入新制Cu(OH) 悬浊液共热,
2
证明有葡萄糖生成
C.在CuSO 溶液中加入过量NaOH溶液振荡,立即加入麦芽糖溶液并加热,能证明
4
麦芽糖具有还原性
D.在乙醇溶液中插入一根红热的铜丝,能证明醇氧化成醛
【解析】选C。钠与乙醇反应比与水反应缓和且钠沉在乙醇下面;在淀粉水解后应
先加NaOH溶液中和硫酸,然后再加入新制Cu(OH) 悬浊液共热;在乙醇溶液中反
2
复插入红热的铜丝多次后,才能闻到乙醛的气味。
12.鉴别淀粉、蛋白质、葡萄糖水溶液,依次可分别使用的试剂和对应的现象正确
的是 ( )A.碘水,变蓝色;浓硝酸,变黄色;新制Cu(OH) 悬浊液,砖红色沉淀
2
B.浓硝酸,变黄色;新制Cu(OH) 悬浊液,砖红色沉淀;碘水,变蓝色
2
C.新制Cu(OH) 悬浊液,砖红色沉淀;碘水,变蓝色;浓硝酸,变黄色
2
D.碘水,变蓝色;新制Cu(OH) 悬浊液,砖红色沉淀;浓硝酸,变黄色
2
【解析】选A。淀粉遇碘水变蓝色;蛋白质遇浓硝酸发生颜色反应,产生黄色沉淀;
葡萄糖与新制Cu(OH) 悬浊液混合加热至沸腾产生砖红色沉淀。
2
二、非选择题(本题包括4小题,共46分)
13.(12分)已知:A是石油裂解气的主要产物之一,其产量是衡量一个国家石油化
工发展水平的标志。下列是有机物A~G之间的转化关系:
请回答下列问题:
(1)A、D中所含官能团的名称分别是____________________;
C的结构简式是____________________。
(2)E是一种具有香味的液体,由B + D→E的反应方程式为________________,
反应类型是____________________。(3)G是一种高分子化合物,其结构简式是 ____________________。
(4)2018年俄罗斯足球世界杯,在比赛中当运动员肌肉扭伤时,队医立即对其受
伤部位喷射物质F进行应急处理。写出由A制F的化学反应方程式: _______
____________________。
(5)H是E的同分异构体,且H能与NaHCO 反应,则H的结构简式可能为(写出2
3
种): ____________________。
【解析】根据A是石油裂解气的主要产物之一,其产量是衡量一个国家石油化工
发展水平的标志,可以确定A 为乙烯。按照题目中转化关系可推知B为乙醇,C为
乙醛,D为乙酸,E为乙酸乙酯,F为氯乙烷,G为聚乙烯。
答案:(1)碳碳双键、羧基 CH CHO
3
(2)CH COOH + CH CH OH
3 3 2
CH COOCH CH + H O
3 2 3 2
取代反应或酯化反应
(3)CH —CH
2 2
(4)CH CH + HCl CH CH Cl
2 2 3 2
(5)CH CH CH COOH、(CH ) CHCOOH
3 2 2 3 214.(12分)牛奶放置时间长了会变酸,这是因为牛奶中含有的乳糖在微生物的作
用下分解变成了乳酸。乳酸最初就是从酸牛奶中得到并由此而得名的。乳酸的结
构简式为CH CH(OH)COOH。完成下列问题:
3
(1)写出乳酸与足量金属钠反应的化学方程式: ____________________。
(2)乳酸发生下列变化:
,所用的试剂a________,b________(写化学式);写出乳酸与少量
碳酸钠溶液反应的化学方程式:__ ____________________。
(3)写出下列反应的化学方程式,并注明反应类型。
乳酸与乙醇反应: ____________________, ____________________。
(4)乳酸在浓硫酸作用下,两分子相互反应生成六元环状结构的物质,写出此生
成物的结构简式: ____________________。
【解析】(1)金属钠与羟基、羧基都能发生反应,生成氢气。
(2)在乳酸中先加入的物质只与羧基反应,不能与羟基发生反应,则加入的物质a
可以是NaOH、NaHCO 或Na CO ,反应产生的 中的醇羟基再发生反应,
3 2 3
则加入的物质是金属Na;羧酸的酸性比碳酸强,碳酸钠能与羧基反应,不能与醇
羟基反应。(3)乳酸含有羧基,可以与乙醇发生酯化反应生成酯和水。
答案:(1) +2Na
(2)NaHCO (或 NaOH或Na CO ) Na
3 2 3
H O+CO ↑+
2 2
(3) C H OH H O+ 酯化反应(或取代反应)
2 5 2
(4)
15.(10分)(2019·济南高一检测)石油是工业的血液,与我们的生产、生活息息
相关,乙烯的产量通常用来衡量一个国家的石油化工水平。根据下面转化关系回
答下列问题:
(1)乙烯的结构简式为_____________。
(2)写出乙烯和水反应生成B的反应③的方程式(注明条件):
___________________________________, 反应类型为_____________。写出反应⑥的化学方程式(注明条件): ________________________。
(3)物质C的沸点为12.27 ℃,常用于局部冷冻麻醉应急处理。物质C可通过反
应④和反应⑥制得,其中最好的方法是反应________(填“④”或“⑥”),理由
为
___________________________________。
【解析】(1)乙烯为平面四边形结构,官能团为碳碳双键,结构简式为CH CH 。
2 2
(2)乙烯和水发生反应生成乙醇,化学方程式为CH CH +H O CH CH OH,该反
2 2 2 3 2
应为加成反应,反应⑥为乙烷与氯气在光照条件下发生取代反应生成氯乙烷,反
应方程式为CH CH +Cl CH CH Cl+HCl。
3 3 2 3 2
(3)氯乙烷可通过乙烯与氯化氢发生加成反应和乙烷与氯气发生取代反应制得,
最好的方法是加成反应④,因为乙烷与氯气反应将得到多种氯代物的混合物,产
物不纯。
答案:(1) CH CH
2 2
(2)CH CH +H O CH CH OH
2 2 2 3 2
加成反应CH CH +Cl CH CH Cl+HCl
3 3 2 3 2
(3)④ 乙烷与氯气反应将得到多种氯代物的混合物,产物不纯16.(12分)现有6瓶失去标签的液体,已知它们可能是乙醇、乙酸、苯、乙酸乙酯
油脂、葡萄糖中的一种。现通过如下实验来确定各试剂瓶中所装液体的名称
:
实验步骤和方法 实验现象
①把6瓶液体分别依次
标号A、B、C、D、E、F,然后 只有F没有气味
闻气味
②各取少量于试管中 ,
只有C、D、E不溶解而浮在水面上
加水稀释
③分别取少量6种液体
只有B使沉淀溶解,F中产生砖红
于试管中,加新制
色沉淀
Cu(OH) 并加热
2
④各取C、D、E少量于试
只有C仍有分层现象,且在D的试
管中,加稀NaOH溶液并
管中闻到特殊香味
加热
(1)写出这6种物质的名称。
A________,B________,C________,D________,
E________,F________。
(2)在D中加入NaOH溶液并加热的化学方程式为_____________。
(3)已知乙醛发生银镜反应的化学方程式为CH CHO+2Ag(NH ) OH CH COONH
3 3 2 3 4
+H O+2Ag↓+3NH ,试写出葡萄糖发生银镜反应的化学方程式___________
2 3
________________________。
【解析】(1)6种物质中只有葡萄糖无气味;苯、乙酸乙酯、油脂不溶于水且密度比
水的小;乙酸呈酸性,能与Cu(OH) 发生中和反应,葡萄糖具有还原性,能与新制
2
Cu(OH) 反应生成砖红色的Cu O沉淀。乙酸乙酯、油脂均在稀NaOH溶液中发生水
2 2解,而不再有分层现象,乙酸乙酯的水解产物之一乙醇有特殊香味,乙醇易溶于
水,苯不溶于水且密度比水的小,二者均不与Cu(OH) 和NaOH溶液反应。
2
(2)乙酸乙酯在NaOH溶液中加热生成乙酸钠和乙醇。(3)根据葡萄糖的结构简式
并结合信息,即可写出化学方程式。
答案: (1)乙醇 乙酸 苯
乙酸乙酯 油脂 葡萄糖
(2)CH COOCH CH +NaOH CH COONa+CH CH OH
3 2 3 3 3 2
(3)HOCH (CHOH) CHO+2Ag(NH ) OH HOCH (CHOH) COONH +H O+2Ag↓+3NH ↑
2 4 3 2 2 4 4 2 3
【等级性考试】(30分钟 30分)
一、选择题(本题包括4小题,每小题4分,共16分)
17.(2019·张掖高一检测)《天工开物》中记载丝织品的处理:“凡帛织就犹是生
丝,煮练方熟。练用稻稿灰入水煮。以猪胰脂陈宿一晚,入汤浣之,宝色烨然。”下
列有关说法不正确的是 ( )
A.生丝的主要成分为蛋白质
B.稻稿灰含有碳酸钾,其入水后溶液呈碱性C.该过程实际就是生丝的除杂过程
D.生丝煮练之后变为熟丝,熟丝的成分是氨基酸
【解析】选D。丝的主要成分是蛋白质,是一种高分子化合物,故A正确;稻稿灰中
含碳酸钾,是强碱弱酸盐,溶于水后溶液显碱性,故B正确;该过程讲述了由生丝
到熟丝的过程,实际是生丝的除杂过程,从而使得生丝变熟后光泽度变好,故C正
确;生丝煮练之后变为熟丝,由于氨基酸是溶于水的,故熟丝的成分不可能是氨
基酸,故D错误。
18.(2019·东城高一检测)下列说法正确的是 ( )
A.分子式为C H Cl的有机物,分子结构中含2个甲基的同分异构体有4种
5 11
B.CH COOH与C OH在浓硫酸作用下加热,反应生成的有机物的结构简式为
3 2
CH COOC H
3 2 5
C.三氯甲烷只有一种结构,不存在同分异构体,证明甲烷是正四面体构型
D.煎炸食物的花生油和牛油都是可皂化的饱和酯类
【解析】选A。分子式为C H Cl且分子结构中含有2个甲基的同分异构体有
5 11
CH CH CH CHClCH 、CH CH CHClCH CH 、CH CH(CH )CH CH Cl、CH ClCH(CH )CH CH ,共
3 2 2 3 3 2 2 3 3 3 2 2 2 3 2 3
4种,故A正确;根据酯化反应的原理可知,生成的有机物的结构简式为CH CO18OC H ,故B错误;如果甲烷是正方形结构,三氯甲烷也只有一种结构,故C
3 2 5
错误;花生油属于不饱和的酯类,故D错误。
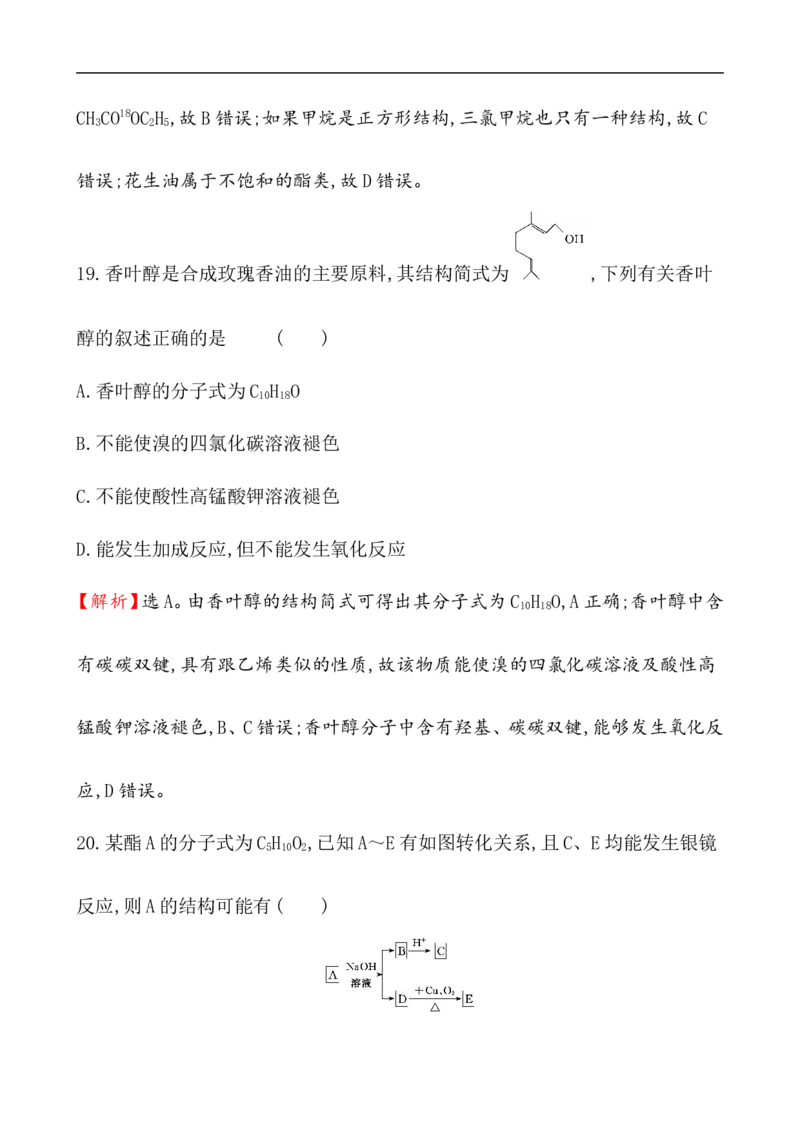
19.香叶醇是合成玫瑰香油的主要原料,其结构简式为 ,下列有关香叶
醇的叙述正确的是 ( )
A.香叶醇的分子式为C H O
10 18
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应,但不能发生氧化反应
【解析】选A。由香叶醇的结构简式可得出其分子式为C H O,A正确;香叶醇中含
10 18
有碳碳双键,具有跟乙烯类似的性质,故该物质能使溴的四氯化碳溶液及酸性高
锰酸钾溶液褪色,B、C错误;香叶醇分子中含有羟基、碳碳双键,能够发生氧化反
应,D错误。
20.某酯A的分子式为C H O ,已知A~E有如图转化关系,且C、E均能发生银镜
5 10 2
反应,则A的结构可能有( )A.2种 B.3种 C.4种 D.5种
【解析】选A。酯在NaOH催化作用下可水解生成羧酸盐和醇,由题给各物质的转化
关系可知B为盐,C为羧酸,D为醇,E为醛;因为C也能发生银镜反应,故C为甲酸
( ),则D为丁醇,因D可氧化为醛,故在D的结构中必含—CH OH原子团,
2
则D的结构简式可能为CH CH CH CH OH或 两种,因此A的结构也有
3 2 2 2
两种。
二、非选择题(本题包括1小题,共14分)
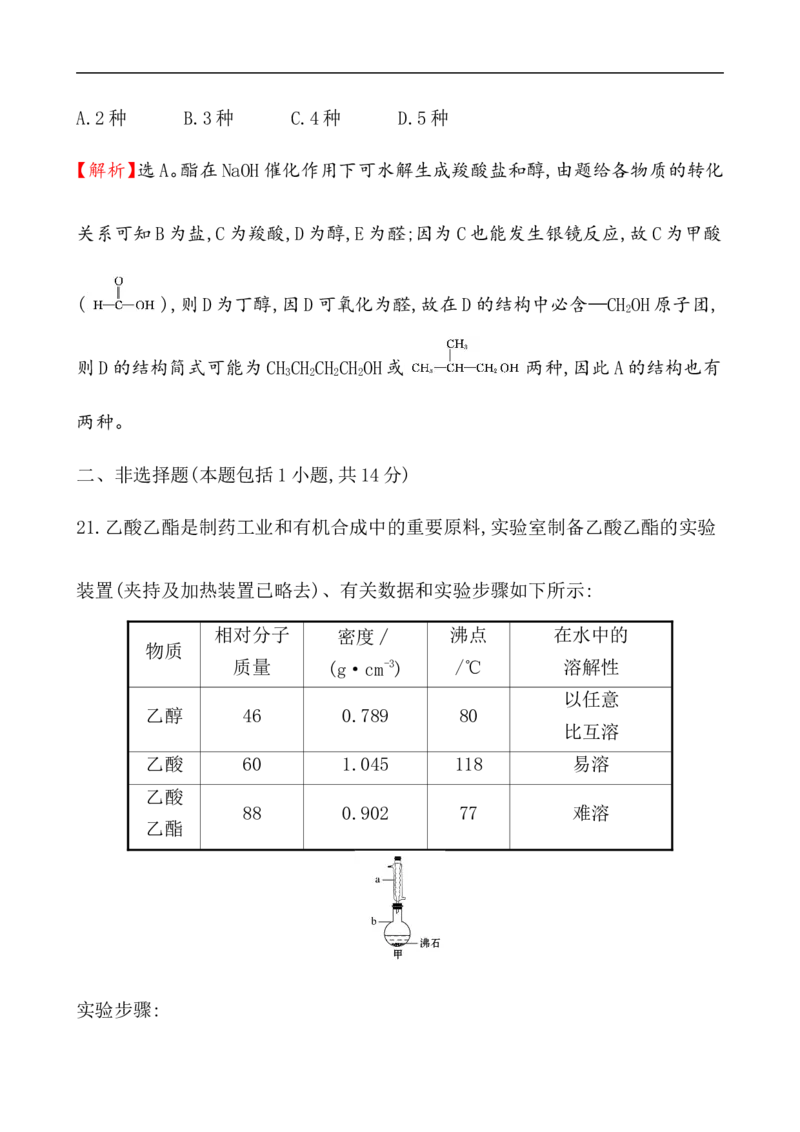
21.乙酸乙酯是制药工业和有机合成中的重要原料,实验室制备乙酸乙酯的实验
装置(夹持及加热装置已略去)、有关数据和实验步骤如下所示:
相对分子 密度∕ 沸点 在水中的
物质
质量 (g·cm-3) /℃ 溶解性
以任意
乙醇 46 0.789 80
比互溶
乙酸 60 1.045 118 易溶
乙酸
88 0.902 77 难溶
乙酯
实验步骤:①向仪器b中加入9.5 mL乙醇(过量)和6 mL乙酸,再缓慢加入2.5 mL浓硫酸,
混合均匀后,加入沸石,然后装上冷凝管(如图甲所示)。
②小火加热仪器b,缓慢回流0.5 h,待瓶内反应物冷却后,将回流装置改成蒸馏
装置,加热蒸出乙酸乙酯。
③向馏出液中缓慢加入5 mL饱和碳酸钠溶液,振荡,直至不再有二氧化碳气体产
生,然后将混合液转移至分液漏斗中,分去水层,将有机层依次用5 mL饱和食盐
水和5 mL饱和氯化钙溶液洗涤后,转移至锥形瓶中,加入少量无水硫酸镁固体,
静置片刻,过滤除去硫酸镁固体,然后将有机层进行蒸馏纯化,收集76~78℃时
的馏分,得到4.2 g乙酸乙酯。
请回答下列问题:
(1)实验原理:乙酸与乙醇在催化剂存在的条件下加热可以发生酯化反应生成乙
酸乙酯,请用氧同位素示踪法写出CH CO18OH与CH CH OH发生酯化反应的化学方
3 3 2
程式 _________________。
(2)仪器a的名称为_________________,
仪器b的规格为__________(填字母)。
A.25 mL B.50 mLC.250 mL D.500 mL
(3)步骤③中,将馏出液经饱和碳酸钠溶液处理后的混合液置于分液漏斗中,振
荡后静置,水层在 _______________ (填“上层”或“下层”)。
(4)在步骤③中,加入少量无水硫酸镁固体的作用是_________________。
(5)酯层厚度的标定:加热回流一段时间后再蒸出产物,为了更好地测定有机层
厚度,可预先向饱和碳酸钠溶液中加入1滴________试液,现象是__ _____
______________________。
(6)该实验中乙酸乙酯的产率为________(计算结果精确到0.1%)。
【解析】(1)乙酸与乙醇在催化剂存在的条件下加热发生酯化反应时,酸脱“羟
基”、醇脱“氢”,反应方程式是CH CO18OH + CH CH OH CH COOCH CH +
3 3 2 3 2 3
O
(2)根据仪器a的结构图可知,a是球形冷凝管;烧瓶b中液体的体积是18 mL,烧
瓶中液体的体积不能超过容积的 ,所以烧瓶的规格为50 mL,选B。
(3)乙酸乙酯的密度比水小,将馏出液经饱和碳酸钠溶液处理后的混合液置于分
液漏斗中,振荡后静置,水层在下层。(4)无水硫酸镁可以吸收酯表面少量的水分,所以在步骤③中,加入少量无水硫
酸镁固体的作用是干燥除水。
(5)碳酸钠能水解,碳酸钠溶液显碱性,为了更好地测定有机层厚度,可预先向饱
和碳酸钠溶液中加入1滴酚酞试液,现象是碳酸钠溶液呈红色。
(6)乙酸乙酯的理论产量是x g
CH COOH + CH CH OH CH COOCH CH +H O
3 3 2 3 2 3 2
60 g 88 g
6 mL×1.045 g·mL-1 xg
x=9.196
乙酸乙酯的产率= ×100%≈45.7%。
答案:(1)CH CO18OH+ CH CH OH
3 3 2
CH COOCH CH + O
3 2 3
(2)球形冷凝管 B (3)下层 (4)干燥除水
(5) 酚酞 溶液呈红色 (6) 45.7%
关闭 Wor d 文档返回原板块