文档内容
2010年黄高优录考试选拔赛试卷6
Ca:40 C:12 O:16 H:16 S:32 Cu:64
Fe:56 Ag:108 Cl: 35.5 Na:23 N:14
一、选择题
1.质子数和电子总数都与NH +相同的微粒是:A.HO- B.Na+ C.K+ D.HO
4 2
2. 我省已开始使用乙醇汽油。乙醇汽油就是在汽油中加入适量的乙醇混合而成的一种燃料。
下列叙述中错误的是 ( )
A.乙醇汽油是一种新型化合物 B.汽车使用乙醇汽油能减少有害气体的排放
C用石油可炼制汽油 D.用玉米、高梁等发酵可以制得乙醇
3.下面报道中,你认为科学的是( )
A.一窖井冒出大火,烧伤行人, 估计是窖井产生可燃性气体和氮气遇明火引起的
B.识别街头贩卖的假银元,可用硫酸铜溶液浸泡, 观察颜色有无变化
C.利用气球内的干冰释放出一氧化碳的原理,使气球始终处于充足了气的状态
D.不是企业消灭污染,就是污染消灭企业
4.某化合物,其组成中没有C、H、O三种元素。这种化合物可能属于:
A.酸 B.碱 C.盐 D.有机物
5、减少“酸雨”产生的措施:①少用煤作燃料;②把工厂烟囱升高;③在已酸化的土壤中加
石灰;④燃料脱硫;⑤开发新能源。其有效措施是( )
A.①②③ B.②③④ C.①④⑤ D.①③④
6.与n个硫酸分子中所含的氧原子个数相等的是:
A.2n个CO分子 B.4n个水分子 C.4n个氧气分子 D.2n个硝酸分子
2
7.当水的温度和压强升高到临界点(t=374.3℃,p=22.05MPa)以上时,水就处于超临界状态,
该状态的水即称之为超临界水。超临界水具有通常状态下水所没有的特殊性质,它可以和空
气、氧气及一些有机物质均匀混合。如果超临界水中同时溶有氧气和有机物,则有机物可迅
速被氧化为二氧化碳、氮气、水等小分子化合物。有关超临界水的叙述错误的是 ( )
A.超临界水可处理有机废物 B.超临界水是一种新物质
C.超临界水不是水 D.超临界水氧化技术不形成二次污染
8.把t℃时50克20%的KNO 溶液在恒温下蒸发掉10克水,有1克KNO 固体析出,则
3 3
KNO 在t℃时的溶解度为: A.10克 B.22.5 C.25克 D.30克
3
9.下列叙述,正确的是:A.可以生成盐和水的反应称为中和反应 B.碱的分子中必定含有氢元素和氧元素
C.生成单质的反应,有可能是置换反应 D.通过化合反应,无法得到单质
10.由于大气中CO含量增加,产生“温室效应”,使地球变热,海平面升高,陆地面积减少。
2
为了减少大气中CO的含量,下列措施可行的有:
2
A.改变能源结构,发展太阳能、核能、水能,以代替矿物燃料
B.用石灰水吸收空气中的CO
2
C.限制汽车工业的发展,减少汽车数量 D.开展植树造林,增大绿化面积。
11.在一个密闭的钢筒内有四种物质,通过电火花引燃后,发生充分反应,测得反应前后各物
质的质量如下:
甲 乙 丙 丁
反应前质量(克) 4 10 1 25
反应后质量(克) 未测 21 10 9
已知甲的相对分子质量为n,丁的相对分子质量为2n,则该反应的化学方程式中甲与丁的系
数比为: A. 1∶1 B. 1∶ 2 C. 1∶3 D.2∶3
12 氯仿 (CHCl )不溶于水密度比水大,是一种良好的有机溶剂,若保存不当受到光照射时,
3
易被氧化而产生剧毒光气(COCl ),同时生成HCl,下列有关氯仿的实验操作正确的是
2
A用石蕊试液检验氯仿是否变质 B.用硝酸银溶液检查氯仿是否变质
C.用蒸馏水检查氯仿是否变质 D.在教室里倾倒氯仿做检查实验
13.冬天,人们常在树干的外表刷上石灰水,其目的是:( )
A,美观 B,防冻 C,消毒 D.防虫
14. 手机使用的锂电池是新型的高能电池,以质量轻、电容量大而受到重视。某种锂电池的
总反应可表示为Li+Mn0 =LiMn0 。下列说法中正确的是 ( )
2 2
A. LiMn0 为新型的氧化物 B.LiMn0 为锂、锰、氧的合金
2 2
C. 该反应属于化合反应 D.该反应中Mn的化合价没有变化
15.1828年德国化学家维勒,将一种无机物的水溶液加热得到了尿素(NH2CONH2),开创了
有机化学人工合成的新纪元。维勒使用的无机物是 ( )
A.(NH ) C0 B.NH N0 C.CH COONH D.NH CNO
4 2 3 4 3 3 4 4
16、向AgN0 、Cu(N0 )2的混合溶液中加入一些铁粉,完全反应后过滤。不可能存在的情况
3 3
是 ( )
A.滤纸上有Ag,滤液中有Ag+、Cu2+、Fe2+ B.滤纸上有Ag、Cu,滤液中有Ag+、Fe2+
C.滤纸上有Ag、Cu、Fe,滤液中有Fe2+ D.滤纸上有Ag、Cu、Fe,滤液中有Ag+Cu2+二、填空与简答题(本题包括5小题,共24分,每空2分)
17.根据下列结构示意图,用序号回答:
①上述微粒有两种能形成XY型离子化合物,X是 ,Y是 。
2
②具有稳定的最外电子层结构的微粒是 。
18.用煤火取暖或使用燃气热水器冲凉,都可能发生煤气中毒的悲剧,请回答:
①煤气的有毒成份的化学式是 。
(2)煤燃烧时产生煤气的条件是 。
(3)煤气使人中毒的生理过程是 。
19.硫原子与氧原子的最外电子层上都有—个电子,它们的化学性质很相似,在某些化合物
中,硫原子可以代替氧原子。写出下列化学方程式:
CO通入CaO的水溶液中 。
2
CS与NaS的水溶液混合振荡 。
2 2
20.八硝基立方烷是一种新型烈性炸药,它的化学式为C (NO ),一经引爆,这种炸药便能分
8 2 8
解为极稳定的气体:CO 和N。八硝基立方烷分子中,各种元素原子的最简整数比为
2 2
,写出八硝基立方烷爆炸反应的化学方程式 。
21、如图由小分子组装而成的具有一定高级结构的巨分子有时也称为“超分子”。图中的十
二面体是1999年合成的迄今最大的非生物高分子,化学式C H N P S O F Pt ,相
2000 2300 60 120 60 200 180 60
对分子质量达61 955,直径达7.5 nm,相当于小蛋白质分子的尺
寸,右边是其原子堆积模型。该种分子由______种元素组成,每个
分子中共有_________个原子。
三、实验与推断题(本题包括4小题,共25分)
22.(4分)有一种固体混合物,可能由CuSO 、CaCO 、NaCO、BaCl 、NaCl中的一种或几种组
4 3 2 3 2
成,现取该混合物进行如下实验:①将固体温合物溶于水中,搅拌后完全溶解得到无色溶液。
②往此溶液滴加盐酸,产生一种能使澄清石灰水变浑浊的无色无味气体。据此,试推断:
该固体混合物中一定有 ,不能肯定是否存在的是 。
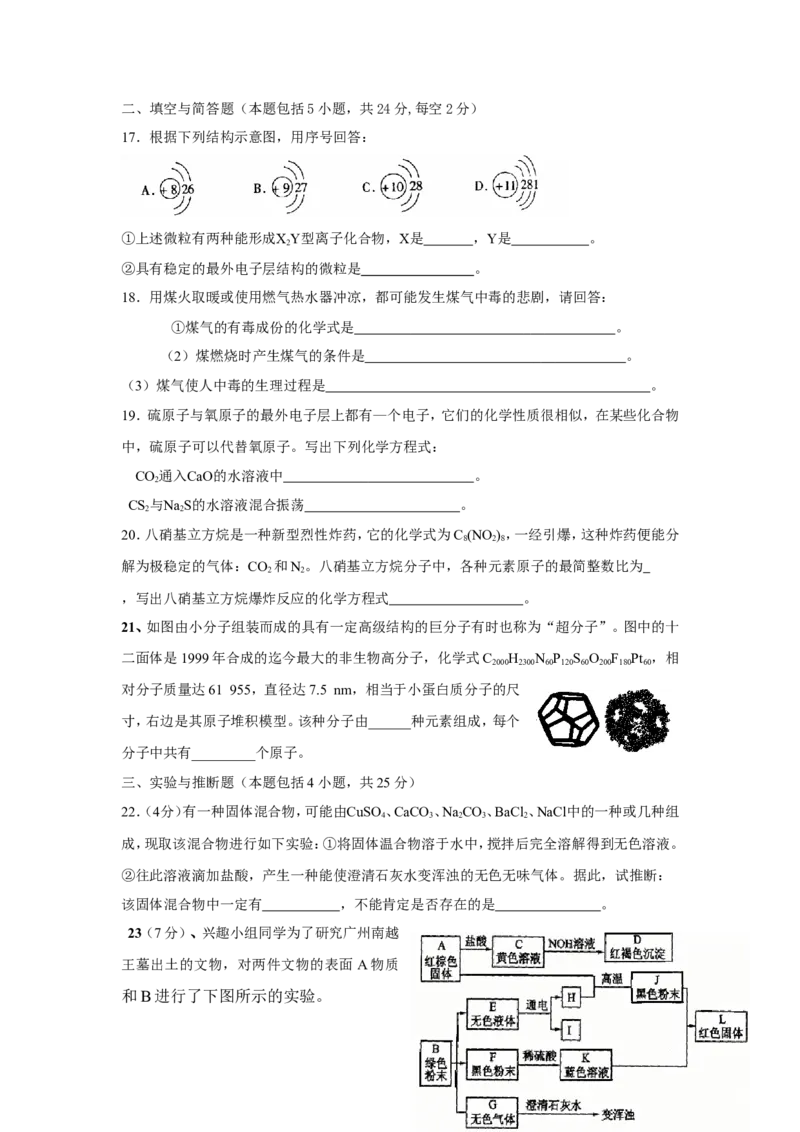
23(7分)、兴趣小组同学为了研究广州南越
王墓出土的文物,对两件文物的表面 A物质
和B进行了下图所示的实验。(1)请你根据下图实验现象推断下列物质的化学式:
A:__________ B_______________G:______________
(2)写出下列转化的化学方程式:
C→D_________________________ ;E→H+I _________________________ ;J+K→L
_________________________ ;
(3)在博物馆里很少见到由J制造的完好文物,原因是什么?
24(7分)、已知CaCO+HO+CO→Ca(HCO) ,Ca(HCO) 易溶于水。某实验小组在含一定量
3 2 2 3 2 3 2
Ca(OH) 的石灰水中通入CO,产生沉淀的量与通入CO 气体的量的关系如图所示,回答下列
2 2 2
问题:
(1)写出在石灰水中刚通入CO 时的化学方程式 。
2
(2)请描述整个实验过程的实验现象 。
(3)通CO 气体前石灰水中溶质的质量为 g。
2
(4)至少通入CO 气体质量 g时溶液的质量是
2
整个实验过程中溶液质量的最大值(不考虑CO 气体在水中的溶
2
解性)。
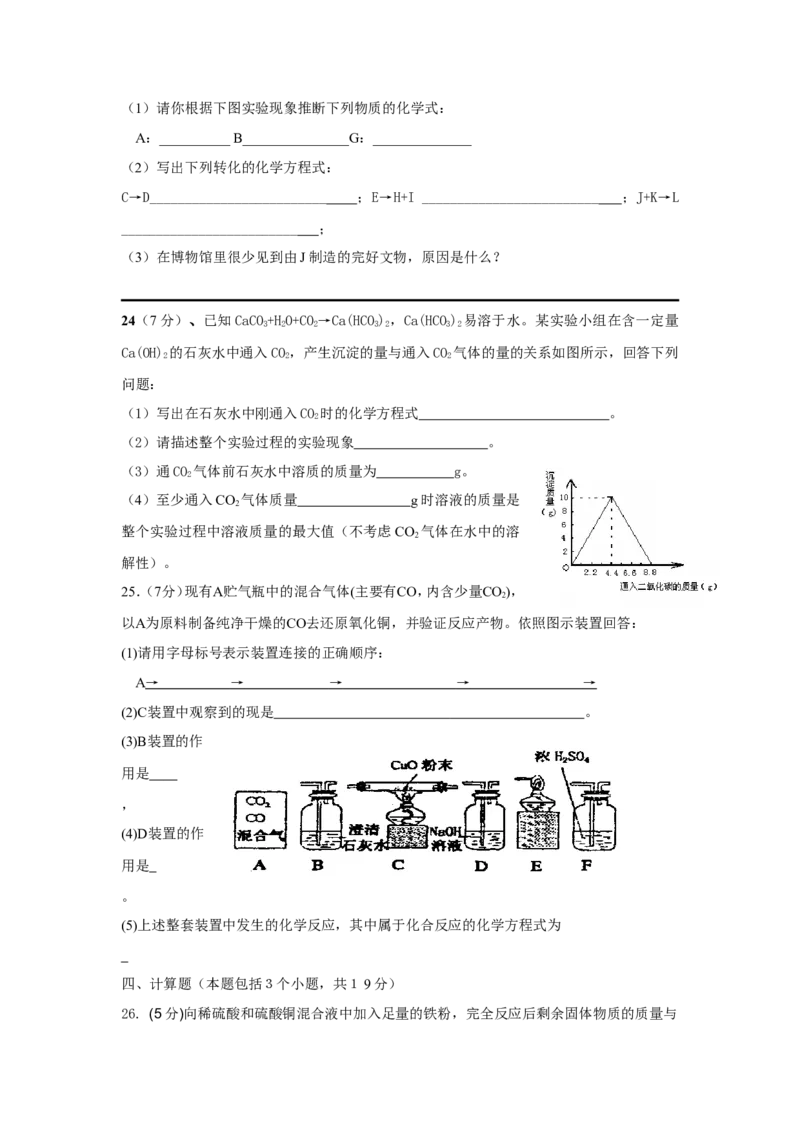
25.(7分)现有A贮气瓶中的混合气体(主要有CO,内含少量CO),
2
以A为原料制备纯净干燥的CO去还原氧化铜,并验证反应产物。依照图示装置回答:
(1)请用字母标号表示装置连接的正确顺序:
A → → → → →
(2)C装置中观察到的现是 。
(3)B装置的作
用是
,
(4)D装置的作
用是
。
(5)上述整套装置中发生的化学反应,其中属于化合反应的化学方程式为
四、计算题(本题包括3个小题,共19分)
26. (5分)向稀硫酸和硫酸铜混合液中加入足量的铁粉,完全反应后剩余固体物质的质量与所加铁粉的质量相待。求原混合液中硫酸和硫酸铜的质量比。
27.(6分)有一种由氯化钠和硝酸钠组成的固体混合物12.35g,加入27g水使其完全溶解,滴
入硝酸银溶液75g,恰好完全反应,生成氯化银沉淀14.35g。计算. :
(1)混合物中,氯化钠的质量。(2)反应后滤液中溶质的质量分数
28.(8分)某种天然碱样品的化学式可以用xNaHCO ·yNaCO·zHO表示(式中x、y、z是最简
3 2 3 2
整数比)。取50克某一浓度的盐酸与3.32克样品充分反应,能生成1.32克CO气体。
2
(1)若改用1.66克样品与50克这种盐酸反应,能产生 克CO。
2
(2)另取3.32克样品在300℃下加热至完全分解(已知NaCO在300℃时不会分解),能产生0.22
2 3
克CO和0.45克HO,试确定该样品的化学式: 。
2 2
(3)写出这种天然碱与盐酸完全反应的化学方程式。若6.64克天然碱样品与50克该盐酸充分
反应时放出的CO 最多,求该盐酸的溶质质量分数。
2
答案
一、 选择题每小题2分,共32分。
1、B 2、A 3、BD 4、C 5、C 6、AB 7、BC 8、D 9、CD 10、AD 11、B 12、AB
13、CD 14、C 15、D 16、BD
二、(本题包括5小题,共24分,每空2分)
17.D B C 18. (1)CO(2)氧气不足,碳不充分燃烧(3)CO与血红蛋白结合使得氧气不能与血红蛋白结合导致人体缺氧
19. (1)CO +CaO=CaCO3 (2)CS2+Na S= Na SO3
2 2 2
20.1:1:2 C (NO ) =8CO +4N
8 2 8 2 2
21.8 4980
三、实验与推断题(本题包括4小题,共26分)
22. (4分) Na CO NaCl
2 3 ,
23(7分,每空1分).
(1)A:Fe O ;B:CuO;G:CO
2 3 2
(2)FeCl +3NaOH==3Cl+Fe(OH) ↓(1分);2H O 2H ↑+O ↑(1分);
3 3 2 通电 2 2
Fe+CuSO ==Cu+FeSO (1分)
4 4
(1) 铁的化学性质比较活泼,在潮湿的空气中容易生锈(被腐蚀)
24(7分)
(1)Ca(OH) +CO ==CaCO ↓+H O(1分)
2 2 3 2
(2)开始产生白色沉淀,随着CO 的不断通入沉淀逐渐增多,然后沉淀不断
2
减少,最后完全消失。(2分)(3)7.4(2分)(4)8.8(2分)
25. (7分)(1)ADFCBE (2分)(2)黑色粉末变红色(1分)
(3)验证生成了CO (1分)(4)除去混合气体中的CO (1分)
2 2
(5)2CO+ O 点燃 2 CO (2分)
2 = == 2
四、计算题(本题包括3个小题,共19分)
26. (5分) 7∶80 27. (6分)(1)5.85g(2)15%
28.(8分) (1)0.66克 (2分)(2) NaHCO ·2Na CO ·2H O(3分)(3)7.28%(3
3 2 3 2
分)