文档内容
化学部分
相对原子质量:H-1 C-12 N-14 O-16
五、选择题(共20分)
请将正确选项的代号用2B铅笔填涂在答题纸相应位置上,更改答案时,用橡皮擦去,重新填
涂。
21~34每题均只有一个正确选项
1. 银元素的符号是
A. Ag B. AG C. In D. Y
2. 过多排放会造成空气污染的是
.
A 二氧化碳 B. 二氧化硫 C. 氮气 D. 氧气
3. 属于氧化物的是
A. B. C. D. NaOH
4. 一些食物的pH如下,呈碱性的是
A. 菠菜:5.1~5.7 B. 牛奶:6.3~6.6 C. 西瓜:6.0~6.8 D. 鸡蛋清:7.6~8.0
5. 互为同素异形体的一组物质是
A. 水和双氧水 B. 活性炭和木炭 C. 石墨和金刚石 D. 液氧和氧气
6. 在足量水中能形成溶液的是
A. 食盐 B. 豆油 C. 冰块 D. 泥沙
7. +3价铝元素与氯元素形成的化合物的化学式为
A. AlCl B. C. D.
8. 下列物质在氧气中燃烧,产生大量白烟的是
A. 铁丝 B. 木炭 C. 硫粉 D. 红磷
9. 下列物质的用途,主要利用了物理性质的是
A. 氧气做助燃剂 B. 氢气做火箭推进剂
C. 氦气填充飞艇 D. 氮气做保护气
10. 自来水生产中主要用于去除异味的物质是
A. 明矾 B. 活性炭 C. 空气 D. 氯气
11. 下列化学方程式书写正确的是
A. B.C. D.
的
12. 有关物质 量,说法正确的是
A. 物质的量的符号是“M”
B. 1mol任何物质都含有相同的微粒数
C. 摩尔是国际单位制中七个基本物理量之一
D. 物质的量可将宏观质量与微粒数量建立联系
13. 关于相对原子质量说法正确的是
A. 相对原子质量就是原子的真实质量 B. 相对原子质量就是该原子的摩尔质量
C. 相对原子质量越大,该原子的质量越大 D. 相对原子质量是一种原子质量对一种碳原子的质
量之比
14. 某反应为 ,相关分析正确的是
A. 物质X是单质 B. n一定为1
C. 与 恰好能完全反应 D. 生成 ,需要 参加反应
35~37题每题均有1~2个正确选项
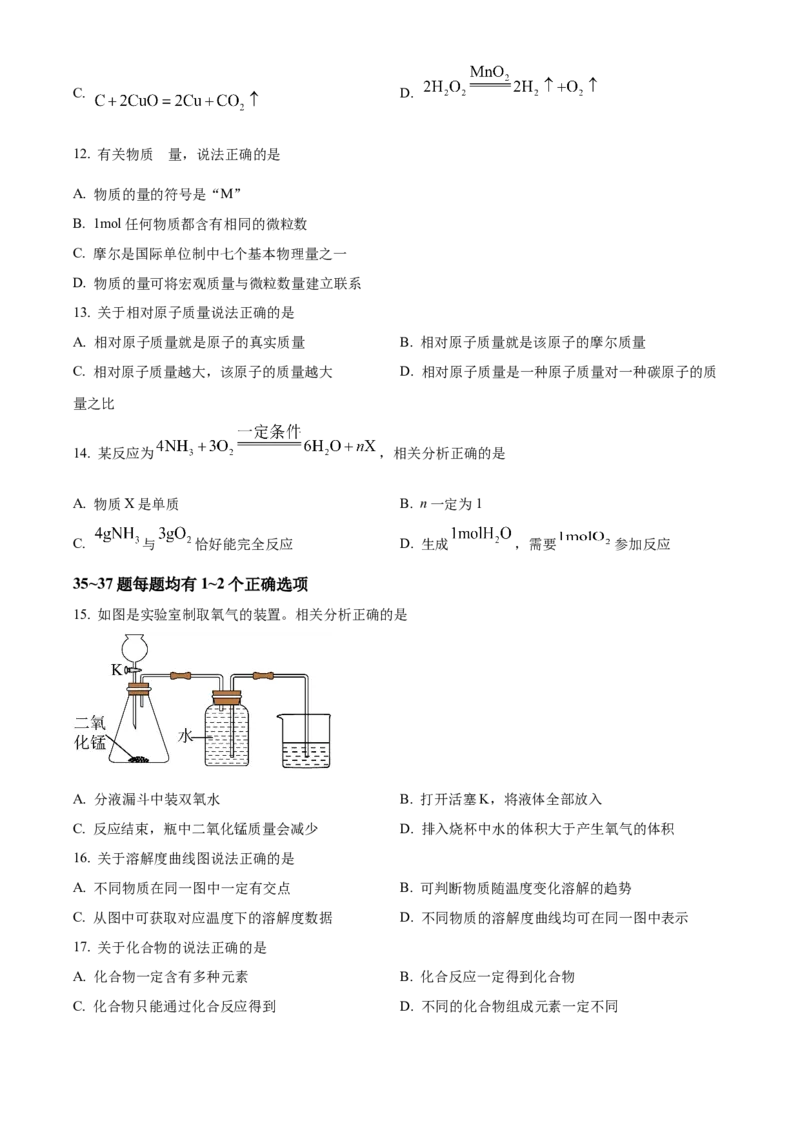
15. 如图是实验室制取氧气的装置。相关分析正确的是
A. 分液漏斗中装双氧水 B. 打开活塞K,将液体全部放入
C. 反应结束,瓶中二氧化锰质量会减少 D. 排入烧杯中水的体积大于产生氧气的体积
16. 关于溶解度曲线图说法正确的是
A. 不同物质在同一图中一定有交点 B. 可判断物质随温度变化溶解的趋势
C. 从图中可获取对应温度下的溶解度数据 D. 不同物质的溶解度曲线均可在同一图中表示
17. 关于化合物的说法正确的是
A. 化合物一定含有多种元素 B. 化合反应一定得到化合物
C. 化合物只能通过化合反应得到 D. 不同的化合物组成元素一定不同六、简答题(共30分)
请根据要求在答题纸相应的位置作答。
18. 碳中和主要是抵消、降低排放二氧化碳和吸收二氧化碳。
(1)自然界中可以通过光合作用吸收二氧化碳。
光合作用是二氧化碳和水生成氧气和葡萄糖( ),光合作用是______(选填“化学变化”或”物
理变化”)。 属于______(填写物质类别);葡萄糖中,元素质量分数最大的是______元素;每生成
1mol葡萄糖,可以吸收 ______mol。
(2)降低对化石燃料的依赖,以及提高燃料的燃烧效率,可以降低排放二氧化碳。
若要煤炭充分燃烧,采取的措施可以是______(写出一条即可);若 完全燃烧,产生的 分
子数约为______个、
(3)工业生产中,对于含 的尾气要进行吸收。
若采用氢氧化钙悬浊液吸收,写出反应的化学方程式______,若用其他物质替代“氢氧化钙”作为吸收剂,
请阐述你选用该物质替代的理由是______(写出一条即可)。
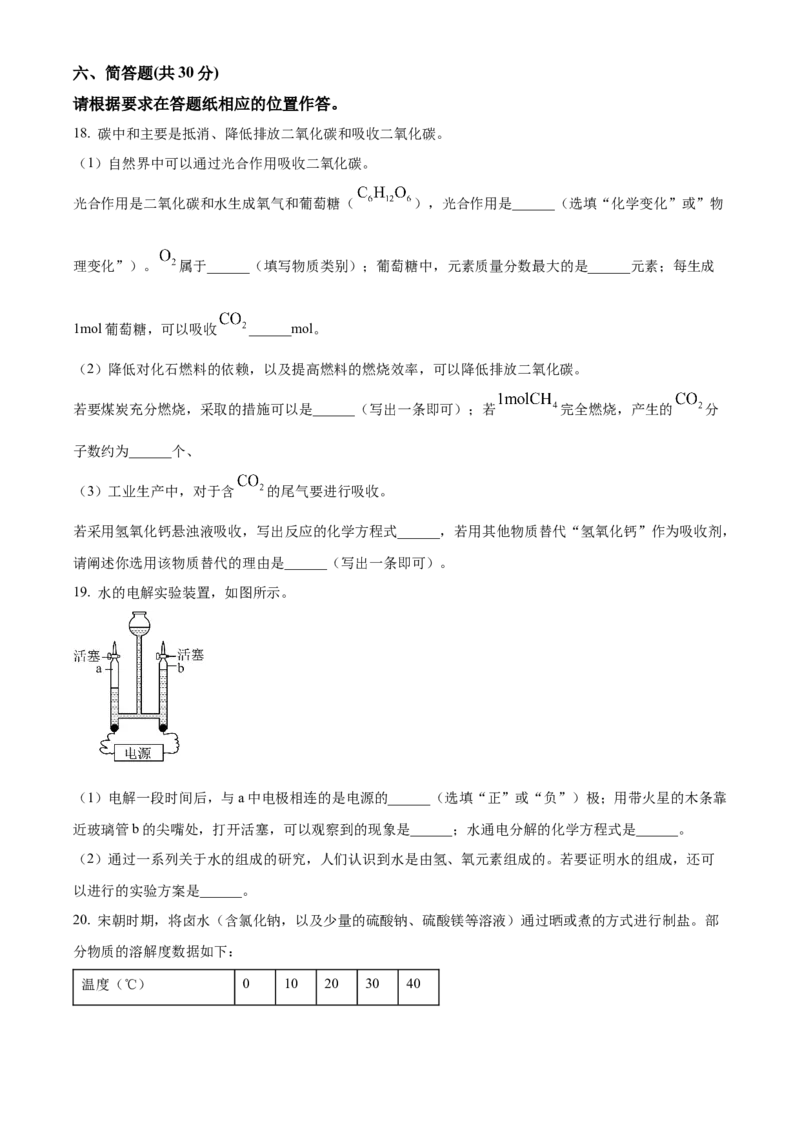
19. 水的电解实验装置,如图所示。
(1)电解一段时间后,与a中电极相连的是电源的______(选填“正”或“负”)极;用带火星的木条靠
近玻璃管b的尖嘴处,打开活塞,可以观察到的现象是______;水通电分解的化学方程式是______。
(2)通过一系列关于水的组成的研究,人们认识到水是由氢、氧元素组成的。若要证明水的组成,还可
以进行的实验方案是______。
20. 宋朝时期,将卤水(含氯化钠,以及少量的硫酸钠、硫酸镁等溶液)通过晒或煮的方式进行制盐。部
分物质的溶解度数据如下:
温度(℃) 0 10 20 30 40氯化
35.7 35.8 36 36.3 36.6
钠
.
溶解度(g/100g 硫酸
4.9 9.1 19.5 40.8 488
水) 钠
硫酸
22 27.7 33.5 39.3 44.5
镁
(1)卤水制取。可以将海水引入到覆盖有茅草的卤坑上,茅草可以将不溶于水的泥沙除去,该方法类似
于化学实验操作中的______(填写操作名称),“茅草”类似于该操作中的______(填写用品名称)。
(2)卤水浓缩。卤水浓度越高,溶液的密度越大。
晒盐通过自然界的风吹日晒得到食盐晶体,该结晶方法称为______。加热熬制卤水达到一定浓度时,采用
一些方法将卤水冷却,进行这样的操作目的是______。
(3)浓度检验。为检验卤水的浓度是否达到熬盐要求,往卤水中投入石莲子(一种植物种子),通过石
莲子的沉浮确定溶液的浓度。
为
验证该方法进行如下实验:
Ⅰ、常温下,配制氯化钠溶液
烧杯编号 1 2 3 4 5 6
需配制溶液 的质
17.0% 19.0% 21.0% 23.0% 25.0% 27.0%
量分数
若要配制25%的溶液100g,需要氯化钠______g;有同学认为27%的溶液是不能配制的,理由是______。
Ⅱ、投入石莲子,进行实验
在编号1~5的溶液中,各投入5枚石莲子,观察到编号“4”中石莲子上浮。产生相同现象是烧杯编号
______。
Ⅲ、反思评价
古人采用石莲子进行浓度检验的优点是______。
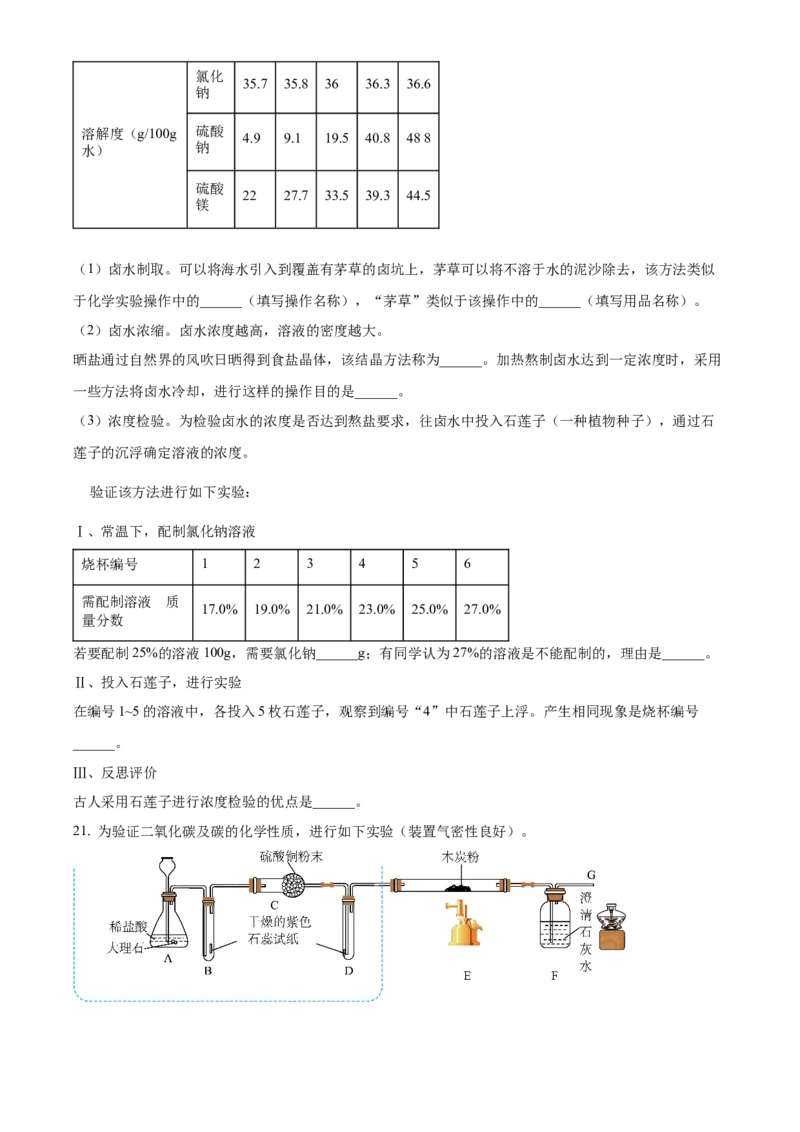
21. 为验证二氧化碳及碳的化学性质,进行如下实验(装置气密性良好)。(1)利用上述实验装置验证二氧化碳的化学性质。
Ⅰ、A中反应的化学方程式是______。C中的现象是______。
Ⅱ、“B、C、D”连续装置的实验目的是______。
Ⅲ、该实验得出二氧化碳能与碳反应的现象是______。
(2)将虚线内的装置改为储气袋,进行碳的充分燃烧与不充分燃烧实验。
Ⅰ、进行该实验需要控制的变量是______。
Ⅱ、使用氧气储气袋,点燃E处的酒精喷灯,通入氧气,玻璃管中的发生反应的化学方程式是______。
Ⅲ、使用空气储气袋进行实验,预计G处尾气能燃烧,结果发现G处尾气未能点燃,请分析可能的原因是
______(写出一条即可)。