文档内容
学年第二学期学业质量发展阶段性训练(二)
2024
九年级化学试卷
本试卷共8页,20小题,满分90分。考试时间60分钟。
注意事项:
1.答卷前,考生务必在答题卡上用黑色字迹的钢笔或签字笔填写自己的考生号、姓名;同时填写考点
考场号、座位号,再用2B铅笔把对应这两个号码的标号涂黑。
2.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦
干净后,再选涂其他答案标号;不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内的相应位置上;
如需改动,先划掉原来的答案,然后再写上新的答案,改动的答案也不能超出指定的区域;不准使
用铅笔、园球笔和涂改液,不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束时,将本试卷和答题卡一并交回。
5.全卷共两大题20小题,请考生检查题数。
可能用到的相对原子质量:C-12 H-1 O-16 N-14 Na-23 Fe-56 S-32 Ca-40
第一部分 选择题(共 42 分)
一、选择题(本题包括 14 小题,每小题 3 分,共 42 分)
注意:每道选择题有四个选项,其中只有一项符合题意。选错、不选、多选或涂改不清的,均不给分。
1、中华民族的发明创造为人类文明进步作出了巨大贡献,我国的下列古代发明及应用中,明显不涉及化学
变化的是( )
A.活字印刷 B.黑火药爆炸 C.用粮食酿醋 D.用黏土烧制陶瓷
2、下列物品的材质属于有机合成材料的是( )
A.用钛合金制造的人造骨 B.用可降解塑料制作的手术缝合线
C.用羊毛制作的羊绒毛衣 D.用大理石制作的天安门华表
3、空气和水都是人类宝贵的自然资源。下列说法正确的是( )
A.空气中含有氧气,因此空气可以直接用于医疗急救
B.铁丝插入盛有氧气的集气瓶中剧烈燃烧,火星四射
C.在电解水实验中,生成的氢气和氧气的质量比是2:1
D.活性炭净水器可以吸附、过滤水中的杂质
4、下列说法正确的是( )
A.食物中的蛋白质能被人体直接用于生长发育
B.钙是人体所需的微量元素,成年人缺钙会导致骨质疏松
C.甘薯和马铃薯中含有淀粉,可以为人体提供能量
D.谷物和肉类不能为人体提供维生素
化学 第1页 (共8页)
{#{QQABRYEk4gC4gAbACR4LEUX4CAgQkJKjJaoMwQCfKARLQAFAFIA=}#}5、对下列宏观事实的微观解释合理的是( )
选项 客观事实 微观解释
A 金刚石和石墨的物理性质差异明显 碳原子的结构不同
B 汽油燃烧 燃烧前后分子种类不变
C 自行车轮胎充气后鼓起 分子间的间隔增大
D KMnO 溶液呈紫红色,KNO 溶液呈无色 MnO -在水溶液中呈紫红色
4 3 4
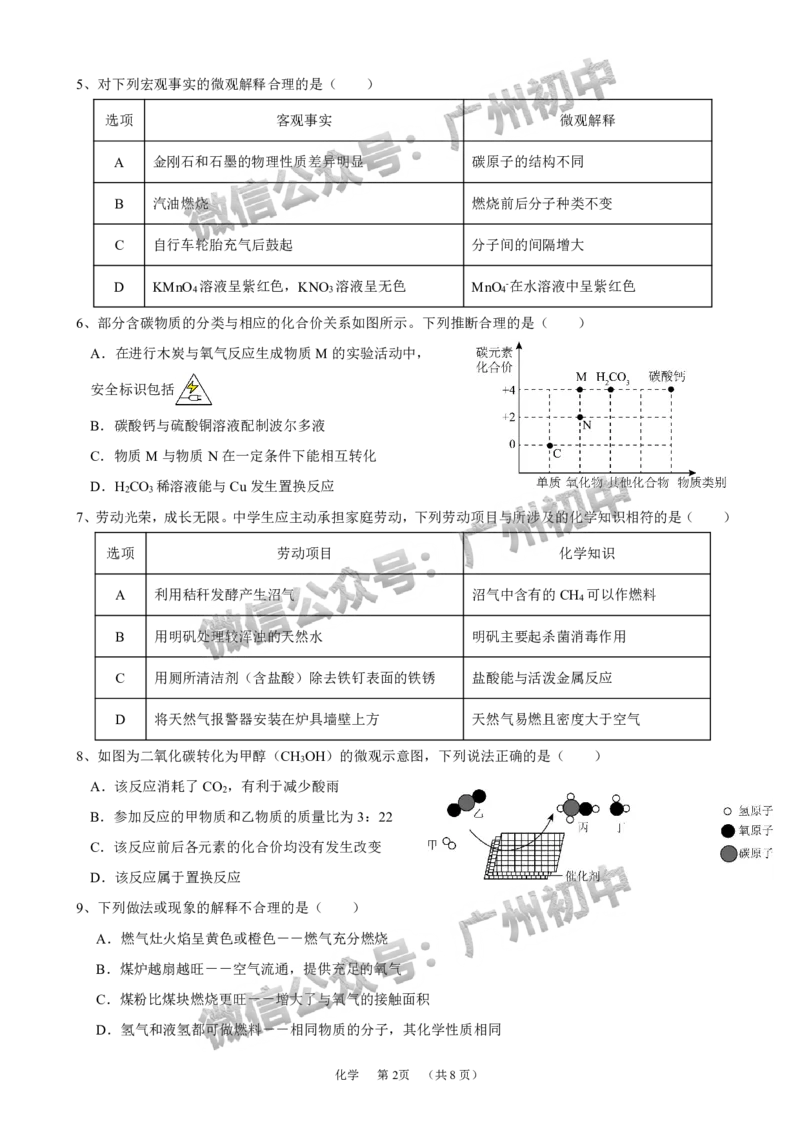
6、部分含碳物质的分类与相应的化合价关系如图所示。下列推断合理的是( )
A.在进行木炭与氧气反应生成物质M的实验活动中,
安全标识包括
B.碳酸钙与硫酸铜溶液配制波尔多液
C.物质M与物质N在一定条件下能相互转化
D.H CO 稀溶液能与Cu发生置换反应
2 3
7、劳动光荣,成长无限。中学生应主动承担家庭劳动,下列劳动项目与所涉及的化学知识相符的是( )
选项 劳动项目 化学知识
A 利用秸秆发酵产生沼气 沼气中含有的CH 可以作燃料
4
B 用明矾处理较浑浊的天然水 明矾主要起杀菌消毒作用
C 用厕所清洁剂(含盐酸)除去铁钉表面的铁锈 盐酸能与活泼金属反应
D 将天然气报警器安装在炉具墙壁上方 天然气易燃且密度大于空气
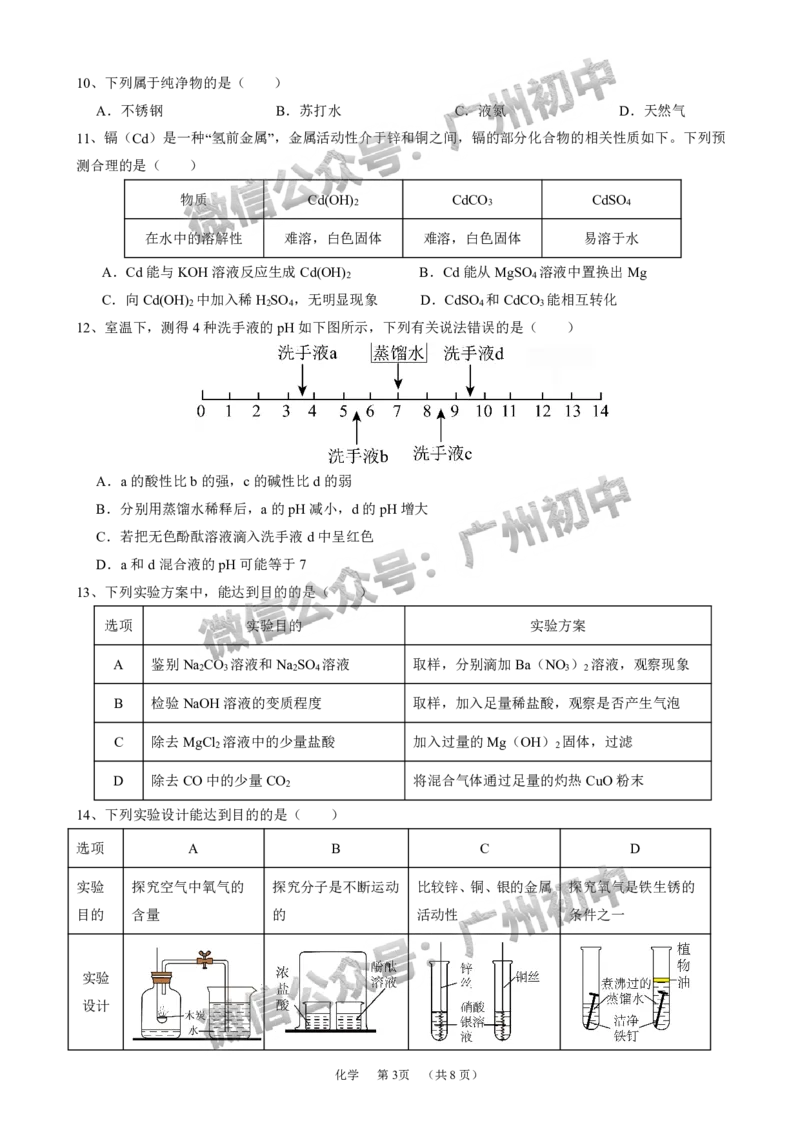
8、如图为二氧化碳转化为甲醇(CH OH)的微观示意图,下列说法正确的是( )
3
A.该反应消耗了CO ,有利于减少酸雨
2
B.参加反应的甲物质和乙物质的质量比为3:22
C.该反应前后各元素的化合价均没有发生改变
D.该反应属于置换反应
9、下列做法或现象的解释不合理的是( )
A.燃气灶火焰呈黄色或橙色--燃气充分燃烧
B.煤炉越扇越旺--空气流通,提供充足的氧气
C.煤粉比煤块燃烧更旺--增大了与氧气的接触面积
D.氢气和液氢都可做燃料--相同物质的分子,其化学性质相同
化学 第2页 (共8页)
{#{QQABRYEk4gC4gAbACR4LEUX4CAgQkJKjJaoMwQCfKARLQAFAFIA=}#}10、下列属于纯净物的是( )
A.不锈钢 B.苏打水 C.液氮 D.天然气
11、镉(Cd)是一种“氢前金属”,金属活动性介于锌和铜之间,镉的部分化合物的相关性质如下。下列预
测合理的是( )
物质 Cd(OH) CdCO CdSO
2 3 4
在水中的溶解性 难溶,白色固体 难溶,白色固体 易溶于水
A.Cd能与KOH溶液反应生成Cd(OH) B.Cd能从MgSO 溶液中置换出Mg
2 4
C.向Cd(OH) 中加入稀H SO ,无明显现象 D.CdSO 和CdCO 能相互转化
2 2 4 4 3
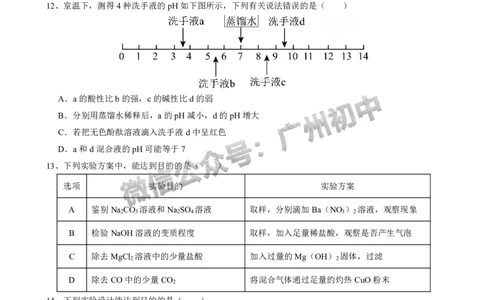
12、室温下,测得4种洗手液的pH如下图所示,下列有关说法错误的是( )
A.a的酸性比b的强,c的碱性比d的弱
B.分别用蒸馏水稀释后,a的pH减小,d的pH增大
C.若把无色酚酞溶液滴入洗手液d中呈红色
D.a和d混合液的pH可能等于7
13、下列实验方案中,能达到目的的是( )
选项 实验目的 实验方案
A 鉴别Na CO 溶液和Na SO 溶液 取样,分别滴加Ba(NO ) 溶液,观察现象
2 3 2 4 3 2
B 检验NaOH溶液的变质程度 取样,加入足量稀盐酸,观察是否产生气泡
C 除去MgCl 溶液中的少量盐酸 加入过量的Mg(OH) 固体,过滤
2 2
D 除去CO中的少量CO 将混合气体通过足量的灼热CuO粉末
2
14、下列实验设计能达到目的的是( )
选项 A B C D
实验 探究空气中氧气的 探究分子是不断运动 比较锌、铜、银的金属 探究氧气是铁生锈的
目的 含量 的 活动性 条件之一
实验
设计
化学 第3页 (共8页)
{#{QQABRYEk4gC4gAbACR4LEUX4CAgQkJKjJaoMwQCfKARLQAFAFIA=}#}第二部分 非选择题(共 48 分)
二、非选择题(本题包括 6 小题,共 48 分)
15、(5分)钠元素和钛元素都是重要的化学元素。
(1)如右图所示,钠的相对原子质量为 。Ti2+的核外电子数为 。
(2)钠元素广泛存在自然界中,亚硝酸钠(NaNO )是一种常用的防腐剂,其中氮元素
2
的化合价为 。
(3)将金属钠与液态氨反应得NaNH ,再将NaNH 与N O反应可生成NaN ,反应的化
2 2 2 3
学方程式为2NaNH +N O=NaN +NaOH+X,则X的化学式为 。
2 2 3
(4)叠氮化钠(NaN )被广泛应用于汽车安全气囊,汽车经撞击后,30毫秒内引发NaN 迅速分解生成两
3 3
种单质,该反应的化学方程式为 。
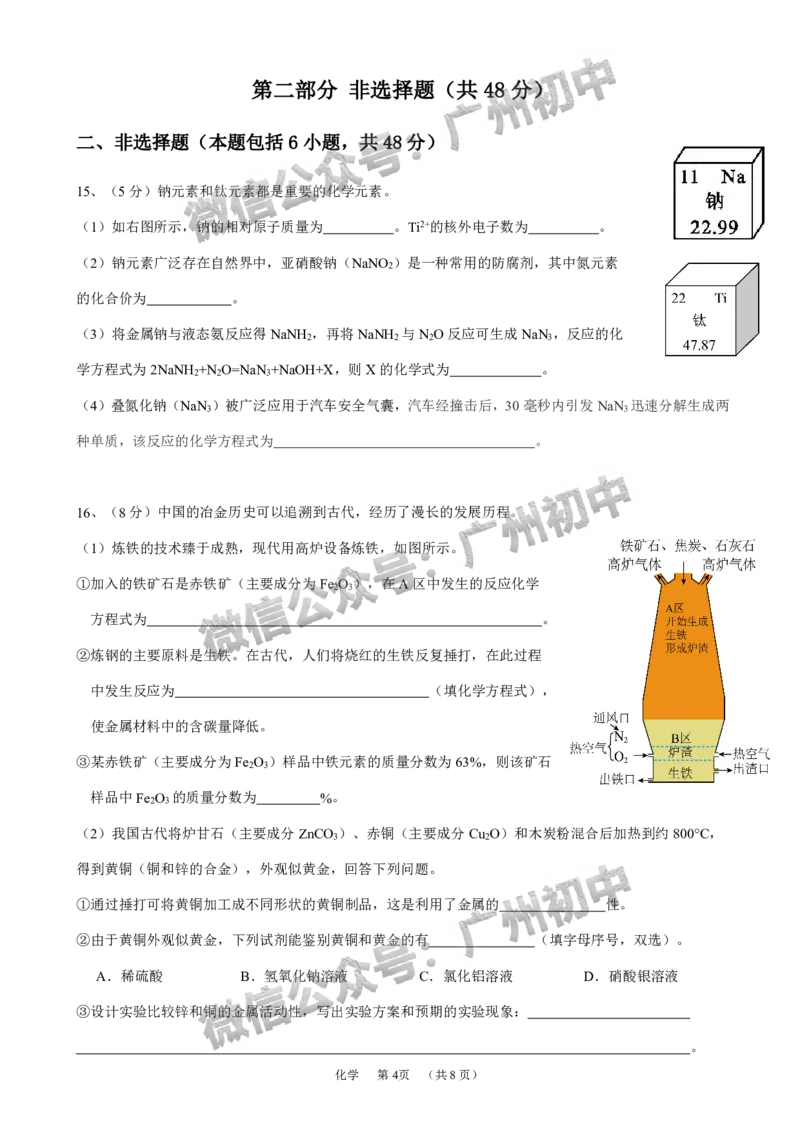
16、(8分)中国的冶金历史可以追溯到古代,经历了漫长的发展历程。
(1)炼铁的技术臻于成熟,现代用高炉设备炼铁,如图所示。
①加入的铁矿石是赤铁矿(主要成分为Fe O ),在A区中发生的反应化学
2 3
方程式为 。
②炼钢的主要原料是生铁。在古代,人们将烧红的生铁反复捶打,在此过程
中发生反应为 (填化学方程式),
使金属材料中的含碳量降低。
③某赤铁矿(主要成分为Fe O )样品中铁元素的质量分数为63%,则该矿石
2 3
样品中Fe O 的质量分数为 %。
2 3
(2)我国古代将炉甘石(主要成分ZnCO )、赤铜(主要成分Cu O)和木炭粉混合后加热到约800°C,
3 2
得到黄铜(铜和锌的合金),外观似黄金,回答下列问题。
①通过捶打可将黄铜加工成不同形状的黄铜制品,这是利用了金属的 性。
②由于黄铜外观似黄金,下列试剂能鉴别黄铜和黄金的有 (填字母序号,双选)。
A.稀硫酸 B.氢氧化钠溶液 C.氯化铝溶液 D.硝酸银溶液
③设计实验比较锌和铜的金属活动性,写出实验方案和预期的实验现象:
。
化学 第4页 (共8页)
{#{QQABRYEk4gC4gAbACR4LEUX4CAgQkJKjJaoMwQCfKARLQAFAFIA=}#}17、(8分)实验室制取氧气、配制溶液、酸碱中和反应等均是初中常见实验。
【实验一】氧气在实验室中常用二氧化锰催化过氧化氢溶液分解制取。
(1)制氧气的化学方程式是 。
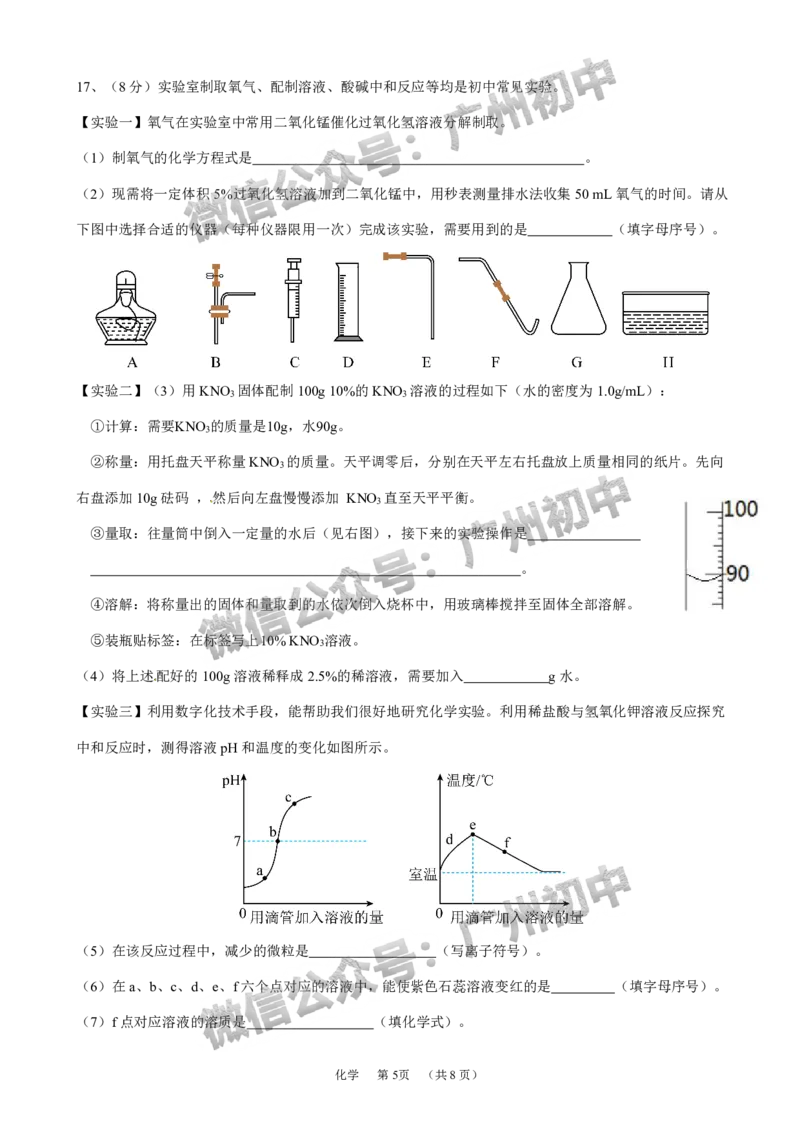
(2)现需将一定体积5%过氧化氢溶液加到二氧化锰中,用秒表测量排水法收集50mL氧气的时间。请从
下图中选择合适的仪器(每种仪器限用一次)完成该实验,需要用到的是 (填字母序号)。
【实验二】(3)用KNO 固体配制100g10%的KNO 溶液的过程如下(水的密度为1.0g/mL):
3 3
①计算:需要KNO 的质量是10g,水90g。[来源:学*科*网Z*X*X*K]
3
②称量:用托盘天平称量KNO 的质量。天平调零后,分别在天平左右托盘放上质量相同的纸片。先向
3
右盘添加10g砝码 ,然后向左盘慢慢添加 KNO 直至天平平衡。
3
③量取:往量筒中倒入一定量的水后(见右图),接下来的实验操作是
。
④溶解:将称量出的固体和量取到的水依次倒入烧杯中,用玻璃棒搅拌至固体全部溶解。
⑤装瓶贴标签:在标签写上10%KNO 溶液。
3
(4)将上述配好的100g溶液稀释成2.5%的稀溶液,需要加入 g水。
【实验三】利用数字化技术手段,能帮助我们很好地研究化学实验。利用稀盐酸与氢氧化钾溶液反应探究
中和反应时,测得溶液pH和温度的变化如图所示。
(5)在该反应过程中,减少的微粒是 (写离子符号)。
(6)在a、b、c、d、e、f六个点对应的溶液中,能使紫色石蕊溶液变红的是 (填字母序号)。
(7)f点对应溶液的溶质是 (填化学式)。
化学 第5页 (共8页)
{#{QQABRYEk4gC4gAbACR4LEUX4CAgQkJKjJaoMwQCfKARLQAFAFIA=}#}18、(10分)氯化钠在自然界中分布很广,海水、盐湖、盐井和盐矿都是氯化钠你的来源。
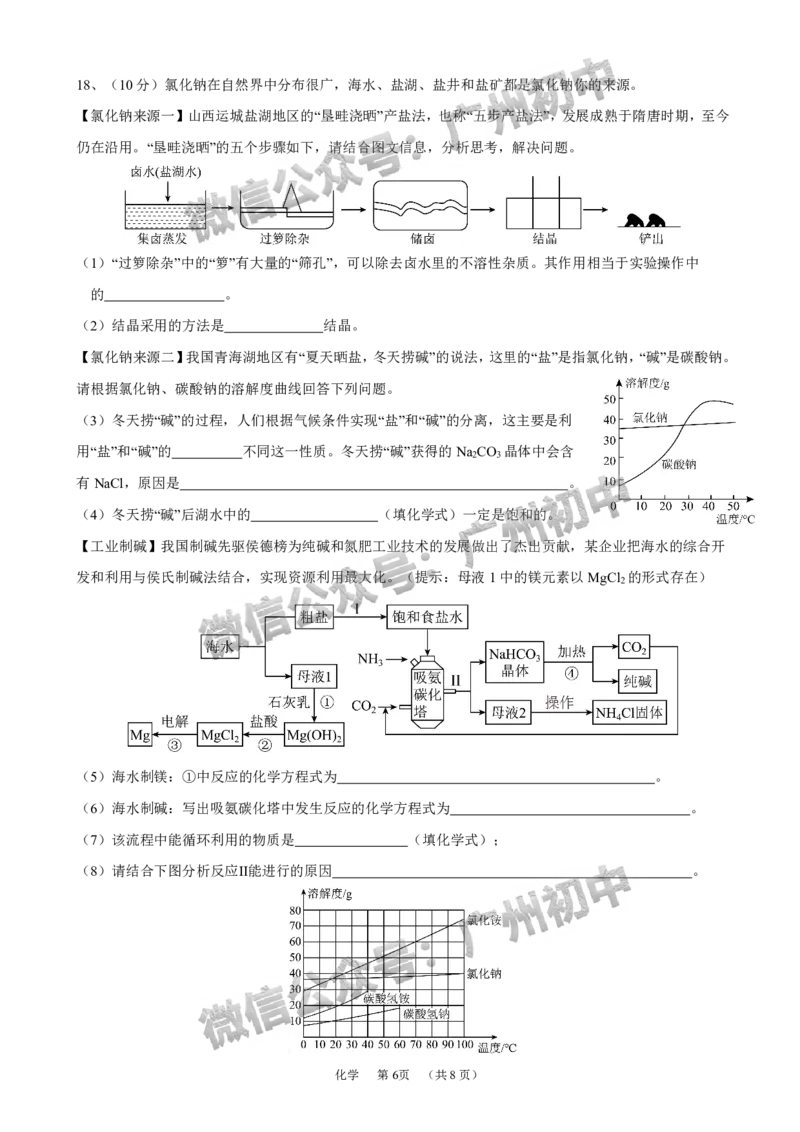
【氯化钠来源一】山西运城盐湖地区的“垦畦浇晒”产盐法,也称“五步产盐法”,发展成熟于隋唐时期,至今
仍在沿用。“垦畦浇晒”的五个步骤如下,请结合图文信息,分析思考,解决问题。
(1)“过箩除杂”中的“箩”有大量的“筛孔”,可以除去卤水里的不溶性杂质。其作用相当于实验操作中
的 。
(2)结晶采用的方法是 结晶。
【氯化钠来源二】我国青海湖地区有“夏天晒盐,冬天捞碱”的说法,这里的“盐”是指氯化钠,“碱”是碳酸钠。
请根据氯化钠、碳酸钠的溶解度曲线回答下列问题。
(3)冬天捞“碱”的过程,人们根据气候条件实现“盐”和“碱”的分离,这主要是利
用“盐”和“碱”的 不同这一性质。冬天捞“碱”获得的Na CO 晶体中会含
2 3
有NaCl,原因是 。
(4)冬天捞“碱”后湖水中的 (填化学式)一定是饱和的。
【工业制碱】我国制碱先驱侯德榜为纯碱和氮肥工业技术的发展做出了杰出贡献,某企业把海水的综合开
发和利用与侯氏制碱法结合,实现资源利用最大化。(提示:母液1中的镁元素以MgCl 的形式存在)
2
(5)海水制镁:①中反应的化学方程式为 。
(6)海水制碱:写出吸氨碳化塔中发生反应的化学方程式为 。
(7)该流程中能循环利用的物质是 (填化学式);
(8)请结合下图分析反应Ⅱ能进行的原因 。
化学 第6页 (共8页)
{#{QQABRYEk4gC4gAbACR4LEUX4CAgQkJKjJaoMwQCfKARLQAFAFIA=}#}19、(8分)丙酸钙为白色固体,易溶于水,可作食品防霉剂,国家标准规定了其用于制作面食、糕点时每
千克面粉中的最大使用量。小组同学实验探究其性质和防霉的效果。
(I)探究丙酸钙的性质
【进行实验】用下图装置(夹持仪器已略去)完成实验,记录如下:
序号 ① ②
装置
现象 试管内壁有水雾 注入稀盐酸后,有气泡产生,石灰水变浑浊
【解释与结论】
(1)②中现象说明有CO 产生。CO 与石灰水反应的化学方程式为 。
2 2
(2)查阅资料得知丙酸钙与盐酸反应无气体生成。由实验②可得出的结论是 。
(Ⅱ)探究丙酸钙防霉的效果
【进行实验】分别按下列①~⑧的配方蒸制8个馒头,冷却后置于密封袋中,记录如下:
组别 第1组 第2组
序号 ① ② ③ ④ ⑤ ⑥ ⑦ ⑧
面粉/g 50 50 50 50 50 50 50 50
酵母/g 0.75 0.75 0.75 0.75 0.75 0.75 0.75 0.75
配
方
蔗糖/g 0 0 0 0 5 5 x 5
丙酸钙/g 0 0.06 0.10 0.15 0 0.06 0.10 y
开始发霉时间 第3天 第4天 第5天 第6天 第3天 第4天 第5天 第6天
【解释与结论】
(3)设计第1组实验的目的是 。
(4)第2组,⑦中x为 ,⑧中y为 。
(5)对比第1组、第2组实验可得到的结论是 。
化学 第7页 (共8页)
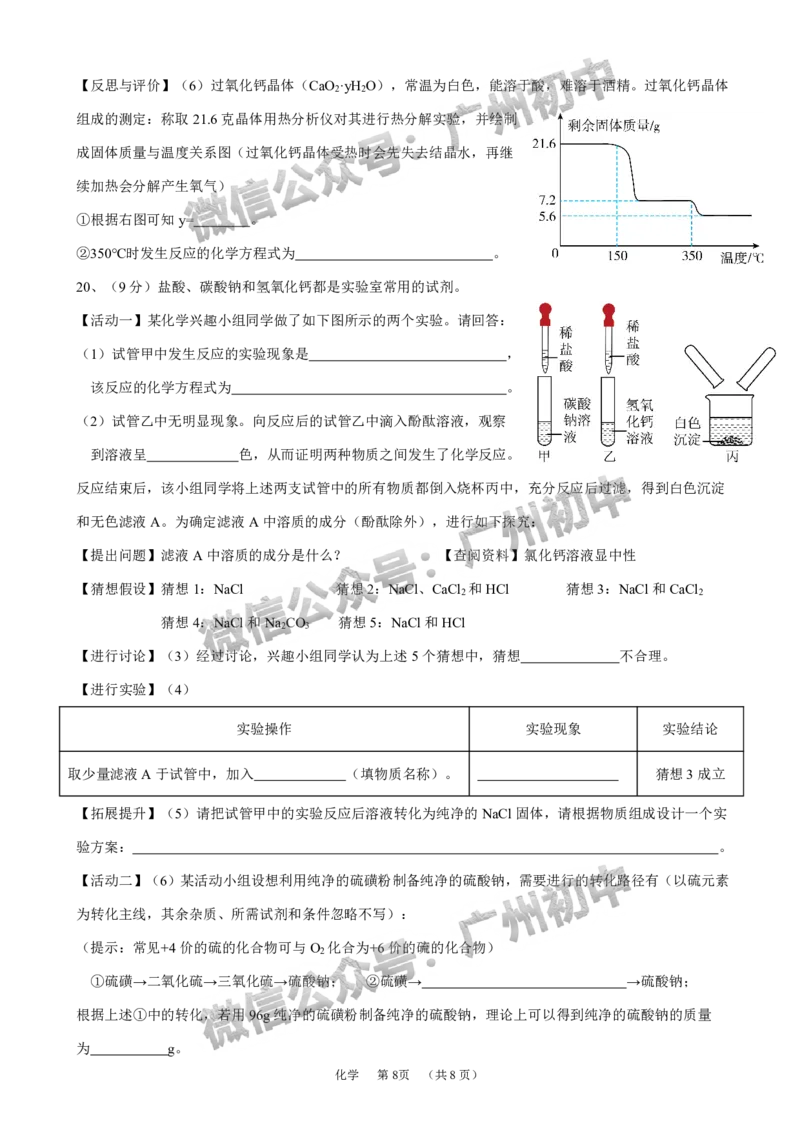
{#{QQABRYEk4gC4gAbACR4LEUX4CAgQkJKjJaoMwQCfKARLQAFAFIA=}#}【反思与评价】(6)过氧化钙晶体(CaO ·yH O),常温为白色,能溶于酸,难溶于酒精。过氧化钙晶体
2 2
组成的测定:称取21.6克晶体用热分析仪对其进行热分解实验,并绘制
成固体质量与温度关系图(过氧化钙晶体受热时会先失去结晶水,再继
续加热会分解产生氧气)
①根据右图可知y= 。
②350℃时发生反应的化学方程式为 。
20、(9分)盐酸、碳酸钠和氢氧化钙都是实验室常用的试剂。
【活动一】某化学兴趣小组同学做了如下图所示的两个实验。请回答:
(1)试管甲中发生反应的实验现象是 ,
该反应的化学方程式为 。
(2)试管乙中无明显现象。向反应后的试管乙中滴入酚酞溶液,观察
到溶液呈 色,从而证明两种物质之间发生了化学反应。
反应结束后,该小组同学将上述两支试管中的所有物质都倒入烧杯丙中,充分反应后过滤,得到白色沉淀
和无色滤液A。为确定滤液A中溶质的成分(酚酞除外),进行如下探究:
【提出问题】滤液A中溶质的成分是什么? 【查阅资料】氯化钙溶液显中性
【猜想假设】猜想1:NaCl 猜想2:NaCl、CaCl 和HCl 猜想3:NaCl和CaCl
2 2
猜想4:NaCl和Na CO 猜想5:NaCl和HCl
2 3
【进行讨论】(3)经过讨论,兴趣小组同学认为上述5个猜想中,猜想 不合理。
【进行实验】(4)
实验操作 实验现象 实验结论
取少量滤液A于试管中,加入 (填物质名称)。 猜想3成立
【拓展提升】(5)请把试管甲中的实验反应后溶液转化为纯净的NaCl固体,请根据物质组成设计一个实
验方案: 。
【活动二】(6)某活动小组设想利用纯净的硫磺粉制备纯净的硫酸钠,需要进行的转化路径有(以硫元素
为转化主线,其余杂质、所需试剂和条件忽略不写):
(提示:常见+4价的硫的化合物可与O 化合为+6价的硫的化合物)
2
①硫磺→二氧化硫→三氧化硫→硫酸钠; ②硫磺→ →硫酸钠;
根据上述①中的转化,若用96g纯净的硫磺粉制备纯净的硫酸钠,理论上可以得到纯净的硫酸钠的质量
为 g。
化学 第8页 (共8页)
{#{QQABRYEk4gC4gAbACR4LEUX4CAgQkJKjJaoMwQCfKARLQAFAFIA=}#}