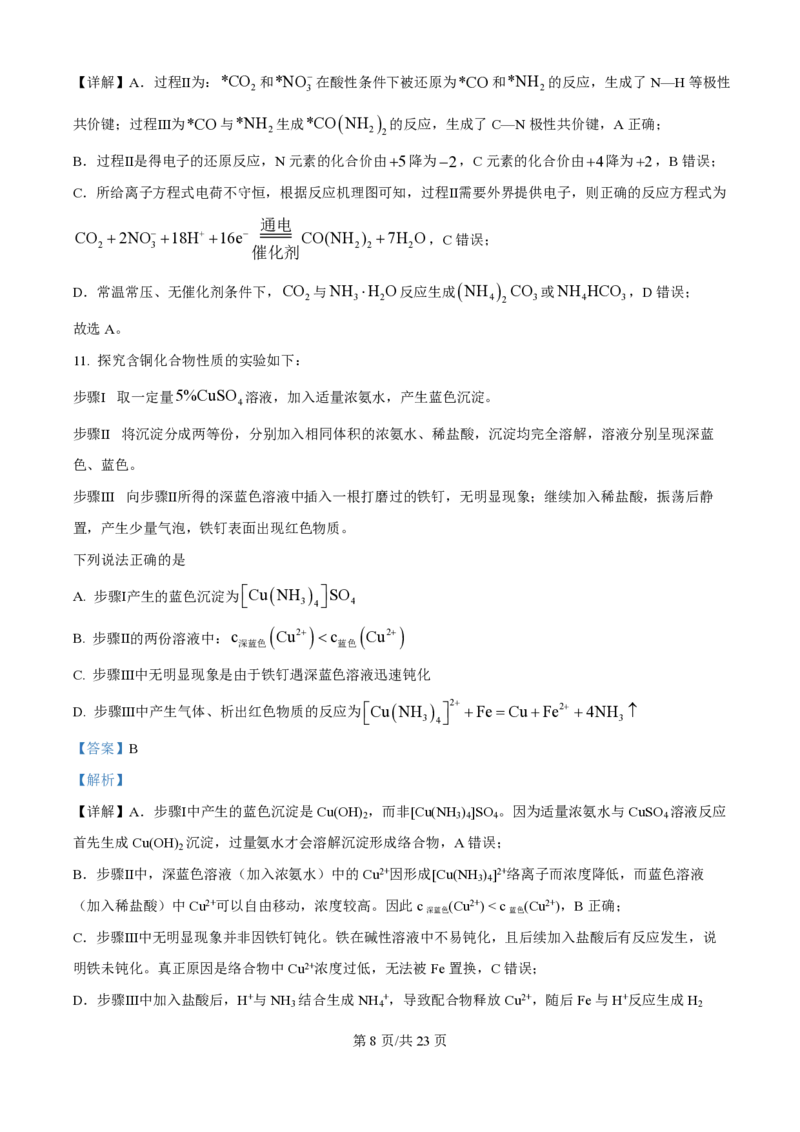文档内容
2025 年普通高中学业水平选择性考试(江苏卷)
化学
本试卷满分 100分,考试时间 75分钟。
H— 1 C— 12 O— 16 S— 32 Cl— 35.5 K— 39
可能用到的相对原子质量:
Fe— 56 Zn— 65 As— 75 Cd— 112 Ce— 140
一、单项选择题:共 13题,每题 3分,共 39分。每题只有一个选项最符合题意。
1. 大气中的氮是取之不尽的天然资源。下列工业生产中以氮气作反应物的是
A. 工业合成氨 B. 湿法炼铜 C. 高炉炼铁 D. 接触法制硫酸
【答案】A
【解析】
【详解】A.工业合成氨的反应为N 和H 反应生成NH ,氮气是直接反应物,A正确;
2 2 3
B.湿法炼铜通过Fe置换CuSO 中的Cu,反应不涉及氮气,B错误;
4
C.高炉炼铁中氮气作为空气成分进入高炉,但未参与还原铁矿石的主要反应,C错误;
D.接触法制硫酸涉及硫或硫化物的氧化,氮气未参与反应,D错误;
故选A。
2. 科学家通过核反应1n+6 Li®3 H+4 He发现氚 3H 。下列说法正确的是
0 3 1 2 1
A. 1n表示一个质子
0
B. 6Li的基态原子核外电子排布式为1s12s2
3
C. 3H与2H互为同位素
1 1
D. 4He的原子结构示意图为
2
【答案】C
【解析】
【详解】A.1n质量数为1,质子数为0,中子数为1,因此其表示一个中子,A错误;
0
B.6Li的基态原子核外电子排布式为1s22s1,B错误;
3
C.质子数相同而中子数不同的同一元素的不同原子互称为同位素,3H与2H质子数相同、中子数不同,
1 1
第1页/共23页
学科网(北京)股份有限公司二者互为同位素,C正确;
D.4He原子核外只有2个电子,原子结构示意图为 ,D错误。
2
故选C。
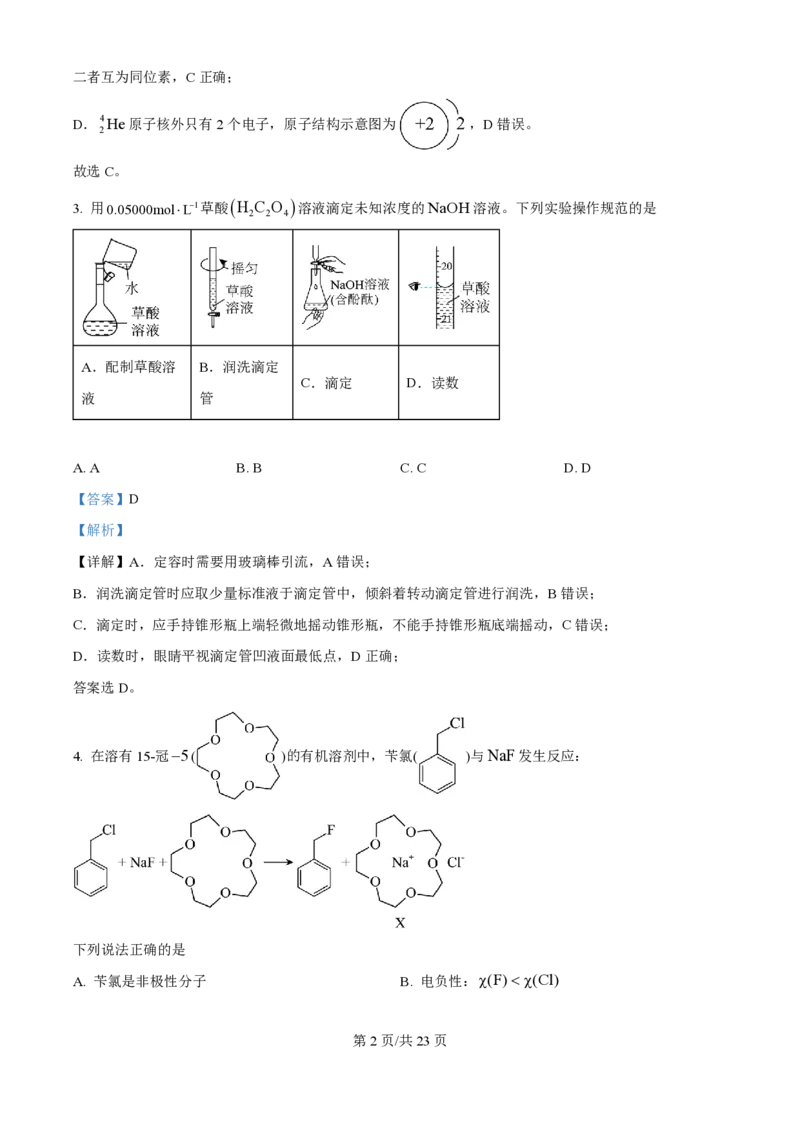
3. 用0.05000mol×L-1草酸 H C O 溶液滴定未知浓度的NaOH溶液。下列实验操作规范的是
2 2 4
A.配制草酸溶 B.润洗滴定
C.滴定 D.读数
液 管
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.定容时需要用玻璃棒引流,A错误;
B.润洗滴定管时应取少量标准液于滴定管中,倾斜着转动滴定管进行润洗,B错误;
C.滴定时,应手持锥形瓶上端轻微地摇动锥形瓶,不能手持锥形瓶底端摇动,C错误;
D.读数时,眼睛平视滴定管凹液面最低点,D正确;
答案选D。
4. 在溶有15-冠-5( )的有机溶剂中,苄氯( )与NaF发生反应:
下列说法正确的是
A. 苄氯是非极性分子 B. 电负性:χ(F)<χ(Cl)
第2页/共23页
学科网(北京)股份有限公司C. 离子半径:r
F-
>r
Na+
D. X中15-冠-5与Na+间存在离子键
【答案】C
【解析】
【详解】A.苄氯分子含有饱和C原子,且饱和碳原子连有三种不同的基团,分子空间结构不对称,故苄氯
为极性分子,A错误;
B.同主族元素从上到下电负性逐渐减小,故电负性:χF>χCl
,B错误;
C.电子层结构相同时,离子半径随原子序数增大而减小,故离子半径:r
F-
>r
Na+
,C正确;
D.15-冠-5是分子,与阳离子Na+之间不存在离子键,二者通过非共价键形成超分子,D错误;
故选C。
阅读材料,完成下列小题:
中国对人类科学进步与技术发展贡献卓著。黑火药(主要成分:KNO 、S和C)是中国古代四大发明之
3
一。侯德榜发明的“联合制碱法”将合成氨法与氨碱法联合,突破了国外制碱技术封锁。我国科学家在世界
上首次人工合成结晶牛胰岛素;采用有机合成与酶促合成相结合的方法,人工合成了酵母丙氨酸转移核糖
核酸。徐光宪提出的稀土串级萃取理论使我国稀土提取技术取得重大进步。屠呦呦等采用低温、乙醚冷浸
提取的青蒿素(C H O ,含— O— O— )在治疗疟疾中起到重要作用。闵恩泽研制新型催化剂解决了重
15 22 5
油裂解难题。
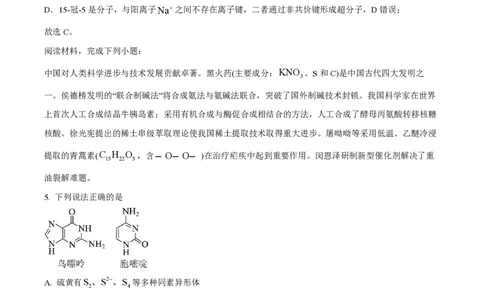
5. 下列说法正确的是
A. 硫黄有S、S2-、S 等多种同素异形体
2 4
B. 高温下青蒿素分子结构稳定
C. NH 分子中H— N— H键角大于CH 分子中H— C— H键角
3 4
D. 题图所示的碱基鸟嘌呤与胞嘧啶通过氢键互补配对
6. 下列化学反应表示正确的是
A. 黑火药爆炸:2KNO +C+3S=K CO +N +3SO
3 2 3 2 2
第3页/共23页
学科网(北京)股份有限公司通电
B. 电解饱和NaCl溶液制NaOH:Cl- +2H O 2OH- +H +ClO-
2 2
C. 重油裂解获得的丙烯制聚丙烯:nCH =CH-CH ¾催¾化¾剂®
2 3
D. 向饱和氨盐水中通入过量CO :NaCl+NH +H O+CO = NaHCO ¯+NH Cl
2 3 2 2 3 4
7. 下列物质组成或性质与分离提纯方法对应关系正确的是
A. 蛋白质能水解,可用饱和 NH SO 溶液提纯蛋白质
4 2 4
B. 乙醚与青蒿素组成元素相同,可用乙醚提取青蒿素
C. CCl 难溶于水、比水易溶解I ,可用CCl 萃取碘水中的I
4 2 4 2
D. 不同的烃密度不同,可通过分馏从石油中获得汽油、柴油
【答案】5. D 6. D 7. C
【解析】
【5题详解】
A.同素异形体是同种元素形成的不同单质间的互称,S2-是离子不是单质,A错误;
B.根据信息可知青蒿素中含有—O—O—,类比双氧水的分子结构可知其不稳定,高温条件下易分解,B
错误;
1
C.NH 中心原子N原子价层电子对数为3+ ´5-1´3=4,采用sp3杂化,孤电子对数为1,CH 中
3 2 4
1
心原子C原子价层电子对数为4+ ´4-1´4=4,采用sp3杂化,孤电子对数为0,中心原子杂化方式
2
相同时,孤电子对数越多,孤电子对对成键电子对的排斥力越大,键角越小,则NH 分子中H—N—H键
3
角小于CH 分子中H—C—H键角,C错误;
4
D.鸟嘌呤、胞嘧啶中含有-NH-、-NH 、O原子、N原子,可形成氢键,从而实现互补配对,如图所
2
示: ,D正确。
故选D。
【6题详解】
第4页/共23页
学科网(北京)股份有限公司A.黑火药爆炸时,KNO 、C和S反应生成K S、N 和CO ,该反应的化学方程式为
3 2 2 2
2KNO +3C+S= K S+N +3CO ,A错误;
3 2 2 2
B.电解饱和NaCl溶液生成Cl 、H 和NaOH,该反应的离子方程式为
2 2
通电
2Cl- +2H O H +Cl +2OH-,B错误;
2 2 2
催化剂
nCH =CH-CH ® [CH -CH]
C.丙烯生成聚丙烯的反应为 2 3 2 | n ,C错误;
CH
3
D.向饱和氨盐水中通入过量CO 生成NH Cl和溶解度较小的NaHCO ,NaHCO 结晶析出,D正
2 4 3 3
确。
故选D。
【7题详解】
A.蛋白质在饱和 NH SO 溶液中会发生盐析,故可用饱和 NH SO 溶液分离提纯蛋白质,与蛋
4 2 4 4 2 4
白质能发生水解反应无关,A错误;
B.青蒿素在乙醚中的溶解度较大,故可用乙醚提取青蒿素,与二者的组成元素无关,B错误;
C.I 在CCl 中的溶解度大于在水中的溶解度,且CCl 与水不互溶,故可用CCl 萃取碘水中的I ,C
2 4 4 4 2
正确;
D.不同烃的沸点不同,故可用分馏法从石油中获得汽油、柴油,与烃的密度无关,D错误。
故选C。
光
8. 以稀H SO 为电解质溶液的光解水装置如图所示,总反应为2H O 2H +O 。下列说法正
2 4 2 2 2
催化剂
确的是
A. 电极a上发生氧化反应生成O
2
第5页/共23页
学科网(北京)股份有限公司B. H+通过质子交换膜从右室移向左室
C. 光解前后,H SO 溶液的pH不变
2 4
D. 外电路每通过0.01mol电子,电极b上产生0.01molH
2
【答案】A
【解析】
【分析】光解过程中,电极a上电子流出,发生氧化反应,a为负极,电极反应式为:2H O-4e- =O +4H+;
2 2
电极b上电子流入,发生还原反应,b为正极,电极反应式为:2H+ +2e- =H 。
2
【详解】A.根据分析,电极a为负极,发生氧化反应,电极反应式为:2H O-4e- =O +4H+,生
2 2
成物有O ,A正确;
2
B.原电池中阳离子向正极移动,电极a上生成H+,电极b上消耗H+,H+通过质子交换膜从左室移向
右室,B错误;
C.在探究溶液浓度变化时,不仅要关注溶质的变化,也要关注溶剂的变化,在光解总反应是电解水,
H SO 溶液中H O减少,H SO 溶液浓度增大,pH减小,C错误;
2 4 2 2 4
D.生成1molH ,转移2mol电子,外电路通过0.01mol电子时,电极b上生成0.005molH ,D错误;
2 2
答案选A。
9. 化合物Z是一种具有生理活性的多环呋喃类化合物,部分合成路线如下:
下列说法正确的是
A. 1molX最多能和4molH 发生加成反应
2
B. Y分子中
sp3
和sp2杂化的碳原子数目比为1:2
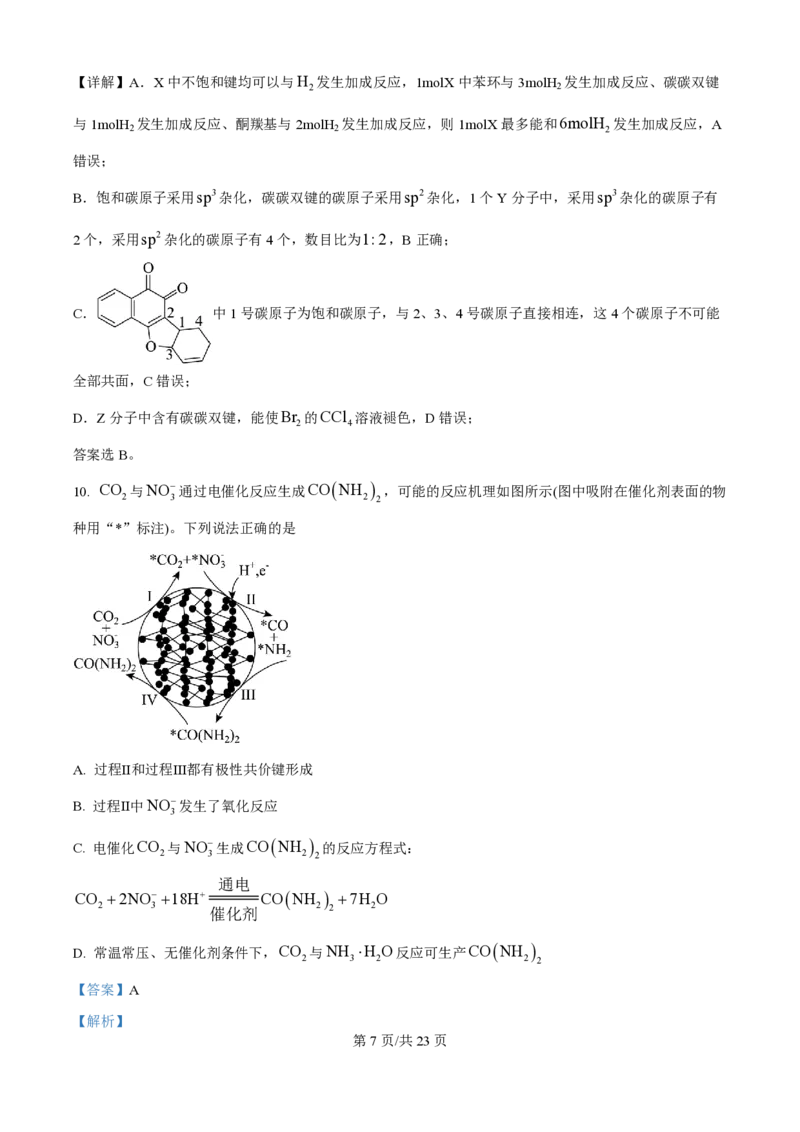
C. Z分子中所有碳原子均在同一个平面上
D. Z不能使Br 的CCl 溶液褪色
2 4
【答案】B
【解析】
第6页/共23页
学科网(北京)股份有限公司【详解】A.X中不饱和键均可以与H 发生加成反应,1molX中苯环与3molH 发生加成反应、碳碳双键
2 2
与1molH 发生加成反应、酮羰基与2molH 发生加成反应,则1molX最多能和6molH 发生加成反应,A
2 2 2
错误;
B.饱和碳原子采用sp3杂化,碳碳双键的碳原子采用sp2杂化,1个Y分子中,采用sp3杂化的碳原子有
2个,采用sp2杂化的碳原子有4个,数目比为1:2,B正确;
C. 中1号碳原子为饱和碳原子,与2、3、4号碳原子直接相连,这4个碳原子不可能
全部共面,C错误;
D.Z分子中含有碳碳双键,能使Br 的CCl 溶液褪色,D错误;
2 4
答案选B。
10. CO 与NO-通过电催化反应生成CONH ,可能的反应机理如图所示(图中吸附在催化剂表面的物
2 3 2 2
种用“*”标注)。下列说法正确的是
A. 过程Ⅱ和过程Ⅲ都有极性共价键形成
B. 过程Ⅱ中NO-发生了氧化反应
3
C. 电催化CO 与NO-生成CONH 的反应方程式:
2 3 2 2
通电
CO +2NO- +18H+ CONH +7H O
2 3 催化剂 2 2 2
D. 常温常压、无催化剂条件下,CO 与NH ×H O反应可生产CONH
2 3 2 2 2
【答案】A
【解析】
第7页/共23页
学科网(北京)股份有限公司【详解】A.过程Ⅱ为:*CO 和*NO-在酸性条件下被还原为*CO和*NH 的反应,生成了N—H等极性
2 3 2
共价键;过程Ⅲ为*CO与*NH 生成*CONH 的反应,生成了C—N极性共价键,A正确;
2 2 2
B.过程Ⅱ是得电子的还原反应,N元素的化合价由+5降为-2,C元素的化合价由+4降为+2,B错误;
C.所给离子方程式电荷不守恒,根据反应机理图可知,过程Ⅱ需要外界提供电子,则正确的反应方程式为
通电
CO +2NO- +18H+ +16e- CO(NH ) +7H O,C错误;
2 3 催化剂 2 2 2
D.常温常压、无催化剂条件下,CO 与NH ×H O反应生成 NH CO 或NH HCO ,D错误;
2 3 2 4 2 3 4 3
故选A。
11. 探究含铜化合物性质的实验如下:
步骤Ⅰ 取一定量5%CuSO 溶液,加入适量浓氨水,产生蓝色沉淀。
4
步骤Ⅱ 将沉淀分成两等份,分别加入相同体积的浓氨水、稀盐酸,沉淀均完全溶解,溶液分别呈现深蓝
色、蓝色。
步骤Ⅲ 向步骤Ⅱ所得的深蓝色溶液中插入一根打磨过的铁钉,无明显现象;继续加入稀盐酸,振荡后静
置,产生少量气泡,铁钉表面出现红色物质。
下列说法正确的是
A. 步骤Ⅰ产生的蓝色沉淀为é ë CuNH 3 4 ù û SO 4
B. 步骤Ⅱ的两份溶液中:c
Cu2+
n
Na+
,同时“沉镍”
提铜 沉镍
过程中加入了 NH C O 溶液,溶液体积增加,因此c Na+ >c Na+ ,D错误;
4 2 2 4 提铜 沉镍
故选B。
13. 甘油 C H O 水蒸气重整获得H 过程中的主要反应:
3 8 3 2
反应Ⅰ C H O (g)=3CO(g)+4H (g) DH>0
3 8 3 2
反应Ⅱ CO(g)+H O(g)=CO (g)+H (g) DH<0
2 2 2
反应Ⅲ CO (g)+4H (g)=CH (g)+2H O(g) DH<0
2 2 4 2
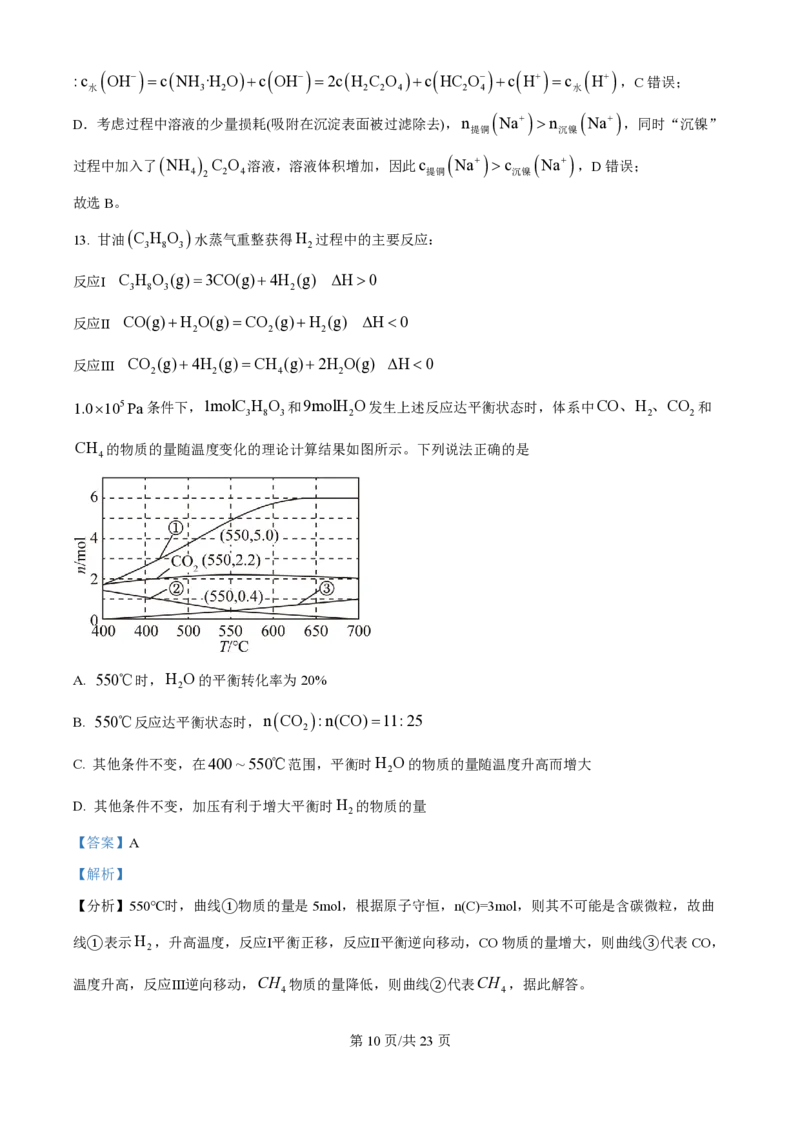
1.0´105Pa条件下,1molC H O 和9molH O发生上述反应达平衡状态时,体系中CO、H 、CO 和
3 8 3 2 2 2
CH 的物质的量随温度变化的理论计算结果如图所示。下列说法正确的是
4
A. 550℃时,H O的平衡转化率为20%
2
B.
550℃反应达平衡状态时,nCO :n(CO)=11:25
2
C. 其他条件不变,在400~550℃范围,平衡时H O的物质的量随温度升高而增大
2
D. 其他条件不变,加压有利于增大平衡时H 的物质的量
2
【答案】A
【解析】
【分析】550℃时,曲线①物质的量是5mol,根据原子守恒,n(C)=3mol,则其不可能是含碳微粒,故曲
线①表示H ,升高温度,反应Ⅰ平衡正移,反应Ⅱ平衡逆向移动,CO物质的量增大,则曲线③代表CO,
2
温度升高,反应Ⅲ逆向移动,CH 物质的量降低,则曲线②代表CH ,据此解答。
4 4
第10页/共23页
学科网(北京)股份有限公司【详解】A.550℃时,nH =5mol,nCO =2.2mol,nCH =nCO=0.4mol,根据C原子
2 2 4
nC-nCO -nCO-nCH
守 恒 , 可 得 nC H O = 2 4 =0, 根 据 O 原 子 守 恒 , 可 得
3 8 3 3
nO-2nCO -nCO-3nC H O
nH O= 2 3 8 3 =7.2mol(也可利用 H 原子守恒计算,结果相同),
2 1
9mol-7.2mol
则αH O= ´100%=20%,A正确;
2 9mol
B.550℃时,nCO =2.2mol,nCO=0.4mol,则nCO :nCO=11:2,B错误;
2 2
C.400~550℃范围,随温度升高,反应Ⅱ、Ⅲ平衡均逆向移动,nCO
增大,说明反应Ⅲ逆向移动程
2
度更大,则H O的物质的量减小,C错误;
2
D.增大压强,反应Ⅰ平衡逆向移动,反应Ⅱ平衡不移动,反应Ⅲ平衡正向移动,H 的物质的量减小,D错
2
误;
故选A。
二、非选择题:共 4题,共 61分。
14. ZnS可用于制备光学材料和回收砷。
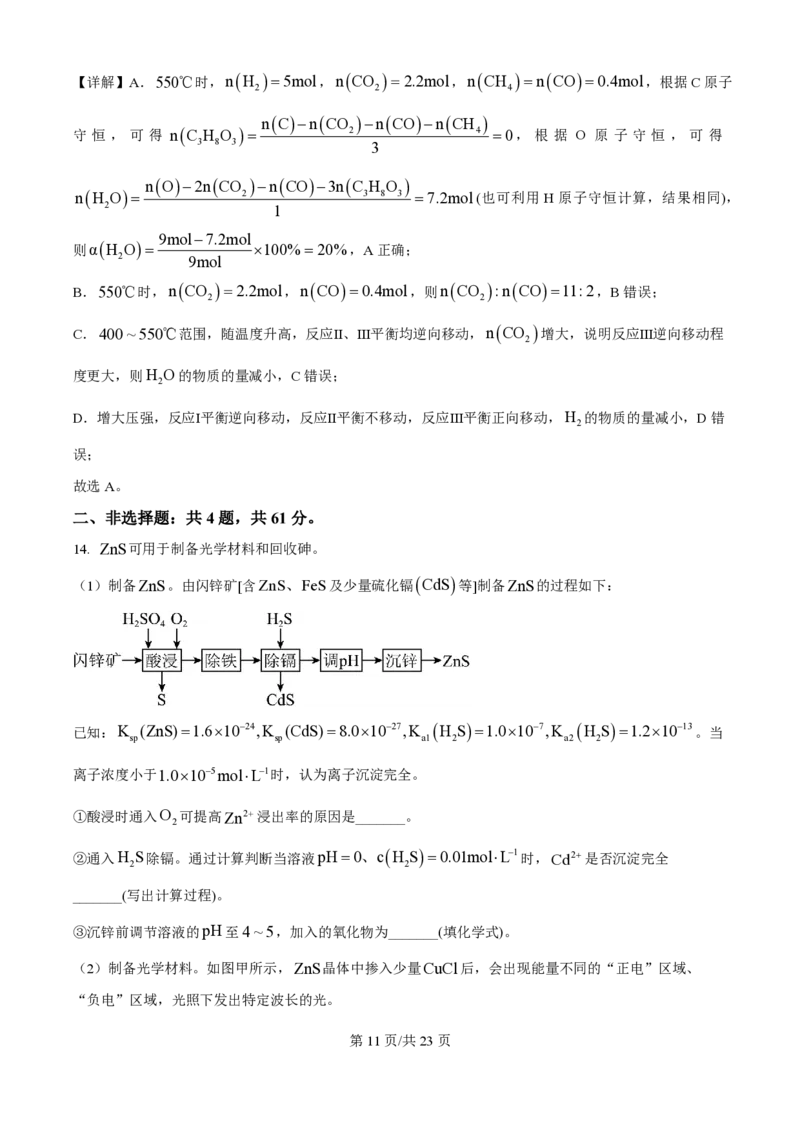
(1)制备ZnS。由闪锌矿[含ZnS、FeS及少量硫化镉 CdS 等]制备ZnS的过程如下:
已知:K (ZnS)=1.6´10-24,K (CdS)=8.0´10-27,K H S=1.0´10-7,K H S=1.2´10-13。当
sp sp a1 2 a2 2
离子浓度小于1.0´10-5mol×L-1时,认为离子沉淀完全。
①酸浸时通入O 可提高Zn2+浸出率的原因是_______。
2
②通入H S除镉。通过计算判断当溶液pH=0、cH S=0.01mol×L-1时,Cd2+是否沉淀完全
2 2
_______(写出计算过程)。
③沉锌前调节溶液的pH至4~5,加入的氧化物为_______(填化学式)。
(2)制备光学材料。如图甲所示,ZnS晶体中掺入少量CuCl后,会出现能量不同的“正电”区域、
“负电”区域,光照下发出特定波长的光。
第11页/共23页
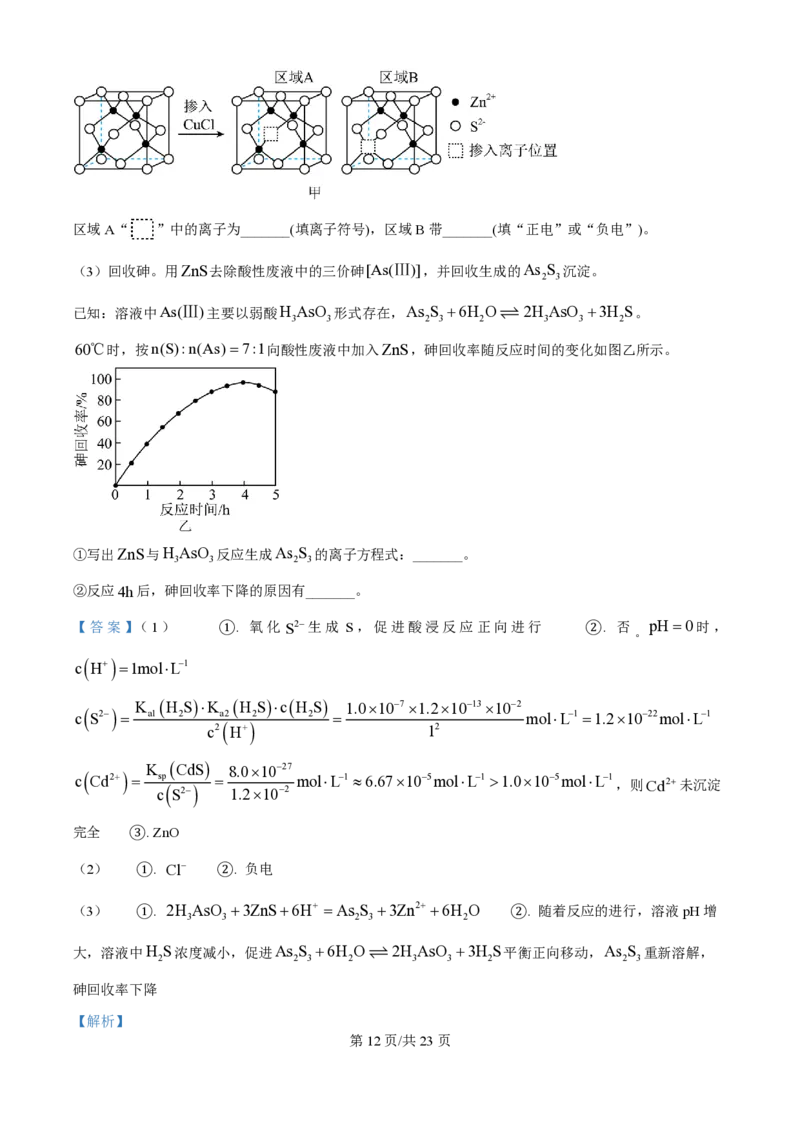
学科网(北京)股份有限公司区域A“ ”中的离子为_______(填离子符号),区域B带_______(填“正电”或“负电”)。
(3)回收砷。用ZnS去除酸性废液中的三价砷[As(Ⅲ)],并回收生成的As S 沉淀。
2 3
已知:溶液中As(Ⅲ)主要以弱酸H
3
AsO
3
形式存在,As
2
S
3
+6H
2
O
ƒ
2H
3
AsO
3
+3H
2
S。
60℃时,按n(S):n(As)=7:1向酸性废液中加入ZnS,砷回收率随反应时间的变化如图乙所示。
①写出ZnS与H AsO 反应生成As S 的离子方程式:_______。
3 3 2 3
②反应4h后,砷回收率下降的原因有_______。
【答案】(1) ①. 氧化 S2-生成 S,促进酸浸反应正向进行 ②. 否 pH=0时,
。
c H+ =1mol×L-1
K H S×K H S×cH S 1.0´10-7´1.2´10-13´10-2
c S2- = a1 2 a2 2 2 = mol×L-1 =1.2´10-22mol×L-1
c2 H+ 12
K CdS 8.0´10-27
c Cd2+ =
c
sp
S2-
=
1.2´10-2
mol×L-1 »6.67´10-5mol×L-1 >1.0´10-5mol×L-1 ,则Cd2+未沉淀
完全 ③. ZnO
(2) ①. Cl- ②. 负电
(3) ①. 2H AsO +3ZnS+6H+ = As S +3Zn2+ +6H O ②. 随着反应的进行,溶液pH增
3 3 2 3 2
大,溶液中H 2 S浓度减小,促进As 2 S 3 +6H 2 O ƒ 2H 3 AsO 3 +3H 2 S平衡正向移动,As 2 S 3 重新溶解,
砷回收率下降
【解析】
第12页/共23页
学科网(北京)股份有限公司【分析】闪锌矿中含 ZnS、FeS、CdS 等,加入 H SO 、O 酸浸后,ZnS、FeS、CdS 分别转化为
2 4 2
Zn2+、Fe3+、Cd2+,硫元素转化为硫单质,经过除铁、除镉除去Fe3+与Cd2+,调pH、沉锌后获得ZnS,
据此解答。
【小问1详解】
①酸浸时,若不通入O
2
,会发生反应:ZnS+H
2
SO
4 ƒ
ZnSO
4
+H
2
S,通入O
2
可以氧化S2-生成S,
促进酸浸反应正向进行,提高Zn2+浸出率;
② 通 入 H S除 镉 , 当 溶 液 pH=0、cH S=0.01mol×L-1时 , c H+ =1mol×L-1, 又 因 为
2 2
K H S=1.0´10-7,K H S=1.2´10-13,
a1 2 a2 2
c(H+)´c(HS-) c(H+)´c(S2-) c2(H+)´c(S2-)
K H S´K H S= ´ = , 则
a1 2 a2 2 c(H S) c(HS-) c(H S)
2 2
1´10-7´1.2´10-13´0.01
c
S2-
= mol/L==1.2´10-22mol/L, 则 此 时
12
K (CdS) 8.0´10-27
c Cd2+ =
c
sp
S2-
=
1.2´10-22
mol/L=6.6´10-5mol/L ,此时Cd2+的浓度大于1.0´10-5mol×L-1,离子
沉淀不完全。
③由②知,除镉时溶液酸性较强,故应在不引入新杂质的同时消耗溶液中的H+,加入的氧化物为ZnO。
【小问2详解】
晶胞掺杂过程中,应由半径相近的微粒进行替换,则区域A中,由Cl-替换S2-,区域B中,由Cu+替换
1 1
Zn2+;按照均摊法,区域B中含Zn2+:3个、Cu+:1个、S2-:8´ +6´ =4个,
8 2
+2´3++1´1+-2´4=-1,则区域B带负电。
【小问3详解】
①根据质量守恒、电荷守恒和题给信息“酸性废液”, ZnS与H AsO 反应除了生成As S 外还有锌离
3 3 2 3
子,写出反应的离子方程式为:2H AsO +3ZnS+6H+ = As S +3Zn2+ +6H O。
3 3 2 3 2
②随着反应的进行,溶液pH增大,溶液中H
2
S浓度减小,促进As
2
S
3
+6H
2
O
ƒ
2H
3
AsO
3
+3H
2
S平衡
正向移动,As S 重新溶解,砷回收率下降,所以反应4h后,砷回收率下降。
2 3
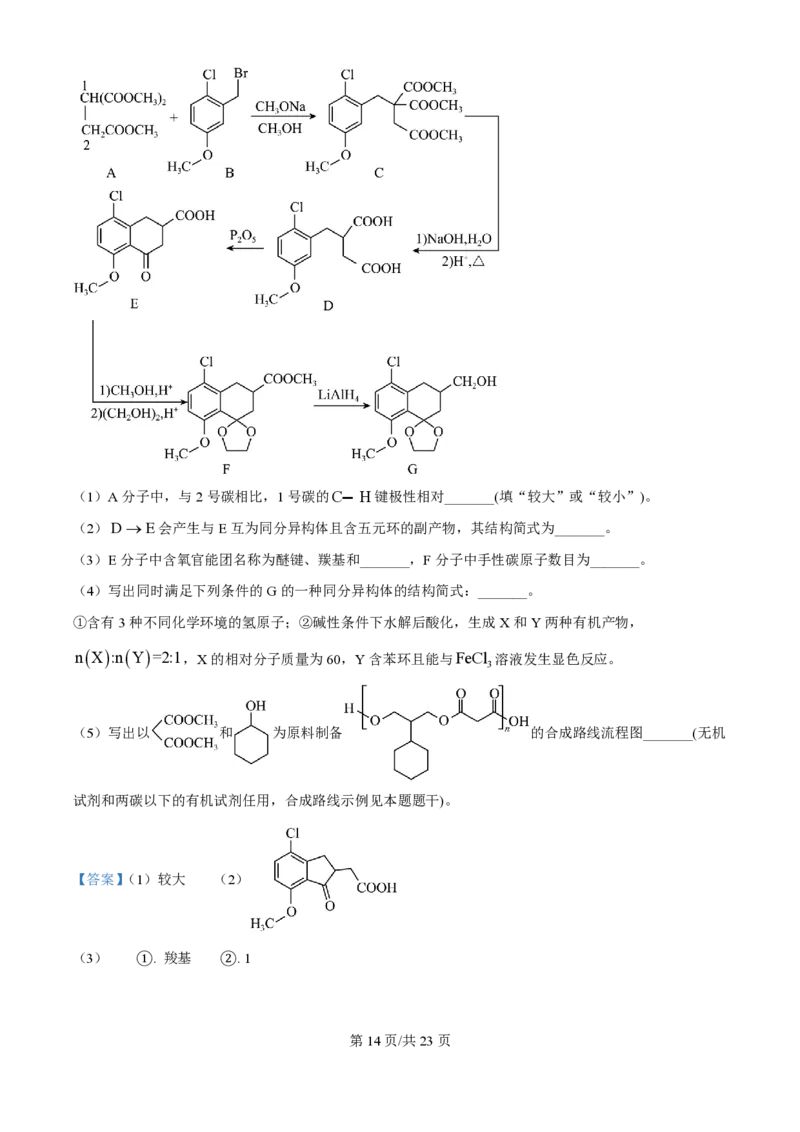
15. G是一种四环素类药物合成中间体,其合成路线如下:
第13页/共23页
学科网(北京)股份有限公司(1)A分子中,与2号碳相比,1号碳的C— H键极性相对_______(填“较大”或“较小”)。
(2)D®E会产生与E互为同分异构体且含五元环的副产物,其结构简式为_______。
(3)E分子中含氧官能团名称为醚键、羰基和_______,F分子中手性碳原子数目为_______。
(4)写出同时满足下列条件的G的一种同分异构体的结构简式:_______。
①含有3种不同化学环境的氢原子;②碱性条件下水解后酸化,生成X和Y两种有机产物,
nX:nY=2:1,X的相对分子质量为60,Y含苯环且能与FeCl
溶液发生显色反应。
3
(5)写出以 和 为原料制备 的合成路线流程图_______(无机
试剂和两碳以下的有机试剂任用,合成路线示例见本题题干)。
【答案】(1)较大 (2)
(3) ①. 羧基 ②. 1
第14页/共23页
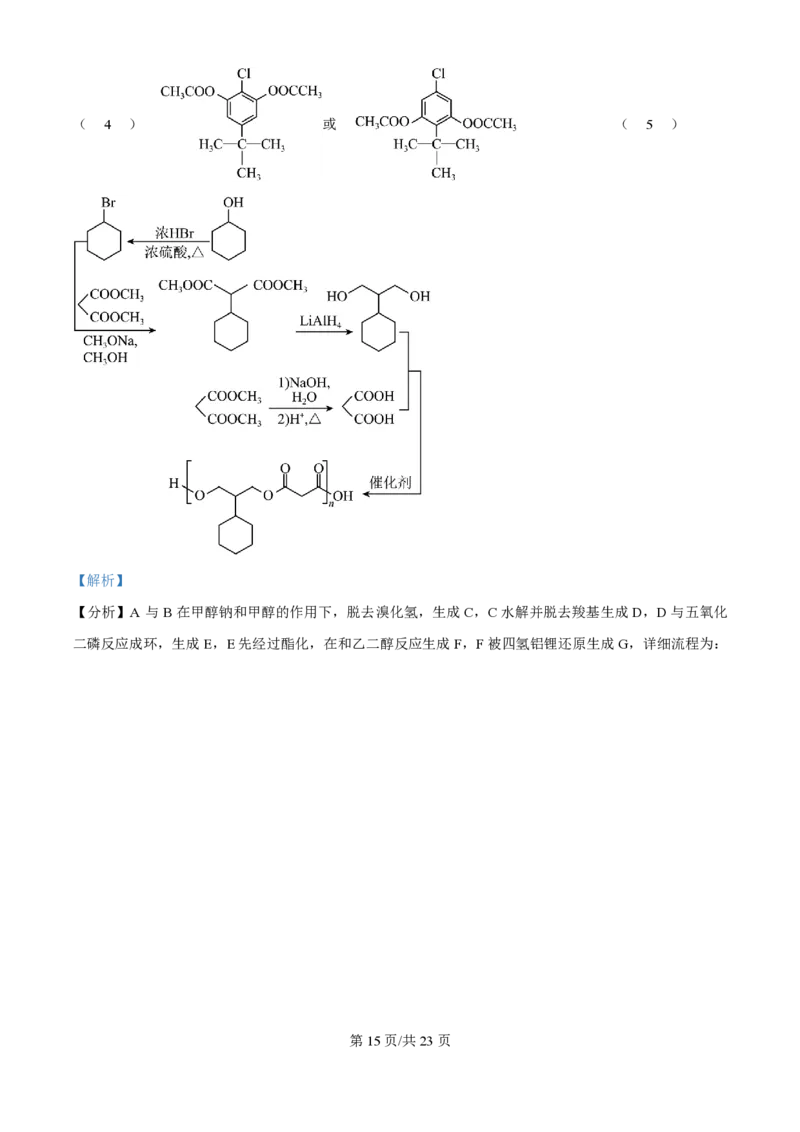
学科网(北京)股份有限公司( 4 ) 或 ( 5 )
【解析】
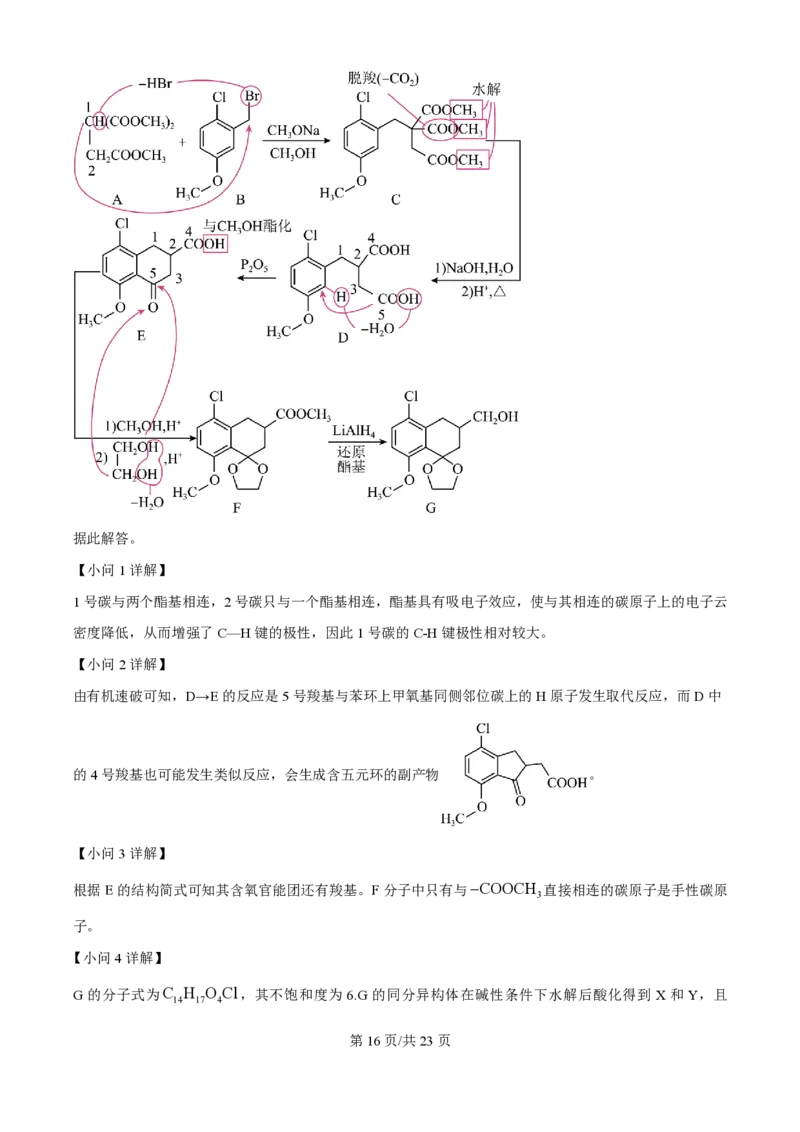
【分析】A 与B在甲醇钠和甲醇的作用下,脱去溴化氢,生成C,C水解并脱去羧基生成D,D与五氧化
二磷反应成环,生成E,E先经过酯化,在和乙二醇反应生成F,F被四氢铝锂还原生成G,详细流程为:
第15页/共23页
学科网(北京)股份有限公司据此解答。
【小问1详解】
1号碳与两个酯基相连,2号碳只与一个酯基相连,酯基具有吸电子效应,使与其相连的碳原子上的电子云
密度降低,从而增强了C—H键的极性,因此1号碳的C-H键极性相对较大。
【小问2详解】
由有机速破可知,D→E的反应是5号羧基与苯环上甲氧基同侧邻位碳上的H原子发生取代反应,而D中
的4号羧基也可能发生类似反应,会生成含五元环的副产物 。
【小问3详解】
根据E的结构简式可知其含氧官能团还有羧基。F分子中只有与-COOCH 直接相连的碳原子是手性碳原
3
子。
【小问4详解】
G 的分子式为C H O Cl,其不饱和度为 6.G 的同分异构体在碱性条件下水解后酸化得到 X 和 Y,且
14 17 4
第16页/共23页
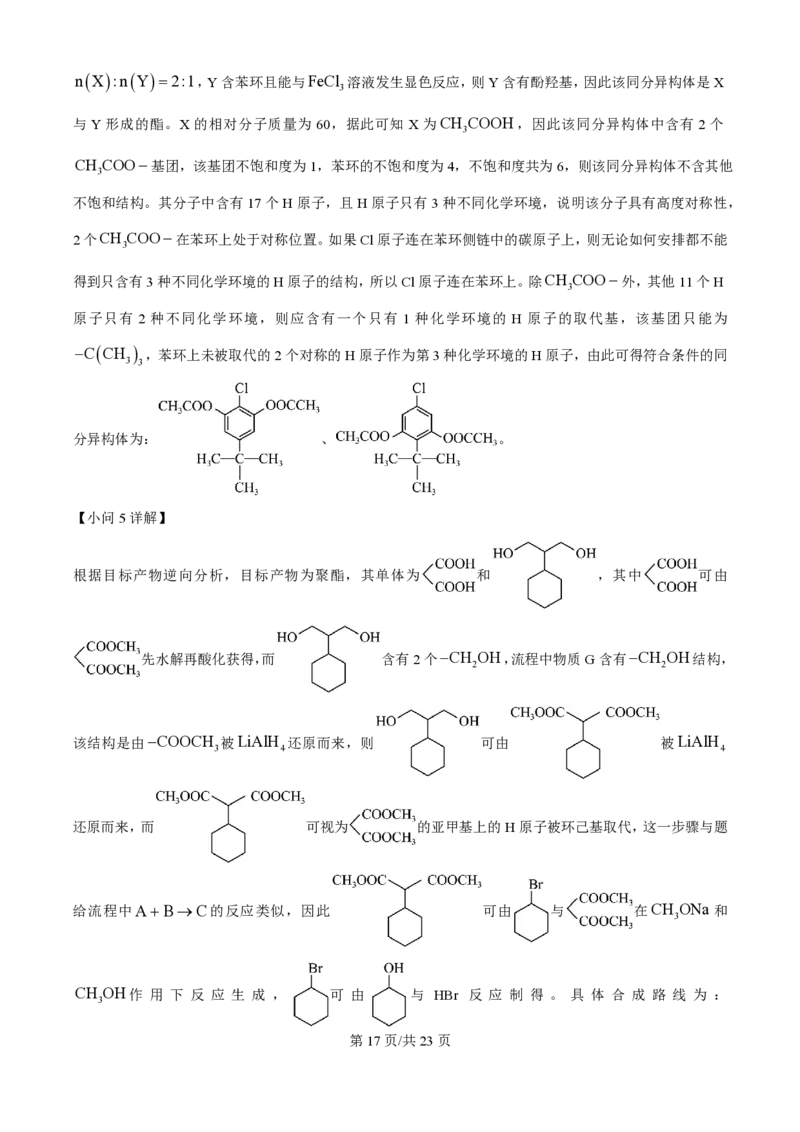
学科网(北京)股份有限公司nX:nY=2:1,Y含苯环且能与FeCl
溶液发生显色反应,则Y含有酚羟基,因此该同分异构体是X
3
与 Y 形成的酯。X 的相对分子质量为 60,据此可知 X 为CH COOH,因此该同分异构体中含有 2 个
3
CH COO-基团,该基团不饱和度为1,苯环的不饱和度为4,不饱和度共为6,则该同分异构体不含其他
3
不饱和结构。其分子中含有17个H原子,且H原子只有3种不同化学环境,说明该分子具有高度对称性,
2个CH COO-在苯环上处于对称位置。如果Cl原子连在苯环侧链中的碳原子上,则无论如何安排都不能
3
得到只含有3种不同化学环境的H原子的结构,所以Cl原子连在苯环上。除CH COO-外,其他11个H
3
原子只有 2 种不同化学环境,则应含有一个只有 1 种化学环境的 H 原子的取代基,该基团只能为
-CCH
,苯环上未被取代的2个对称的H原子作为第3种化学环境的H原子,由此可得符合条件的同
3 3
分异构体为: 、 。
【小问5详解】
根据目标产物逆向分析,目标产物为聚酯,其单体为 和 ,其中 可由
先水解再酸化获得,而 含有2个-CH OH,流程中物质G含有-CH OH结构,
2 2
该结构是由-COOCH 被LiAlH 还原而来,则 可由 被LiAlH
3 4 4
还原而来,而 可视为 的亚甲基上的H原子被环己基取代,这一步骤与题
给流程中A+B®C的反应类似,因此 可由 与 在CH ONa 和
3
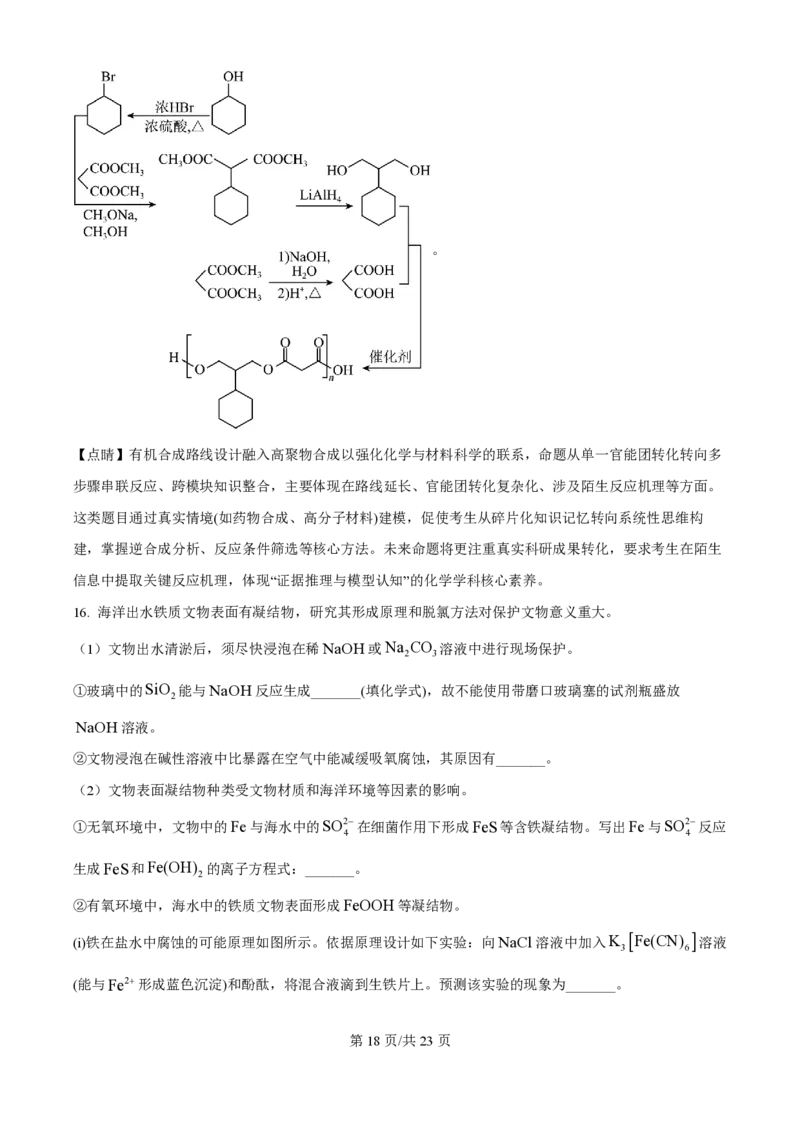
CH OH作 用 下 反 应 生 成 , 可 由 与 HBr 反 应 制 得 。 具 体 合 成 路 线 为 :
3
第17页/共23页
学科网(北京)股份有限公司。
【点睛】有机合成路线设计融入高聚物合成以强化化学与材料科学的联系,命题从单一官能团转化转向多
步骤串联反应、跨模块知识整合,主要体现在路线延长、官能团转化复杂化、涉及陌生反应机理等方面。
这类题目通过真实情境(如药物合成、高分子材料)建模,促使考生从碎片化知识记忆转向系统性思维构
建,掌握逆合成分析、反应条件筛选等核心方法。未来命题将更注重真实科研成果转化,要求考生在陌生
信息中提取关键反应机理,体现“证据推理与模型认知”的化学学科核心素养。
16. 海洋出水铁质文物表面有凝结物,研究其形成原理和脱氯方法对保护文物意义重大。
(1)文物出水清淤后,须尽快浸泡在稀NaOH或Na CO 溶液中进行现场保护。
2 3
①玻璃中的SiO 能与NaOH反应生成_______(填化学式),故不能使用带磨口玻璃塞的试剂瓶盛放
2
NaOH溶液。
②文物浸泡在碱性溶液中比暴露在空气中能减缓吸氧腐蚀,其原因有_______。
(2)文物表面凝结物种类受文物材质和海洋环境等因素的影响。
①无氧环境中,文物中的Fe与海水中的SO2-在细菌作用下形成FeS等含铁凝结物。写出Fe与SO2-反应
4 4
生成FeS和Fe(OH) 的离子方程式:_______。
2
②有氧环境中,海水中的铁质文物表面形成FeOOH等凝结物。
(i)铁在盐水中腐蚀的可能原理如图所示。依据原理设计如下实验:向NaCl溶液中加入K Fe(CN) 溶液
3 6
(能与Fe2+形成蓝色沉淀)和酚酞,将混合液滴到生铁片上。预测该实验的现象为_______。
第18页/共23页
学科网(北京)股份有限公司(ii)铁的氢氧化物吸附某些阳离子形成带正电的胶粒,是凝结物富集Cl-的可能原因。该胶粒的形成过程
中,参与的主要阳离子有_______(填离子符号)。
(3)为比较含氯FeOOH在NaOH溶液与蒸馏水中浸泡的脱氯效果,请补充实验方案:取一定量含氯
FeOOH模拟样品,将其分为两等份,_______,比较滴加AgNO 溶液体积[K (AgCl)=1.8´10-10。实
3 sp
验须遵循节约试剂用量的原则,必须使用的试剂:蒸馏水、0.5mol×L-1NaOH溶液、0.5mol×L-1HNO
3
溶液、0.05mol×L-1AgNO
溶液]。
3
【答案】(1) ①. Na SiO ②. 碱性环境抑制吸氧腐蚀正极反应的进行,反应速率减慢;碱性溶
2 3
液中,O 溶解度较小,减少文物与O 的接触,减缓吸氧腐蚀
2 2
细菌
(2) ①. 4Fe+SO2- +4H O FeS+3Fe(OH) +2OH- ②. 滴加混合溶液后,铁片表面将
4 2 2
出现蓝色和红色区域,较长时间后出现黄色斑点 ③. Fe3+、Fe2+
(3)分别加入等体积(如 5mL)的0.5mol×L-1NaOH溶液和蒸馏水至浸没样品,在室温下,搅拌、浸泡
30min;过滤,各取等量上清液(如2mL)置于两支小试管中,分别滴加3mL0.5mol×L-1HNO 溶液酸化,再
3
分别滴加0.05mol×L-1AgNO 溶液;记录每份上清液至出现AgCl白色沉淀时消耗的AgNO 溶液体积
3 3
【解析】
【小问1详解】
①SiO 是酸性氧化物,可与NaOH溶液发生反应生成硅酸钠和水,化学方程式为
2
SiO +2NaOH= Na SiO +H O。
2 2 3 2
②吸氧腐蚀时正极反应式为O +4e- +2H O=4OH-,根据化学平衡移动原理,碱性溶液中,OH-浓度
2 2
较大,会抑制O 得电子,使吸氧腐蚀的速率减慢;O 在高离子浓度的液体中溶解度较小,碱性溶液比纯
2 2
水溶解氧的能力低,减少了文物与O 的接触,减缓吸氧腐蚀。
2
【小问2详解】
第19页/共23页
学科网(北京)股份有限公司①无氧、弱碱性的海水中,Fe在细菌作用下,被SO2-氧化为+2价的FeS、FeOH
,根据得失电子守
4 2
恒、电荷守恒、原子守恒可写出该反应的离子方程式:
细菌
4Fe+SO2- +4H O FeS+3Fe(OH) +2OH-。
4 2 2
②(ⅰ)由题图知,铁片在NaCl溶液中发生吸氧腐蚀,开始时,负极反应式为Fe-2e- =Fe2+,正极反应式
为O +4e- +2H O=4OH-。Fe2+与K éFeCN ù反应生成KFeéFeCN ù蓝色沉淀,即铁片上会
2 2 3ë 6 û ë 6 û
出现蓝色区域;溶液中酚酞遇到OH-变红,铁片上会出现红色区域;由“有氧环境中,海水中的铁质文物
表面形成FeOOH”知,Fe2+在盐水中被O 氧化成黄色的FeOOH,故现象是滴加混合溶液后,铁片表面将
2
出现蓝色和红色区域,较长时间后出现黄色斑点;
(ⅱ)铁片发生吸氧腐蚀,负极区生成Fe2+,被O 进一步氧化为Fe3+,此时体系中的阳离子主要有
2
Fe3+、Fe2+。
【小问3详解】
要检验脱氯效果,应控制样品用量、脱氯时间、取用体积等变量相同,利用Ag+与Cl-的反应进行实验。
实验中,首先需要将等量的含氯FeOOH模拟样品分别用等体积的NaOH溶液与蒸馏水浸泡脱氯,然后过
滤,得到上清液,取等体积的两种上清液,先用HNO 溶液酸化,再加入AgNO 溶液,通过比较出现
3 3
AgCl白色沉淀时消耗。AgNO 溶液体积的大小,即可比较脱氯效果。
3
17. 合成气(CO和H )是重要的工业原料气。
2
(1)合成气制备甲醇:CO(g)+2H (g)=CH OH(g)。CO的结构式为CºO,估算该反应的DH需要
2 3
_______(填数字)种化学键的键能数据。
(2)合成气经“变换”“脱碳”获得纯H 。
2
①合成气变换。向绝热反应器中通入CO、H 和过量的H O(g):
2 2
低温型催化剂
CO(g)+H O(g) CO (g)+H (g) DH<0。催化作用受接触面积和温度等因素影响,
2 约230°C、3MPa 2 2
H Og 的比热容较大。H Og 过量能有效防止催化剂活性下降,其原因有_______。
2 2
②脱碳在钢制吸收塔中进行,吸收液成分:质量分数30%的K CO 吸收剂、K CrO (Cr正价有+3、+6)
2 3 2 4
第20页/共23页
学科网(北京)股份有限公司缓蚀剂等。K CO 溶液浓度偏高会堵塞设备,导致堵塞的物质是_______(填化学式)。K CrO 减缓设备腐
2 3 2 4
蚀的原理是_______。
x
(3)研究CH 、H O(g)与不同配比的铁铈载氧体[ Fe O ×(1-x)CeO ,0£x £1,Ce是活泼金属,正
4 2 2 2 3 2
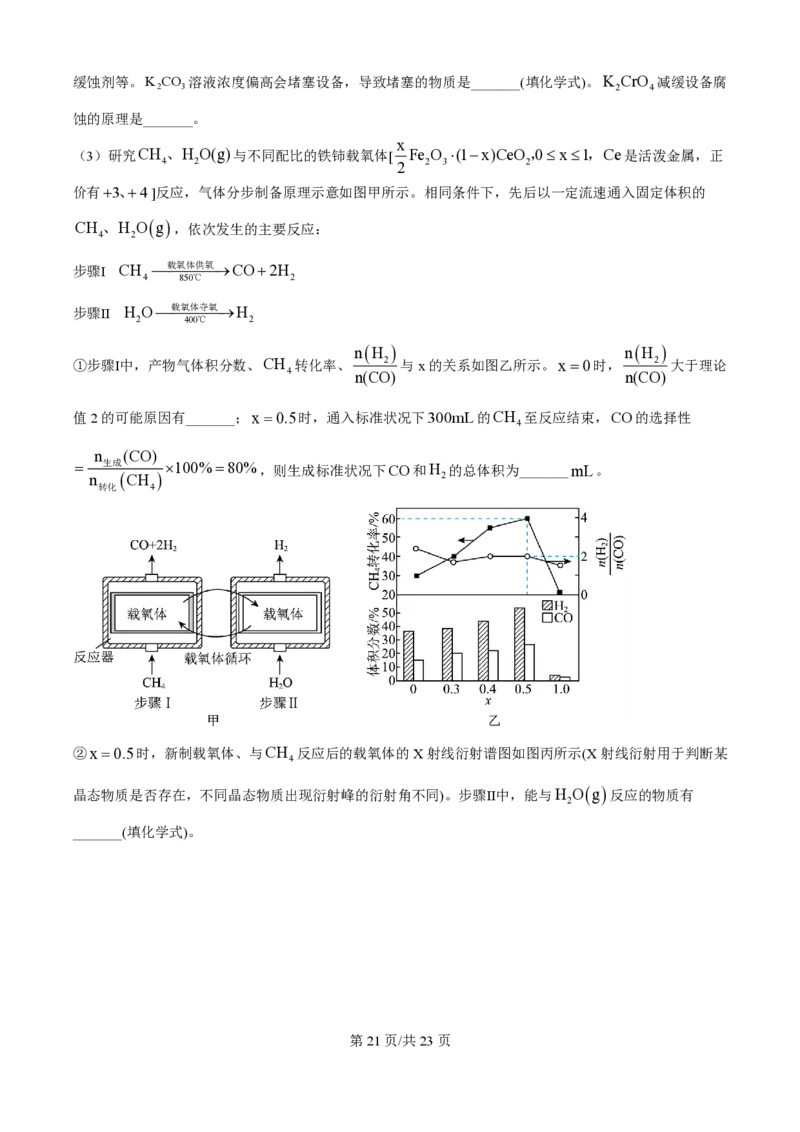
价有+3、+4]反应,气体分步制备原理示意如图甲所示。相同条件下,先后以一定流速通入固定体积的
CH 、H Og ,依次发生的主要反应:
4 2
步骤Ⅰ CH ¾载¾氧¾体供¾氧®CO+2H
4 850℃ 2
步骤Ⅱ H O¾载¾氧¾体夺¾氧®H
2 400℃ 2
nH nH
①步骤Ⅰ中,产物气体积分数、CH 转化率、 2 与x的关系如图乙所示。x =0时, 2 大于理论
4 n(CO) n(CO)
值2的可能原因有_______;x =0.5时,通入标准状况下300mL的CH 至反应结束,CO的选择性
4
n (CO)
= 生成 ´100%=80%,则生成标准状况下CO和H 的总体积为_______mL。
n CH 2
转化 4
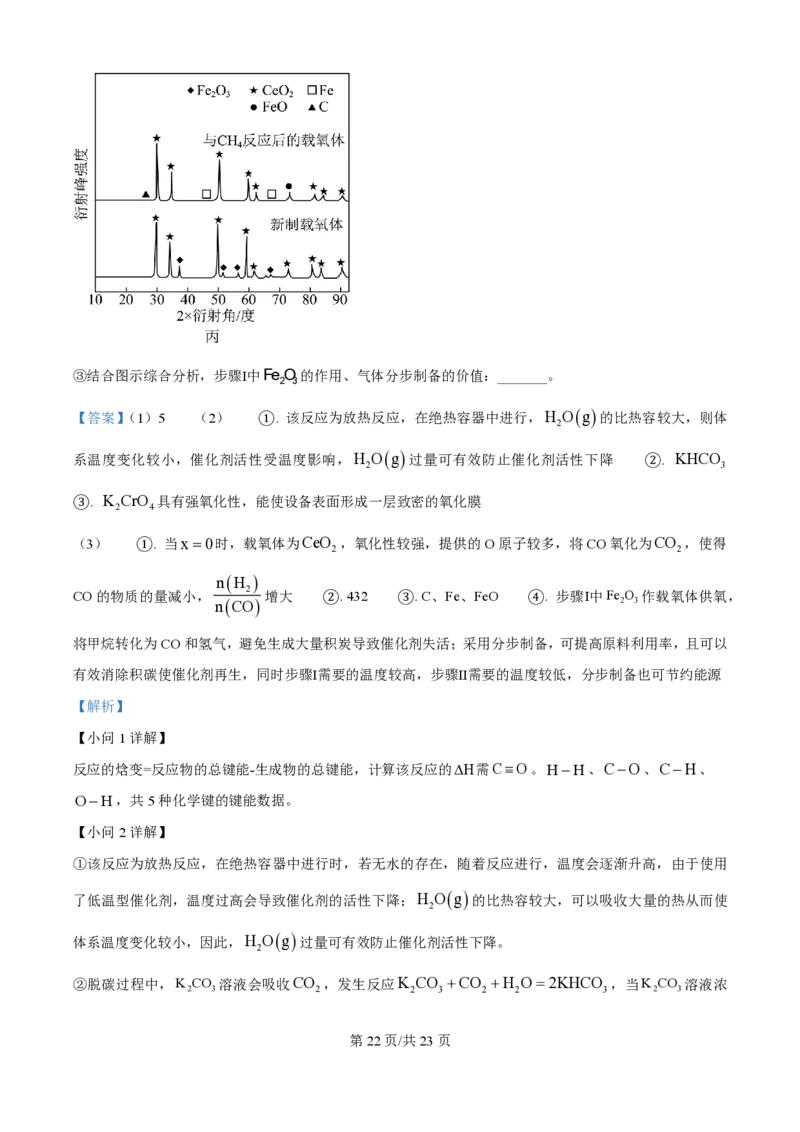
②x =0.5时,新制载氧体、与CH 反应后的载氧体的X射线衍射谱图如图丙所示(X射线衍射用于判断某
4
晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。步骤Ⅱ中,能与H Og 反应的物质有
2
_______(填化学式)。
第21页/共23页
学科网(北京)股份有限公司③结合图示综合分析,步骤Ⅰ中Fe O的作用、气体分步制备的价值:_______。
2 3
【答案】(1)5 (2) ①. 该反应为放热反应,在绝热容器中进行,H Og 的比热容较大,则体
2
系温度变化较小,催化剂活性受温度影响,H Og 过量可有效防止催化剂活性下降 ②. KHCO
2 3
③. K CrO 具有强氧化性,能使设备表面形成一层致密的氧化膜
2 4
(3) ①. 当x =0时,载氧体为CeO ,氧化性较强,提供的O原子较多,将CO氧化为CO ,使得
2 2
nH
2
CO的物质的量减小, 增大 ②. 432 ③. C、Fe、FeO ④. 步骤Ⅰ中Fe O 作载氧体供氧,
nCO 2 3
将甲烷转化为CO和氢气,避免生成大量积炭导致催化剂失活;采用分步制备,可提高原料利用率,且可以
有效消除积碳使催化剂再生,同时步骤Ⅰ需要的温度较高,步骤Ⅱ需要的温度较低,分步制备也可节约能源
【解析】
【小问1详解】
反应的焓变=反应物的总键能-生成物的总键能,计算该反应的DH需CºO。H-H、C-O、C-H、
O-H,共5种化学键的键能数据。
【小问2详解】
①该反应为放热反应,在绝热容器中进行时,若无水的存在,随着反应进行,温度会逐渐升高,由于使用
了低温型催化剂,温度过高会导致催化剂的活性下降;H Og 的比热容较大,可以吸收大量的热从而使
2
体系温度变化较小,因此,H Og 过量可有效防止催化剂活性下降。
2
②脱碳过程中,K CO 溶液会吸收CO ,发生反应K CO +CO +H O=2KHCO ,当K CO 溶液浓
2 3 2 2 3 2 2 3 2 3
第22页/共23页
学科网(北京)股份有限公司度偏高时,会生成较多KHCO ,而KHCO 溶解度相对较小,容易在溶液中达到饱和后结晶析出,从而堵
3 3
塞设备。K CrO 中的Cr元素化合价为+6,处于最高价态,具有强氧化性,在钢制吸收塔的环境中,它
2 4
会与铁发生氧化还原反应,使铁表面形成一层由铁的氧化物和铬的氧化物组成的致密氧化膜,这层氧化膜
可以将钢铁与腐蚀性介质隔离开,阻止氧气、水和其他腐蚀性物质与钢铁接触,从而减缓腐蚀。
【小问3详解】
①当x =0时,载氧体中没有Fe O,只有CeO ,由于CeO 的氧化性较强,且其提供的O原子较多,可
2 3 2 2
nH
以将CO氧化为CO ,使得CO的物质的量减小, 2 增大;由题图乙可知,当x =0.5时,CH 转化
2 nCO 4
n CO
率为 60%,则n CH =300mL´60% =180mL,已知 CO 的选择性= 生成 ´100% =80%,
转化 4 n CH
转化 4
nH
则 n CO=180mL´80% =144mL,根据图乙中数据可知,此时产物气中 2 =2,则
生成 nCO
n H =144mL´2=288mL,故生成标准状况下CO和H 的总体积为432mL。
生成 2 2
②新制载氧体与CH 反应后新生成的晶态物质,在步骤Ⅱ中会与H Og 反应,使载氧体再生从而继续与
4 2
CH 反应,因此,在新制载氧体中不存在,而在与CH 反应后的载氧体中含有的晶态物质,会在步骤Ⅱ中
4 4
与H Og 反应。因此,对比二者X射线衍射谱图可知,C、Fe、FeO在步骤Ⅱ中均可与H Og 反应。
2 2
③步骤Ⅰ中Fe O 作载氧体供氧,将甲烷转化为CO和氢气,可以避免生成大量积炭致催化剂活性降低甚至
2 3
失活;采用分步制备,可提高原料利用率,且可以有效消除积碳使催化剂再生,同时步骤Ⅰ需要的温度较
高,步骤Ⅱ需要的温度较低,分步制备也可节约能源。
第23页/共23页
学科网(北京)股份有限公司