3区3.9分!AI让术前CT"看见"卵巢癌小肠播散!3D深度学习灵敏度86%准确率81%,集成23模型策略攻克上腹部影像盲区,还深入分析失效场景
 卵巢癌手术方案怎么定?术前CT看不见小肠播散是老大难!本研究用3D卷积神经网络+增强CT影像,集成23个模型预测腹膜和小肠播散——小肠播散诊断灵敏度高达86.4%,准确率超81%,远超传统CT的20-30%!高分文章不仅要有SOTA性能,更要有扎实的失败case分析——研究还深入分析了模型失效的临床场景(如腹水量大、CA125极高)。想做影像AI发顶刊?这个分析思路值得参考!
卵巢癌手术方案怎么定?术前CT看不见小肠播散是老大难!本研究用3D卷积神经网络+增强CT影像,集成23个模型预测腹膜和小肠播散——小肠播散诊断灵敏度高达86.4%,准确率超81%,远超传统CT的20-30%!高分文章不仅要有SOTA性能,更要有扎实的失败case分析——研究还深入分析了模型失效的临床场景(如腹水量大、CA125极高)。想做影像AI发顶刊?这个分析思路值得参考!福利大放送!!!关注回复“资料”2字,即可免费领取生信资料,包括数据集、绘图代码、图表复现、思路总结、参考文献……0代码鼠标点一点,就能轻松完成5—10分生信SCI全文复现!(持续关注我们,每天为您解读最新见刊的文献!)


新鲜出炉!今天给大家深度剖析一篇2026年3月发表在《Scientific Reports》上的文章,题目为:使用术前增强CT成像检测上皮性卵巢癌腹膜和小肠播散的人工智能诊断性能。

团队成员合影(位于上海陆家嘴中心,可随时预约参观)


CNSknowall 平台 Pubmed+AI 快速提炼
研究亮点·研究思路·研究结果·研究结论


1.AI在小肠播散诊断上的突破:该研究是首次应用人工智能方法进行术前诊断上皮性卵巢癌小肠播散的研究,并达到了超过80%的准确率,特别是86.40%的高灵敏度,这对于术前规划至关重要,因为该区域传统影像学诊断率极低(20-30%)。
2.模型性能的系统性分析:研究不仅报告了最佳准确率,还深入分析了模型表现不佳的临床情况(如腹水量极端、CA125水平极端、PCI评分低),揭示了模型可能受训练数据中特征影响的局限性,并指出了通过扩大数据集来改进的方向。


1.首次应用AI于小肠播散检测:研究明确指出这是首个针对上皮性卵巢癌小肠播散的AI诊断模型,填补了该领域的研究空白。
2.采用集成预测策略:研究采用了多个模型(23个模型)进行集成预测,相较于单一模型,显著提升了诊断的稳定性和准确性,并缩小了性能波动范围。
3.模型架构选择:选取了MobileNetV2这一轻量级深度神经网络架构,其优势在于能有效减少在小数据量情况下的过拟合问题,并已在医学图像分析领域得到验证。


1.临床挑战:约60-70%的上皮性卵巢癌患者诊断时已为晚期(FIGO III/IV期),伴有广泛的腹腔播散。准确的术前评估对于选择最佳治疗方案(初次减灭术PDS vs. 新辅助化疗后间隔减灭术NAC/IDS)至关重要,目标是实现无残留病灶(R0切除)。
2.现有影像学局限:CT是评估腹腔播散的标准影像学方法,但其诊断准确性不足,常常需要诊断性腹腔镜或开腹手术来确认。特别对于小肠及肠系膜表面的播散,术前影像学诊断非常困难,文献报道准确率低至20-30%。
3.研究动机:鉴于传统CT的局限性,该研究旨在通过整合增强CT影像与机器学习方法,优化对腹腔,特别是小肠播散的术前诊断准确性,以期改善临床决策。


1.数据收集:回顾性收集2019年10月至2024年12月间,两家医院227名上皮性卵巢癌患者术前增强CT影像及相关临床数据(年龄、BMI、CA125、术中PCI评分、病理学等)。
2.模型构建:
基于MobileNetV2架构,构建两个独立的3D卷积神经网络模型。
P-Model:检测CT图像中是否存在腹膜播散。
SB-Model:检测CT图像中是否存在小肠播散。
3.训练与验证:
采用八折交叉验证,将病例分为8组,7组训练,1组评估。
对训练数据进行了960倍的数据增强,并随机选择。
共生成192个模型(24组交叉验证集 × 8个模型)。
4.性能评估:
图像单元评估:基于单个CT切片进行评估。
病例单元评估:基于连续CT切片(5-30张)计算阳性预测率,以确定每例患者的最终诊断。
评估指标:敏感度、特异度、准确率。
评估了两种图像处理方式:完整CT图像和裁剪至中心75%的图像。
对比了单一模型预测和23个模型的集成预测。
5.低准诊断病例分析:
定义P-Model准确率≤25%的病例为低准确率组。
回顾性分析这些病例的放射科医生解读报告。
将低准确率组与高准确率组(>25%)患者的临床特征(腹水、CA125、PCI评分)进行对比。


1.P-Model诊断性能(病例单元评价):
最佳性能:使用21张连续切片、75%裁剪图像的集成预测。
准确率:77.30% (95%CI: 71.76%~82.02%)
敏感度:68.75% (95%CI: 59.86%~76.43%)
特异度:85.84% (95%CI: 79.02%~90.70%)
2.SB-Model诊断性能(病例单元评价):
最佳性能:使用9张连续切片、75%裁剪图像的集成预测。
准确率:81.93% (95%CI: 76.73%~86.17%)
敏感度:86.40% (95%CI: 74.69%~93.18%)
特异度:77.47% (95%CI: 73.07%~81.33%)
3.低准确率病例分析:
在P-Model准确率≤25%的病例中,放射科医生的诊断敏感度为63.0%,特异度为57.9%。
对于无腹膜播散的患者:低AI准确率组相比高准确率组,术前CT显示大量腹水、累及上腹部,且术前CA125水平显著更高。
对于有腹膜播散的患者:低AI准确率组相比高准确率组,腹水体积显著更小(多≤300ml,局限于盆腔),术前CA125水平和PCI评分显著更低。
4.模型稳定性:集成预测的准确率波动范围远小于单一模型,表明其具有更高的稳定性。


1.主要结论:基于术前增强CT的AI深度学习能够以优化的准确率预测卵巢癌患者的腹膜播散,特别是小肠播散。这是首个针对小肠播散的AI诊断研究,其超过80%的准确率(尤其高敏感度86.40%)超越了传统CT诊断。这有助于临床医生更及时地制定治疗决策(选择PDS或NAC),并提前进行多学科手术规划。
2.临床意义:准确的术前预测,尤其是对小肠播散的高灵敏度,可以避免不必要的诊断性手术,减少治疗延误,其临床价值超过了对“残留病灶<1cm”的考量。
3.与现有技术对比:
与全腹部MRI和超声相比,CT扫描更方便、易获取、患者舒适度更高。但AI分析CT在诊断小肠播散上的性能优于此前报道的放射科医师对CT的解读。
SB-Model的高灵敏度对于术前检测小肠播散至关重要,能够避免因漏诊导致的手术方案不当。
4.局限性与未来方向:
模型只能判断有无播散,无法定位具体位置、评估肿瘤负荷或预测术后残留病灶。未来需开发更详细的功能。
缺乏外部验证,模型的泛化能力未知。未来的临床实施前必须进行外部验证。
存在病例选择偏倚,但论文作者认为增加病例可能导致准确率下降。
模型性能受训练数据限制,当遇到与训练数据特征差异大的病例(如腹水极端)时,准确性会下降。扩大并多样化训练数据集是改进方向。



补充表S1总结了P-模型在诊断腹膜播散方面的基于图像单元的评估结果,比较了两种图像类型(完整CT图像和75%裁剪图像)上的单一模型预测和集成预测。结果显示,使用完整CT图像的集成预测达到了最高的诊断性能,准确率为69.49%(灵敏度=62.26%,特异度=76.73%)。
补充图S1展示了使用P-模型进行基于图像单元评估的准确率变异性。水平线表示所有模型的平均准确率。垂直线是从最差准确率到最佳准确率绘制的线。该图表明,集成预测的准确率变异范围远小于单一模型预测。
图1和补充表S2展示了P-模型在诊断腹膜播散方面的基于病例单元的评估结果,比较了两种图像类型(完整CT图像和75%裁剪图像)上的单一模型和集成预测。该表的行表示用于计算每个病例阳性预测率的连续切片图像数量。
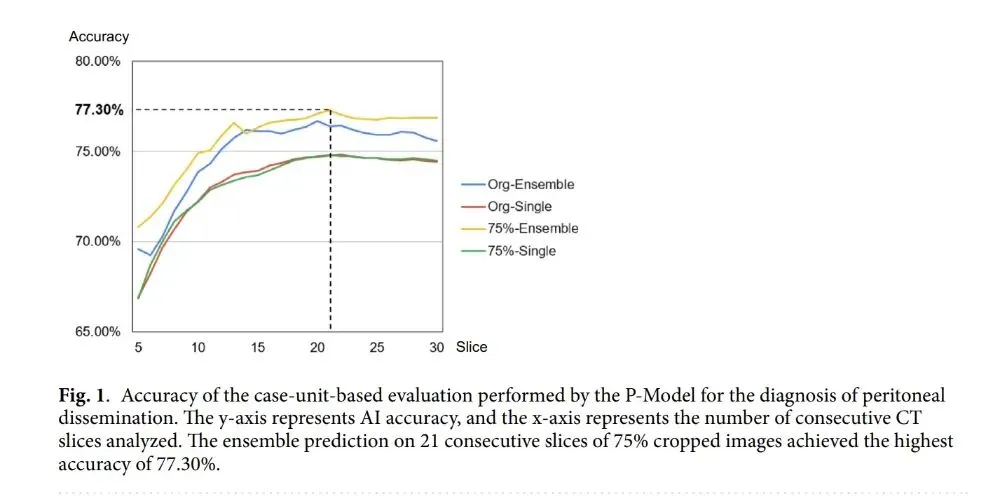
最佳性能是通过对75%裁剪图像的21个连续切片进行集成预测实现的,准确率为77.30%(95%置信区间(CI)=71.76~82.02%),灵敏度为68.75%(95%CI=59.86~76.43%),特异度为85.84%(95%CI=79.02~90.7%)。
补充图S2展示了使用P-模型进行基于病例单元评估的准确率变异性。水平线表示所有模型的平均准确率。垂直线是从最差准确率到最佳准确率绘制的线。该图表明,集成预测的准确率变异范围远小于单一模型预测。
所有评估的详细灵敏度和特异度见补充表S3。

补充表S4总结了SB-模型在诊断小肠播散方面的基于图像单元的评估结果,比较了完整CT图像和75%裁剪图像上的单一模型和集成预测。使用75%裁剪图像的集成预测实现了最佳准确率72.79%(灵敏度=65.24%,特异度=80.34%)。
补充图S3展示了使用SB-模型进行基于图像单元评估的准确率变异性。水平线表示所有模型的平均准确率。垂直线是从最差准确率到最佳准确率绘制的线。该图表明,集成预测的准确率变异范围远小于单一模型预测。
图2和补充表S5展示了基于病例单元的评估结果。表的行表示用于计算每个病例阳性预测率的连续切片图像数量。最佳性能是通过对75%裁剪图像的9个连续切片进行集成预测实现的,准确率为81.93%(95%CI=76.73~86.17%),灵敏度为86.40%(95%CI=74.69~93.18%),特异度为77.47%(95%CI=73.07~81.33%)。
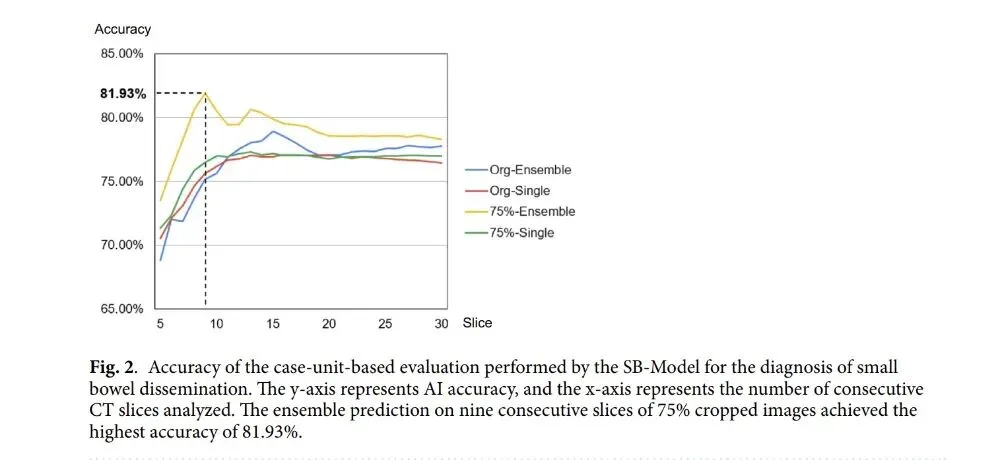
补充图S4展示了使用SB-模型进行基于病例单元评估的准确率变异性。水平线表示所有模型的平均准确率。垂直线是从最差准确率到最佳准确率绘制的线。该图表明,集成预测的准确率变异范围远小于单一模型预测。
所有评估的详细灵敏度和特异度见补充表S6。

表1显示了对于P-模型AI准确性≤25%的病例,放射科医生术前是否正确判读。在这些病例中,放射科医生判读的灵敏度和特异度分别为63.0%和57.9%。
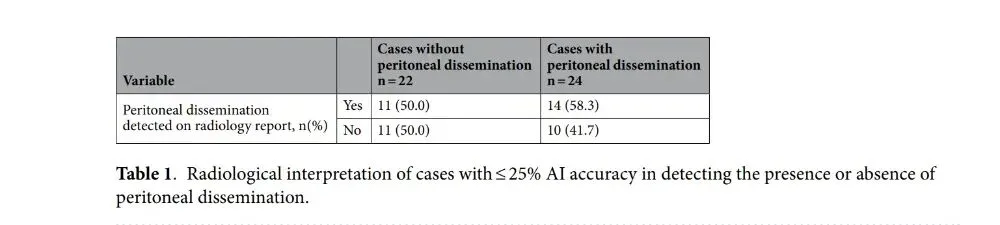
表2根据术中宏观发现是否存在腹膜播散进行分层,比较了P-模型AI诊断准确性≤25%与>25%患者的临床特征。
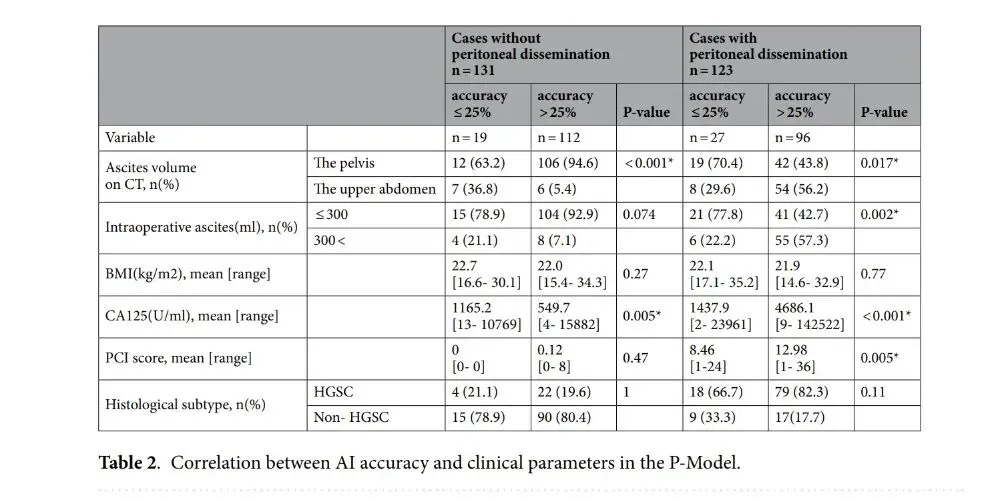
在无腹膜播散的患者中,与准确性>25%的患者相比,AI准确性≤25%的患者在术前CT上的腹水量显著更大。腹水延伸至上腹部在低准确性组中更常见(p<0.001)。此外,该组的术前CA125水平显著更高(p=0.005)。相反,在有腹膜播散的患者中,AI准确性≤25%的患者比高准确性患者表现出显著更低的腹水量。低准确性组中的大多数病例在术前CT上腹水局限于盆腔(p=0.017),并且大多数病例术中腹水量≤300mL(p=0.002)。此外,与高准确性组相比,低准确性组的术前CA125水平和PCI评分显著更低(分别为p<0.001和p=0.005)。无论是否存在腹膜播散,BMI或组织学亚型的准确性均无差异。如补充表S7所示,当准确性截止值设为50%时,获得了类似的结果。在无腹膜播散的患者中,低准确性组术前CT腹水量显著高于高准确性组(P=0.007)。相反,在有腹膜播散的患者中,与高准确性组相比,低准确性组在术前CT和术中评估中的腹水量均显著更小(分别为P=0.002和P<0.001)。此外,低准确性组的术前CA125水平和PCI评分显著低于高准确性组(分别为P=0.002和P=0.004)。




更多结果和补充图表:
PMID:41872308
PMCID:PMC13009186
DOI:10.1038/s41598-026-41728-4
不想做实验,没数据,还想要快速发表文章,没问题的!公共数据库就是我们的数据宝藏!没思路不用担心,作为专业的生信团队,我们很乐意为您效劳,提供研究路线设计和数据挖掘分析,扫码联系我们吧!


长按二维码关注我们,用最短的时间和最高的效率学习更多数据分析方法!

扫描上方二维码或登录平台官网后添加CNSknowall客服微信咨询!官网地址:https://cnsknowall.com
CNSknowall:24年最新问世的遥遥领先的科研数据(0代码生信+统计学)分析平台,同时含有机制图模块+汉化版Pubmed融合Deepseek高效筛选目标文献+SCI文献例句/语料检索模块+OPenAI官方GPT接口,>500款CNS级别图表皆可一秒内一键出图,登录即秒变数据分析大神,体验前所未有的便捷数据分析之旅,开启科研天骄之路!
可向下滑动批阅!

 夜雨聆风
夜雨聆风