基于眼底影像的青光眼AI筛查:从卷积神经网络到临床落地
青光眼作为全球首位不可逆致盲性眼病,早期发现是防治关键,但“低症状、高漏诊”的特性使其筛查面临巨大挑战。近年来,基于深度学习的眼底影像分析技术为大规模青光眼筛查开辟了新路径。
本文从技术原理入手,系统回顾关键研究进展、多模态融合趋势及分级诊疗部署实践,探讨AI在青光眼筛查中的临床价值与落地前景。
全球青光眼患病率持续攀升,根据世界卫生组织预测,2040年全球青光眼患者将达1.118亿例。该病发病隐匿,近40%的患者在确诊时已发展至中晚期,错过最佳干预时机。传统青光眼诊断依赖视盘形态评估、OCT结构参数及视野功能检查,在基层及体检场景中,存在设备依赖性强、青光眼专科医生匮乏、阅片一致性不足等突出问题——仅在美国,OCT检测青光眼进展的灵敏度为75%-90%,且不同阅片者之间的一致性存在显著差异。
近年,基于深度学习的眼底彩照AI分析技术取得突破性进展,凭借高通量、低成本、全自动的优势,为青光眼的早期筛查提供了新的技术范式。
深度卷积神经网络(CNN)是目前基于眼底影像进行青光眼检测的主流技术框架,其核心任务可归纳为三类:
分割任务:自动勾画视盘(Optic Disc)和视杯(Optic Cup)的精确边界;
参数计算:基于分割结果计算杯盘比(C/D)等关键形态学参数,C/D值≥0.65为青光眼的高可靠指标;
疾病分类:直接从原图进行“正常 vs 青光眼”的二元分类,部分研究甚至做到了轻、中、晚期的多级分级。
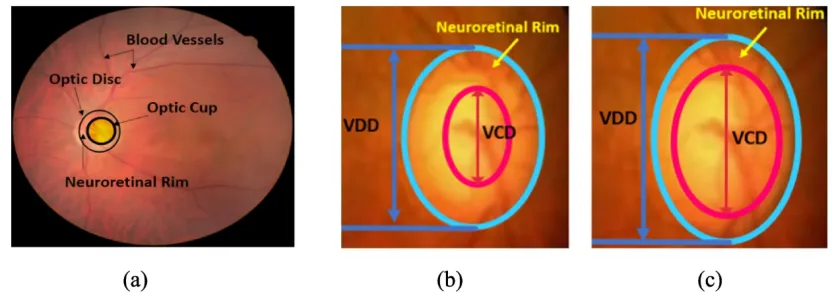
a Fundus image, b normal disc, c glaucoma disc
Fig1.From: Advancements in Deep Learning for Glaucoma Detection from Fundus Images: A Comprehensive Analysis
常用骨干网络框架包括:U-Net及其改进型(Attention U-Net)在医学图像分割中占据主导地位;ResNet、EfficientNet、DenseNet等则常见于分类任务。近年来,Vision Transformer等自注意力模型也开始被引入眼底图像分析中,在某些任务上展现出优于传统CNN的泛化能力。
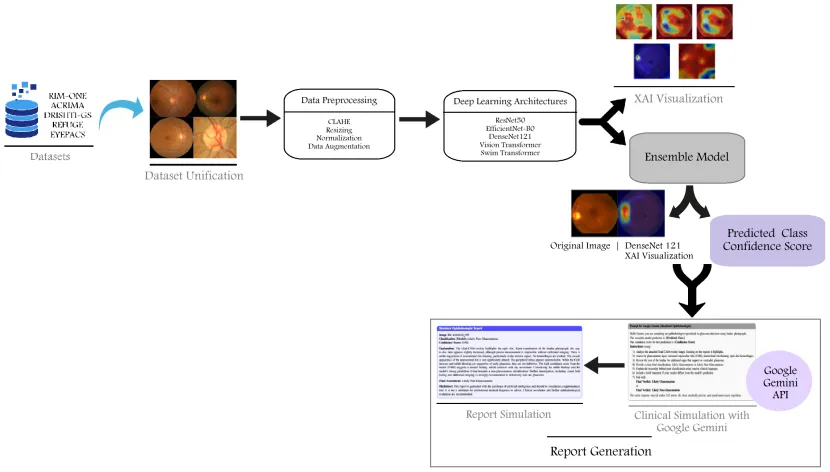
Fig2.Overview of the glaucoma detection methodology including datasetprocessing, model training,ensemble inference,and clinical simulation.
注意:这些AI模型的核心逻辑并非“理解”青光眼疾病的病理生理机制,而是在高维的特征空间中学习并匹配与“青光眼性视神经损伤”相关的图像表型模式。形象地说,模型并非阅读教科书,而是通过大量病例的“影像-标签”配对,逐渐掌握了哪些视盘形态更像青光眼。
早期探索:验证可行性
Ting等在2017年发表于JAMA的研究,基于约50万张眼底图像开发的深度学习系统,实现了包括青光眼在内的多病种识别,AUC超过0.94,首次在超大规模数据集中验证了深度学习模型在眼科疾病筛查中的可行性。
随后,Li等2018年进一步聚焦青光眼性视神经损伤检测,使用48,116张标注眼底图像训练深度学习系统,在检测可转诊青光眼性视神经病变方面实现了0.986的AUC,并强调多中心数据和跨设备验证对泛化能力的重要性。
系统性评估:性能量化与趋势识别
随着研究深入,系统性综述与荟萃分析为评估AI的整体表现提供了重要依据。2025年Thommy等发表的一项纳入48项研究的meta分析显示,基于眼底彩照的深度学习模型在青光眼检测中的敏感度和特异度分别达到0.92(95% CI: 0.89-0.94)和0.93(95% CI: 0.90-0.95),汇总AUC为0.90(95% CI: 0.88-0.92)。该研究同时指出,在进展预测方面,深度学习模型的表现则相对较弱,提示应当整合多模态随访数据提升预测能力。另一项2025年发表的综述进一步系统梳理了AI在青光眼筛查、进展预测和手术结局预测中的应用,特别强调了多模态融合和个性化风险分层的前景。
从“黑箱”到可解释:临床信任的关键
然而,深度学习模型的“黑盒”特性限制了其在临床中的信任度。张秀兰教授团队2024年发表长篇综述,强调需要引入联合学习、生成式数据合成增强等技术以克服数据孤岛与标注瓶颈。基于Grad-CAM等注意力机制的可视化方案是目前提升可解释性的主流手段。2025年的一项前沿研究更是进一步探索了深度模型结合大语言模型(如Google Gemini 1.5 Flash):模型不仅能给出诊断结论,还能生成类似医生文书风格的结构化诊断报告,在提升准确性的同时,显著增强了AI与临床工作流的可衔接性。
多模态融合:性能突破方向
青光眼的诊疗向来是一个综合结构OCT、功能视野及临床信息的综合判断过程,2025年发表的一项研究开发了一种多模态神经网络青光眼检测模型,整合眼底彩色照片、OCT和Humphrey视野分析数据,结果显示,通过多模态整合后,模型的AUC可从0.57~0.74提升至0.86,特异度从0.77~0.82提升至0.85,提示综合考虑结构和功能数据可通过“整体方法”增强AI的诊断性能。另一项研究采用OCT视盘照片和OCT成像构建多模态基础模型,整合后模型的AUC达到0.94(95% CI: 0.91-0.97),显著优于单用眼底照片的0.86。
另一个极具临床价值的研究方向,是从结构预测功能。近期发表的综述明确指出深度学习模型已可通过卷积神经网络、循环神经网络、Transformer等架构,利用OCT序列扫描预测疾病进展。一项2025年的系统综述进一步证实,AI在预测青光眼发展和进展方面均表现出良好的性能,且其在预测已确诊患者进展的能力对于优化“阻止疾病进展”的诊疗体系具有显著潜力。
进展预测:AI赋能长期管理
如前所述,相较于跨sectional(横向)检测任务,深度学习在预测青光眼纵向进展方面表现相对较弱。2025年的最新meta分析指出,在进展预测方面,目前的模型尚不如诊断任务稳健。这提示未来的突破点应更多依赖于整合多模态随访数据,如融合功能检查(视野)、日常临床随访结构化数据等。目前已有研究指出模型通过整合OCT、视野和临床数据,在预测患者未来是否需要接受侵入性手术方面取得了AUROC达0.92的成绩。
更有研究显示,在整合多模态数据(眼底、OCT、视野)后,模型已能将进展预测时间窗口拉长至4年。若此技术日趋成熟,眼科医生将从被动的“疾病监测者”转变为主动的“干预计划者”,为个性化的围手术期干预决策开启全新可能。
虽然实验室数据亮眼,但AI模型从论文走进临床,还面临三座大山:
1. 数据偏倚与泛化能力不足:大多数模型基于单一中心、单一种族、特定相机的数据训练,一旦移至跨机构、跨种族或不同设备采集的数据,性能会出现显著“跳水”。多中心外部验证的比例仍然有限。张秀兰教授团队发表长篇综述,系统性地将青光眼AI研发所面临的挑战归纳为三大类:数据标注难度大、泛化性差及可解释性差,并特别指出多数研究因青光眼诊断标准不一而导致的AI泛化困境,并强调需要引入联邦学习、生成式数据合成增强等技术以克服数据孤岛与标注瓶颈。
2. 真实世界的图像质控挑战:AI系统对图像质量高度敏感。在实验室内,经过严格质控的眼底照片保证了模型表现。但在基层筛查或真实世界部署时,低质图像的比例大幅上升,这将直接导致AI效率降低和准确性急剧下降。
3. 证实性偏差与“金标准”缺失:多数AI模型的性能评价是基于临床专家的主观标注进行的。然而,青光眼诊断本身在不同专家之间可能存在较大一致性差异,这就造成了一种“证实性偏差”。特别是在早期青光眼诊断和进展判断上,缺乏绝对的“金标准”影响了AI评价的绝对客观性。
在国际顶刊npj Digital Medicine上发布的“Multi-Glau”三层级AI系统(2025),是立足于中国分级诊疗大背景的一个重大医工融合范例。
该系统三大核心模块精准对接不同层级医院的现实痛点:通过XGBoost模块实现不依赖罕见影像设备的低成本初筛;通过强大的缺失模态鲁棒处理技术克服二级医院数据不足或质量差的窘境(在40%图像缺失率下仍保持高AUC);最终在三级医院依靠M3-VF模块完成眼底及视功能的四级精细分型。该系统在多中心验证中分别达到了AUC 0.9254(基层初筛)、0.8650(二级预诊断)和0.9516(三级精准分型)的优异成果。
一项在墨西哥三级眼科保健中心开展的临床研究给出了有力的实证:在青光眼可疑判断上,AI模型(采用Inception V3和U-Net架构)准确度达88.6%,优于住院医师的82.9%;杯盘比评估方面,AI的平均绝对误差为0.056,同样优于住院医师的0.105(p<0.001)。然而,最亮眼的结果来自人机协同思路:AI与住院医师的“协同模式”在青光眼可疑判断中实现了80.4%的敏感性,显著高于AI(63.0%)或医师(50.0%)任何一方的独立表现。该结果清晰地表明一种科学且务实的定位——AI的理想角色是“第一读片人和高级辅助”,而非替代医生,并且只有人才能承担诊断的相应责任。
本文基于眼底影像的青光眼AI筛查技术进行了系统性梳理——从CNN驱动的视盘分割与分类,到多模态融合与进展预测,再到“Multi-Glu”等系统在分级诊疗中的落地实践。我们试图勾勒出一条清晰的技术进化路径:从“单点分类”走向“结构化解释”,从“实验室高精度”走向“真实世界泛化”。目前我们更侧重于概览与趋势分析,旨在提供一个快速理解该领域全貌的“导航图”。对于算法内部的技术细节——例如UNet与Vision Transformer在视杯分割中的精度对比、不同注意力机制对可解释性的实际增益、多模态融合中特征对齐与缺失模态处理的具体实现方案——这些“医工结合”的技术核心,尚未在此展开。
后续我们将推出系列深度拆解,逐一结合文献探索以下问题:
分割任务中,Attention UNet是否比原始UNet更适合杯盘边界检测?
分类模型里,EfficientNet与ResNet在跨设备泛化能力上的差异在哪里?
多模态融合,究竟是用特征级拼接还是基于注意力机制的跨模态交互更优?
临床部署时,如何通过数据增强、联邦学习或域自适应技术对抗真实世界的图像质量波动?
 我们相信,真正让AI从论文走进诊室的,不是一篇全景综述,而是一次次对技术细节的“庖丁解牛”。敬请期待后续的技术拆解系列文章。
我们相信,真正让AI从论文走进诊室的,不是一篇全景综述,而是一次次对技术细节的“庖丁解牛”。敬请期待后续的技术拆解系列文章。
本账号内容仅用于专业医学人士信息交流!
2.Ting DSW, Cheung CY, Lim G, et al. Development and validation of a deep learning system for diabetic retinopathy and related eye diseases using retinal images from multiethnic populations with diabetes. JAMA. 2017;318(22):2211-2223. DOI: 10.1001/jama.2017.18152
3.Li Z, He Y, Keel S, et al. Efficacy of a deep learning system for detecting glaucomatous optic neuropathy based on color fundus photographs. Ophthalmology. 2018;125(8):1199-1206. DOI: 10.1016/j.ophtha.2018.01.023
4Li F, Wang D, Yang Z, et al. The AI revolution in glaucoma: Bridging challenges with opportunities. Progress in Retinal and Eye Research. 2024;103:101291. DOI: 10.1016/j.preteyeres.2024.101291
5.Lan CH, et al. Artificial intelligence in glaucoma: Advances in diagnosis, progression forecasting, and surgical outcome prediction. International Journal of Molecular Sciences. 2025;26(10):4473. DOI: 10.3390/ijms26104473
6.Shroff S, et al. Artificial intelligence in the prediction of glaucoma development and progression: A systematic review. Ophthalmic and Physiological Optics. 2025. DOI: 10.1111/opo.70000
7.Zhou Y, et al. A three-tier AI solution for equitable glaucoma diagnosis across China‘s hierarchical healthcare system. NPJ Digital Medicine. 2025. DOI: 10.1038/s41746-025-00000-0
8.Ramirez DA, et al. Synergistic AI-resident approach achieves superior diagnostic accuracy in tertiary ophthalmic care for glaucoma and retinal disease. Frontiers in Ophthalmology. 2025;5:1581212. DOI: 10.3389/fopht.2025.1581212
9.多模态融合性能参考:Utilization of image-based deep learning in multimodal glaucoma detection neural network from a primary patient cohort. Ophthalmology Science. 2025. DOI: 10.1016/j.xops.2025.100001
编辑:SUNI
审校:Jesu
 夜雨聆风
夜雨聆风




