文档内容
2 0 2 4 年 上 教 师 资 格 笔 试 · 化 学 学 科 知 识 与 教 学 能 力
理 论 精 讲 - 元 素 化 合 物 1
讲师:沈蕾
更多干货关注 粉笔教师教育 粉笔教师目
录
content
碱金属及其化合物 碳、硅及其化合物
1 4
镁、铝及其化合物 氯、溴、碘及其化合物
2 5
铁、铜及其化合物 硫及其化合物
3 6
氮及其化合物
7碱金属及其化合物一、钠及其化合物 P35
(一)钠的性质
1.钠的物理性质
颜色 状态 硬度 密度 熔点 导电、导热性
银白色、有 小,可用小刀
固体 ρ(H O)>ρ(Na)>ρ(煤油) 97.8℃ 良好
2
金属光泽 切割P35
2.钠的化学性质
钠原子的结构:
钠易失去最外层的一个电子,其第一电离能小,化学性质活泼,
表现出强还原性。钠元素在化合物中均呈+1价。
第一电离能是基态的气态原子失去最外层的一个电子所需能量。
第一电离能数值越小,原子越容易失去一个电子。P36
(1)与非金属反应
4Na+O 2Na O(白色固体)
2 2
2Na+O Na O (淡黄色固体)
2 2 2
2Na+Cl 2NaCl(白烟)
2P36
(2)与水反应
2Na+2H O 2NaOH+H ↑
2 2
现象及解释:
①(浮)浮在水面上——密度比水小;
②(熔)熔成小球——钠的熔点低,反应放热;
③(游)四处游动——生成气体;
④(响)有“嘶嘶”的响声——反应剧烈;
⑤(红)酚酞变红——反应中生成了碱。P36
(3)与酸反应
2Na+2H+ 2Na++H ↑(直接与 H+ 反应)
2
【粉笔提示】
钠与稀硫酸、盐酸等非氧化性酸反应时,首先是钠直接与酸反应,过
量的钠再与水反应,而不能认为钠先与水反应,生成的 NaOH 再与酸中和。
(4)与碱溶液反应
钠与碱溶液反应的实质是钠与水反应。但要注意Na与NaOH溶液、澄清石
灰水反应时,可能会引起溶液浓度的变化。P36
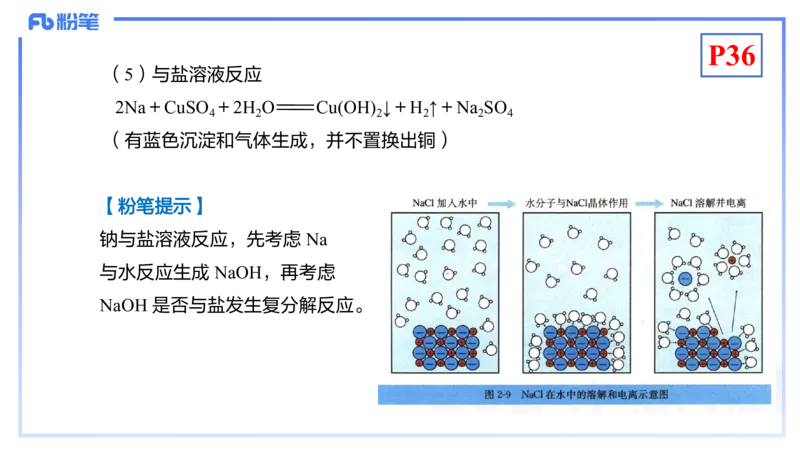
(5)与盐溶液反应
2Na+CuSO +2H O Cu(OH) ↓+H ↑+Na SO
4 2 2 2 2 4
(有蓝色沉淀和气体生成,并不置换出铜)
【粉笔提示】
钠与盐溶液反应,先考虑 Na
与水反应生成 NaOH,再考虑
NaOH 是否与盐发生复分解反应。P37
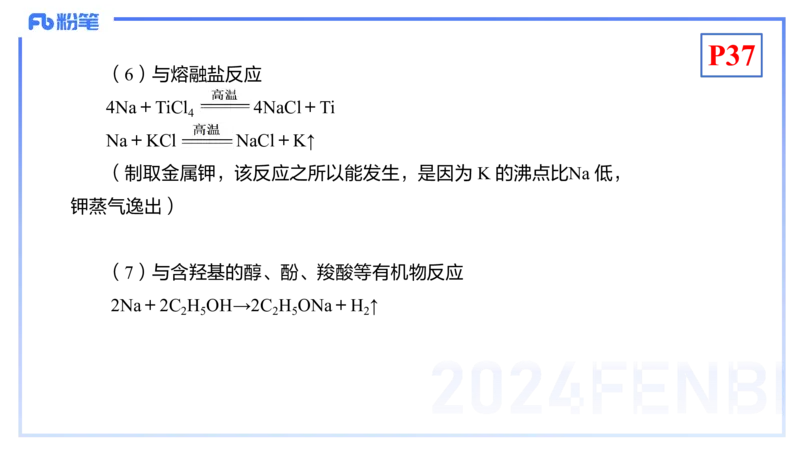
(6)与熔融盐反应
4Na+TiCl 4NaCl+Ti
4
Na+KCl NaCl+K↑
(制取金属钾,该反应之所以能发生,是因为 K 的沸点比Na 低,
钾蒸气逸出)
(7)与含羟基的醇、酚、羧酸等有机物反应
2Na+2C H OH→2C H ONa+H ↑
2 5 2 5 2P37
3.钠的制取和保存
(1)制取:2NaCl(熔融) 2Na+Cl ↑
2
通电
电解饱和食盐水:2NaCl+2H O 2NaOH+Cl ↑+H ↑
2 2 2
(2)保存:通常保存于煤油或石蜡油中。(二)常见的钠的化合
P37
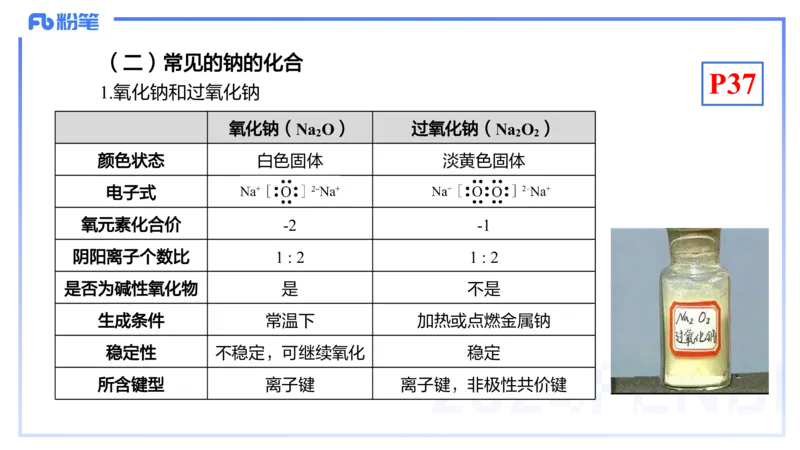
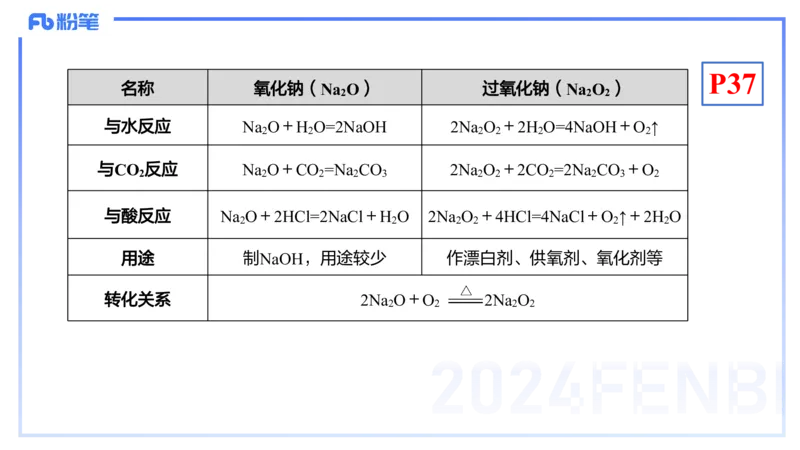
1.氧化钠和过氧化钠
氧化钠(Na O) 过氧化钠(Na O )
2 2 2
颜色状态 白色固体 淡黄色固体
电子式
氧元素化合价 -2 -1
阴阳离子个数比 1 : 2 1 : 2
是否为碱性氧化物 是 不是
生成条件 常温下 加热或点燃金属钠
稳定性 不稳定,可继续氧化 稳定
所含键型 离子键 离子键,非极性共价键P37
名称 氧化钠(Na O) 过氧化钠(Na O )
2 2 2
与水反应 Na O+H O=2NaOH 2Na O +2H O=4NaOH+O ↑
2 2 2 2 2 2
与CO 反应 Na O+CO =Na CO 2Na O +2CO =2Na CO +O
2 2 2 2 3 2 2 2 2 3 2
与酸反应 Na O+2HCl=2NaCl+H O 2Na O +4HCl=4NaCl+O ↑+2H O
2 2 2 2 2 2
用途 制NaOH,用途较少 作漂白剂、供氧剂、氧化剂等
转化关系 2Na O+O 2Na O
2 2 2 2P38
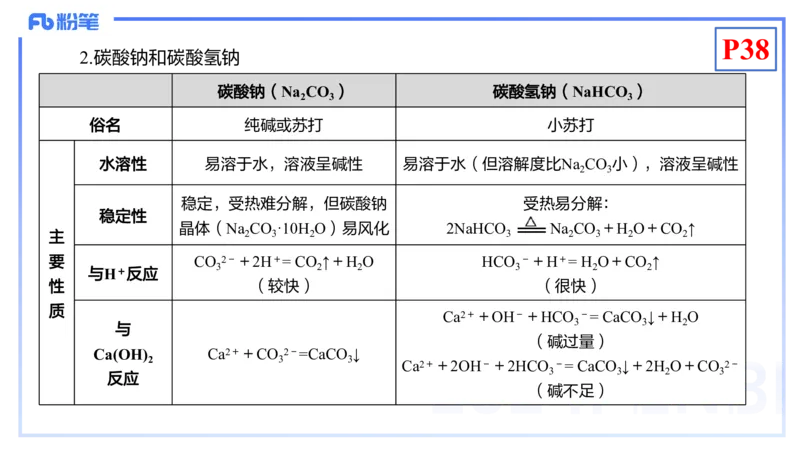
2.碳酸钠和碳酸氢钠
碳酸钠(Na CO ) 碳酸氢钠(NaHCO )
2 3 3
俗名 纯碱或苏打 小苏打
水溶性 易溶于水,溶液呈碱性 易溶于水(但溶解度比Na CO 小),溶液呈碱性
2 3
稳定,受热难分解,但碳酸钠 受热易分解:
稳定性
晶体(Na CO ·10H O)易风化 2NaHCO Na CO +H O+CO ↑
主 2 3 2 3 2 3 2 2
要 CO 2-+2H+= CO ↑+H O HCO -+H+= H O+CO ↑
3 2 2 3 2 2
与H+反应
性 (较快) (很快)
质
Ca2++OH-+HCO -= CaCO ↓+H O
3 3 2
与
(碱过量)
Ca(OH) Ca2++CO 2-=CaCO ↓
2 3 3
Ca2++2OH-+2HCO -= CaCO ↓+2H O+CO 2-
3 3 2 3
反应
(碱不足)P38
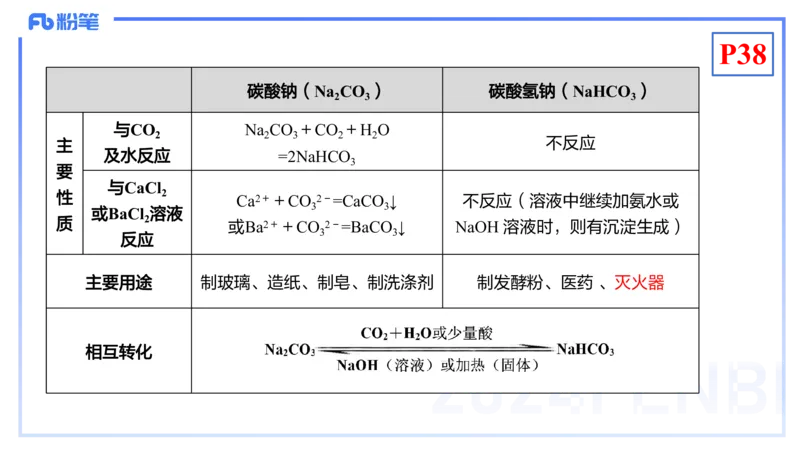
碳酸钠(Na CO ) 碳酸氢钠(NaHCO )
2 3 3
与CO Na CO +CO +H O
2 2 3 2 2
不反应
主
及水反应 =2NaHCO
3
要
与CaCl
性 2
Ca2++CO 2-=CaCO ↓ 不反应(溶液中继续加氨水或
3 3
或BaCl 溶液
质 2
或Ba2++CO 2-=BaCO ↓ NaOH 溶液时,则有沉淀生成)
3 3
反应
主要用途 制玻璃、造纸、制皂、制洗涤剂 制发酵粉、医药 、灭火器
相互转化P39
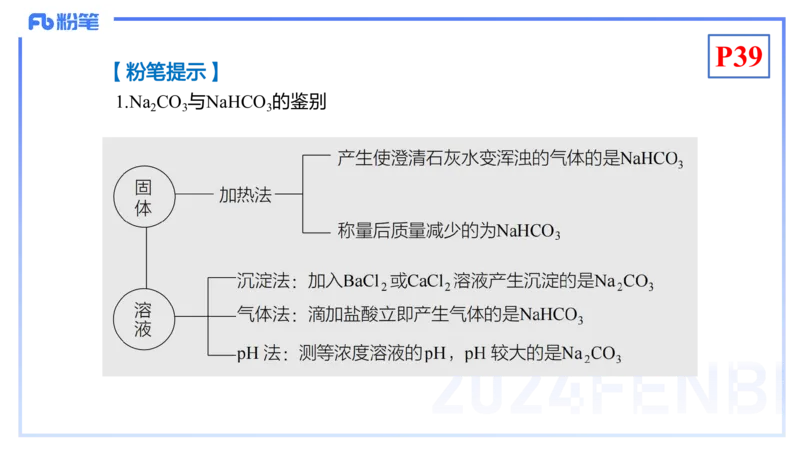
【粉笔提示】
1.Na CO 与NaHCO 的鉴别
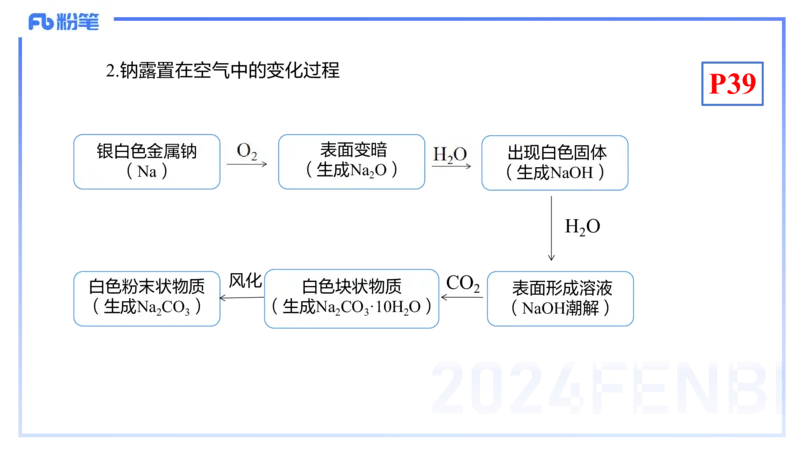
2 3 32.钠露置在空气中的变化过程
P39
银白色金属钠 表面变暗 出现白色固体
(Na) (生成Na O) (生成NaOH)
2
H O
2
风化 CO
白色粉末状物质 白色块状物质 2 表面形成溶液
(生成Na CO ) (生成Na CO ·10H O) (NaOH潮解)
2 3 2 3 2P39
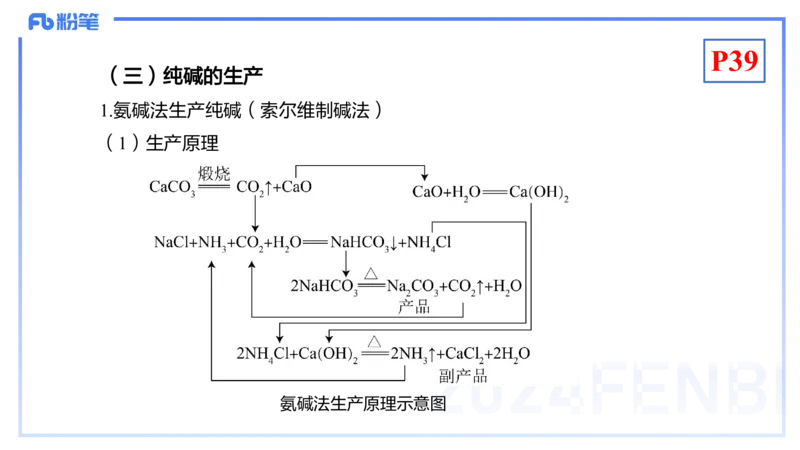
(三)纯碱的生产
1.氨碱法生产纯碱(索尔维制碱法)
(1)生产原理
氨碱法生产原理示意图P39
(2)主要生产过程
①盐水的精制:利用熟石灰、纯碱等除去食盐水中的Mg2+和Ca2+。
②盐水氨化:使溶液显碱性,更易吸收CO ,增大溶液中的HCO -浓
2 3
度,促使Na+和HCO -结合生成NaHCO ,从而结晶析出。
3 3
③氨盐水碳酸化:NH +CO +H O+NaCl NaHCO ↓+NH Cl 。
3 2 2 3 4
④碳酸氢钠的转化:煅烧得到纯碱,同时回收近一半的二氧化碳再利
用。
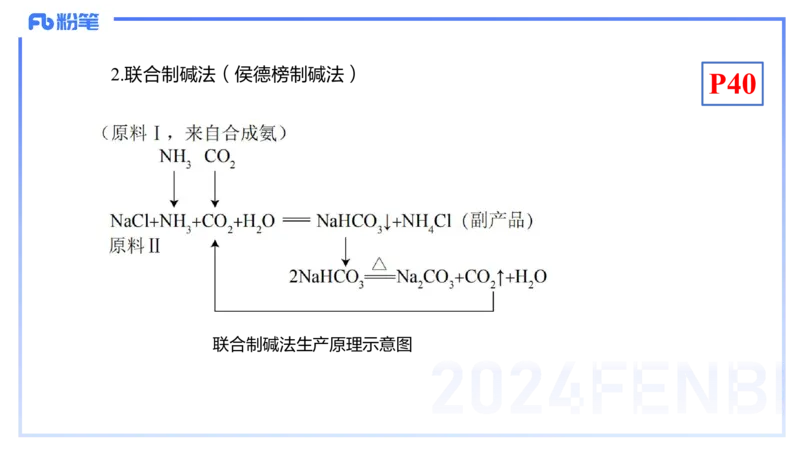
⑤氨的循环:向母液中加入石灰乳,回收氨循环利用。2.联合制碱法(侯德榜制碱法)
P40
联合制碱法生产原理示意图3.两种制碱法的对比
P40
(1)相同点:原理相同。
NH +CO +H O+NaCl NaHCO ↓+NH Cl
3 2 2 3 4
2NaHCO Na CO +H O+CO ↑
3 2 3 2 2
(2)不同点:原料的来源与副产物不同。P40
(3)优缺点:
氨碱法 联合制碱法
生产过程中所需要的NH 和CO 都是由合成氨厂提供的,
3 2
原料(食盐和石灰石)便宜易得、产品纯度高、从滤出NaHCO 后所得到的母液中可回收 NH Cl,因此,
3 4
NH 和部分CO 可循环利用、制造步骤简单、生 它保留了氨碱法的优点,克服了它的缺点,使 NaCl的
3 2
优点
产过程连续且规模大等 利用率提高到了96%以上。体现了大规模联合生产的
优越性,也是综合利用原料、降低成本、减少环境污
染的典型代表
原料食盐中的另一成分氯(Cl-)和石灰石中
的另一成分钙(Ca2+)生成CaCl ,如何处理它
2
成为氨碱法生产的一个问题; 设备循环处理量大,加重了设备的腐蚀
缺点
氨碱法生产中食盐的利用率不高,大约为70%,
如何提高食盐的利用率成为氨碱法生产的另一
个问题书上无
优缺点:
优缺点 氨碱法 联合制碱法
①氨和二氧化碳都是由合成氨厂提供的
原料(食盐和石灰石)便宜易得、
②母液中的氯化铵为副产物,可回收
产品纯度高、NH 和部分CO 可
3 2
③食盐利用率提高到了96%以上
优点 循环利用、制造步骤简单、生产
④体现了大规模联合生产的优越性,也是
过程连续且规模大等
综合利用原料、降低成本、减少环境污染
的典型代表
①难以处理产生的副产物CaCl 设备循环处理量大,加重了设备的腐蚀
2
缺点
②食盐利用率不高,大约为70%二、碱金属元素
P41
碱金属元素包含锂(Li)、钠(Na)、钾(K)、铷(Rb)、铯(Cs)、钫(Fr)六种。
(一)相似性
1.原子结构:最外层上都只有1个电子,次外层均为8个(Li为2个)电子。
2.单质的物理性质:都具有银白色金属光泽(铯略带金色光泽),质软,
密度小,熔点低,导热、导电性好。锂电池的比容量(单位质量的电极材料所
能转换的电量)特别大(这与锂的摩尔质量小有关),因而具有广泛的应用。3.单质的化学性质:都能与氧气和水反应,生成物都是含R+(R为
P41
碱金属元素)的离子化合物。
4.最高价氧化物对应的水化物(ROH)均是强碱。P41
(二)递变性
1.原子结构:随着核电荷数递增,核外电子层数依次增多,原子半径逐渐
增大。
2.单质的物理性质:随着核电荷数递增,熔、沸点逐渐降低(与卤素、氧
族单质相反),密度逐渐增大(K的密度小于Na;Li、Na、K的密度<1 g/cm3,
Rb、Cs的密度>1 g/cm3)。
3.单质的化学性质:随着 Li、Na、K、Rb、Cs 核电荷数的递增,原子核
对最外层电子的吸引力逐渐减弱,失电子能力逐渐增强,因此元素的金属性逐
渐增强,ROH 的碱性逐渐增强。P42
下列氢氧化物中碱性最强的是( )。
A. KOH B. NaOH
C. LiOH D. CsOH【粉笔提示】
P41
1. 与 O 反应时,Li 只生成 Li O,Na 在常温时生成 Na O,加热
2 2 2
时易形成 Na O 。
2 2
2. 与 H O 反应:2R+2H O 2ROH+H ↑,剧烈程度由 Li至Cs
2 2 2
逐渐增强。(三)特殊性
P41
1. 锂的密度比煤油小,不能保存在煤油中,通常密封在石蜡里。
2. 碱金属 Li ~ Cs 的密度呈增大趋势,但 ρ(Na)>ρ(K)。
3. 酸式盐的溶解度一般比相应的正盐大,但S(Na CO )>S(NaHCO )。
2 3 3
4. 锂易与氮气反应(生成Li N)。
3
5. 锂的熔点最高,金属性最弱,因而锂与水反应较慢且反应时锂并不熔化。
6. 碱金属单质及其离子的焰色反应呈现不同的颜色。
7. 试剂瓶中的药品取出后,一般不能放回原瓶,但金属Na、K等需立即放回
原瓶。P42
(四)焰色反应
1.概念:某些金属或它们的化合物在无色火焰中灼烧时会使火焰呈
现特殊颜色的反应。其原理是碱金属元素灼烧时发生电子跃迁释放出
不同能量的光子,使火焰呈现出不同的颜色。焰色反应为物理变化,
属于元素自身的性质。
2.操作步骤:洗、烧、蘸、烧、观、洗、烧。
铂丝 至无色,蘸取待测物 (固体也可以直接蘸取)
观察火焰颜色 至无色P42
3.常见元素的焰色
钠:黄色;
钾:紫色(透过蓝色钴玻璃)。
4.应用:检验部分金属元素的存在(包括单质和化合物)。镁、铝及其化合物P43
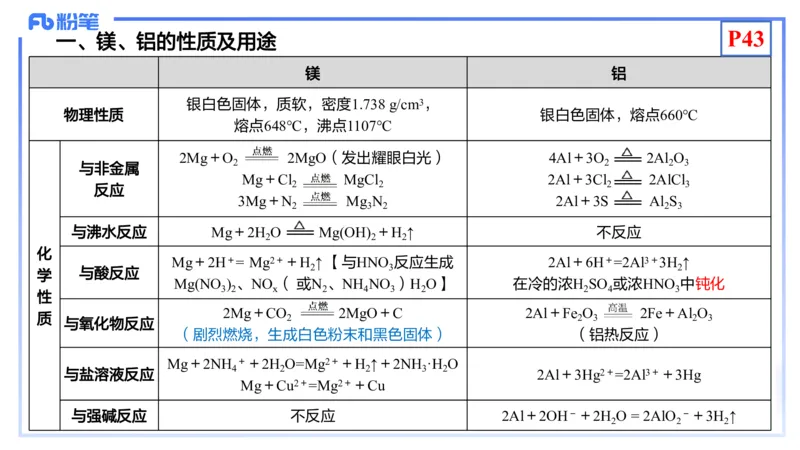
一、镁、铝的性质及用途
镁 铝
银白色固体,质软,密度1.738 g/cm3,
物理性质 银白色固体,熔点660℃
熔点648℃,沸点1107℃
2Mg+O 2MgO(发出耀眼白光) 4Al+3O 2Al O
2 2 2 3
与非金属
Mg+Cl MgCl 2Al+3Cl 2AlCl
2 2 2 3
反应
3Mg+N Mg N 2Al+3S Al S
2 3 2 2 3
与沸水反应 Mg+2H O Mg(OH) +H ↑ 不反应
2 2 2
化
Mg+2H+= Mg2++H ↑ 【与HNO 反应生成 2Al+6H+=2Al3+3H ↑
2 3 2
学 与酸反应
Mg(NO ) 、NO ( 或N 、NH NO )H O】 在冷的浓H SO 或浓HNO 中钝化
3 2 x 2 4 3 2 2 4 3
性
2Mg+CO 2MgO+C 2Al+Fe O 2Fe+Al O
质 2 2 3 2 3
与氧化物反应
(剧烈燃烧,生成白色粉末和黑色固体) (铝热反应)
Mg+2NH ++2H O=Mg2++H ↑+2NH ·H O
4 2 2 3 2
与盐溶液反应 2Al+3Hg2+=2Al3++3Hg
Mg+Cu2+=Mg2++Cu
与强碱反应 不反应 2Al+2OH-+2H O = 2AlO -+3H ↑
2 2 2P43
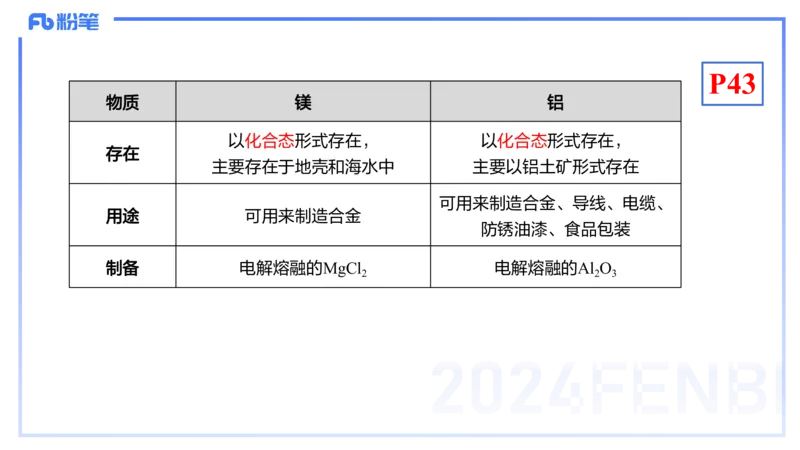
物质 镁 铝
以化合态形式存在, 以化合态形式存在,
存在
主要存在于地壳和海水中 主要以铝土矿形式存在
可用来制造合金、导线、电缆、
用途 可用来制造合金
防锈油漆、食品包装
制备 电解熔融的MgCl 电解熔融的Al O
2 2 3