文档内容
石家庄市第一中学 2025-2026 学年高三上学期期中考试
化学试卷
注意事项:
1.本卷满分 100 分,考试时间 75 分钟。答题前,先将自己的姓名、准考证号填写在试题卷和答题卡上,
并将准考证号条形码粘贴在答题卡上的指定位置。2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡
上对应题目的答案标号涂黑写在试题卷、草稿纸和答题卡上的非答题区域均无效。3.非选择题的作答:用
签字笔直接答在答题卡上对应的答题区域内。写在试题卷、草稿纸和答题卡上的非答题区域均无效。
4.考试结束后,请将本试题卷和答题卡一并上交。
可能用到的相对原子质量: H 1 O 16 B 11 N 14 K 39 Ca 40 Zn 65 Cu 64
一、选择题:本题共 14 小题,每小题3分,共 42分。每小题只有一个选项符合题目要求。
1. 保护文化遗产,弘扬民族精神,共筑中华之魂。下列文物的主要成分为金属材料的是( )
A.元青花人物纹 C.清胭脂红釉罐 D.西周兽面纹青铜盉
B.阳春孔雀石
玉壶春瓶
A. A B. B C. C D. D
2.科学生产中蕴藏着丰富的化学知识。下列劳动项目与所述的化学知识解读错误的是( )
选
劳动项目 化学知识解读
项
课外实践:利用活性炭制作简易水净化处
A 活性炭具有吸附性,可用于除臭、去色
理器
B 自主探究:用石膏制作豆腐 点卤时,CaSO 用作凝固剂
4
“可回收物”中的废纸、塑料、玻璃均属于高分子化
C 社区服务:将社区垃圾进行分类回收
合物
D 学农活动:使用草木灰对蔬菜施肥 草木灰含有钾盐,属于钾肥
A.A B.B C.C D.D
3. 劳动才能创造价值。下列对职业的工作内容以及工作实例的描述不恰当的是选项 职业 工作内容 工作实例
用 断代法测定伊犁吉仁台沟口青铜
A 科技考古研究员 文物断代
文物的历史年代
研究不同类型的电池构成材料在不同用
B 电池研发人员 性能测试
途时对温度,湿度等环境因素的适应性
C 环境保护工程师 环境监测 用滴定法测定南湖湖水中的氨氮含量
用高精度化学检测仪器检测八一钢铁厂
D 测试工程师 材料测试
出厂钢材的元素含量
A. A B. B C. C D. D
4.下列化学用语或图示表达正确的是( )
A.乙烯分子中的 键: B.次氯酸的电子式:
C. 的VSEPR模型: D.基态 原子的价电子排布式:
5.室温下,下列各组离子在指定溶液中能大量共存的是
A.FeCl 溶液中:K+、H+、NO 、SO B.中性透明溶液中:K+、SO 、NO 、Fe3+
2
C.无色透明溶液中:K+、Mg2+、Cl-、NO D.FeCl 溶液中:Na+、SO 、SCN-、NO
3
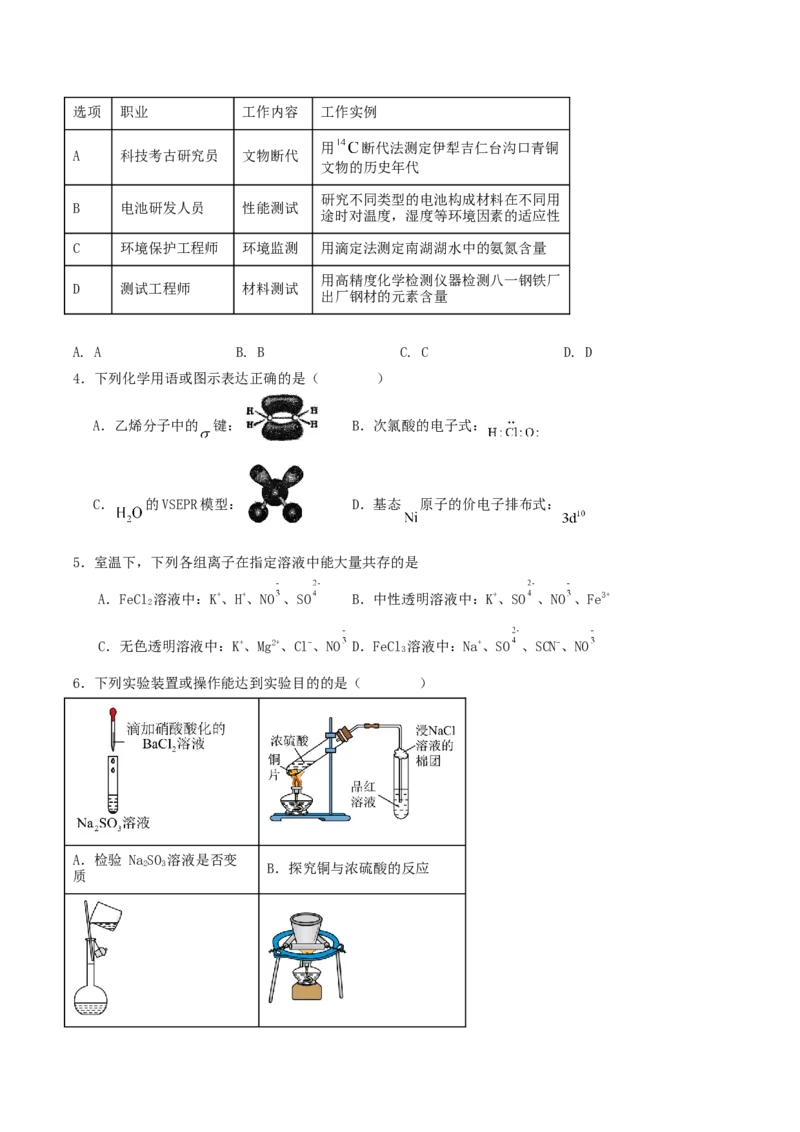
6.下列实验装置或操作能达到实验目的的是( )
A.检验 NaSO 溶液是否变
2 3 B.探究铜与浓硫酸的反应
质C.向容量瓶中转移溶液 D.观察钾在空气中燃烧的现象
A.A B.B C.C D.D
7.下列操作能促进水的电离且使溶液中 的是( )
A.将水加热煮沸 B.向水中加入一小块钠
C.向水中加入 D.向水中加入
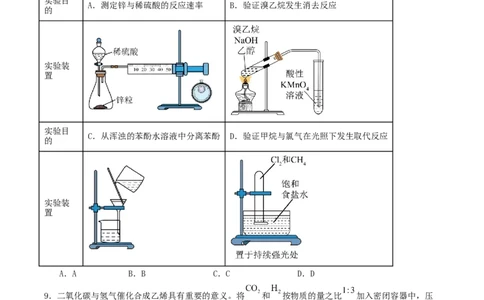
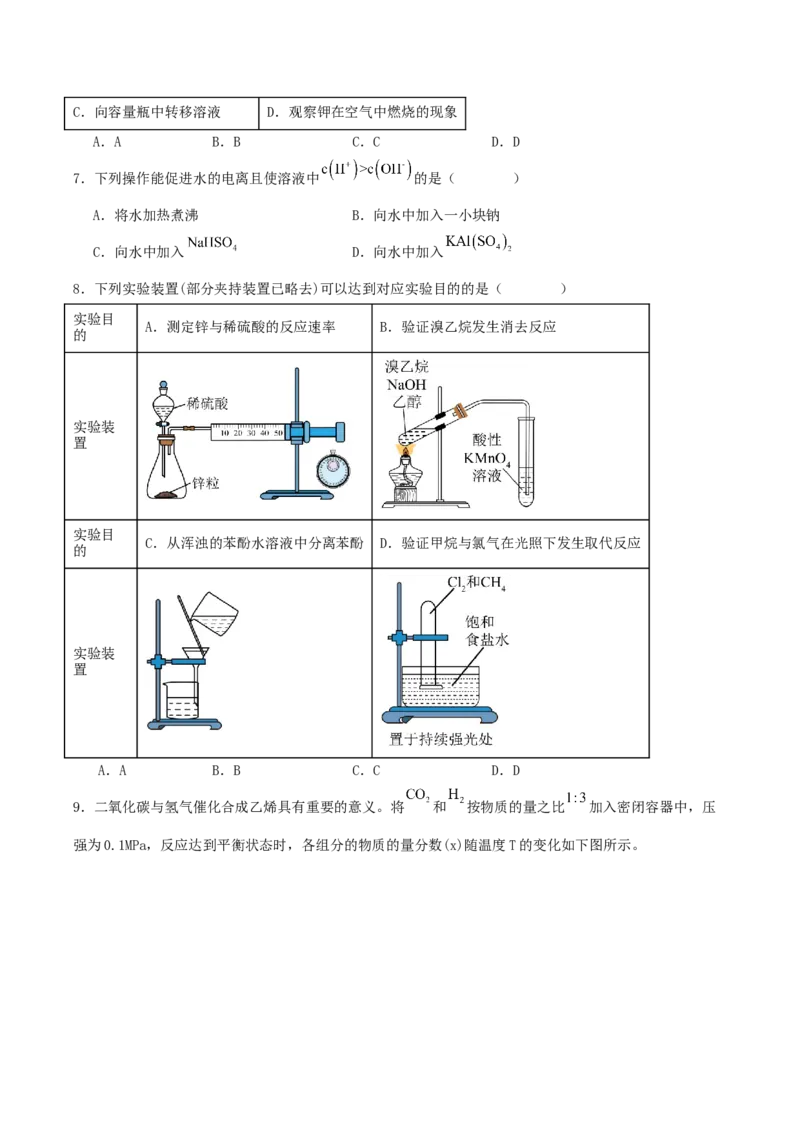
8.下列实验装置(部分夹持装置已略去)可以达到对应实验目的的是( )
实验目
A.测定锌与稀硫酸的反应速率 B.验证溴乙烷发生消去反应
的
实验装
置
实验目
C.从浑浊的苯酚水溶液中分离苯酚 D.验证甲烷与氯气在光照下发生取代反应
的
实验装
置
A.A B.B C.C D.D
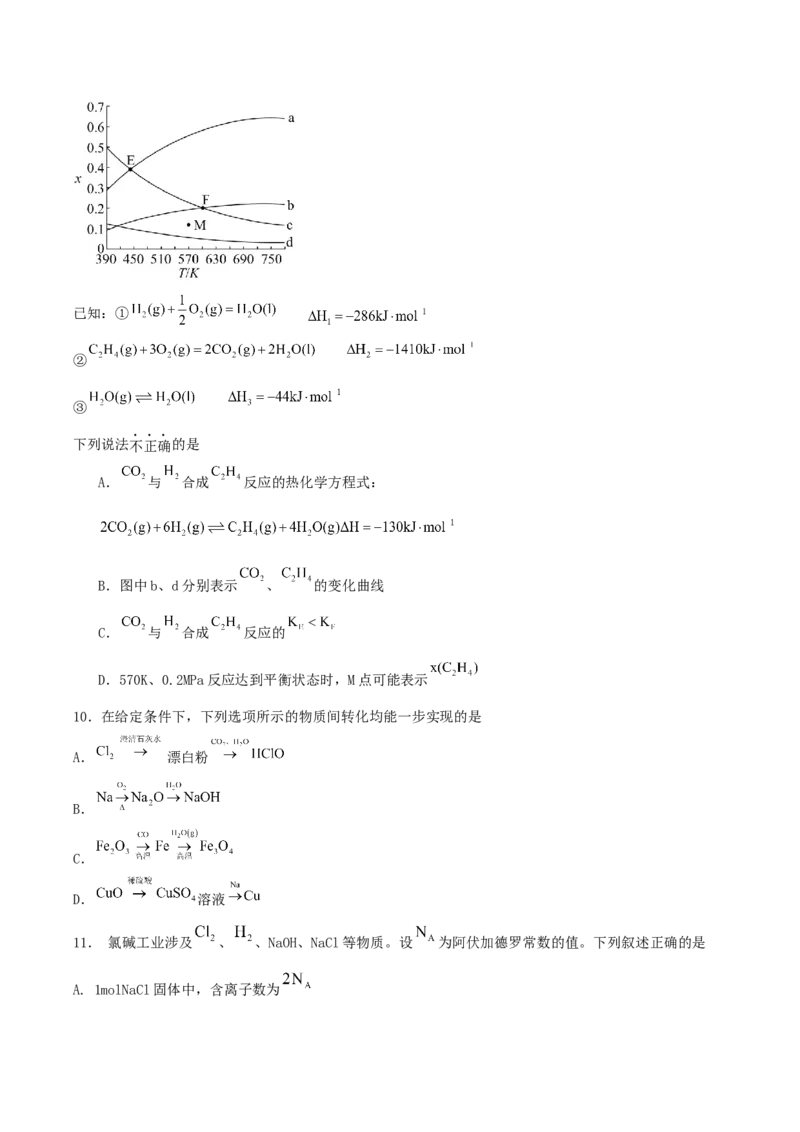
9.二氧化碳与氢气催化合成乙烯具有重要的意义。将 和 按物质的量之比 加入密闭容器中,压
强为0.1MPa,反应达到平衡状态时,各组分的物质的量分数(x)随温度T的变化如下图所示。已知:①
②
③
下列说法不正确的是
A. 与 合成 反应的热化学方程式:
B.图中b、d分别表示 、 的变化曲线
C. 与 合成 反应的
D.570K、0.2MPa反应达到平衡状态时,M点可能表示
10.在给定条件下,下列选项所示的物质间转化均能一步实现的是
A. 漂白粉
B.
C.
D. 溶液
11. 氯碱工业涉及 、 、NaOH、NaCl等物质。设 为阿伏加德罗常数的值。下列叙述正确的是
A. 1molNaCl固体中,含离子数为B. 1L 的NaOH溶液中,含有氧原子数为
C. 标准状况下,22.4L 和 的混合气体含有共价键数目为
D. 将 与NaOH溶液反应制备消毒液,消耗1mol 转移电子数为
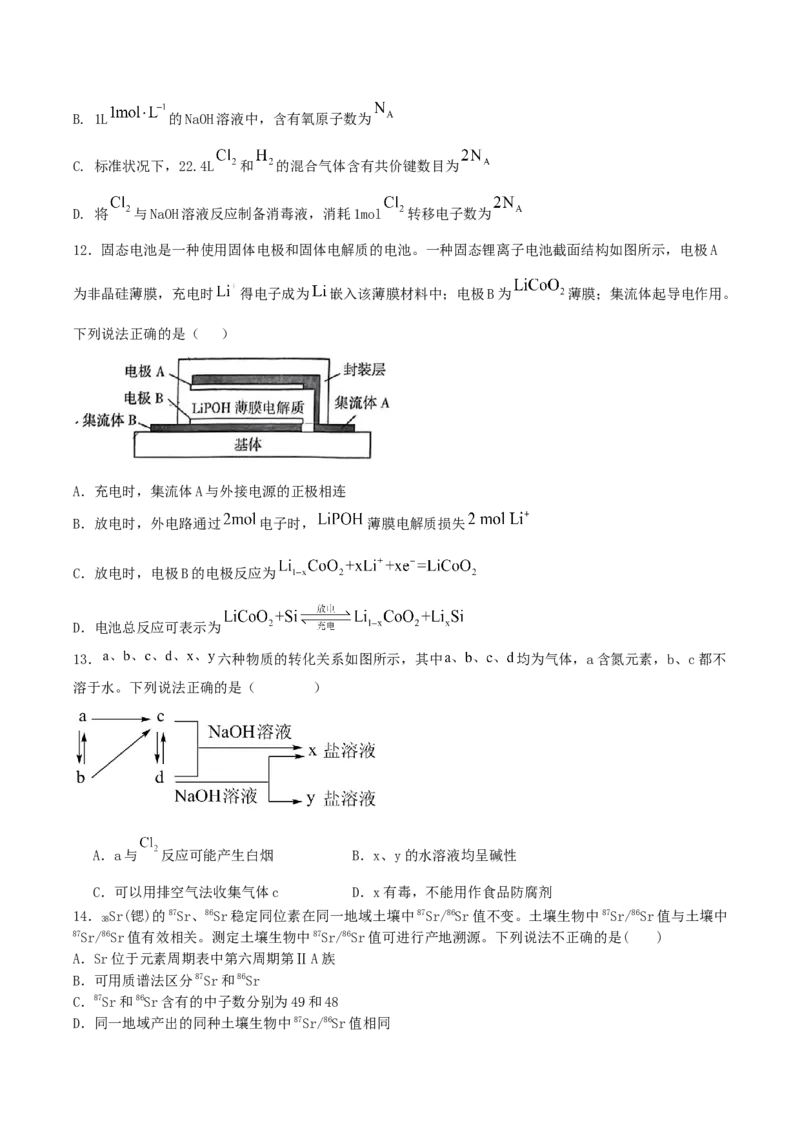
12.固态电池是一种使用固体电极和固体电解质的电池。一种固态锂离子电池截面结构如图所示,电极A
为非晶硅薄膜,充电时 得电子成为 嵌入该薄膜材料中;电极B为 薄膜;集流体起导电作用。
下列说法正确的是( )
A.充电时,集流体A与外接电源的正极相连
B.放电时,外电路通过 电子时, 薄膜电解质损失
C.放电时,电极B的电极反应为
D.电池总反应可表示为
13. 六种物质的转化关系如图所示,其中 均为气体,a含氮元素,b、c都不
溶于水。下列说法正确的是( )
A.a与 反应可能产生白烟 B.x、y的水溶液均呈碱性
C.可以用排空气法收集气体c D.x有毒,不能用作食品防腐剂
14. Sr(锶)的87Sr、86Sr稳定同位素在同一地域土壤中87Sr/86Sr值不变。土壤生物中87Sr/86Sr值与土壤中
38
87Sr/86Sr值有效相关。测定土壤生物中87Sr/86Sr值可进行产地溯源。下列说法不正确的是( )
A.Sr位于元素周期表中第六周期第ⅡA族
B.可用质谱法区分87Sr和86Sr
C.87Sr和86Sr含有的中子数分别为49和48
D.同一地域产出的同种土壤生物中87Sr/86Sr值相同二、非选择题:本题共4小题,共 58 分。
15.(1) 与 反应生成 和氢气,在 、 下,已知每消耗
NaBH (s) H O(l) NaBO (s) 25 ℃ 101 kPa
4 2 2
放热 ,该反应的热化学方程式是
3.8 g NaBH (s) 21.6 kJ
4
。
(2) [北京师大附中2022期中]CO 在催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,
2
乙二醇会深度加氢生成乙醇。
ΔH=−131.9 kJ⋅mol−1
ΔH=−94.8 kJ⋅mol−1
获取乙二醇的反应历程可分为两步:
Ⅰ.
Ⅱ.EC 加氢生成乙二醇与甲醇
步骤Ⅱ的热化学方程式是 。
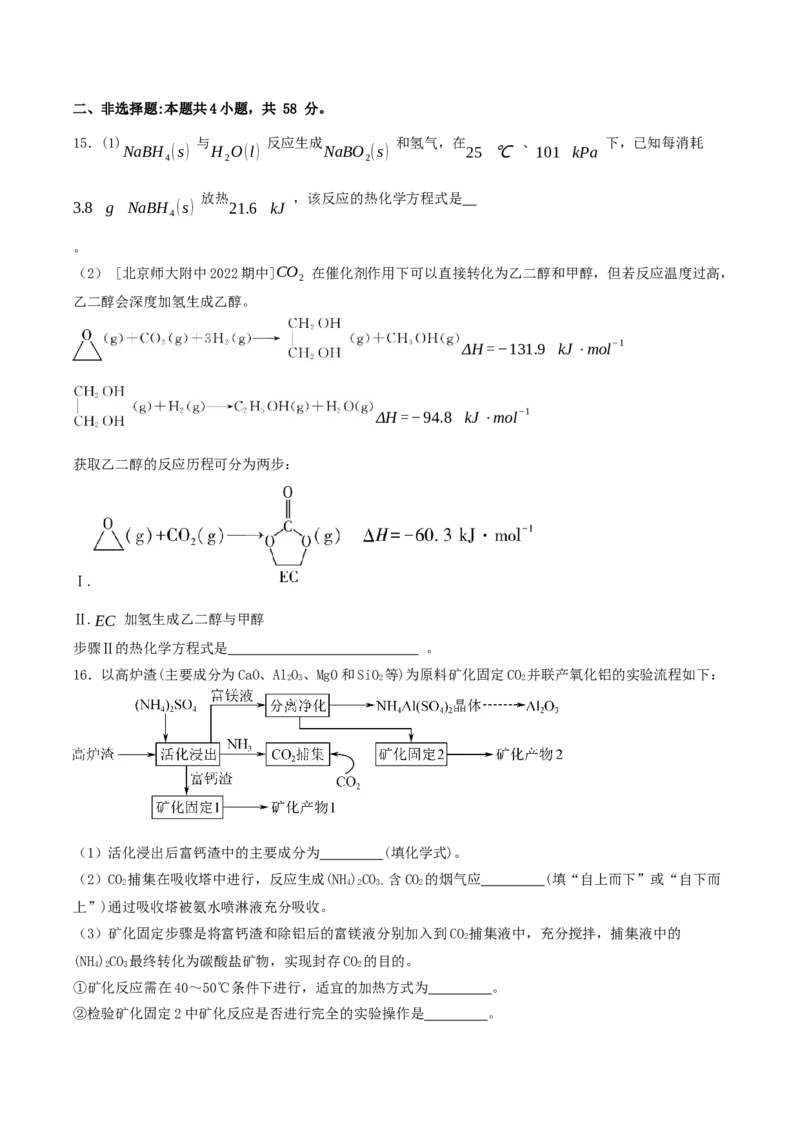
16.以高炉渣(主要成分为CaO、AlO、MgO和SiO 等)为原料矿化固定CO 并联产氧化铝的实验流程如下:
2 3 2 2
(1)活化浸出后富钙渣中的主要成分为 (填化学式)。
(2)CO 捕集在吸收塔中进行,反应生成(NH)CO 含CO 的烟气应 (填“自上而下”或“自下而
2 4 2 3。 2
上”)通过吸收塔被氨水喷淋液充分吸收。
(3)矿化固定步骤是将富钙渣和除铝后的富镁液分别加入到CO 捕集液中,充分搅拌,捕集液中的
2
(NH)CO 最终转化为碳酸盐矿物,实现封存CO 的目的。
4 2 3 2
①矿化反应需在40~50℃条件下进行,适宜的加热方式为 。
②检验矿化固定2中矿化反应是否进行完全的实验操作是 。③将两步矿化后的母液合并,结晶处理得到 (填化学式),可循环利用。
(4)分离净化得到的NHAl(SO) 晶体可制备高纯AlO。请补充完整相应的实验方案:取一定量
4 4 2 2 3
NHAl(SO) 晶体,经提纯后配成溶液, ,控制反应温度为55℃, ,干燥,置于马弗炉
4 4 2
中900℃煅烧,获得高纯AlO 产品。已知:酸性环境中生成的Al(OH) 黏性大,不易过滤。实验中可选用
2 3 3
的试剂:1 mol·L-1的氨水、BaCl 溶液、蒸馏水。
2
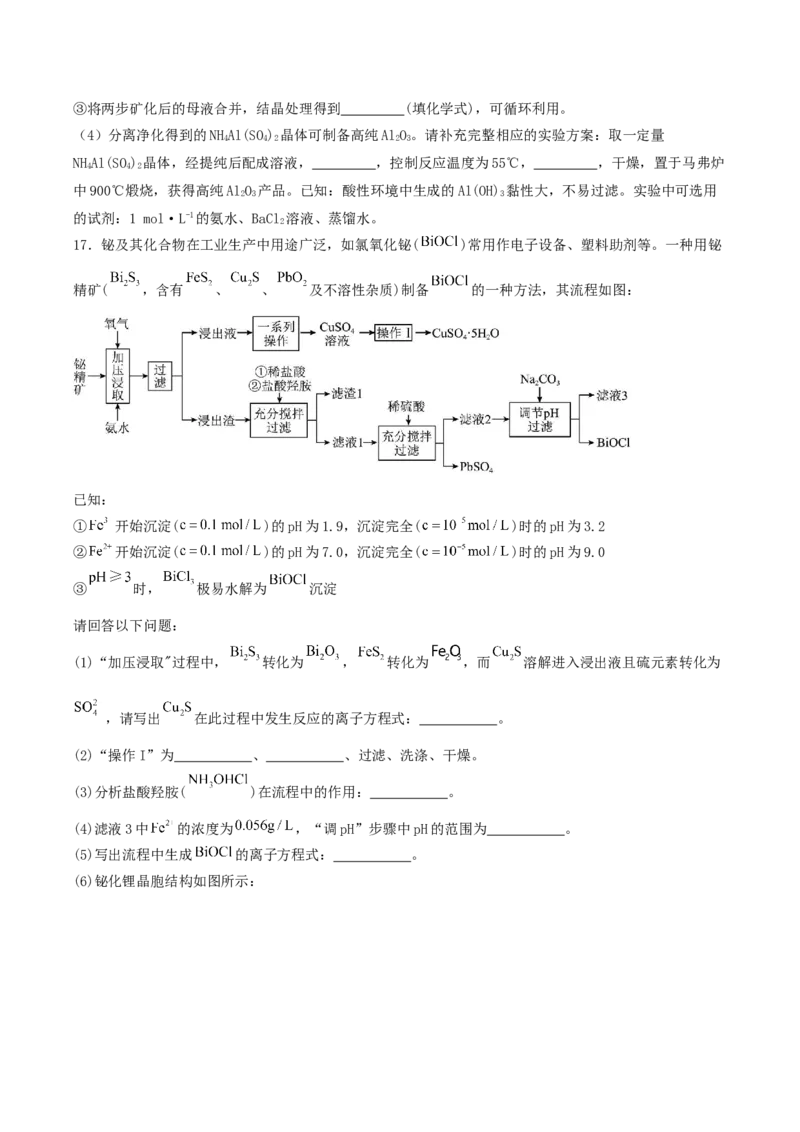
17.铋及其化合物在工业生产中用途广泛,如氯氧化铋( )常用作电子设备、塑料助剂等。一种用铋
精矿( ,含有 、 、 及不溶性杂质)制备 的一种方法,其流程如图:
已知:
① 开始沉淀( )的pH为1.9,沉淀完全( )时的pH为3.2
② 开始沉淀( )的pH为7.0,沉淀完全( )时的pH为9.0
③ 时, 极易水解为 沉淀
请回答以下问题:
(1)“加压浸取"过程中, 转化为 , 转化为 ,而 溶解进入浸出液且硫元素转化为
,请写出 在此过程中发生反应的离子方程式: 。
(2)“操作I”为 、 、过滤、洗涤、干燥。
(3)分析盐酸羟胺( )在流程中的作用: 。
(4)滤液3中 的浓度为 ,“调pH”步骤中pH的范围为 。
(5)写出流程中生成 的离子方程式: 。
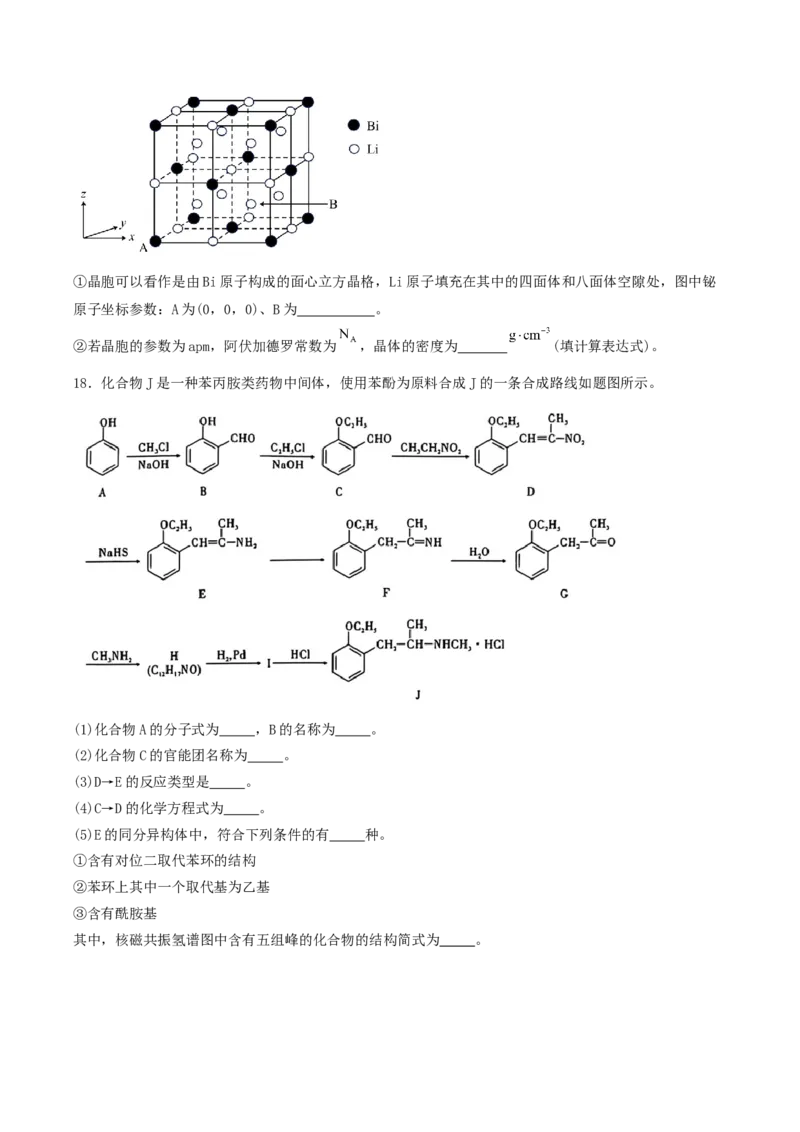
(6)铋化锂晶胞结构如图所示:①晶胞可以看作是由Bi原子构成的面心立方晶格,Li原子填充在其中的四面体和八面体空隙处,图中铋
原子坐标参数:A为(0,0,0)、B为 。
②若晶胞的参数为apm,阿伏加德罗常数为 ,晶体的密度为 (填计算表达式)。
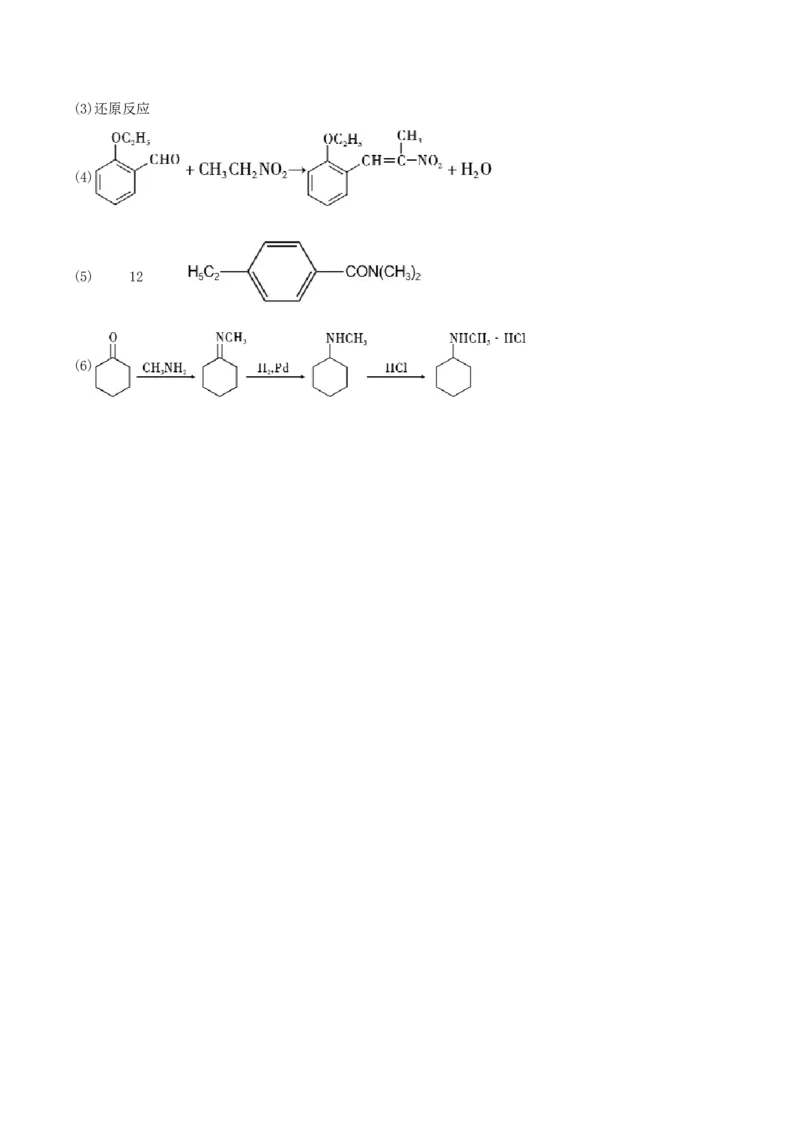
18.化合物J是一种苯丙胺类药物中间体,使用苯酚为原料合成J的一条合成路线如题图所示。
(1)化合物A的分子式为 ,B的名称为 。
(2)化合物C的官能团名称为 。
(3)D→E的反应类型是 。
(4)C→D的化学方程式为 。
(5)E的同分异构体中,符合下列条件的有 种。
①含有对位二取代苯环的结构
②苯环上其中一个取代基为乙基
③含有酰胺基
其中,核磁共振氢谱图中含有五组峰的化合物的结构简式为 。(6)请参照上述合成路线,以环已酮( )和必要的其他试剂为原料,制备药物中间体N-甲基环已胺盐酸
盐( )的合成路线 。石家庄市第一中学 2025-2026 学年高三上学期期中考试
化学答案
1.D 2.C 3.A 4.C 5.C 6.D 7.D 8.A 9.C 10.C 11.A 12.C 13.A
14.A
15.(1)NaBH (s)+2H O(l) ΔH=−216 kJ⋅mol−1;(2)
4 2 ¿
ΔH=−71.6 kJ⋅mol−1
16.(1)CaSO、SiO
4 2
(2)自下而上
(3)40~50℃水浴加热 取矿化反应后的悬浊液静置,向上层清液中继续滴加除铝后的富镁液,若无
沉淀生成,说明矿化反应已经进行完全 (NH)SO
4 2 4
(4)在搅拌下将其缓慢加入到1 mol/L的氨水中 直至不再产生沉淀;过滤,所得沉淀用蒸馏水洗涤
2~3次,取最后一次洗涤后的滤出液,加入BaCl 溶液,不产生白色沉淀
2
17.(1) 或
(2) 蒸发浓缩 冷却结晶
(3)将铅元素从+4价还原为+2价,便于后续“沉铅”;将 还原为 ,提高产品纯度
(4)
(5)
(6)
18.(1) 邻羟基苯甲醛(或2-羟基苯甲醛)
(2)醛基、醚键(3)还原反应
(4)
(5) 12
(6)