文档内容
2025 年 1 月浙江卷化学试题
一、单选题
1.下列属于极性分子的是
A.HCl B.N C.He D.CH
2 4
2.下列化学用语表示不正确的是
...
A.基态S原子的电子排布式:2s22p4 B.质量数为14的碳原子: 14C
6
C.乙烯的结构简式:CH =CH D.H O的电子式:
2 2 2
3.化学与生产生活密切相关,下列说法不正确的是
...
A.ClO 具有强氧化性,可用于杀菌消毒
2
B.聚丙烯是高分子材料,可用作吸水剂
C.Na CO 溶液呈碱性,可用于除油污
2 3
D.硬铝密度小、强度高,抗腐蚀能力强,可用作飞机材料
4.根据元素周期律,下列说法不正确的是
...
A.第一电离能:N>O>S B.化合物中键的极性:SiCl >PCl
4 3
C.碱性:LiOH>KOH D.化合物中离子键百分数:MgO>Al O
2 3
5.关于实验室安全,下列说法不正确的是
...
A.若不慎盐酸沾到皮肤上,应立即用大量水冲洗,然后用3%~5%NaHCO 溶液冲洗
3
B.实验室制备Cl 时,可用NaOH溶液吸收尾气
2
C.水银易挥发,若不慎有水银洒落,无需处理
D.PbS难溶于水,可用Na S处理废水中的Pb2+,再将沉淀物集中送至环保单位进一步处理
2
6.关于溴的性质,下列说法不正确的是
...
A.Br-可被Cl 氧化为Br
2 2
B.Br 与SO 水溶液反应的还原产物为Br-
2 2
C.Br +2Fe2+=2Fe3++2Br-,说明氧化性:Br >Fe3+
2 2
D.1molBr 与足量NaOH溶液反应生成NaBr和NaBrO ,转移5mol电子
2 3
7.下列物质的结构或性质不能说明其用途的是
..
A.葡萄糖分子结构中有多个羟基,故葡萄糖可与银氨溶液反应制作银镜
B.具有网状结构的交联橡胶弹性好、强度高,故可用作汽车轮胎材料
C.SiC的碳、硅原子间通过共价键形成空间网状结构,硬度大,故SiC可用作砂轮磨料
D.NaHCO 能中和酸并受热分解产生气体,故可用作加工馒头的膨松剂
3
8.下列方程式不正确的是
...
A.MnO 与浓盐酸反应:MnO +4H++2Cl− ≜Mn2++Cl ↑+2H O
2 2 2 2
B.NO 与H O反应:3NO +H O=2H++2NO−+NO
2 2 2 2 3
Δ
C.将少量灼热的CuO加入CH CH OH中:CH CH OH+CuO→CH CHO+Cu+H O
3 2 3 2 3 2
D.将SO 通入酸性KMnO 溶液:5SO +2MnO−+4H+ =5SO2−+2Mn2++2H O
2 4 2 4 4 2
9.抗坏血酸(维生素C)是常用的抗氧化剂。
下列说法不正确的是
...A.可用质谱法鉴别抗坏血酸和脱氢抗坏血酸 B.抗坏血酸可发生缩聚反应
C.脱氢抗坏血酸不能与NaOH溶液反应 D.1个脱氢抗坏血酸分子中有2个手性碳原子
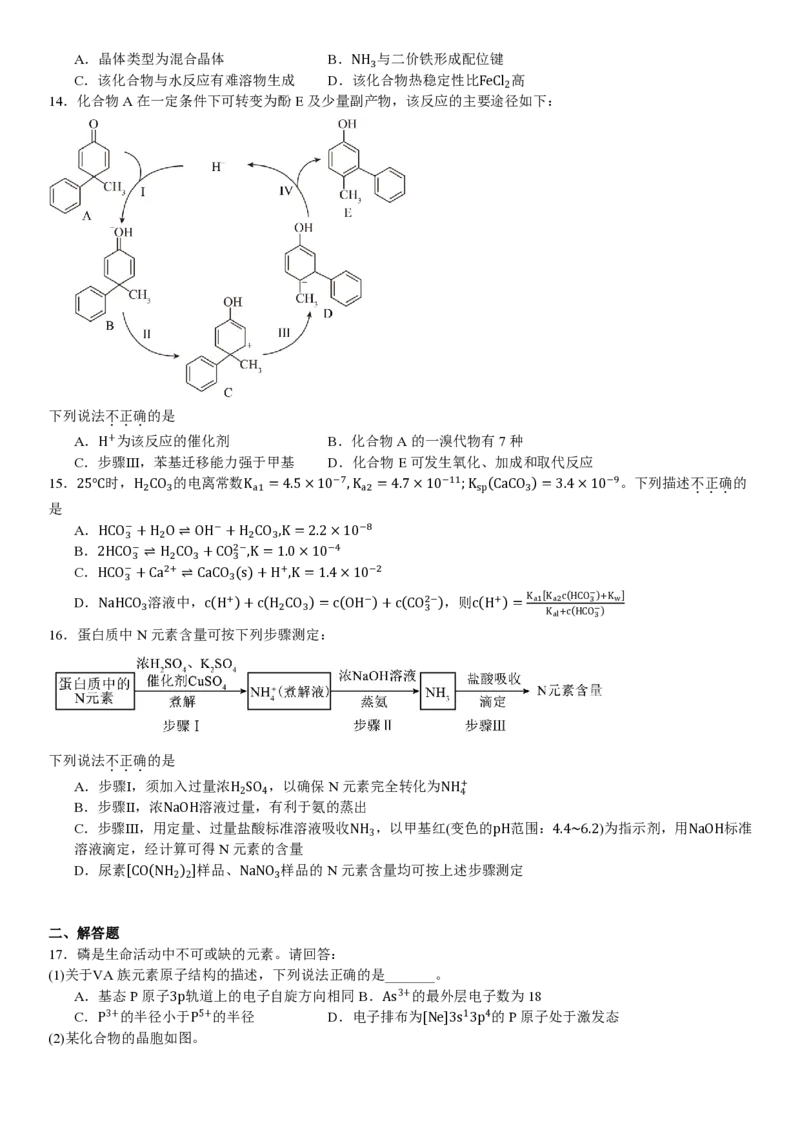
10.提纯NaCl粗品(含少量的Ca2+、Mg2+、K+和SO2−)得到NaCl纯品的方案如下,所用试剂为BaCl 溶液、Na CO 溶
4 2 2 3
液、盐酸和NaOH溶液。
下列说法不正确的是
...
A.用过量的BaCl 溶液除去SO2−
2 4
B.Ca2+、Mg2+、SO2−通过生成沉淀后过滤除去
4
C.4种试剂的使用顺序为BaCl 溶液、Na CO 溶液、盐酸、NaOH溶液
2 2 3
D.调pH后的滤液蒸发至大量固体析出,趁热过滤、洗涤、干燥后即得NaCl纯品
11.下列说法正确的是
A.常温常压下H (g)和O (g)混合无明显现象,则反应2H (g)+O (g)=2H O(l)在该条件下不自发
2 2 2 2 2
B.3H (g)+N (g)⇌2NH (g) ΔH<0,升高温度,平衡逆移,则反应的平衡常数减小
2 2 3
C.CO(g)+H (g)⇌C(s)+H O(g) ΔH<0,则正反应的活化能大于逆反应的活化能
2 2
D.Na(s)+ 1 Cl (g)=NaCl(s) ΔH<0, Na+(g)+Cl−(g)=NaCl(s) ΔH<0,则Na(s)+ 1 Cl (g)=Na+(g)+
2 2
2 2
Cl−(g) ΔH<0
12.一种可充放电Li−O 电池的结构示意图如图所示。该电池放电时,产物为Li O和Li O ,随温度升高Q(消耗
2 2 2 2
1molO 转移的电子数)增大。下列说法不正确的是
2 ...
A.熔融盐中LiNO 的物质的量分数影响充放电速率
3
B.充放电时,Li+优先于K+通过固态电解质膜
C.放电时,随温度升高Q增大,是因为正极区O2−转化为O2−
2
D.充电时,锂电极接电源负极
13.某化合物Fe(NH ) Cl 的晶胞如图所示,下列说法不正确的是
3 2 2 ...A.晶体类型为混合晶体 B.NH 与二价铁形成配位键
3
C.该化合物与水反应有难溶物生成 D.该化合物热稳定性比FeCl 高
2
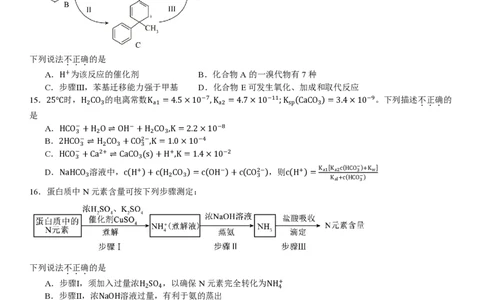
14.化合物A在一定条件下可转变为酚E及少量副产物,该反应的主要途径如下:
下列说法不正确的是
...
A.H+为该反应的催化剂 B.化合物A的一溴代物有7种
C.步骤Ⅲ,苯基迁移能力强于甲基 D.化合物E可发生氧化、加成和取代反应
15.25℃时,H CO 的电离常数K =4.5×10−7,K =4.7×10−11;K (CaCO )=3.4×10−9。下列描述不正确的
2 3 a1 a2 sp 3 ...
是
A.HCO−+H O⇌OH−+H CO ,K=2.2×10−8
3 2 2 3
B.2HCO− ⇌H CO +CO2−,K=1.0×10−4
3 2 3 3
C.HCO−+Ca2+ ⇌CaCO (s)+H+,K=1.4×10−2
3 3
D.NaHCO 溶液中,c(H+)+c(H CO )=c(OH−)+c(CO2−),则c(H+)= Ka1 [Ka2c(HCO3 −)+Kw ]
3 2 3 3 Kal+c(HCO
3
−)
16.蛋白质中N元素含量可按下列步骤测定:
下列说法不正确的是
...
A.步骤Ⅰ,须加入过量浓H SO ,以确保N元素完全转化为NH+
2 4 4
B.步骤Ⅱ,浓NaOH溶液过量,有利于氨的蒸出
C.步骤Ⅲ,用定量、过量盐酸标准溶液吸收NH ,以甲基红(变色的pH范围:4.4~6.2)为指示剂,用NaOH标准
3
溶液滴定,经计算可得N元素的含量
D.尿素[CO(NH ) ]样品、NaNO 样品的N元素含量均可按上述步骤测定
2 2 3
二、解答题
17.磷是生命活动中不可或缺的元素。请回答:
(1)关于ⅤA族元素原子结构的描述,下列说法正确的是_______。
A.基态P原子3p轨道上的电子自旋方向相同 B.As3+的最外层电子数为18
C.P3+的半径小于P5+的半径 D.电子排布为[Ne]3s13p4的P原子处于激发态
(2)某化合物的晶胞如图。①化学式是 ;
②将0.01mol该化合物加入到含少量石蕊的10mLH O中,实验现象是 (从酸碱性和溶解性角度推测)。
2
(3)两分子H PO (K =4.8×10−13)脱水聚合得到一分子H P O (K =2.0×10−7),从PO3−、HP O3−的结构角度分
3 4 a3 4 2 7 a3 4 2 7
析K 差异的原因 。
a3
(4)兴趣小组对某磷灰石[主要成分为Ca (PO ) OH、Ca (PO ) F、Ca (PO ) Cl和少量SiO ]进行探究,设计了两种制
5 4 3 5 4 3 5 4 3 2
备H PO 的方法:
3 4
Ⅰ.用稍过量的浓H SO 与磷灰石反应,得到H PO 溶液、少量SiF 气体、渣(主要成分为CaSO )。
2 4 3 4 4 4
Ⅱ.将磷灰石脱水、还原,得到的白磷(P )燃烧后与水反应制得H PO 溶液。
4 3 4
①方法I,所得H PO 溶液中含有的杂质酸是 。
3 4
②以方法Ⅰ中所得渣为硫源,设计实验制备无水Na SO ,流程如下:
2 4
溶液A是 ,系列操作B是 ,操作C是 。
③方法Ⅱ中,脱水得到的Ca (PO ) O(足量)与炭(C)、SiO 高温下反应,生成白磷(P )和另一种可燃性气体,该反应
10 4 6 2 4
的化学方程式是 。
18.二甲胺[(CH ) NH]、N,N-二甲基甲酰胺[HCON(CH ) ]均是用途广泛的化工原料。请回答:
3 2 3 2
(1)用氨和甲醇在闭容器中合成二甲胺,反应方程式如下:
Ⅰ.NH (g)+CH OH(g)⇌CH NH (g)+H O(g)
3 3 3 2 2
Ⅱ.CH NH (g)+CH OH(g)⇌(CH ) NH(g)+H O(g)
3 2 3 3 2 2
Ⅲ.(CH ) NH(g)+CH OH(g)⇌(CH ) N(g)+H O(g)
3 2 3 3 3 2
可改变甲醇平衡转化率的因素是_______。
A.温度 B.投料比[n(NH ):n(CH OH)] C.压强 D.催化剂
3 3
(2)25℃下,(CH ) NH·H O的电离常数为Kb,-lgK =3.2,则1mol/L[(CH ) NH ] +Cl-水溶液的pH= 。
3 2 2 b 3 2 2
(3)在[(CH ) NH ] +Cl-的有机溶液中电化学还原CO 制备HCON(CH ) 阴极上生成HCON(CH ) 的电极反应方程式
3 2 2 2 3 2 3 2
是 。
(4)上述电化学方法产率不高,工业中常用如下反应生产HCON(CH ) :(CH ) NH(g)+CO(g)=HCON(CH ) (l)。
3 2 3 2 3 2
某条件下反应自发且熵减,则反应在该条件下ΔH 0(填“>”、“<”或“=”)。
(5)有研究采用CO 、H 和(CH ) NH催化反应制备HCON(CH ) 。在恒温密闭容器中,投料比
2 2 3 2 3 2
n(CO ):n(H ):n[(CH ) NH]=20:15:1,催化剂M足量。反应方程式如下:
2 2 3 2
催化剂
Ⅳ.CO (g)+H (g) HCOOH(g)
2 2
碱性物质
V.HCOOH(g)+(CH ) NH(g)=HCON(CH ) (g)+H O(g)
3 2 3 2 2
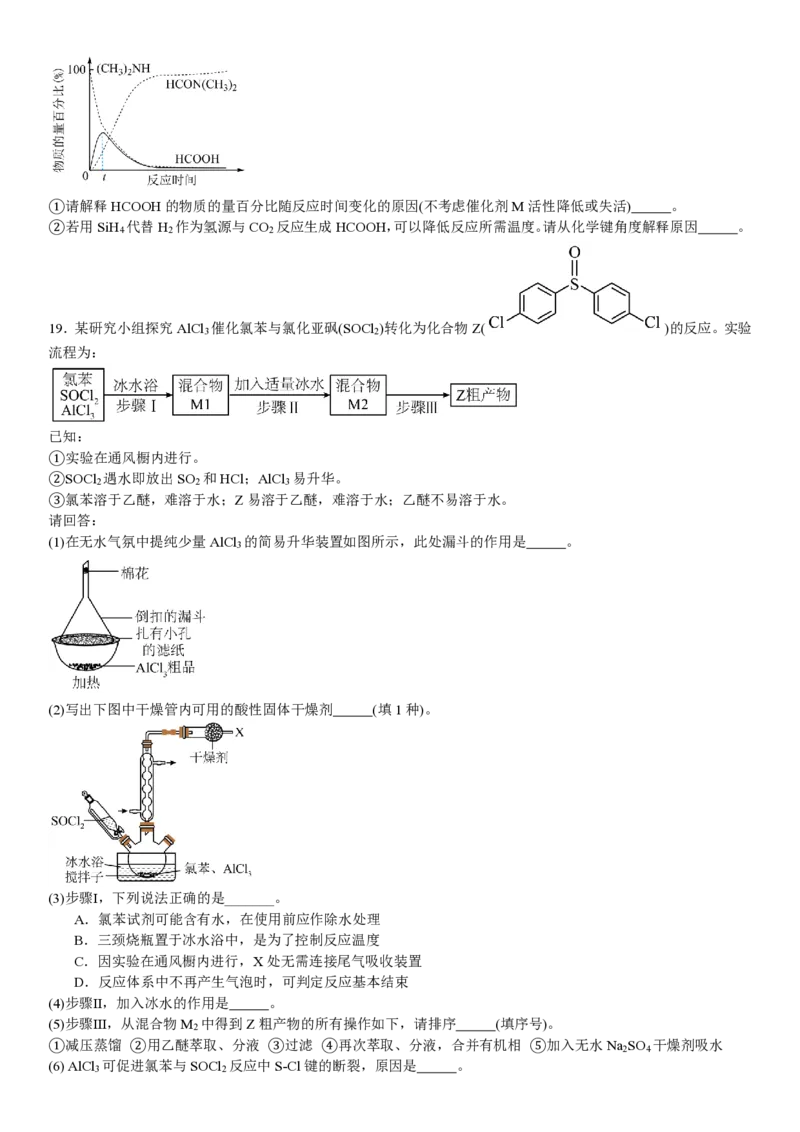
HCOOH、(CH ) NH、HCON(CH ) 三种物质的物质的量百分比随反应时间变化如图所示。
3 2 3 2
(例:HCOOH的物质的量百分比= n(HCOOH) ×100%)
n(HCOOH)+n[(CH3 ) 2NH]+n[HCON(CH3 )
2
]①请解释HCOOH的物质的量百分比随反应时间变化的原因(不考虑催化剂M活性降低或失活) 。
②若用SiH 代替H 作为氢源与CO 反应生成HCOOH,可以降低反应所需温度。请从化学键角度解释原因 。
4 2 2
19.某研究小组探究AlCl 催化氯苯与氯化亚砜(SOCl )转化为化合物Z( )的反应。实验
3 2
流程为:
已知:
①实验在通风橱内进行。
②SOCl 遇水即放出SO 和HCl;AlCl 易升华。
2 2 3
③氯苯溶于乙醚,难溶于水;Z易溶于乙醚,难溶于水;乙醚不易溶于水。
请回答:
(1)在无水气氛中提纯少量AlCl 的简易升华装置如图所示,此处漏斗的作用是 。
3
(2)写出下图中干燥管内可用的酸性固体干燥剂 (填1种)。
(3)步骤Ⅰ,下列说法正确的是_______。
A.氯苯试剂可能含有水,在使用前应作除水处理
B.三颈烧瓶置于冰水浴中,是为了控制反应温度
C.因实验在通风橱内进行,X处无需连接尾气吸收装置
D.反应体系中不再产生气泡时,可判定反应基本结束
(4)步骤Ⅱ,加入冰水的作用是 。
(5)步骤Ⅲ,从混合物M 中得到Z粗产物的所有操作如下,请排序 (填序号)。
2
①减压蒸馏 ②用乙醚萃取、分液 ③过滤 ④再次萃取、分液,合并有机相 ⑤加入无水Na SO 干燥剂吸水
2 4
(6) AlCl 可促进氯苯与SOCl 反应中S-Cl键的断裂,原因是 。
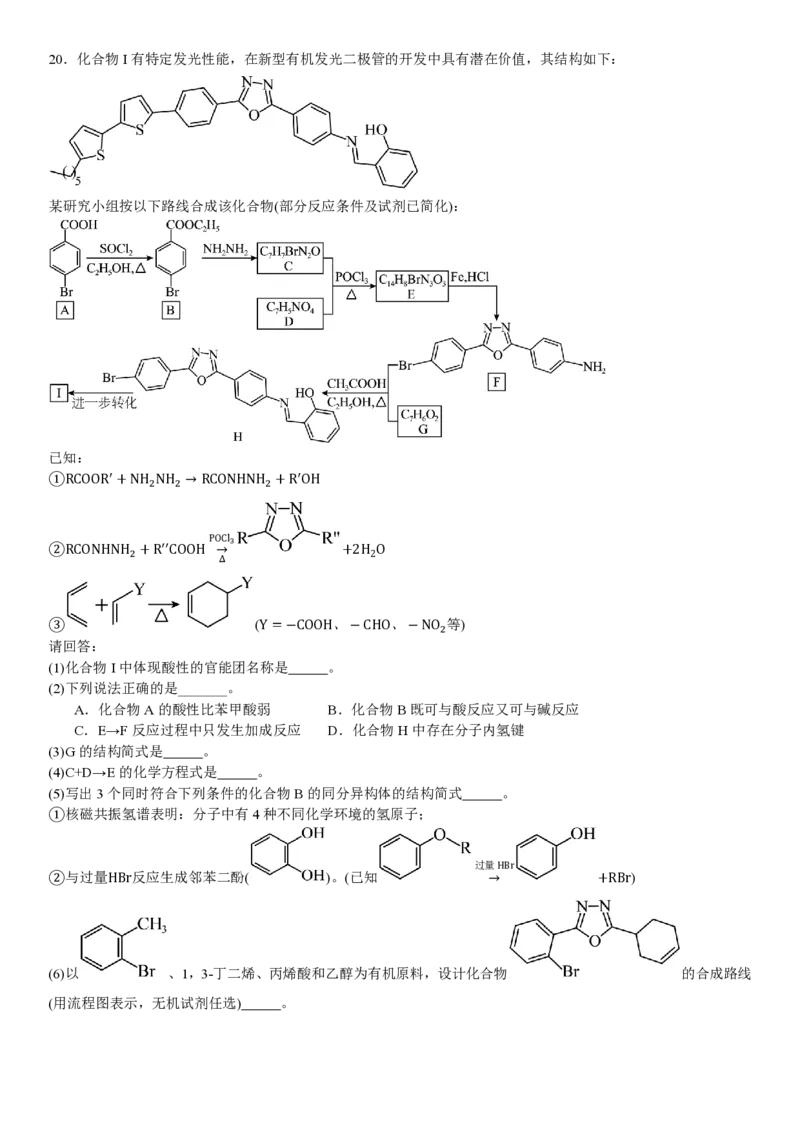
3 220.化合物I有特定发光性能,在新型有机发光二极管的开发中具有潜在价值,其结构如下:
某研究小组按以下路线合成该化合物(部分反应条件及试剂已简化):
已知:
①RCOOR′+NH NH →RCONHNH +R′OH
2 2 2
②RCONHNH +R′′COOH
PO
→
Cl3
+2H O
2 2
Δ
③ (Y=−COOH、−CHO、−NO 等)
2
请回答:
(1)化合物I中体现酸性的官能团名称是 。
(2)下列说法正确的是_______。
A.化合物A的酸性比苯甲酸弱 B.化合物B既可与酸反应又可与碱反应
C.E→F反应过程中只发生加成反应 D.化合物H中存在分子内氢键
(3)G的结构简式是 。
(4)C+D→E的化学方程式是 。
(5)写出3个同时符合下列条件的化合物B的同分异构体的结构简式 。
①核磁共振氢谱表明:分子中有4种不同化学环境的氢原子;
过量HBr
②与过量HBr反应生成邻苯二酚( )。(已知 → +RBr)
(6)以 、1,3-丁二烯、丙烯酸和乙醇为有机原料,设计化合物 的合成路线
(用流程图表示,无机试剂任选) 。