文档内容
重难点 04 元素推断与元素周期律
1.(2024·高一上·江苏省南京市·期末)根据“位置-结构-性质”关系可预测某些物质的性质。下列说
法不正确的是
A.氩位于0族,其单质的化学性质稳定
B.铯是ⅠA族元素,其单质能与水剧烈反应
C.溴是ⅦA族元素,其单质能与 溶液发生置换反应
D.锗位于周期表中金属与非金属元素的分界处,其单质可作半导体材料
2.(2024·高一上·山西省部分学校·期末)已知Te为第五周期第ⅥA族元素。下列结论错误的是
A.粒子半径: B.氧化性:
C.酸性: D.金属性:
3.(2024·高一上·河南省洛阳市·期末)部分短周期元素常见化合价与原子序数的关系如图所示,下列说
法正确的是
A.X元素的最高价氧化物溶于水能导电,是电解质
B.R非金属性强于W,R的氧化物对应的水化物的酸性也强于W的氧化物对应的水化物的酸性
C.物质 中既含有离子键又含有共价键
D.物质YR中,每个粒子最外层均达到8电子稳定结构
4.(2024·高一上·天津市重点校·期末)硒( )位于第四周期第VI 族,由元素周期表和周期律的知识,
下列说法不正确的是
A.热稳定性: B.还原性:
C.非金属性: D.酸性:
5.(2024·高一上·湖北省十堰市·期末)W、X、Y、Z为短周期主族元素,原子序数依次增大,这4种元
素的最外层电子数之和为20。 为空气中含量最多的气体,元素X和Z位于同一主族且X为地壳中
含量最多的元素。下列说法正确的是
A.原子半径:Z>Y
B.最简单氢化物的沸点:W>X
C.相同条件下,密度:
D.化合物 既可溶于强酸也可溶于强碱
1
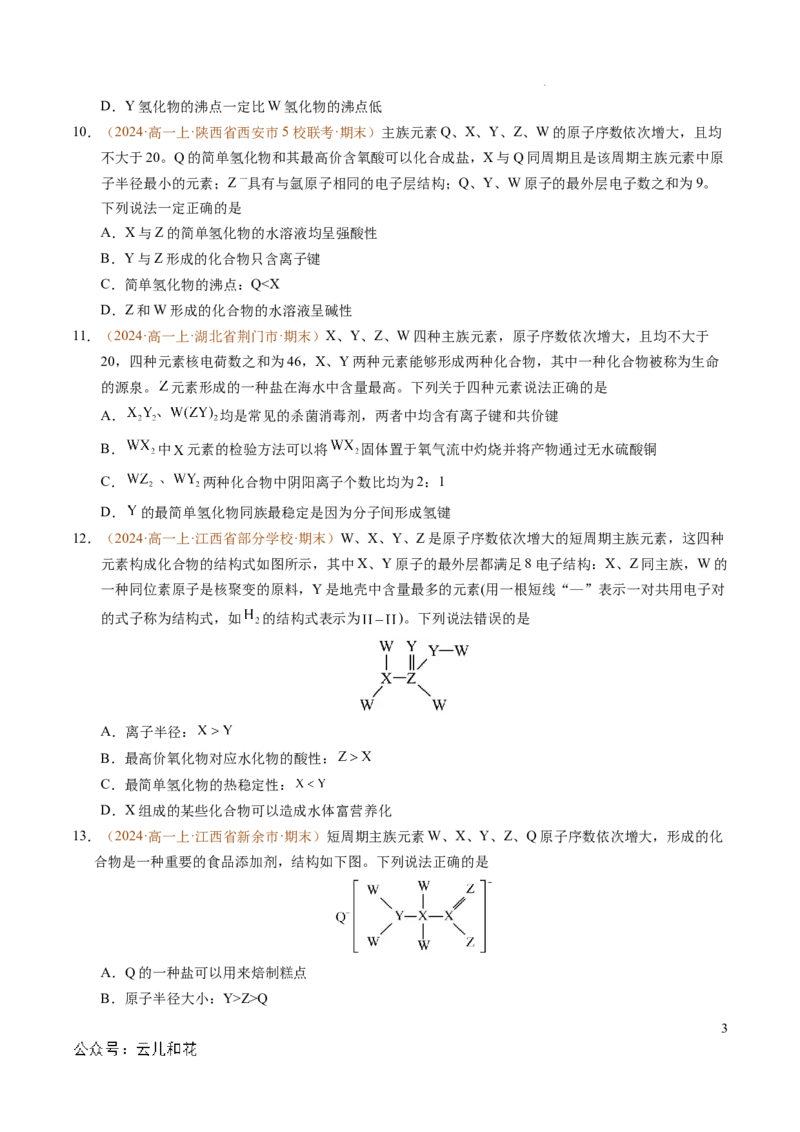
学科网(北京)股份有限公司6.(2024·高一上·陕西省西安市5校联考·期末)短周期主族元素X、Y、Z、W的原子序数依次增加,
K、L、M均是由这些元素组成的氧化物,甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是
常见的气体。K是红棕色气体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法
不正确的是( )
A.Y、Z、W三种元素电负性:W>Z>Y
B.Y、Z、W三种元素的第一电离能:W>Z>Y
C.Y、Z、W与氢元素均可形成含非极性键的二元化合物
D.由X、Y、Z、W构成的化合物中可能含有离子键
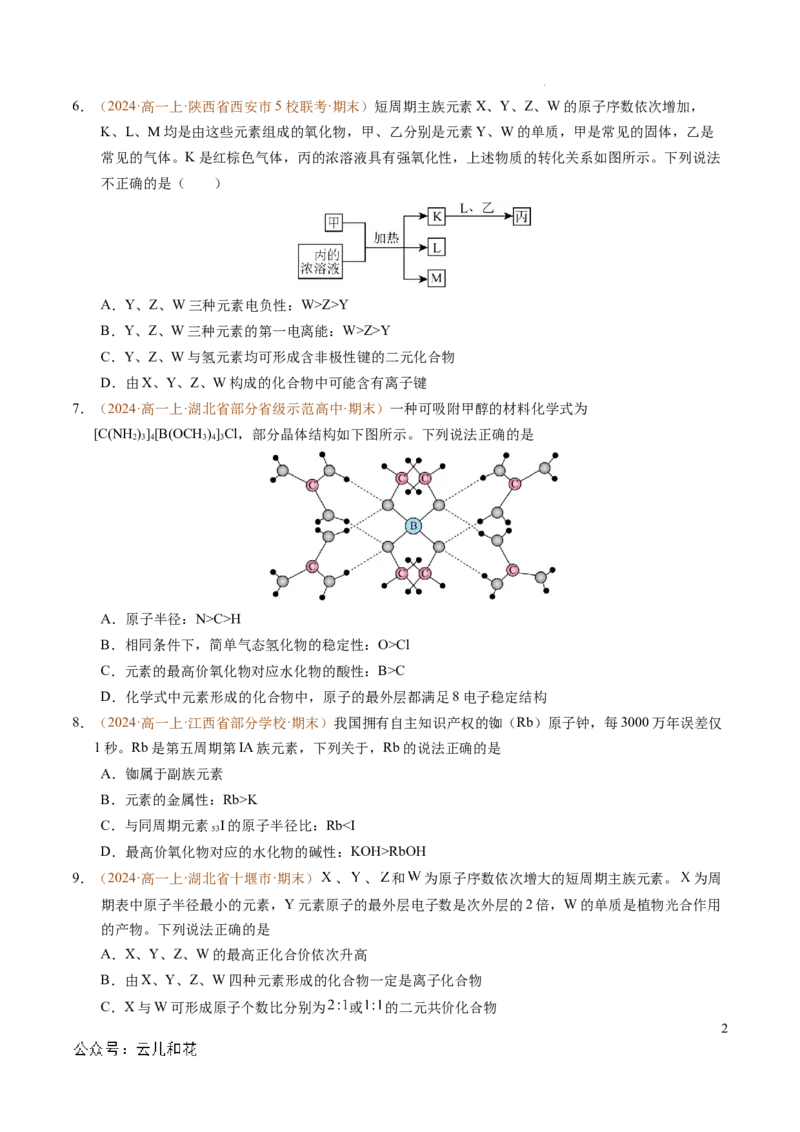
7.(2024·高一上·湖北省部分省级示范高中·期末)一种可吸附甲醇的材料化学式为
[C(NH )][B(OCH )]Cl,部分晶体结构如下图所示。下列说法正确的是
2 3 4 3 4 3
A.原子半径:N>C>H
B.相同条件下,简单气态氢化物的稳定性:O>Cl
C.元素的最高价氧化物对应水化物的酸性:B>C
D.化学式中元素形成的化合物中,原子的最外层都满足8电子稳定结构
8.(2024·高一上·江西省部分学校·期末)我国拥有自主知识产权的铷(Rb)原子钟,每3000万年误差仅
1秒。Rb是第五周期第IA族元素,下列关于,Rb的说法正确的是
A.铷属于副族元素
B.元素的金属性:Rb>K
C.与同周期元素 I的原子半径比:RbRbOH
9.(2024·高一上·湖北省十堰市·期末) 、 、 和 为原子序数依次增大的短周期主族元素。 为周
期表中原子半径最小的元素,Y元素原子的最外层电子数是次外层的2倍,W的单质是植物光合作用
的产物。下列说法正确的是
A.X、Y、Z、W的最高正化合价依次升高
B.由X、Y、Z、W四种元素形成的化合物一定是离子化合物
C.X与W可形成原子个数比分别为 或 的二元共价化合物
2
学科网(北京)股份有限公司D.Y氢化物的沸点一定比W氢化物的沸点低
10.(2024·高一上·陕西省西安市5校联考·期末)主族元素Q、X、Y、Z、W的原子序数依次增大,且均
不大于20。Q的简单氢化物和其最高价含氧酸可以化合成盐,X与Q同周期且是该周期主族元素中原
子半径最小的元素;Z一具有与氩原子相同的电子层结构;Q、Y、W原子的最外层电子数之和为9。
下列说法一定正确的是
A.X与Z的简单氢化物的水溶液均呈强酸性
B.Y与Z形成的化合物只含离子键
C.简单氢化物的沸点:QZ>Q
3
学科网(北京)股份有限公司C.W和Z只能形成两种10电子微粒
D.该化合物中Z原子不满足8电子稳定结构
14.(2024·高一上·吉林省部分名校·期末)X、Y、Z、W、R为原子序数依次增大的短周期主族元素,元
素X的原子核内只有1个质子,元素R的原子比元素W的原子多8个电子,由上述元素组成的一种化
合物M的结构式如图所示。下列说法错误的是
A.M分子中含有极性共价键和非极性共价键
B.化合物M中的原子均满足8电子稳定结构
C. 可用于自来水消毒
D. 分子呈正四面体形
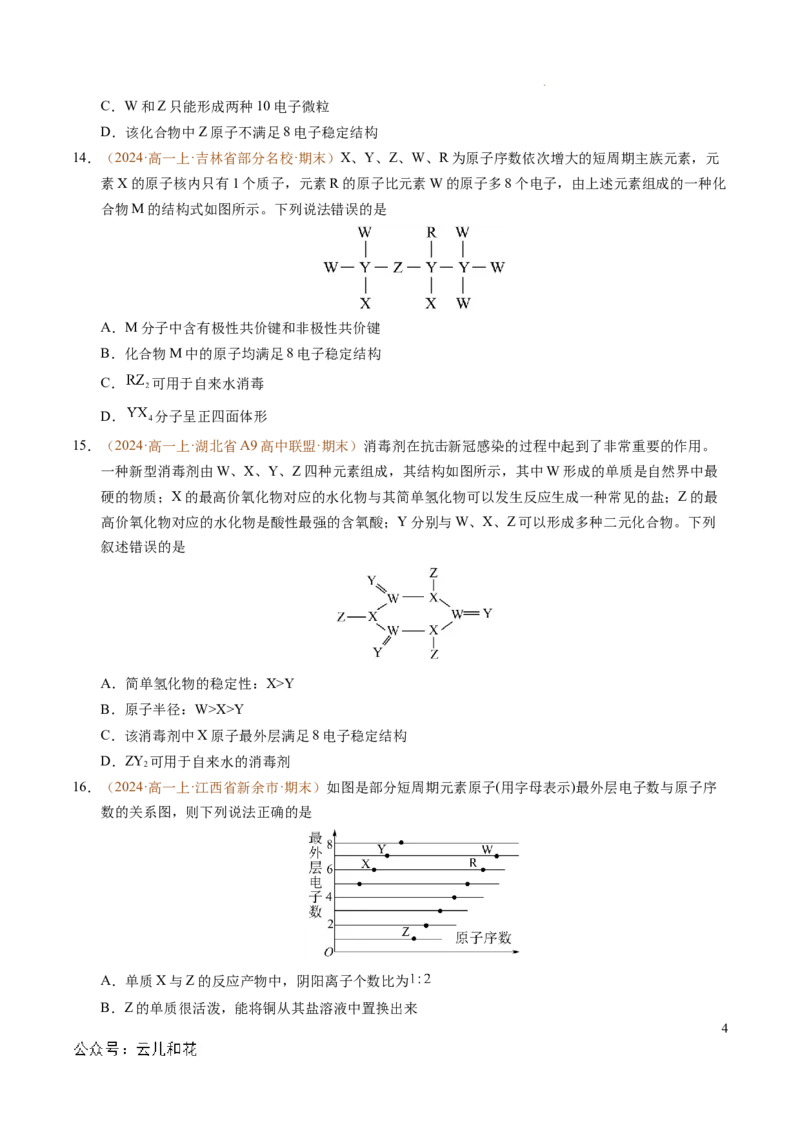
15.(2024·高一上·湖北省A9高中联盟·期末)消毒剂在抗击新冠感染的过程中起到了非常重要的作用。
一种新型消毒剂由W、X、Y、Z四种元素组成,其结构如图所示,其中W形成的单质是自然界中最
硬的物质;X的最高价氧化物对应的水化物与其简单氢化物可以发生反应生成一种常见的盐;Z的最
高价氧化物对应的水化物是酸性最强的含氧酸;Y分别与W、X、Z可以形成多种二元化合物。下列
叙述错误的是
A.简单氢化物的稳定性:X>Y
B.原子半径:W>X>Y
C.该消毒剂中X原子最外层满足8电子稳定结构
D.ZY 可用于自来水的消毒剂
2
16.(2024·高一上·江西省新余市·期末)如图是部分短周期元素原子(用字母表示)最外层电子数与原子序
数的关系图,则下列说法正确的是
A.单质X与Z的反应产物中,阴阳离子个数比为
B.Z的单质很活泼,能将铜从其盐溶液中置换出来
4
学科网(北京)股份有限公司C.X与R的氢化物稳定性:
D.W的单质有毒,不能用于自来水的消毒
17.(2024·高一上·湖南省怀化市·期末)短周期主族元素 X、Y、Z、W 原子序数依次增大,X 是地壳中
含量最多的元素,Y 原子的最外层只有一个电子,Z 位于元素周期表ⅢA族,W 与X属于同一主
族。下列说法正确的是
A.原子半径:r(W) > r(Z) > r(Y)
B.由X、Y 组成的化合物中均不含共价键
C.Y 的最高价氧化物的水化物的碱性比Z的弱
D.X 的简单气态氢化物的热稳定性比W的强
18.(2024·高一上·江西省新余市·期末)A、B、C、D、E为常见的主族元素,根据下表信息回答问题。
元素 元素性质或原子结构信息
A A元素是地壳中含量最多的金属元素
B B元素的原子失去2个电子,所得到的微粒具有与氖原子相同的电子层结构
C C元素原子核外M层比L层少2个电子
D 与A同周期,化合价有 , 价等
E 原子结构示意图:
(1)写出A单质溶于 溶液的化学方程式 。
(2)比较A、B最高价氧化物对应水化物的碱性强弱 (用化学式表示)。
(3)用电子式表示B和D形成化合物的过程: 。
(4)元素E在周期表中的位置 ,关于元素D、E非金属性强弱的判断不正确的是 (填标
号)。
a.D、E与 反应D更容易
b.D的单质可与E的钠盐水溶液发生置换反应
c.最高价氧化物对应水化物的酸性:E>D
d.气态氢化物稳定性:D>E
(5)R的原子序数比C大,且与C处于相邻周期同一主族,关于元素R及其化合物的有关说法正确
的是_______(填标号)。
A.R原子的半径比C原子的大
B. 的稳定性比 的强
5
学科网(北京)股份有限公司C. 能与 溶液反应
D. 可以使酸性高锰酸钾溶液褪色
19.(2024·高一上·吉林省部分名校·期末)已知a、b、c、d、e、f为原子序数依次增大的短周期主族元
素。b与e的原子序数之和等于c与d的原子序数之和,且b、c处于不同周期。其中a、b、e、f在元
素周期表中的相对位置如图。请回答下列问题:
a b
e f
(1)e在元素周期表中的位置是 。
(2)e、f的最高价氧化物对应的水化物中,酸性较强的是 (填化学式)。
(3)a的气态氢化物与其最高价氧化物对应的水化物反应,生成的化合物中所含的化学键类型有
。
(4)加热条件下,b的单质 与c的单质反应的生成物的电子式为 。
(5)d的单质与c的最高价氧化物对应的水化物的溶液反应的离子方程式为 。
(6)c、d、e、f原子的原子半径由大到小的顺序为 (用元素符号表示),简单离子的半径由
大到小的顺序为 (用离子符号表示)。
20.(2024·高一上·江苏省南京市·期末)随着原子序数的递增,7种短周期元素(用字母表示)原子半径
的相对大小、最高正化合价或最低负化合价的变化如图所示。
请回答下列问题:
(1)b在元素周期表中的位置是 。
(2)a、c、d可形成一种原子个数比为 的化合物,其电子式是 。
(3)比较d、e简单离子的半径大小 (用离子符号表示)。
(4)比较f、g的最高价氧化物的水化物的酸性强弱 (用化学式表示)。
(5)设计一个实验比较g的单质与 的氧化性强弱 (须使用淀粉-KI溶液)。
(6)g的一种含氧酸钾盐(g元素为 价)可与 溶液在强碱性条件下制取绿色消毒剂
,反应的离子方程式为 ,反应每转移 电子时,生成 的物质的量为
。
21.(2024·高一上·湖南省怀化市·期末)Ⅰ.根据已学过的化学知识,回答下列问题:
(1)科学家称硅是“21世纪的能源”,硅在元素周期表中的位置是 。
6
学科网(北京)股份有限公司(2)常用硝酸银溶液检验氯离子,写出该反应的离子方程式 。
(3)运用“纳米药物分子运输车”(如图所示)可提高治疗肿瘤的效果。回答下列问题:
①“纳米药物分子运输车”分散于水中所得的分散系 (填“属于”或“不属于”)胶体。
②“有机物外充”中含有酒精、蔗糖、醋酸这三种有机物,其中属于电解质的是 。
③Fe O 是一种非常重要的磁性材料,可用还原铁粉与水蒸气高温制得,写出该反应的化学方程式
3 4
。
(4)下列物质:N、CO、CH、KOH、NaHCO 、CaO、HSO 其中属于酸性氧化物的是
2 2 4 3 2 4
(写化学式,下同);属于有机物的是 。
II.下表是元素周期表的一部分,除标出的元素外,表中每个序号代表一种元素,请根据要求回答问
题:
IA 0
1 H IIA ⅢA IVA VA VIA VIIA
2 ① ②
3 ③ ④ ⑤ ⑥ Ar
4 ⑦
(5)短周期中金属性最强的元素是 (填元素符号);其中形成的非金属单质不含化学键的
是 (填化学式)。
(6)③、④、⑦三种元素按原子半径由大到小的顺序排列为 (用元素符号表达)。
(7)⑤、⑥的最高价氧化物对应的水化物相互反应的离子方程式为 。
(8)由H、①组成的最简单化合物所含化学键类型为 写出该化合物的电子式
。
(9)灼烧③、⑥形成的化合物,火焰呈 。
7
学科网(北京)股份有限公司