文档内容
湖北省部分名校 2025-2026 学年度上学期高三 9 月月考
高三化学试卷
命制单位:新高考试题研究中心
考试时间:2025年9月19日下午14:30-17:05 试卷满分:100分
注意事项:
1.答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将准考证号条形码粘贴
在答题卡上的指定位置。
2.选择题的作答:每小题选出答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。
写在试卷、草稿纸和答题卡上的非答题区域均无效。
3.非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。写在试卷、草稿
纸和答题卡上的非答题区域均无效。
可能用到的相对原子质量:H-1 C-12 N-14 O-16
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是
符合题目要求的。
1. 下列与生活相关的叙述中,不正确的是
A.氯化镁和亚硝酸钠均能用作食品添加剂
B.服用抗酸药时,一般嚼碎后吞服能尽快发挥药效
C.铁粉易被氧化,可在富脂食品中作为脱氧剂
D.高压法聚乙烯密度低,用来制造塑料瓶或桶
2. 下列化学用语或图示表达正确的是
A.2P 电子云轮廓图
y
B.氯仿分子的空间填充模型
C.1mol Li Ti O (Ti为+4价)中所含过氧键的数目为4N
2 5 15 A
D.BCl 的电子式为:
3
3. 生活中有许多现象或做法都蕴含着化学原理,下面说法正确的是
A.红酒中添加适量SO 可以起到杀菌、抗氧化作用
2
B.酒酿制技艺涉及淀粉、葡萄糖的水解反应
C.变质的油脂有“哈喇”味是因为油脂发生了氢化反应
D.误食可溶性钡盐可尽快用5%的Na CO 溶液洗胃
2 3
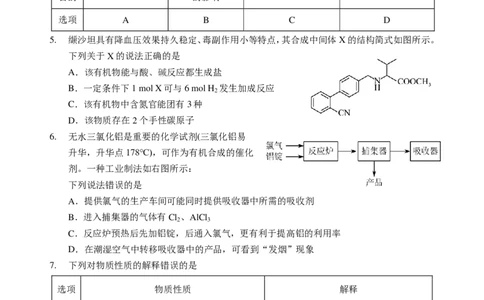
学科网(北京)股份有限公司4. 利用下列装置进行的相应实验不能达到实验目的的是
装置
实验 验证温度对平衡
测定醋酸的浓度 验证Fe与S反应放热 产生持续稳定电流
目的 的影响
选项 A B C D
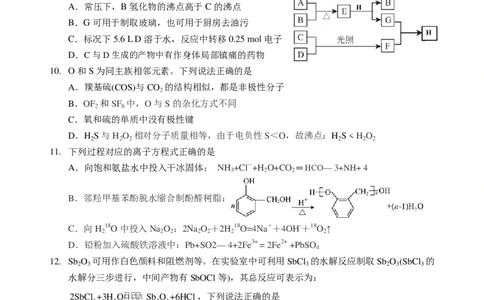
5. 缬沙坦具有降血压效果持久稳定、毒副作用小等特点,其合成中间体X的结构简式如图所示。
下列关于X的说法正确的是
A.该有机物能与酸、碱反应都生成盐
B.一定条件下1 mol X可与6 mol H 发生加成反应
2
C.该有机物中含氮官能团有3种
D.该物质存在2个手性碳原子
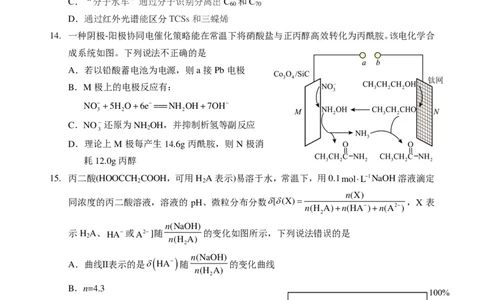
6. 无水三氯化铝是重要的化学试剂(三氯化铝易
升华,升华点 178℃),可作为有机合成的催化
剂。一种工业制法如右图所示:
下列说法错误的是
A.提供氯气的生产车间可能同时提供吸收器中所需的吸收剂
B.进入捕集器的气体有Cl 、AlCl
2 3
C.反应炉预热后先加铝锭,后通入氯气,更有利于提高铝的利用率
D.在潮湿空气中转移吸收器中的产品,可看到“发烟”现象
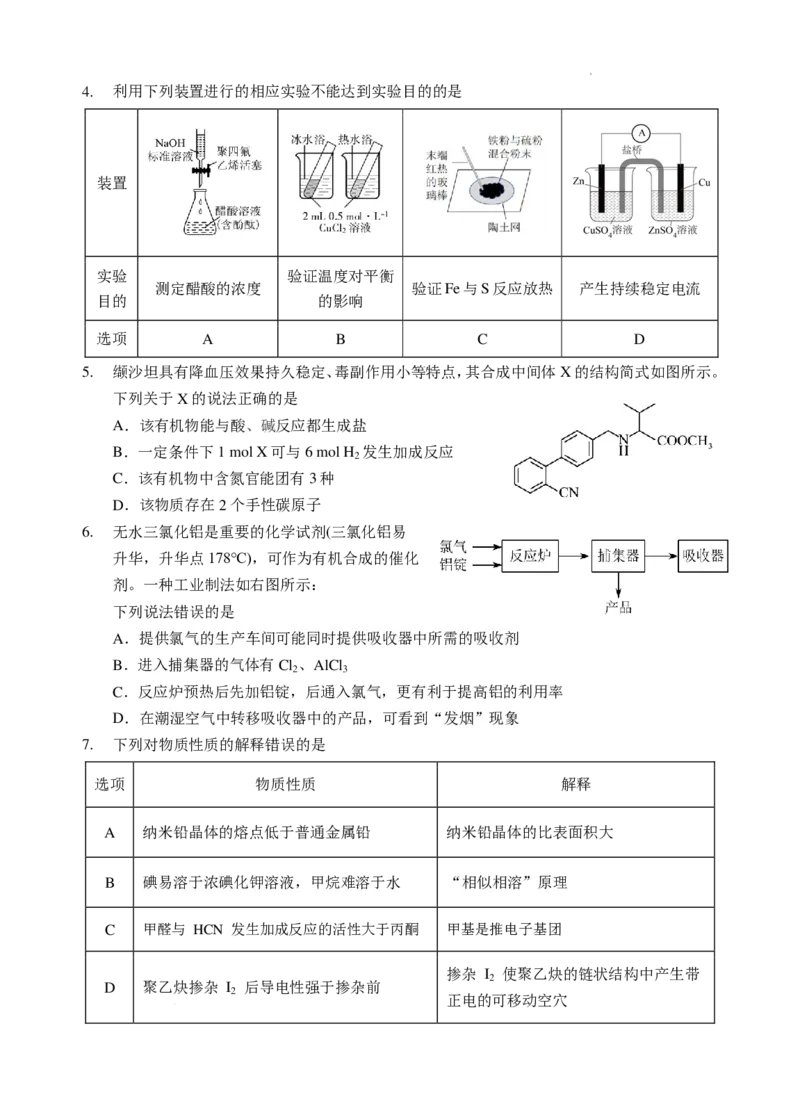
7. 下列对物质性质的解释错误的是
选项 物质性质 解释
A 纳米铅晶体的熔点低于普通金属铅 纳米铅晶体的比表面积大
B 碘易溶于浓碘化钾溶液,甲烷难溶于水 “相似相溶”原理
C 甲醛与 HCN 发生加成反应的活性大于丙酮 甲基是推电子基团
掺杂 I 使聚乙炔的链状结构中产生带
2
D 聚乙炔掺杂 I 后导电性强于掺杂前
2
正电的可移动空穴
学科网(北京)股份有限公司8. 已知 X、Y、Z、W 为原子序数依次增大的第三周期元素,Z 的最高价氧化物具有两性,在
XW、ZW 的熔融混合物中存在X+、W−、ZW−、Z W−等离子。下列叙述正确的是
3 4 2 7
A.化合物熔点:XZW >XZ W B.第一电离能:Z>Y>X
4 2 7
C.简单离子半径:Y>Z>W D.键角:ZW− < ClO−
4 3
9. 下图是部分短周期元素的单质及其化合物(或其溶液)的转化关系。已知B、D是非金属单
质,且在常温常压下都是气体,D 常用于自来水的杀菌、消毒;化合物 C、F、H 通常状况
下呈气态,C是含有18个电子且原子个数比为1:3的烃分子,化合物G的焰色试验呈黄色,
下列说法不正确的是
A.常压下,B氢化物的沸点高于C的沸点
B.G可用于制取玻璃,也可用于厨房去油污
C.标况下5.6 L D溶于水,反应中转移0.25 mol电子
D.C与D生成的产物中有作身体局部镇痛的药物
10. O和S为同主族相邻元素。下列说法正确的是
A.羰基硫(COS)与CO 的结构相似,都是非极性分子
2
B.OF 和SF 中,O与S的杂化方式不同
2 6
C.氧和硫的单质中没有极性键
D.H S与H O 相对分子质量相等,由于电负性S<O,故沸点:H S < H O
2 2 2 2 2 2
11. 下列过程对应的离子方程式正确的是
A.向饱和氨盐水中投入干冰固体: NH +Cl—+H O+CO ═ HCO— 3+NH+ 4
3 2 2
B.邻羟甲基苯酚脱水缩合制酚醛树脂:
C.向H 18O中投入Na O :2Na O +2H 18O=4Na++4OH-+18O ↑
2 2 2 2 2 2 2
D.铅粉加入硫酸铁溶液中:Pb+SO2— 4+2Fe3+ = 2Fe2+ +PbSO
4
12. Sb O 可用作白色颜料和阻燃剂等。在实验室中可利用SbCl 的水解反应制取Sb O (SbCl 的
2 3 3 2 3 3
水解分三步进行,中间产物有SbOCl等),其总反应可表示为:
2SbCl +3H O������ Sb O +6HCl,下列说法正确的是
3 2 2 3
A.SbCl 水解生成Sb O 的反应是基元反应
3 2 3
B.为了得到较多的产品,操作时要将SbCl 缓慢加入大量水中
3
C.将SbCl 固体研磨为粉末有利于得到较多的Sb O
3 2 3
D.Sb O 为分子晶体,熔点和燃点较低
2 3
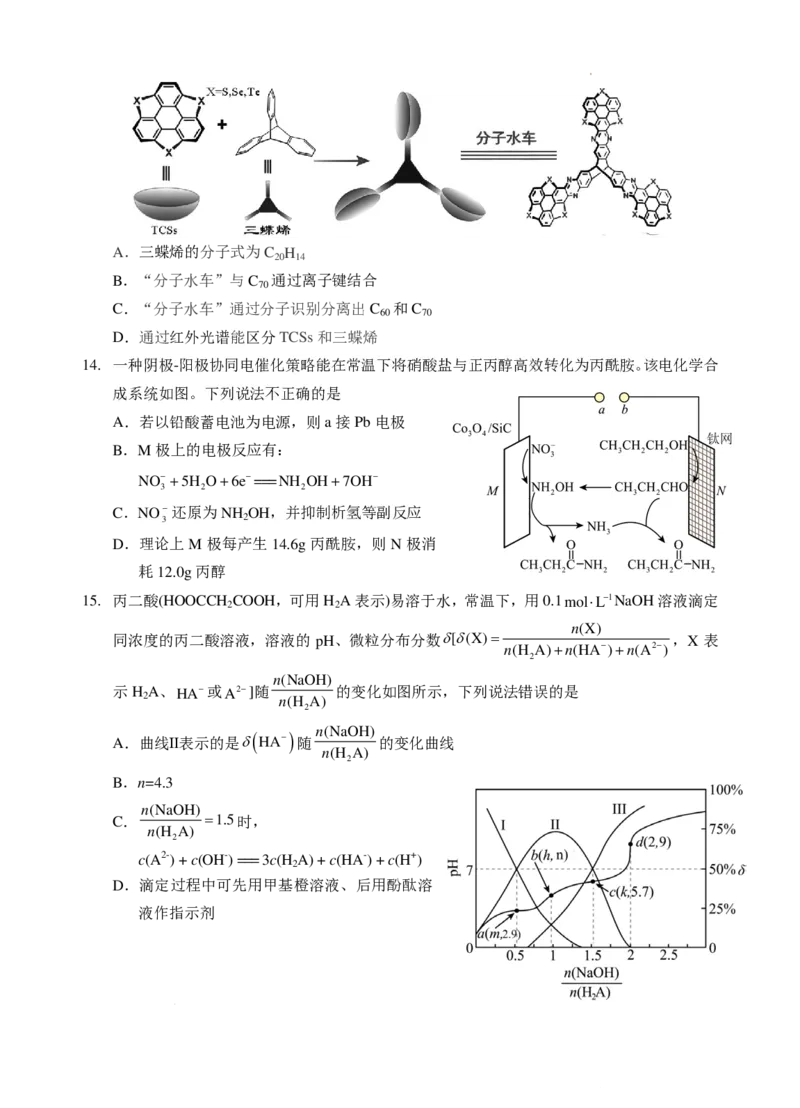
13. 三蝶烯和硫族元素杂化素馨烯(TCSs)通过吡嗪单元相融合,合成了具有三维空间结构的“水
车”状分子。“分子水车”能从C 和C 的混合溶液中选择性地分离出C 分子,纯度高达
60 70 60
99.5%,下列说法错误的是
学科网(北京)股份有限公司A.三蝶烯的分子式为C H
20 14
B.“分子水车”与C 通过离子键结合
70
C.“分子水车”通过分子识别分离出C 和C
60 70
D.通过红外光谱能区分TCSs和三蝶烯
14. 一种阴极-阳极协同电催化策略能在常温下将硝酸盐与正丙醇高效转化为丙酰胺。该电化学合
成系统如图。下列说法不正确的是
A.若以铅酸蓄电池为电源,则a接Pb电极
B.M极上的电极反应有:
NO− +5H O+6e−===NH OH+7OH−
3 2 2
C.NO−还原为NH OH,并抑制析氢等副反应
3 2
D.理论上M极每产生14.6g 丙酰胺,则N极消
耗12.0g丙醇
15. 丙二酸(HOOCCH COOH,可用H A表示)易溶于水,常温下,用0.1mol⋅L−1NaOH溶液滴定
2 2
n(X)
同浓度的丙二酸溶液,溶液的 pH、微粒分布分数δ[δ(X)= ,X 表
n(H A)+n(HA−)+n(A2−)
2
n(NaOH)
示H
2
A、HA−或A2−]随
n(H A)
的变化如图所示,下列说法错误的是
2
n(NaOH)
A.曲线Ⅱ表示的是δ
( HA−)
随 的变化曲线
n(H A)
2
B.n=4.3
n(NaOH)
C. =1.5时,
n(H A)
2
c(A2-) + c(OH-) === 3c(H A) + c(HA-) + c(H+)
2
D.滴定过程中可先用甲基橙溶液、后用酚酞溶
液作指示剂
学科网(北京)股份有限公司二、非选择题:本题共4小题,共55分。
16. (14分)
以银锰精矿(主要含Ag S、MnS、FeS )和氧化锰矿(主要含MnO )为原料,联合提取银和锰
2 2 2
可充分利用资源、节约试剂。其中一种流程示意图如下。
已知:①酸性条件下,MnO 的氧化性强于Fe3+;2Fe3++2Ag ������ 2Fe2+ +2Ag+
2
②MnSO 的溶解度随温度升高而显著增大
4
(1)“浸锰”过程是在酸性条件下,使两种矿石发生反应而将锰元素浸出,同时去除FeS ,
2
有利于后续银的浸出;浸锰渣主要成分为Ag S、S。
2
①“浸锰”过程中,MnS发生反应:MnS+2H+ =Mn2++H S↑。其中基态锰原子的价电子排
2
布式为: ,H S的VSEPR模型为: ;
2
②该过程加入的酸是: (用字母作答)
A.稀硝酸 B.浓硝酸 C.浓盐酸 D.稀硫酸
(2)“浸银”时,使用过量FeCl、HCl和CaCl 的混合液作为浸出剂,将Ag S中的银以
3 2 2
[AgCl ]−形式浸出。混合液中Cl−需保持较高的浓度,否则银会以 (填化学式)形式,
2
从溶液中析出。
(3)“沉银”过程中需要过量的铁粉作为还原剂,将[AgCl ]−转化为Ag 。一定温度下,Ag
2
的沉淀率随反应时间的变化如图所示。t分钟后(铁粉已耗尽),Ag的沉淀率逐渐减小,用离子
反应方程式解释原因: 、 。
(4)将“浸锰液”除杂、提纯后,得到MnSO 溶液,从中获取硫酸锰晶体的操作为:
4
、 、过滤、洗涤、干燥。
学科网(北京)股份有限公司17. (14分)
某研究小组按下列路线合成药物氯氮平。
NO
2
CH Cl Cl H N N CH
3 3
I II A �� B CH 3 OH C D E F
H 2 SO 4 C 8 H 9 NO 2 ��� C 14 H 11 ClN 2 O 4
H
H N
H N
G 2 ���
C 18 H 19 ClN 4 O 3 ��� Cl NH O 2 C N N CH 3 Cl N N N CH 3
H ���
已知:苯环上已存在的基团,对后续进入苯环的基团位置有影响:当苯环上有甲基、氨基或
羟基等基团时,后续进入苯环的基团,位于该基团的邻位或对位;当苯环上有羧基或硝基等基团
时,后续进入苯环的基团,位于该基团的间位。
(1)A为邻硝基苯甲酸,则Ⅰ为 反应(选用“硝化”或“氧化”填答)。
(2)C的结构简式为: 。
(3)D的官能团名称 。
δ+ δ−
(4)已知氨基可发生反应:N−H+X−Y→N−X+H−Y(X、Y分别代表带一定正电荷
和一定负电荷的原子)
①相对于Y,氨基中的N显负电性更倾向于与X成键,N显负电性的原因是: 。
②以环氧乙烷( )和CH NH 等为原料合成F的路线如下。
3 2
NH 环氧乙烷→MCH 3 NH 2→F
3
写出氨与环氧乙烷按1:2的系数比生成M的化学反应方程式 。
(5)同时符合下列条件的化合物F的同分异构体有 种(不考虑立体异构);写出其
中1种的结构简式 。
a. 1H−NMR谱和IR谱表明:分子中共有3种不同化学环境的氢原子,有N−H键
b.分子中含一个环,其成环原子数≥4
学科网(北京)股份有限公司18. (14分)
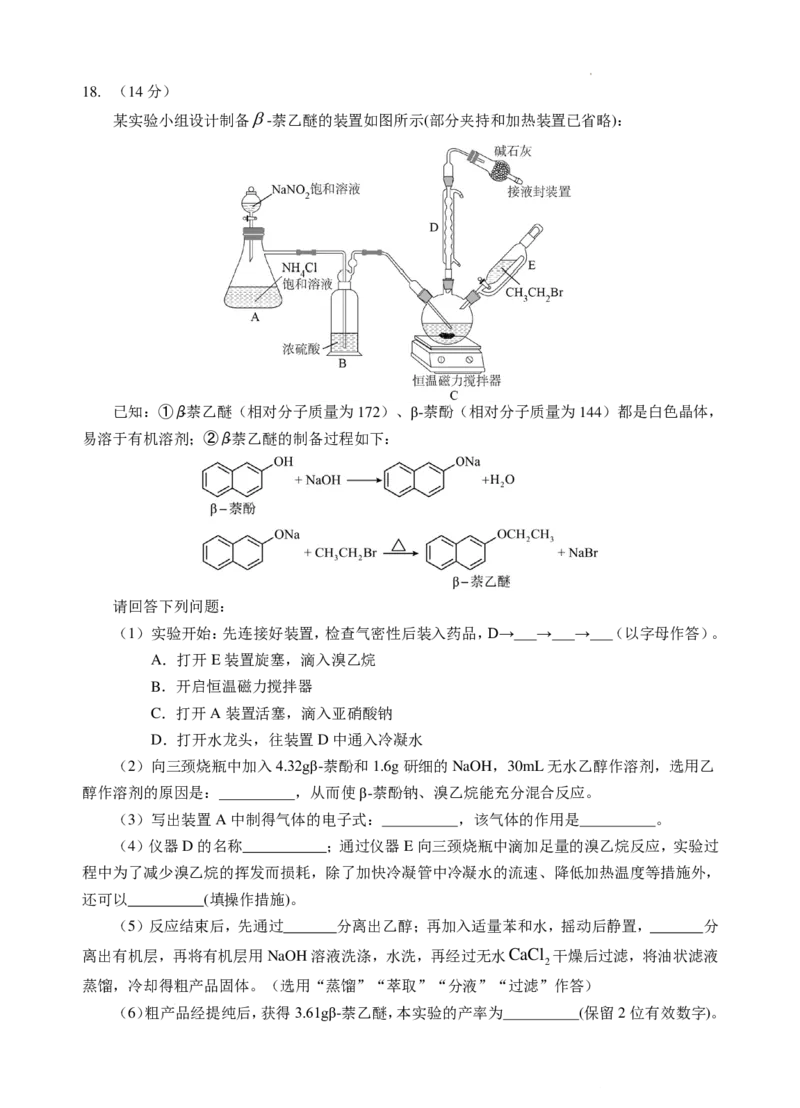
某实验小组设计制备β-萘乙醚的装置如图所示(部分夹持和加热装置已省略):
已知:①β-萘乙醚(相对分子质量为172)、β-萘酚(相对分子质量为144)都是白色晶体,
易溶于有机溶剂;②β-萘乙醚的制备过程如下:
请回答下列问题:
(1)实验开始:先连接好装置,检查气密性后装入药品,D→ → → (以字母作答)。
A.打开E装置旋塞,滴入溴乙烷
B.开启恒温磁力搅拌器
C.打开A装置活塞,滴入亚硝酸钠
D.打开水龙头,往装置D中通入冷凝水
(2)向三颈烧瓶中加入4.32gβ-萘酚和1.6g研细的NaOH,30mL无水乙醇作溶剂,选用乙
醇作溶剂的原因是: ,从而使β-萘酚钠、溴乙烷能充分混合反应。
(3)写出装置A中制得气体的电子式: ,该气体的作用是 。
(4)仪器D的名称___________;通过仪器E向三颈烧瓶中滴加足量的溴乙烷反应,实验过
程中为了减少溴乙烷的挥发而损耗,除了加快冷凝管中冷凝水的流速、降低加热温度等措施外,
还可以 (填操作措施)。
(5)反应结束后,先通过 分离出乙醇;再加入适量苯和水,摇动后静置, 分
离出有机层,再将有机层用NaOH溶液洗涤,水洗,再经过无水CaCl 干燥后过滤,将油状滤液
2
蒸馏,冷却得粗产品固体。(选用“蒸馏”“萃取”“分液”“过滤”作答)
(6)粗产品经提纯后,获得3.61gβ-萘乙醚,本实验的产率为 (保留2位有效数字)。
学科网(北京)股份有限公司19. (13分)
(1)2024年10月30日中国航天员搭载神舟十九号载人飞船顺利进入“太空之家”,中国
空间站设有完整的可再生生命保障系统,对二氧化碳进行收集和再生处理,实现了对二氧化碳的
加氢甲烷化,生成甲烷与水,并伴有副反应。
Ⅰ. C O ( g ) + 4 H ( g ) � C H ( g ) + 2 H O ( g ) ∆ H = -165kJ⋅mol−1 (主反应)
2 2 4 2 1
Ⅱ. C O ( g ) + H ( g ) � C O ( g ) + H O ( g ) ∆H =+41.2kJ⋅mol−1 (副反应)
2 2 2 2
回答下列问题:
①反应Ⅰ在 条件,是自发进行的反应(以字母作答)。
A.高温 B.低温 C.任何温度
② 几 种 化 学 键 的 键 能 为 : E(H-H)=436kJ⋅mol−1 、 E(O-H)=463kJ⋅mol−1 、
E(C=O)=745kJ⋅mol−1,则E(C≡O)= kJ⋅mol−1
(2)T℃时,在固定容积的容器中充入1molCO 和4molH 进行上述反应,平衡时CO 的转
2 2 2
化率为80%,甲烷的选择性为50%,则反应Ⅱ的K = (保留两位有效数字,K 为用各
p p
n(CH )
气体分压表示的平衡常数,分压=总压×物质的量分数,CH 的选择性= 4 ×100%)。
4 n(CO)+n(CH )
4
(3)一种铁氮化合物具有高磁导率,可用于制电子元件,其晶胞结构如图所示。
①该铁氮化合物中Fe(III)、Fe(II)、N数目比为 。
②该晶体结构的另一种晶胞表示中,N处于顶点位置,则位于体心的是: (选用
Fe(III)、Fe(II)、N作答)。
(4)①25C时,将10mL0.04mol⋅L−1NH Cl溶液和10mL0.01mol⋅L−1AgNO 溶液混合(忽
4 3
略溶液混合后的体积变化),混合后溶液中c ( Ag+) 为 [25℃时,K (AgCl)=1.8×10−10]。
sp
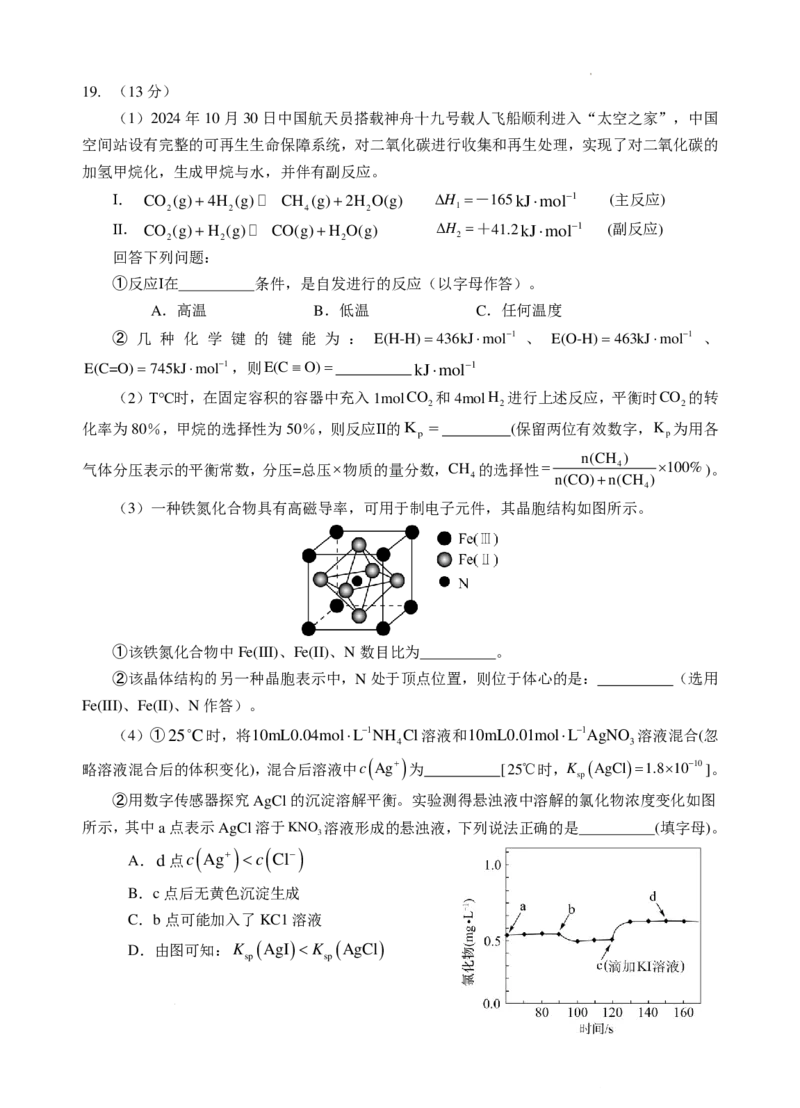
②用数字传感器探究AgCl的沉淀溶解平衡。实验测得悬浊液中溶解的氯化物浓度变化如图
所示,其中a点表示AgCl溶于KNO 溶液形成的悬浊液,下列说法正确的是 (填字母)。
3
A.d点c
( Ag+)