文档内容
2025 届新高考春季学期五月仿真联合测试
化学试题答案
题序
1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案
B C B C B A D A D C C D D C
15.(14分)
(1) (1分)
(2)SiO (1分)2ZnS+O +8NH +2H O=2[Zn(NH ) ]2++2S+4OH−(2分)
2 2 3 2 3 4
(3)防止NH 的挥发和碳酸铵分解,提高锌元素的浸取率(2分)
3
(4) (2分)
(5)盐酸中Cl−与Cd2+形成[CdCl₄]2−配离子,有利于提高Cd2+的反萃取率(2分)
(6) NH (1分)
3
3
(7) a (1分) 7、8、11(2分)
4
16. (15分)
(1)恒压滴液漏斗(1分)
70~80C
(2)4NaHCO FeCl H Y NaFeY3NaCl4CO 4H O(2分)
3 3 4 2 2
(3)pH过低,H Y电离出的 Y4浓度小,pH过高,Fe3转为Fe(OH) ,溶液中Fe3浓度减小(2
4 3
分)
(4)NaFeY3H O难溶于乙醇,加入乙醇使其结晶析出(或降低乙二胺四乙酸铁钠的溶解度)
2
(2分)
(5)AgNO 溶液、稀硝酸(2分)
3
421cV
(6)滴入最后半滴Na S O ,溶液蓝色褪去,且半分钟不恢复(2分) ×100%(2分)
2 2 3 m
偏大(2分)
17.(14分)
(1)+255.7 (1分) 高温(1分)
(2)①b (2分) 反应Ⅰ、Ⅲ均为吸热反应,升温平衡正移。低温时,以反应Ⅰ为主,反应Ⅲ几
乎没有发生,因此H 的产率随温度升高而增大;高温时,以反应Ⅲ为主,反应Ⅲ消耗H 的量大
2 2
于反应Ⅰ产生H 的量,因此H 的产率减小。 (2分)
2 2
2025届新高考春季学期五月适应性联合测试·化学答案 第1页 共6页
学科网(北京)股份有限公司② (2分)
(3) (2分)
(4)C H OH-4e+4OH=CH COOH+3H O(2分) CH COONH (2分)
2 5 3 2 3 4
18.(15分)
(1)3,4-二羟基苯甲酸(1分)
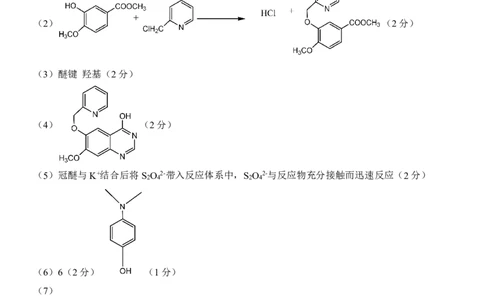
(2) (2分)
(3)醚键 羟基(2分)
(4) (2分)
(5)冠醚与K+结合后将S O 2-带入反应体系中,S O 2-与反应物充分接触而迅速反应(2分)
2 4 2 4
(6)6(2分) (1分)
(7)
(3分)
2025届新高考春季学期五月适应性联合测试·化学答案 第2页 共6页
学科网(北京)股份有限公司1.B 【详解】A. 陆川铁锅属于合金,熔点低于纯铁,A错误;C. 高分子化合物一般指相对分子
质量在一万以上的化合物,而油脂的相对分子质量相对于高分子而言很小,所以油脂不属于天然
高分子化合物,C错误; D. 纤维素与淀粉分子式均为C H O ,但二者n值不同,不属于同
6 10 5 n
分异构体,D错误。
2.C 【详解】A. 基态溴原子的电子排布式: Ar 3d104s24p5,A错误;B. 次氯酸是共价化合物,
O分别与H和Cl各形成一个共用电子对,电子式为: ,B错误;C.OF 分子中心原子
2
6-21
O的价层电子对数为2 =4,含有2对孤对电子,其VSEPR模型为四面体形,C正确;
2
D.中子数为10的氧原子,质子数为8、质量数为18,该原子表示为18O,故D错误。
8
3.B【详解】A. 加热硝酸铁溶液,Fe3+水解程度增加,生成氢氧化铁和氢离子,氢离子与硝酸根
形成易挥发的硝酸,因此装置③得到的是氢氧化铁,A错误;C.84消毒液中含NaClO,可使pH
试纸褪色,应选pH计测定,C错误;D. 氨气能与CaCl 反应,故不可用CaCl 干燥氨气,D错误
2 2
4.C 【详解】A. 该分子中含有羟基、醚键和酯基共三种含氧官能团,A项错误;B.羟基直接连
在苯环上,不能发生消去反应,B项错误;D. 该分子中含有酚羟基、和酚酯基,酯基水解产生的
羧基和酚羟基,则1mol该物质最多消耗3molNaOH,D项错误
5.B 【详解】B.CO 中C为sp2杂化,没有孤电子对,B不合理。
2
6.A 【详解】A.NaClO、FeCl 在强碱性溶液中反应生成Na FeO 、NaCl和水,根据得失电子守
3 2 4
恒,原子守恒得出离子方程式为:3ClO2Fe3 10OH 2FeO23Cl5H O,A正确;B.铁
4 2
氰化钾与氯化亚铁反应生成深蓝色沉淀:K Fe2 Fe(CN)3 KFeFe(CN) ,B错误;由于
6 6
硫酸铜少量,相当于硫氢化钠过量,方程式为:Cu2 2HS CuS H S,C错误;D.白醋
2
中醋酸为弱酸,不能拆开,要写成化学式,则反应的离子方程式为:
CaCO 2CH COOH CO H OCa2 2CH COO,D错误。
3 3 2 2 3
7.D 【详解】短周期主族元素X、Y、Z、W的原子序数依次增大,X形成一个共价键,Y形成
四个共价键, Z形成两个共价键,W形成六个共价键, 基态W原子次外层电子数等于其他各层
电子数之和,则W为S,Z为O,由YX+离子可确定Y最外层电子数为5,Y为N,X为H,据
4
此解答;
2025届新高考春季学期五月适应性联合测试·化学答案 第3页 共6页
学科网(北京)股份有限公司A.N的氧化物对应水化物可能为HNO (强酸),也可能为HNO (弱酸),A错误;
3 2
B.-O-O-中的O为-1价,其余O为-2价,B错误;
C.NH +中N与H+形成的配位键,N提供孤电子对,H+提供空轨道,C错误;
4
D.同周期元素的电负性从左至右增强,N的电负性大于H,故电负性:ONH,D正确。
8.A 【详解】A.实验a中生成沉淀,闻到刺激性气味,可推测反应的离子方程式:
2Al3 3S O2 3H O2AlOH 3SO 3S,A错误;B.由实验现象可知
2 3 2 3 2
Fe3 3S
2
O
3
2 FeS
2
O
3
3
3
速率快,溶液先变成紫黑色,之后S
2
O
3
2- 将Fe3+还原成Fe2+,使
Fe3 3S
2
O
3
2 FeS
2
O
3
3
3
平衡逆移,溶液几乎变为无色,B正确;C.S
2
O
3
2- 具有还原性,会与
酸性高锰酸钾溶液反应,C正确;
9.D 【详解】A.没有给定标准状况,无法计算18O 的物质的量,A项错误;
2
B.没有给氨水的体积,无法求算OH-数目,B项错误;
C.1mol[Cu(NH ) ]2+中含有N-Hσ键为12mol,铜离子与氮原子之间的配位键也是σ键,为4mol,
3 4
所以1mol[Cu(NH ) ]2+中含有σ键数为16N ,C项错误;
3 4 A
D.转移1mol电子时,消耗0.25molO ,D项正确。
2
10.C【详解】A.物质能量越低越稳定,物质稳定性:I < II,故A正确;
B.*N H→*NHNH过程N 中π键断裂,H O+中σ键断裂,故B正确;
2 2 3
C.图乙表示的是单个分子的相对能量变化关系,且H O+能量未知,故C错误;
3
D.I为*NHNH ,转化过程中可能发生副反应:*NHNH +H O++e−=*N H +H O,故D正确。
2 2 3 2 4 2
11.C 【详解】A.该晶胞中S 原子的个数为8,Fe 和 Cu原子的个数均为4,由此可知化学式为
CuFeS ,A正确;
2
B.由晶胞结构可知,以面心的Fe原子为研究对象,Fe原子周围紧邻的硫原子有4个,Fe原子的
配位数为4,B正确;
C.由晶胞结构可知,分数坐标为( , , )的原子为S原子,C错误;
311
D.该晶胞中 S 原子的个数为8,4Fe48和Cu 原子的个数均为 4,化学式为CuFeS ,设晶胞边长为
2
4M1030
gcm3
apm、bpm,N
A
为阿伏加德罗常数的值,则黄铜矿晶体的密度为 N
A
a2b ,D正确;
12.D【详解】A.放电时,Zn为负极,发生反应Zn-2e-=Zn2+,b为正极,Na+向b电极移动;
B.放电时,b为正极,发生反应NaFe[Fe(CN) ]+xe-+xNa+=Na Fe[Fe(CN) ];
6 1+x 6
C.自充电时,Na Fe[Fe(CN) ]与H O 发生氧化还原生成NaFe[Fe(CN) ]和水,每消耗1molH O ,
1+x 6 2 2 6 2 2
转移2mol电子,释放出2molNa+,b电极质量减小46g;
D.根据自充电的原理,H O 作为氧化剂将Na Fe[Fe(CN) ]复原为NaFe[Fe(CN) ],O 也具有氧化
2 2 1+x 6 6 2
性,也可能实现自充电。
13.D【详解】A.升高温度,反应I平衡正向移动,反应II平衡逆向移动,CO增大,CH
4
减小;增大压强,反应II平衡正向移动,CH 增大,CO减小,则压强为1.0MPa时,
4
COg、CH g的摩尔分数随温度变化的曲线分别是d、a;压强为0.1MPa时,COg、
4
CH g的摩尔分数随温度变化的曲线分别是c、b;
4
B.反应过程中及时移走产物H O,可以提高CH 的产率,但因浓度减小,反应速率减小;
2 4
2025届新高考春季学期五月适应性联合测试·化学答案 第4页 共6页
学科网(北京)股份有限公司C.反应I为吸热反应,温度越高,K值越大,N点平衡常数大于M点;
D.M、P两点温度相同,压强相同,CO g的转化率相同,CH 为80%,CO为10%,则
2 4
ηCO 为10%,而N点ηCH 为40%,CO为40%,则ηCO 为20%,说明N点CO g
2 4 2 2
的转化率较小,M、N、P三点对应CO g的转化率大小关系为:MPN。
2
14.C 【详解】A.二元弱酸有两次滴定突变,一元酸有一次滴定突变,故X曲线代表H B,Y曲
2
线代表HA;
B.曲线X第一次突变时溶质为NaHB,由图像可知此时溶液呈酸性,则HB-的电离程度大于水解程
K
度,即K H B w ,故K (H B)×K (H B)>10-14;
a2 2 K H B a1 2 a2 2
a1 2
C.若b点的横坐标为8.50mL,即半滴定点,存在电荷守恒:c(Na+)+c(H+)=c(A-)+c(OH-),物料守
恒:2c(Na+)=c(A-)+c(HA),结合两个式子可得c(HA)-c(A-)=2c(OH-)-2c(H+);
D.若a点的横坐标为8.40mL,占消耗氢氧化钠总体积的四分之三,则溶质为NaHB与Na B,且二
2
者的浓度比为1:1,由于此时溶液呈酸性,则c(HB-)<c(B2-)。
15.【详解】(1)铜元素的原子序数为29,Cu2+价电子排布式为3d9,价电子排布图为
;
(2)由分析可知,滤渣1中含有S、Fe(OH)CO 及未反应的SiO ,故答案为SiO ;氨浸中O 与碳酸
3 2 2 2
铵和ZnS反应生[Zn(NH ) ]2+、S,反应的离子方程式为 2ZnS+O +8NH +2H O=2[Zn(NH ) ]2++2S
3 4 2 3 2 3 4
+4OH−;
(3) 氨浸中用到的碳酸铵受热易分解,NH 在溶液中受热易挥发,故在实际生产中采取常温浸取而
3
不采用加热的方法;
(4)“除杂”时,(NH 4 ) 2 S用量过多会发生反应:S2 ZnNH 3 4 2 ZnS 4NH 3 ,该反应的平衡
常数为
;
(5)根据平衡MnnHA 有机层 MA 有机层nH水层,反萃取盐酸和硫酸都能提高氢离子浓
n
度,使平衡逆向移动,两试剂的重大区别是阴离子不同,根据题意Cl⁻可以与Cd²⁺形成[CdCl₄]²⁻配
离子,有利于形成[CdCl₄]²⁻配离子,进一步提高Cd²⁺的反萃取率。
(6) 蒸氨步骤可以获得氨气,可以投入到氨浸中循环使用。
(7)该其晶胞参数为anm,晶胞中Cd原子和Te原子之间的最短距离为四面体重心到顶点的距离,
3
则最短距离为 apm;根据图示,如果沿晶胞面对角线方向上的投影如图2所示,则代表Te原
4
子的位置有7、8、11。
16.【详解】(3)pH过低,H Y在水中电离量小,pH过大,Fe3+转为Fe(OH) ,所以产率降低,
4 3
故答案为:pH过低,H Y电离出的Y4−浓度小(或pH过低,H Y在水中溶出量小),pH过大,Fe3+
4 4
转为Fe(OH) ,溶液中Fe3+浓度减小。
3
2025届新高考春季学期五月适应性联合测试·化学答案 第5页 共6页
学科网(北京)股份有限公司NaFeY3H O
(4) 2 难溶于乙醇,使用乙醇降低乙二胺四乙酸铁钠的溶解度,有利于其产品析出。
(5)由于溶液中存在大量未消耗的氯离子,所以应该检测洗涤液中是否存在氯离子,故答案为:
AgNO 溶液和稀硝酸。
3
(6)由2Fe3++2I-=2Fe2++I 、I 2Na S O 2NaINa S O 可知存在2NaFeY3H O~I ~2Na SO ,平
2 2 2 2 3 2 4 6 2 2 2 2 3
均消耗Na S O 标准溶液VmL,则n(Na SO )=c×V×10-3mol,样品中
2 2 3 2 2 3
n(NaFeY3H O)=10n(Na S O )=cV×10-2mol,m(NaFeY3H O)=cV×10-2mol×421g/mol=4.21cVg,样
2 2 2 3 2
4.21cVg 421cV
品中NaFeY3H O的质量分数= 100%= %;
2 mg m
若滴定过程较缓慢,则过量的KI可能被空气中的氧气氧化为I ,则消耗Na S O 标准溶液体积偏
2 2 2 3
大,测得样品中NaFeY3H O的质量分数偏大。
2
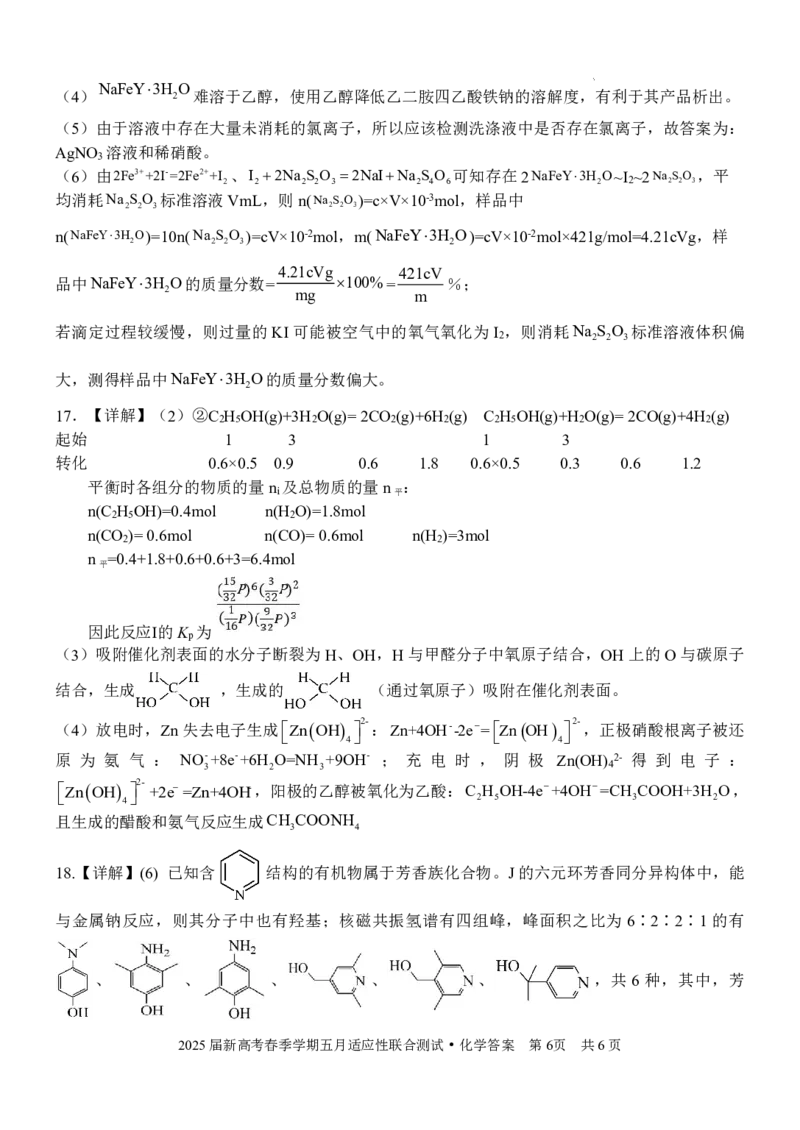
17.【详解】(2)②C H OH(g)+3H O(g)=2CO (g)+6H (g) C H OH(g)+H O(g)=2CO(g)+4H (g)
2 5 2 2 2 2 5 2 2
起始 1 3 1 3
转化 0.6×0.5 0.9 0.6 1.8 0.6×0.5 0.3 0.6 1.2
平衡时各组分的物质的量n 及总物质的量n :
i 平
n(C H OH)=0.4mol n(H O)=1.8mol
2 5 2
n(CO )=0.6mol n(CO)=0.6mol n(H )=3mol
2 2
n =0.4+1.8+0.6+0.6+3=6.4mol
平
因此反应Ⅰ的K 为
p
(3)吸附催化剂表面的水分子断裂为H、OH,H与甲醛分子中氧原子结合,OH上的O与碳原子
结合,生成 ,生成的 (通过氧原子)吸附在催化剂表面。
(4)放电时,Zn失去电子生成ZnOH 2-:Zn+4OH--2e= Zn OH 2-,正极硝酸根离子被还
4 4
原 为 氨 气 : NO-+8e-+6H O=NH +9OH- ; 充 电 时 , 阴 极 Zn(OH) 2- 得 到 电 子 :
3 2 3 4
ZnOH 2- +2e=Zn+4OH-,阳极的乙醇被氧化为乙酸:C H OH-4e+4OH=CH COOH+3H O,
4 2 5 3 2
且生成的醋酸和氨气反应生成CH COONH
3 4
18.【详解】(6) 已知含 结构的有机物属于芳香族化合物。J的六元环芳香同分异构体中,能
与金属钠反应,则其分子中也有羟基;核磁共振氢谱有四组峰,峰面积之比为 6∶2∶2∶1 的有
、 、 、 、 、 ,共 6 种,其中,芳
2025届新高考春季学期五月适应性联合测试·化学答案 第6页 共6页
学科网(北京)股份有限公司香环上为二取代的结构简式为 。
2025届新高考春季学期五月适应性联合测试·化学答案 第7页 共6页
学科网(北京)股份有限公司