文档内容
六中 2023 年秋学期高三年级第二次月考
化学试卷
满分:100分 时间:75分钟
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Na-23 K-39 Fe-56 Cu-64
Ba-137
一、单选题(本题共12小题,每小题3分,共36分。在每小题给出的四个选项中,只有一项
是符合题目要求的)
1. 不断进步的材料逐渐构筑了我们现代社会的文明。下列说法错误的是( )
A. “唐三彩”和景德镇瓷器的主要化学成分都是硅酸盐
B. 玻璃是一种常见的无机非金属材料,在一定温度下软化可制得玻璃仪器
C. 高铁和城铁所用镁合金具有密度小、强度高、耐腐蚀等特点
D. 以高纯硅制成的光导纤维内窥镜可直接窥视有关器官部位的变化
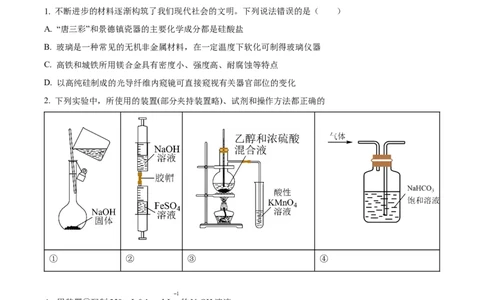
2. 下列实验中,所使用的装置(部分夹持装置略)、试剂和操作方法都正确的
① ② ③ ④
A. 用装置①配制250 mL 0.1 mol·L 的NaOH溶液
.
B 用装置②制备少量 固体
C. 用装置③验证乙烯的生成
D. 用装置④除去 中的少量 气体
3. 二氧化氯(ClO )是一种黄绿色易溶于水的气体,常用于饮用水消毒。下列有关ClO 制备与杀菌的说
2 2
法不合理的是( )A. NaClO 在酸性条件下歧化生成ClO 和NaCl,则n(氧化剂):n(还原剂)=1:4
2 2
B. ClO 在强碱性环境中使用失效,可能的原因是:2ClO +2OH- =ClO - + ClO -+H O
2 2 3 2 2
C. 可用饱和食盐水除去ClO 中的NH
2 3
D. 等物质的量的ClO 杀菌效果比Cl 强
2 2
4. 根据下列实验操作和现象得出的结论正确的是
选
实验操作 现象 结论
项
与
A 向 溶液中滴加过量氨水 得到澄清溶液
能大量
共存
具
向酸性 溶液中滴入适量的 溶
B 溶液紫色褪去 有还原
液
性
部分
向久置的 溶液中加入足量 溶 出现白色沉淀;再加入足量稀盐酸,部
C
分沉淀溶解
液
被氧化
该钠盐
为
向某钠盐粉末上滴加浓盐酸,将产生的气体
D 品红溶液褪色 ,
通入品红溶液
或
A. A B. B C. C D. D
5. N 代表阿伏加 德罗常数的值,以下说法正确的是
A
A. 2N 个HCl分子与44.8 L H 和Cl 的混合气体所含的原子数目均为4N
A 2 2 A
B. 32gCu将足量浓、稀硝酸分别还原为NO 和NO,浓、稀硝酸得到的电子数均为N
2 A
C. 物质的量浓度均为1mol/L的NaCl和MgCl 混合溶液中,含有Cl-的数目为3N
2 A
D. 1mol D18O+(其中D代表 )中含有的中子数为10 N
3 A
6. 下列各组物质的稀溶液相互反应,把前者逐滴滴入后者与把后者逐滴滴入前者,边滴边振荡,所产生的
现象相同的是
A. 和 B. 和C. 氨水和 D. 和
7. 下列离子方程式书写正确的是
A. 新制氯水中加入少量 :
B. 向酸性高锰酸钾溶液加入草酸:
C. 溶液中滴加 溶液至 恰好完全沉淀:
D. 碘化亚铁溶液与等物质的量的氯气:
8. 工业上制备下列物质的生产流程中,合理的是
A. 从海水中提取溴:浓缩海水
B. 从海水中提取镁:海水
C. 由NaCl制漂白粉:饱和食盐水 漂白粉
D. 由黄铁矿制硫酸:黄铁矿
9. 已知A、B、C、D、E是五种短周期主族元素,其原子半径与原子序数的关系如图1,且A、B、C、D
形成的化合物X如图2,C与E同主族。下列说法错误的是
A. 化合物X在高温下稳定性较弱
B. 均由A、C、D、E四种元素形成的化合物在溶液中都显碱性
C. D元素的单质能与C元素的单质直接化合生成两种化合物
D. C元素的氢化物的沸点不一定高于B元素的氢化物的沸点
10. 海洋深处某种细菌能够在无氧条件下通过微生物产生的醋酸与含MnO 的矿石反应生成Mn2+,其反应
2
过程如图所示。下列说法正确的是A. 升高温度一定能够加快反应速率
B. 生成22.4LCO 时,转移电子为1mol
2
C. 过程②③的总反应为MnO +2HX=Mn2++2X+2OH-
2
D. 过程①中既有极性键和非极性键的断裂,又有极性键和非极性键的形成
11. 有一混合物的水溶液,可能含有以下离子中的若干种:
、 、 、 、 ,现取三份100mL溶液进行如下实验:
第一份加入 溶液有沉淀产生;
第二份加足量NaOH溶液加热后,收集到0.03mol气体;
第三份加足量 溶液后,得到干燥沉淀4.30g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。综合上
述实验,你认为以下结论正确的是
A. 该混合液中一定含有: 、 、 、 ,不含
B. 该混合液中一定含有: 、 、 ,可能含 、
C. 该混合液中一定含有: 、 、 、 ,可能含
D. 该混合液中:
12. 常温下,在20 mL 0.1 mol/L 溶液中逐滴加入0.1 mol/L盐酸40 mL,溶液的pH逐渐降低,此
时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化( 因逸出未画出),如图所示。下
列说法不正确的是A. 0.1 mol/L 溶液中
B. 在A点:
C. 常温下 饱和溶液的pH约为5.6
D. 当加入20 mL盐酸时,混合溶液的pH约为8
二、不定项选择题:(本大题共4小题,每小题4分,共16分;在每小题给出的四个选项中,
有一个或两个选项符合题意。全部选对得4分,选对但不全得2分,多选、错选均不得分。)
的
13. 由一种阳离子与两种酸根离子组成 盐称为混盐, 是一种常见的混盐,下列说法不正确的
是
A. 中氯元素为-1价
B. 水溶液呈碱性,具有较强的氧化性
C. 由氯气为原料,每生成1 mol ,转移的电子数为
D. 溶液中加入足量浓硫酸,可有黄绿色气体产生
14. 下列各组分离子在指定溶液中一定能大量共存的是
A. 由水电离出 的 mol⋅L 的溶液中: 、 、 、
B. 能与铝反应生成 的溶液中: 、 、 、
C. 含有大量 的溶液中: 、 、 、
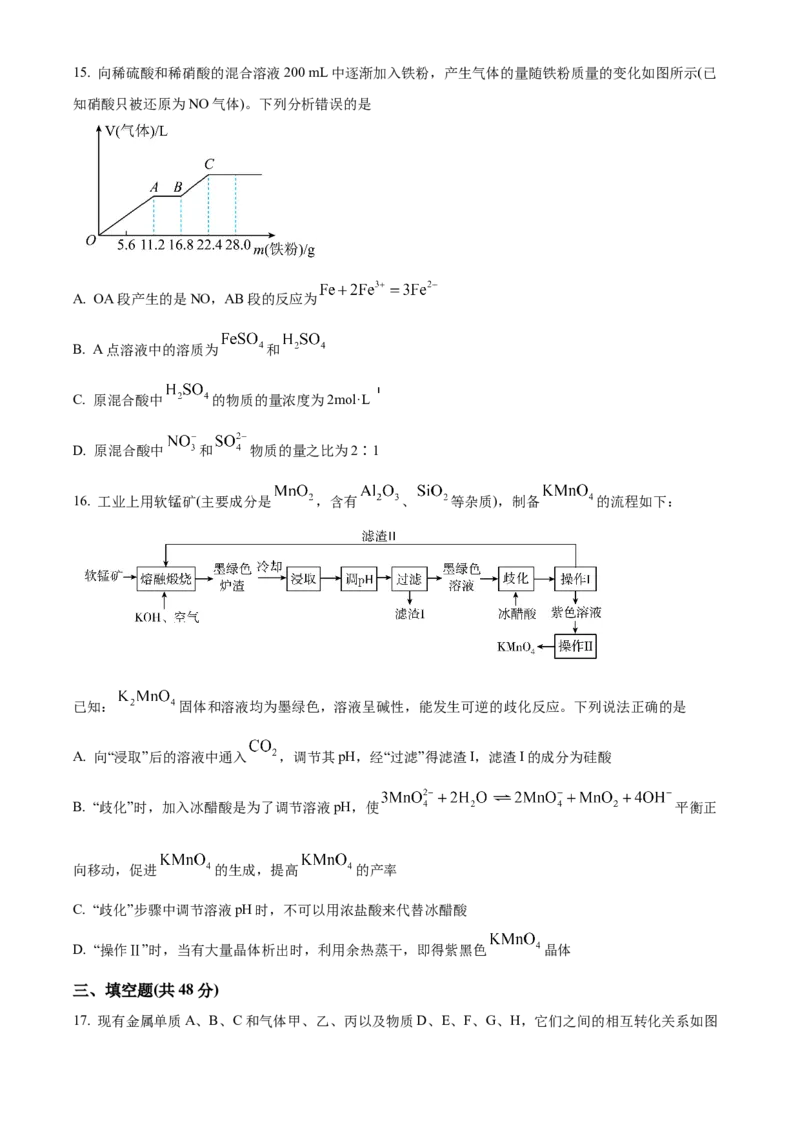
D. 中性溶液中: 、 、 、15. 向稀硫酸和稀硝酸的混合溶液200 mL中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示(已
知硝酸只被还原为NO气体)。下列分析错误的是
A. OA段产生的是NO,AB段的反应为
B. A点溶液中的溶质为 和
C. 原混合酸中 的物质的量浓度为2mol·L
D. 原混合酸中 和 物质的量之比为2∶1
16. 工业上用软锰矿(主要成分是 ,含有 、 等杂质),制备 的流程如下:
已知: 固体和溶液均为墨绿色,溶液呈碱性,能发生可逆的歧化反应。下列说法正确的是
A. 向“浸取”后的溶液中通入 ,调节其pH,经“过滤”得滤渣I,滤渣I的成分为硅酸
B. “歧化”时,加入冰醋酸是为了调节溶液pH,使 平衡正
向移动,促进 的生成,提高 的产率
C. “歧化”步骤中调节溶液pH时,不可以用浓盐酸来代替冰醋酸
D. “操作Ⅱ”时,当有大量晶体析出时,利用余热蒸干,即得紫黑色 晶体
三、填空题(共48分)
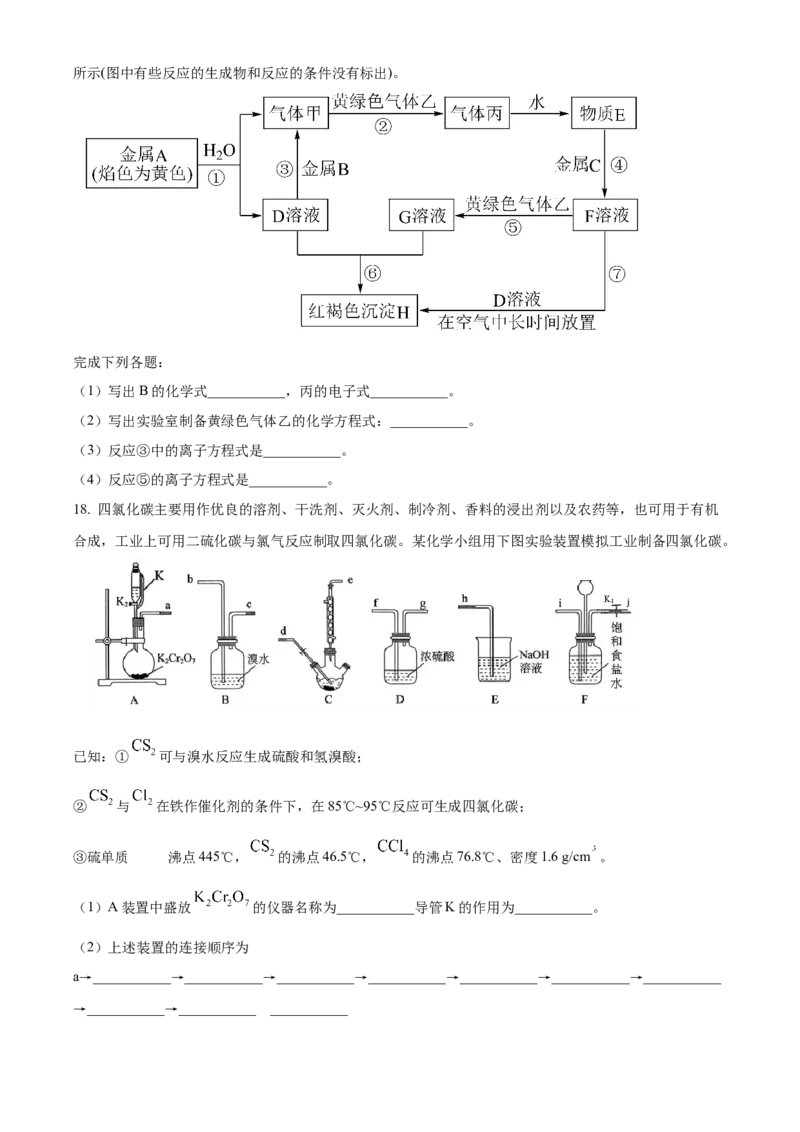
17. 现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示(图中有些反应的生成物和反应的条件没有标出)。
完成下列各题:
(1)写出B的化学式___________,丙的电子式___________。
(2)写出实验室制备黄绿色气体乙的化学方程式:___________。
(3)反应③中的离子方程式是___________。
(4)反应⑤的离子方程式是___________。
18. 四氯化碳主要用作优良的溶剂、干洗剂、灭火剂、制冷剂、香料的浸出剂以及农药等,也可用于有机
合成,工业上可用二硫化碳与氯气反应制取四氯化碳。某化学小组用下图实验装置模拟工业制备四氯化碳。
已知:① 可与溴水反应生成硫酸和氢溴酸;
② 与 在铁作催化剂的条件下,在85℃~95℃反应可生成四氯化碳;
的
③硫单质 沸点445℃, 的沸点46.5℃, 的沸点76.8℃、密度1.6 g/cm 。
(1)A装置中盛放 的仪器名称为___________导管K的作用为___________。
(2)上述装置的连接顺序为
a→___________→___________→___________→___________→___________→___________→___________
→___________→___________ ___________(3)反应结束后关闭 , ,此时F装置的作用为___________。
(4)装置B中若1 mol 完全反应,转移的电子数目为___________。
(5)反应结束先过滤除去固体催化剂,再经过___________(填操作名称)可得到 。
(6)若用 提取碘水中的碘单质,振荡静置后的现象为___________。
19. 钠、钾的碘化物在生产和科学实验中有十分重要的应用。工业上利用碘、烧碱和铁屑为原料可生产碘
化钠,其生产流程如图所示:
(1)NaOH溶液和碘反应时需要严格控制温度,如果温度过低,所得副产物的化学式是___________。
(2)生产流程中加入过量铁屑的目的是___________,过滤所得固体中除剩余铁屑外,还有红褐色固体,
则加入铁屑时发生反应的化学方程式是___________。
(3)溶液2中除含有 外,一定含有的阳离子是___________。
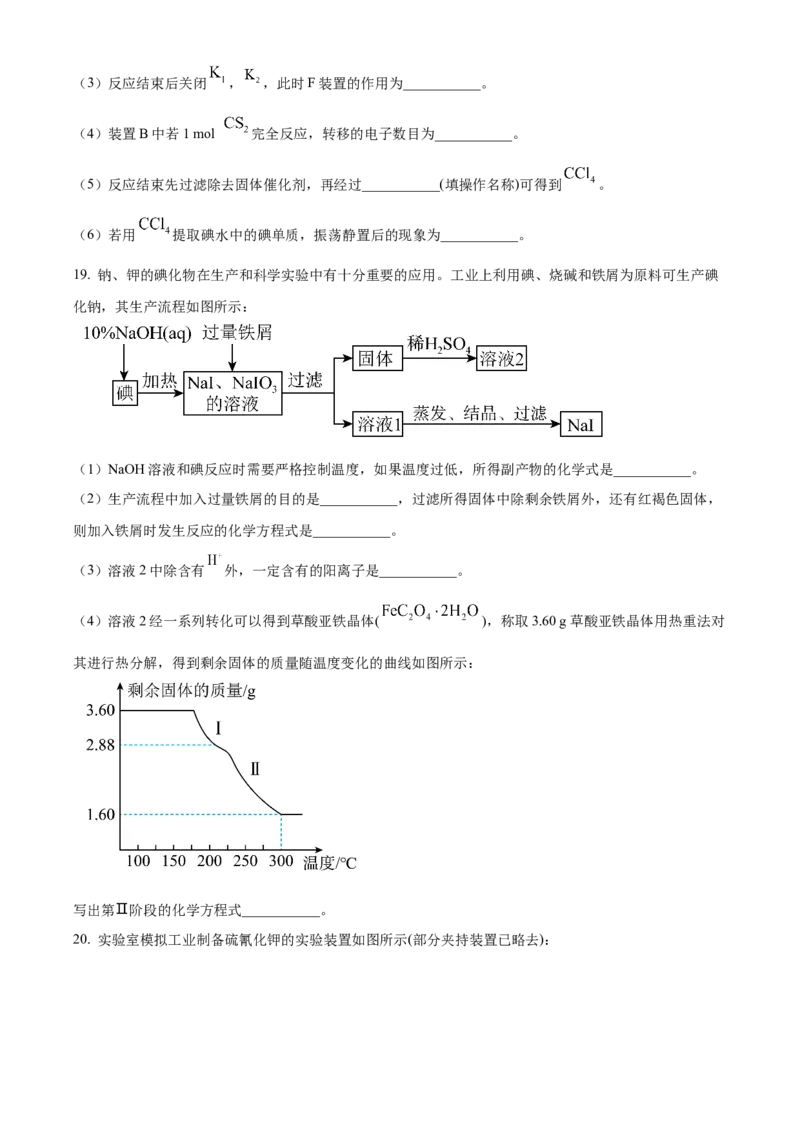
(4)溶液2经一系列转化可以得到草酸亚铁晶体( ),称取3.60 g草酸亚铁晶体用热重法对
其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示:
写出第Ⅱ阶段的化学方程式___________。
20. 实验室模拟工业制备硫氰化钾的实验装置如图所示(部分夹持装置已略去):已知:NH 不溶于CS,在一定条件下发生反应CS+3NH NH SCN+NH HS,生成物中
3 2 2 3 4 4
NH HS的热稳定性较NH SCN差
4 4
回答下列问题:
(1)装置A中反应的化学方程式是___________
的
(2)三颈烧瓶内盛放有CS、HO和催化剂,进气导管口必须插入下层CS 液体中,目 是
2 2 2
___________,该反应比较缓慢,实验中可通过观察C中现象来控制A中NH 的生成速率,则X的化学式
3
为___________
(3)反应一段时间后,关闭K,保持三颈烧瓶内液温105 ℃一段时间,其目的是___________;然后打开
1
K,继续保持液温105 ℃,缓缓滴入适量的KOH溶液,制得较纯净的KSCN溶液
2
(4)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再减压___________、___________、过滤、
洗涤、干燥,得到硫氰化钾晶体