文档内容
第三章 晶体结构与性质
第二节 分子晶体与共价晶体
第1课时 分子晶体
培优第一阶——基础过关练
1.下列关于分子晶体的说法不正确的是
A.分子晶体中含有分子 B.固态或熔融态时均能导电
C.分子间以分子间作用力相结合 D.熔、沸点一般比较低
2.(2022·广东云浮·高二期末)下列物质中,属于含有非极性共价键的分子晶体的是
A.Si B.HCl C.N D.NH Cl
2 4
3.(2022·陕西·西安市阎良区关山中学高二阶段练习)下列物质属于分子晶体的是
①冰;②二氧化硅;③碘;④铜;⑤固态的氩
A.仅①③ B.仅②③⑤ C.仅⑤ D.仅①③⑤
4.(2022·天津市宁河区芦台第一中学高二阶段练习)下列叙述与范德华力无关的是
A.气体物质加压或降温时能凝结或凝固 B.白磷易自燃
C.干冰易升华 D.S 的熔、沸点较低
8
5.(2022·北京市宣武外国语实验学校高二期中)下列有关冰和干冰的叙述不正确的是
A.干冰和冰都是由分子密堆积形成的晶体
B.冰中存在氢键,每个水分子周围有4个紧邻的水分子
C.干冰比冰的熔点低,常压下易升华
D.干冰中只存在范德华力不存在氢键
6.(2022·河北·高二阶段练习)类比是中学学习化学常用的一种方法,下列说法正确的是
A.硫酸铜和乙酸均可以形成晶体,因此它们的晶体均有自范性
B.C与Si是同一主族元素,CO 是分子晶体,推测SiO 也是分子晶体
2 2
C.F与Br是同一主族元素,HF是弱酸,推测HBr也是弱酸
D.HS和HO均是分子晶体,因此在HS和HO晶体中,每个分子周围紧邻的分子数均是12
2 2 2 2
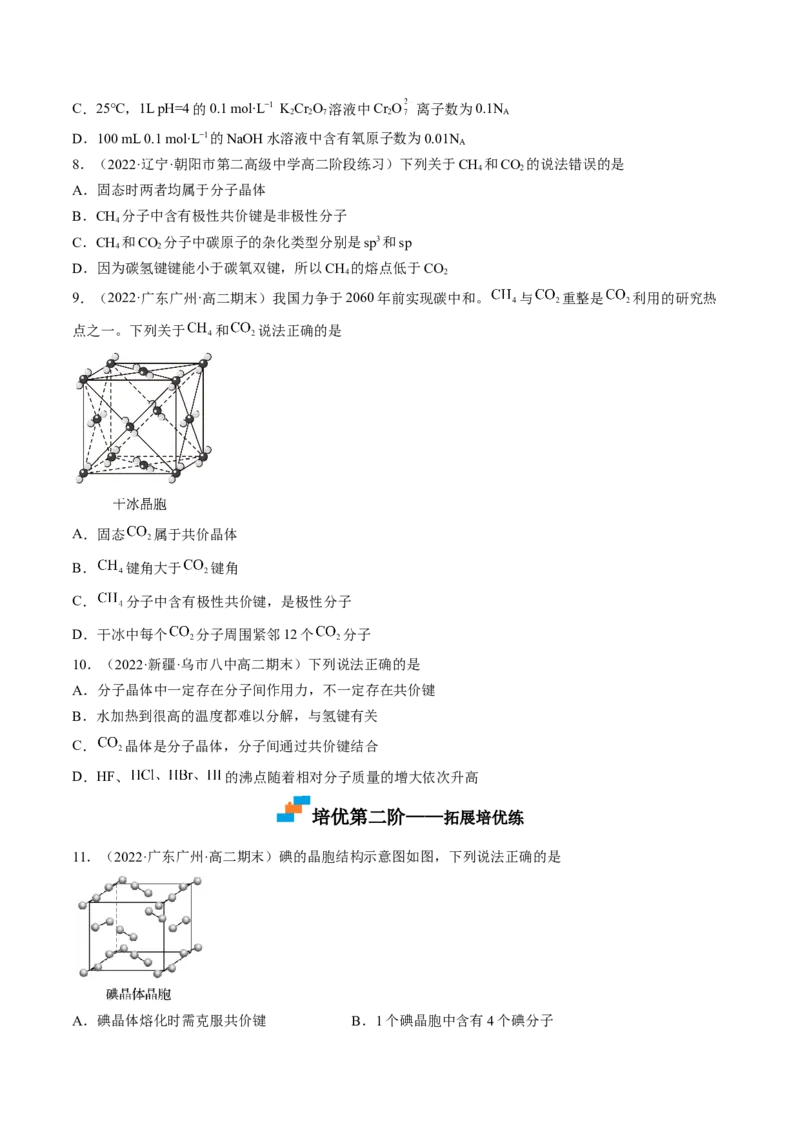
7.(2022·浙江温州·高二期末)以N 表示阿伏加德罗常数的值,下列说法正确的是
A
A.18 g冰(如图1)中含氢键数目为4N
A
B.88 g干冰(如图2)中含有0.5N 个晶胞结构单元
AC.25℃,1L pH=4的0.1 mol∙L−1 KCr O 溶液中Cr O 离子数为0.1N
2 2 7 2 A
D.100 mL 0.1 mol∙L−1的NaOH水溶液中含有氧原子数为0.01N
A
8.(2022·辽宁·朝阳市第二高级中学高二阶段练习)下列关于CH 和CO 的说法错误的是
4 2
A.固态时两者均属于分子晶体
B.CH 分子中含有极性共价键是非极性分子
4
C.CH 和CO 分子中碳原子的杂化类型分别是sp3和sp
4 2
D.因为碳氢键键能小于碳氧双键,所以CH 的熔点低于CO
4 2
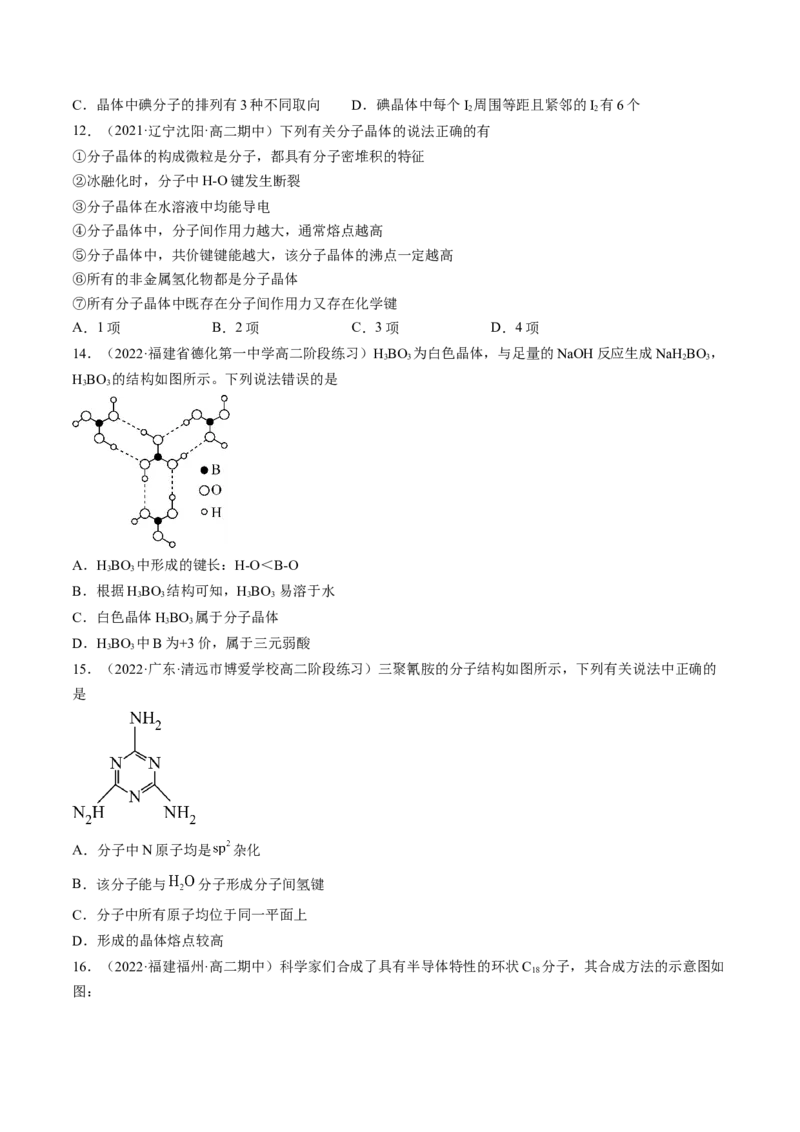
9.(2022·广东广州·高二期末)我国力争于2060年前实现碳中和。 与 重整是 利用的研究热
点之一。下列关于 和 说法正确的是
A.固态 属于共价晶体
B. 键角大于 键角
C. 分子中含有极性共价键,是极性分子
D.干冰中每个 分子周围紧邻12个 分子
10.(2022·新疆·乌市八中高二期末)下列说法正确的是
A.分子晶体中一定存在分子间作用力,不一定存在共价键
B.水加热到很高的温度都难以分解,与氢键有关
C. 晶体是分子晶体,分子间通过共价键结合
D.HF、 的沸点随着相对分子质量的增大依次升高
培优第二阶——拓展培优练
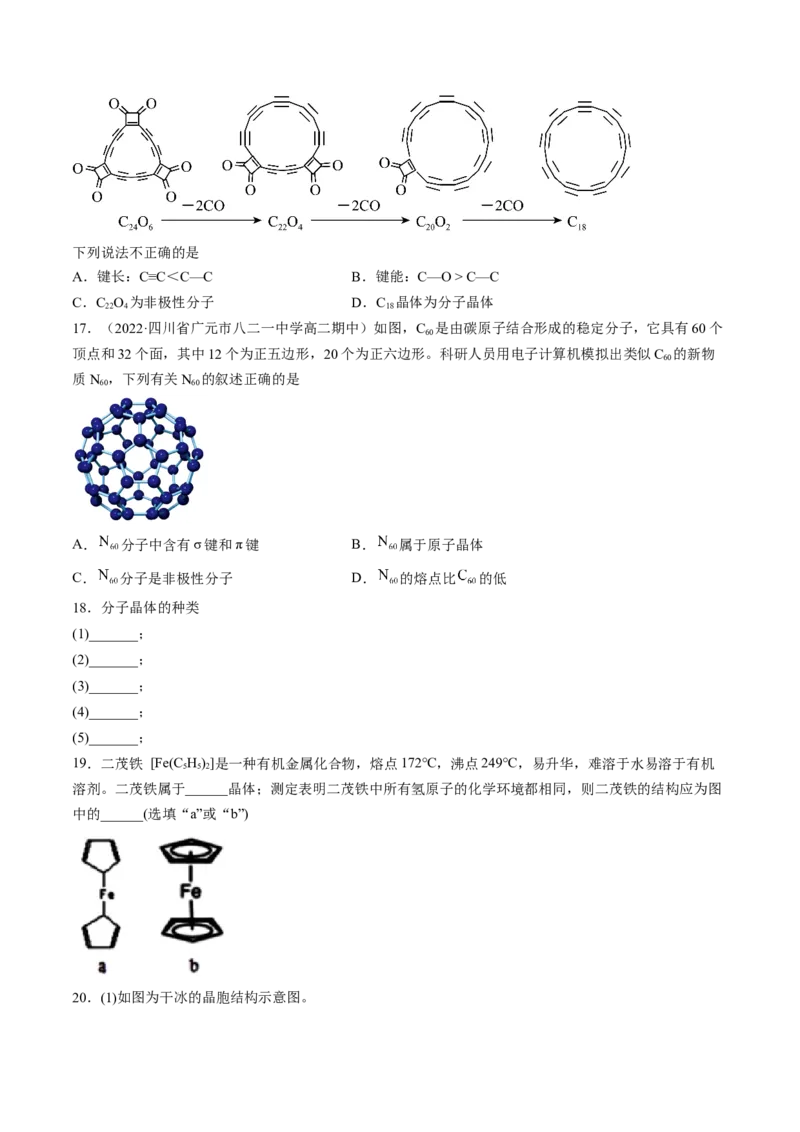
11.(2022·广东广州·高二期末)碘的晶胞结构示意图如图,下列说法正确的是
A.碘晶体熔化时需克服共价键 B.1个碘晶胞中含有4个碘分子C.晶体中碘分子的排列有3种不同取向 D.碘晶体中每个I 周围等距且紧邻的I 有6个
2 2
12.(2021·辽宁沈阳·高二期中)下列有关分子晶体的说法正确的有
①分子晶体的构成微粒是分子,都具有分子密堆积的特征
②冰融化时,分子中H-O键发生断裂
③分子晶体在水溶液中均能导电
④分子晶体中,分子间作用力越大,通常熔点越高
⑤分子晶体中,共价键键能越大,该分子晶体的沸点一定越高
⑥所有的非金属氢化物都是分子晶体
⑦所有分子晶体中既存在分子间作用力又存在化学键
A.1项 B.2项 C.3项 D.4项
14.(2022·福建省德化第一中学高二阶段练习)HBO 为白色晶体,与足量的NaOH反应生成NaH BO,
3 3 2 3
HBO 的结构如图所示。下列说法错误的是
3 3
A.HBO 中形成的键长:H-O<B-O
3 3
B.根据HBO 结构可知,HBO 易溶于水
3 3 3 3
C.白色晶体HBO 属于分子晶体
3 3
D.HBO 中B为+3价,属于三元弱酸
3 3
15.(2022·广东·清远市博爱学校高二阶段练习)三聚氰胺的分子结构如图所示,下列有关说法中正确的
是
A.分子中N原子均是 杂化
B.该分子能与 分子形成分子间氢键
C.分子中所有原子均位于同一平面上
D.形成的晶体熔点较高
16.(2022·福建福州·高二期中)科学家们合成了具有半导体特性的环状C 分子,其合成方法的示意图如
18
图:下列说法不正确的是
A.键长:C≡C<C—C B.键能:C—O > C—C
C.C O 为非极性分子 D.C 晶体为分子晶体
22 4 18
17.(2022·四川省广元市八二一中学高二期中)如图,C 是由碳原子结合形成的稳定分子,它具有60个
60
顶点和32个面,其中12个为正五边形,20个为正六边形。科研人员用电子计算机模拟出类似C 的新物
60
质N ,下列有关N 的叙述正确的是
60 60
A. 分子中含有σ键和π键 B. 属于原子晶体
C. 分子是非极性分子 D. 的熔点比 的低
18.分子晶体的种类
(1)_______;
(2)_______;
(3)_______;
(4)_______;
(5)_______;
19.二茂铁 [Fe(C H)]是一种有机金属化合物,熔点172℃,沸点249℃,易升华,难溶于水易溶于有机
5 5 2
溶剂。二茂铁属于______晶体;测定表明二茂铁中所有氢原子的化学环境都相同,则二茂铁的结构应为图
中的______(选填“a”或“b”)
20.(1)如图为干冰的晶胞结构示意图。通过观察分析,每个CO 分子周围紧邻且等距离的CO 分子有__个,有__种取向不同的CO 分子。
2 2 2
(2)在冰晶体中,水分子之间的主要作用力是__,还有__,由于该主要作用力与共价键一样具有__性,故1
个水分子周围只有__个紧邻的水分子,这些水分子位于__的顶角。这种排列方式使冰晶体中水分子的空间
利用率__(填“较高”或“较低”),故冰的密度比液态水的密度要__(填“大”或“小”)。
21.分子晶体的结构特征
(1)只有范德华力,无分子间氢键_______ 。干冰晶胞是一种 _______, 每个晶胞中有_______个CO 分子。
2
每个CO 分子周围等距离紧邻的CO 分子数为_______ 个。有分子间氢键不具有分子密堆积特征:如
2 2
HF、冰、NH 等。
3
(2)分子晶体堆积方式
分子间作用
堆积方式 实例
力
_____ _____ ______
______ ______ ____________
21.据报道,科研人员应用计算机模拟出结构类似C 的物质N 。
60 60
已知:①N 分子中每个氮原子均以N—N结合3个氮原子而形成8电子稳定结构;
60
②N—N的键能为167 kJ•mol-1。请回答下列问题:
N 分子组成的晶体为_____晶体,其熔、沸点比N 晶体的____(填“高”或“低”),原因是______。
60 2