文档内容
第三节 无机非金属材料--课时训练 2022-2023学年高一下
学期化学人教版(2019)必修第二册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.《厉害了,我的国》“中国名片”中航天、军事天文等领域的发展受到世界瞩目,
它们与化学有着密切联系。下列说法正确的是
A.“中国天眼”的“眼眶”是钢铁结成的圈梁,属于新型无机非金属材料
B.“复兴号”车厢连接处关键部位使用的增强聚四氟乙烯板属于无机金属材料
C.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷是新型无机非金属材料
D.“天宫二号”空间实验室的太阳能电池板是将太阳能转化为化学能再转化为电能
2.含硅元素的物质有很多用途,下列说法不正确的是
A.水玻璃是硅酸钠的水溶液,可用作木材防火剂的原料
B.玛瑙的主要成分是SiO
2
C.青花瓷胎体的原料为高岭土[AlSi O(OH) ],若以氧化物形式可表示为
2 2 5 4
Al O·2SiO·2H O
2 3 2 2
D.光导纤维主要成份为Si
3.下列叙述不正确的是
A.工业上常用焦炭还原石英砂制备粗硅
B.为防止粮食、罐头、水果等食品腐烂,常用氮气做保护气
C. 与HCl气体反应生成 不属于氮的固定
D. 有毒,不能做食品添加剂
4.下列说法正确的是
A.光导纤维的主要成分是硅
B.常用氢氟酸(HF)来刻蚀玻璃
C.制普通玻璃的主要原料是烧碱、石灰石、石英
D.实验室用带玻璃塞的试剂瓶保存氢氧化钠溶液
5.下列各项操作中,会出现“先沉淀后溶解”现象的是( )
A.向氯化铝溶液中滴加氢氧化钠至过量
B.向饱和的NaCO 溶液中通入CO 气体直至过量
2 3 2
C.向NaSiO 溶液中通入氯化氢气体直至过量
2 3
D.向CaCl 溶液中通入CO 气体直至过量
2 26.下列关于二氧化碳的说法正确的是
A.CO 支持镁的燃烧
2
B.CO 的水溶液不能导电
2
C.干冰与SiO 都不能与酸反应
2
D.呼吸面具中CO 与NaO 反应利用了CO 的氧化性
2 2 2 2
7.下列离子方程式不正确的是
A.向Mg(HCO ) 溶液中加入过量的NaOH溶液:Mg2++2HCO +4OH-=Mg(OH) ↓+2CO
3 2 2
+2H O
2
B.Fe O 溶于过量氢碘酸溶液中:Fe O+6H++2I-=2Fe2++I +3H O
2 3 2 3 2 2
C.二氧化硅和氢氧化钠溶液反应:SiO+2OH-=SiO +H O
2 2
D.向NH HSO 稀溶液中逐滴加入Ba(OH) 稀溶液至SO 刚好沉淀完全:Ba2++OH-
4 4 2
+H++SO =BaSO ↓+H O
4 2
8.下列物质的性质与用途之间的对应关系不正确的是
选
性质 用途
项
A NaO 可与CO 反应放出氧气 制作呼吸面具
2 2 2
B SiO 具有导电性 制作光导纤维和光电池
2
C 聚四氟乙烯耐酸碱腐蚀 作酸碱通用滴定管的活塞
D 氢氧化铝有弱碱性 用于中和过多的胃酸
A.A B.B C.C D.D
9.下列由实验或已有知识得出的结论错误的是
A.SO 可用于杀菌、消毒,但不可用来加工食品
2
B.液氨汽化时要吸收大量热,因此氨常用作制冷剂
C.二氧化硅与水不反应,说明二氧化硅不是酸性氧化物
D.铝箔在酒精灯上加热铝熔化但不滴落,说明氧化铝的熔点高于铝的熔点
10.化学与生产、生活、科技息息相关,下列叙述错误的是
A.华为首款5G手机搭载了智能7nm制程SoC“麒麟980”手机芯片主要成分是二氧化
硅
试卷第2页,共3页B.国产飞机C919用到氮化硅陶瓷是新型无机非金属材料
C.减少燃煤的使用可减少二氧化硫的排放,减少酸雨的危害
D.铵盐具有受热易分解的性质,在储存铵态氮肥时,应密封包装并放在阴凉通风处
11.下列说法错误的是
A.生产玻璃和水泥的原料中均有石灰石
B.陶瓷由黏土高温烧制而成,主要成分是硅酸盐
C.耐高温的石英玻璃属于硅酸盐材料
D.在雷雨天,空气中N 和O 可反应生成NO
2 2
12.关于以下科技成果,下列说法正确的是()
A.中国“人造太 C.“鲲龙”两栖飞 D.“墨子”通信
B.电磁炮成功装船
阳” 机 卫星
利用氘和氚发生化 飞机大量使用熔点 通讯中使用的光导
电磁炮发射过程中
学反应产生上亿度 高、硬度大的铝锂 纤维主要成分是单
电能转化为机械能
高温 合金 晶硅
A.A B.B C.C D.D
二、填空题
13.(1)写出氨的催化氧化化学方程式__。
(2)写出实验室制备NH 的化学方程式__。
3
(3)实验室盛放碱溶液的试剂瓶应用橡胶塞,不能用玻璃塞,用化学方程式解释原因___。
(4)Cu与稀硝酸的化字万程式___。
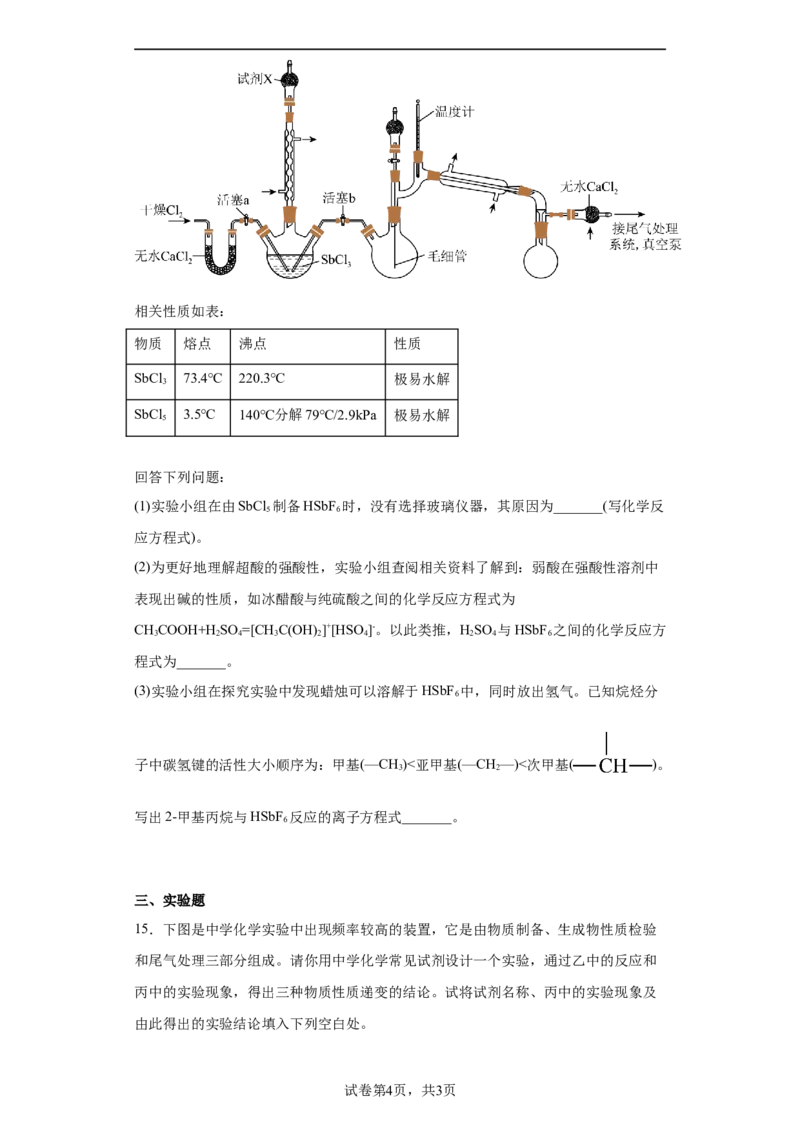
14.超酸是一类比纯硫酸更强的酸,在石油重整中用作高效催化剂。某实验小组对超
酸HSbF 的制备及性质进行了探究。由三氯化锑(SbCl )制备HSbF 的反应如下:
6 3 6
、SbCl +6HF=HSbF +5HCl。制备SbCl 的初始实验装置如图(毛
5 6 5
细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):相关性质如表:
物质 熔点 沸点 性质
SbCl 73.4℃ 220.3℃ 极易水解
3
SbCl 3.5℃ 140℃分解79℃/2.9kPa 极易水解
5
回答下列问题:
(1)实验小组在由SbCl 制备HSbF 时,没有选择玻璃仪器,其原因为_______(写化学反
5 6
应方程式)。
(2)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中
表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为
CHCOOH+H SO =[CH C(OH) ]+[HSO ]-。以此类推,HSO 与HSbF 之间的化学反应方
3 2 4 3 2 4 2 4 6
程式为_______。
(3)实验小组在探究实验中发现蜡烛可以溶解于HSbF 中,同时放出氢气。已知烷烃分
6
子中碳氢键的活性大小顺序为:甲基(—CH)<亚甲基(—CH—)<次甲基( )。
3 2
写出2-甲基丙烷与HSbF 反应的离子方程式_______。
6
三、实验题
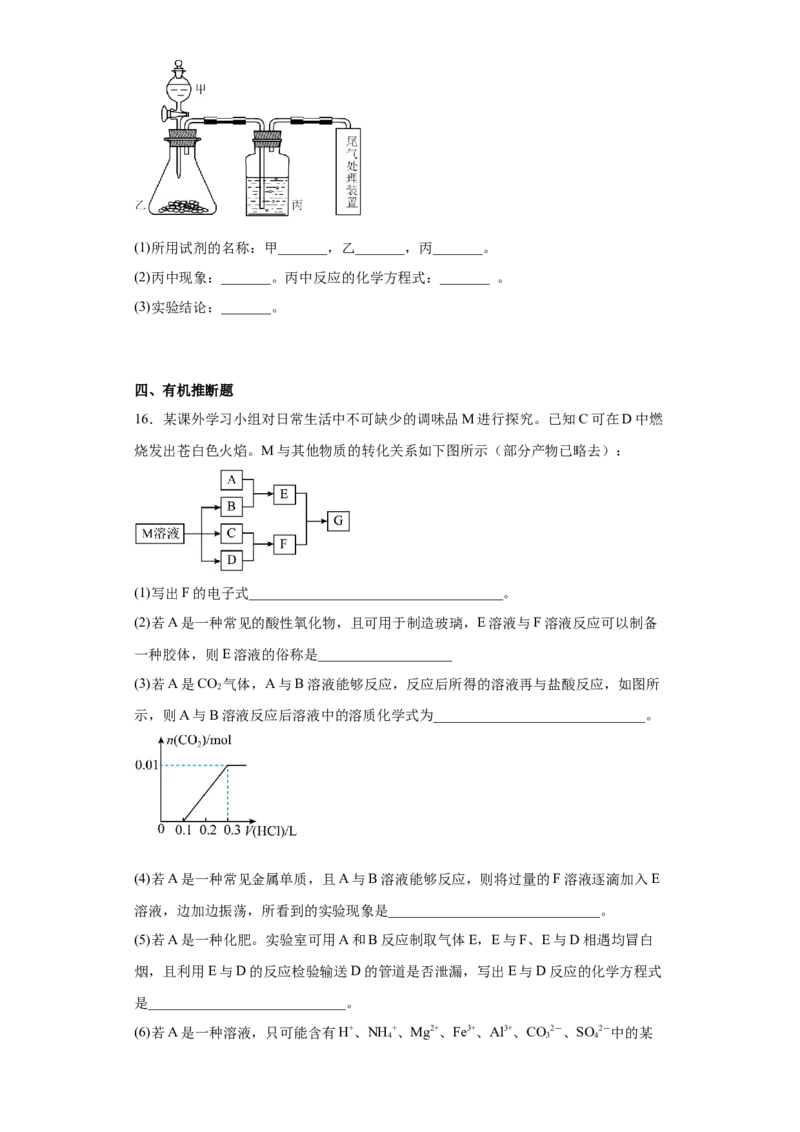
15.下图是中学化学实验中出现频率较高的装置,它是由物质制备、生成物性质检验
和尾气处理三部分组成。请你用中学化学常见试剂设计一个实验,通过乙中的反应和
丙中的实验现象,得出三种物质性质递变的结论。试将试剂名称、丙中的实验现象及
由此得出的实验结论填入下列空白处。
试卷第4页,共3页(1)所用试剂的名称:甲_______,乙_______,丙_______。
(2)丙中现象:_______。丙中反应的化学方程式:_______ 。
(3)实验结论:_______。
四、有机推断题
16.某课外学习小组对日常生活中不可缺少的调味品M进行探究。已知C可在D中燃
烧发出苍白色火焰。M与其他物质的转化关系如下图所示(部分产物已略去):
(1)写出F的电子式____________________________________。
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,E溶液与F溶液反应可以制备
一种胶体,则E溶液的俗称是___________________
(3)若A是CO 气体,A与B溶液能够反应,反应后所得的溶液再与盐酸反应,如图所
2
示,则A与B溶液反应后溶液中的溶质化学式为______________________________。
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E
溶液,边加边振荡,所看到的实验现象是______________________________。
(5)若A是一种化肥。实验室可用A和B反应制取气体E,E与F、E与D相遇均冒白
烟,且利用E与D的反应检验输送D的管道是否泄漏,写出E与D反应的化学方程式
是____________________________。
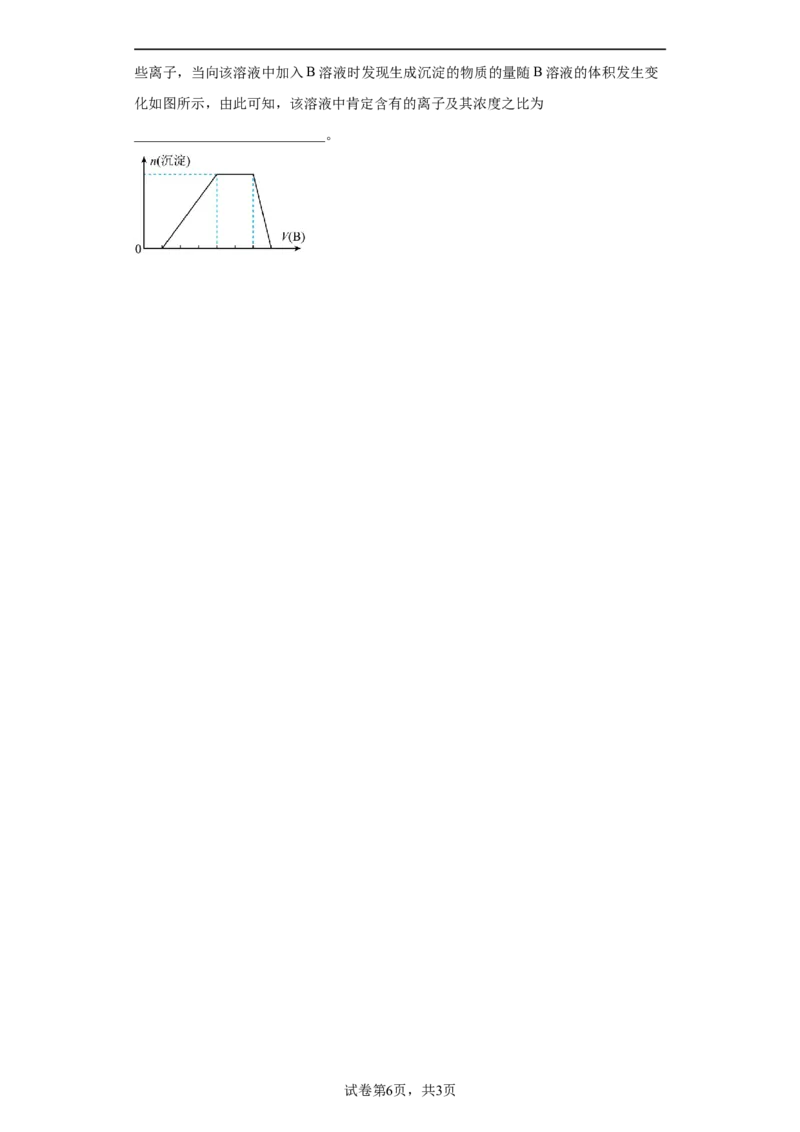
(6)若A是一种溶液,只可能含有H+、NH +、Mg2+、Fe3+、Al3+、CO2-、SO 2-中的某
4 3 4些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变
化如图所示,由此可知,该溶液中肯定含有的离子及其浓度之比为
___________________________。
试卷第6页,共3页参考答案:
1.C
【详解】A.钢铁是铁的一种合金,属于金属材料,不属于新型无机非金属材料,故A错
误;
B.聚四氟乙烯板属于有机材料,不属于无机金属材料,故B错误;
C.高温结构陶瓷属于耐高温的新型无机非金属材料,故C正确;
D.太阳能电池板的主要材料是晶体硅,将太阳能转化为电能,故D错误;
答案选C。
2.D
【详解】A.水玻璃是硅酸钠(NaSiO)的水溶液,可用作木材防火剂的原料,故A正确;
2 3
B.玛瑙是熔融态二氧化硅快速冷却形成的,主要成分是SiO,故B正确;
2
C.青花瓷胎体的原料为高岭土[AlSi O(OH) ],高岭土是硅酸盐,可以写成氧化物的形式:
2 2 5 4
Al O·2SiO·2H O,故C正确;
2 3 2 2
D.光导纤维主要成份为SiO,故D错误;
2
故选D。
3.D
【详解】A.工业上常用焦炭还原石英砂制备粗硅,反应的化学方程式为2C+SiO
2
Si+2CO↑,A正确;
B.氮气中氮氮三键键能大,氮气很稳定,难以与其它物质反应,常用作粮食、罐头、水
果等的保护气,B正确;
C.将大气中游离态的氮转化为氮的化合物的过程叫做氮的固定,NH 中为化合态的氮,故
3
NH 与HCl反应生成NH Cl不属于氮的固定,C正确;
3 4
D.二氧化硫可做食品添加剂,食品中添加适量二氧化硫可以起到漂白、防腐和抗氧化等
作用,如在葡萄酒中常添加适量二氧化硫,D错误;
答案选D。
4.B
【详解】A.光导纤维的主要成分是二氧化硅,A不正确;
B.氢氟酸能与二氧化硅反应,而玻璃中含有二氧化硅,则HF可用于雕刻玻璃,B正确;
C.制普通玻璃的主要原料是纯碱、石灰石、石英砂,C不正确;
D.保存氢氧化钠溶液不能用带玻璃塞的试剂瓶,因为NaOH与玻璃的主要成分二氧化硅
反应生成具有黏性的硅酸钠,时间长了瓶塞会打不开,D不正确;答案选B。
5.A
【详解】A. 氯化铝溶液中滴加氢氧化钠会先生成Al(OH) 沉淀,滴加氢氧化钠至过量,
3
Al(OH) 会溶解反应产生NaAlO ,符合题意,故A选;
3 2
B. 向饱和的NaCO 溶液中通入CO 气体直至过量,会产生NaHCO 沉淀,因为NaHCO
2 3 2 3 3
溶解度低于NaCO 而析出,不会继续溶解,不符合题意,故B不选;
2 3
C. NaSiO 溶液中通入氯化氢气体产生HSiO 沉淀,氯化氢气体加至过量,HSiO 沉淀也
2 3 2 3 2 3
不会溶解,不符合题意,故C不选;
D. 弱酸不能制强酸,CaCl 与CO 不反应,不符合题意,故D不选。
2 2
故答案选A。
6.A
【详解】A.Mg可以在CO 中燃烧,CO+2Mg C+2MgO,A正确;
2 2
B.CO 与HO反应生成HCO,CO+H O HCO,HCO 是弱电解质,水溶液可以导电,
2 2 2 3 2 2 2 3 2 3
B错误;
C.SiO 可以与HF反应,SiO+ 4HF=SiF +2H O,C错误;
2 2 4 2
D.CO 与NaO 反应为2NaO+2CO=2Na CO+O,CO 中C和O没有变价,该反应的
2 2 2 2 2 2 2 3 2 2
氧化剂和还原剂均为NaO,D错误;
2 2
故选A。
7.D
【详解】A.向Mg(HCO ) 溶液中加入过量的NaOH溶液,生成溶解度更小的氢氧化镁沉
3 2
淀,同时碳酸氢根完全反应,离子方程式为Mg2++2HCO +4OH-=Mg(OH) ↓+2CO
2
+2H O,A正确;
2
B.Fe O 溶于过量氢碘酸溶液中,铁离子将碘离子氧化为碘单质,离子方程式为
2 3
Fe O+6H++2I-=2Fe2++I +3H O,B正确;
2 3 2 2
C.二氧化硅和氢氧化钠溶液反应生成硅酸钠和水,离子方程式为SiO+2OH-=SiO
2
+H O,C正确;
2
答案第2页,共2页D.向NH HSO 稀溶液中逐滴加入Ba(OH) 稀溶液至SO 刚好沉淀完全,NH HSO 和
4 4 2 4 4
Ba(OH) 按照1:1反应,所以铵根也可以反应,离子方程式为NH +Ba2++2OH-+H++SO
2
=BaSO ↓+H O+NH ·H O,D错误;
4 2 3 2
综上所述答案为D。
8.B
【详解】A.过氧化钠为固体,与二氧化碳发生氧化还原反应生成氧气,可用于制作呼吸
面具,选项A正确;
B.二氧化硅对光具有良好的全反射作用,则用于制作光导纤维,而Si为半导体材料可作
光电池材料,选项B错误;
C.聚四氟乙烯与酸、碱均不反应,可用作酸碱通用滴定管的活塞,选项C正确;
D.氢氧化铝能与盐酸反应生成盐和水,且其碱性较弱对人体无害,常用于中和过多的胃
酸,选项D正确;
答案选B。
9.C
【详解】试题分析:A、二氧化硫有毒,不可用来加工食品,故A正确;B、氨气容易液化,
液氨汽化吸收大量的热,氨可以用作制冷剂,故B正确;C、二氧化硅与氢氧化钠反应生
成硅酸钠与水,故二氧化硅属于酸性氧化物,故C错误;D、铝和氧气反应生成了氧化铝,
氧化铝膜兜住熔化铝不滴落,说明氧化铝的熔点高于铝的熔点,故D正确;故选C。
考点:考查了元素及其化合物的性质和应用的相关知识。
10.A
【详解】A.芯片的成分是单质硅,不是二氧化硅,二氧化硅可用作光导纤维,选项A错
误;
B.氮化硅陶瓷属于无机物,是新型无机非金属材料,选项B正确;
C.燃煤中含有硫,燃烧会产生二氧化硫,所以减少燃煤的使用能减少酸雨的危害,选项C
正确;
D.铵盐具有受热易分解的性质,在储存铵态氮肥时,应密封包装并放在阴凉通风处,防
止受热分解,选项D正确;
答案选A。
11.C【详解】A.水泥的原料是粘土和石灰石,玻璃的原料是纯碱、石灰石和石英,所以原料
中均有石灰石,故A正确;
B.陶瓷由黏土经高温烧结而成,其主要成分是硅酸盐,如硅酸钙、硅酸钠等,故B正确;
C.石英玻璃成分为二氧化硅,为氧化物,不是硅酸盐,故C错误;
D.放电条件下氮气和氧气发生氧化还原反应生成NO,反应方程式为N+O 2NO,故
2 2
D正确;
故选:C。
12.B
【详解】A.人造太阳反生核聚变,不是化学反应,A项错误;
B.电磁炮利用强大的电磁力来加速弹丸,是将电能转化为机械能,B项正确;
C.合金的熔点会比纯金属的熔点低,故铝锂合金的熔点较低,C项错误;
D.光导纤维的主要成分为二氧化硅,D项错误;
答案选B。
13.
【详解】(1)氨气在催化剂作用下与氧气反应生成NO和HO,化学方程式为:
2
。
(2)实验室用氯化铵和碱石灰在加热的条件下制取氨气,反应方程式为:
。
(3)玻璃中的二氧化硅是酸性氧化物,会与碱反应生成盐和水,化学方程式为:
。
(4)Cu与稀硝酸反应生成硝酸铜、一氧化氮和水,反应化学方程式为:
答案第4页,共2页。
14.(1)SiO+4HF=SiF ↑+2H O
2 4 2
(2)H SO +HSbF =[H SO ]+[SbF ]-
2 4 6 3 4 6
(3)CH CH(CH )CH+HSbF =(CH )C++SbF +H ↑
3 3 3 6 3 3 2
【分析】干燥的氯气通过无水氯化钙进入三颈烧瓶中与SbCl 在80℃下反应生成SbCl ,反
3 5
应完成后,关闭活塞a、打开活塞b,减压使三颈烧瓶中生成的SbCl 转移至双口烧瓶中,
5
SbCl 、SbCl 极易水解,试剂X可防止空气中的水蒸气进入三颈烧瓶,同时吸收氯气,防
3 5
止污染空气。
(1)
由题意可知,由SbCl 制备HSbF 时,需用HF,而HF可与玻璃中的二氧化硅反应,因此
5 6
不能选择玻璃仪器,反应的化学方程式为:SiO+4HF=SiF ↑+2H O。
2 4 2
(2)
根据已知反应可知,冰醋酸与纯硫酸反应时,纯硫酸给出的氢离子加在了冰醋酸的双键氧
原子上形成了另一个羟基,由于纯硫酸的结构简式为: ,故其与超酸
HSbF 反应可生成 ,反应的化学方程式为:HSO +HSbF =[H SO ]+
6 2 4 6 3 4
[SbF ]-。
6
(3)
2-甲基丙烷的结构简式为CHCH(CH )CH,根据题目信息可知,CHCH(CH )CH 中
3 3 3 3 3 3上的氢参与反应,反应的离子方程式为:CHCH(CH )CH+HSbF =(CH )C+
3 3 3 6 3 3
+SbF +H ↑。
2
15.(1) 稀硫酸 纯碱(或亚硫酸钠等) 苯酚钠溶液(或硅酸钠溶液)
(2) 澄清溶液变浑浊 CO +H O+C HONa→C HOH+NaHCO
2 2 6 5 6 5 3
(3)酸性:硫酸>碳酸(或亚硫酸)>苯酚(或硅酸)
【解析】略
16.(1)
(2)水玻璃
(3)NaHCO 、NaCO
3 2 3
(4)溶液中逐渐有白色絮状沉淀生成,且不断地增加,随后沉淀逐渐溶解最终消失
(5)3Cl + 8NH =N + 6NH Cl
2 3 2 4
(6)c(H+)∶c(Al3+)∶c(NH +)∶c(SO 2-)=1∶1∶2∶3
4 4
【分析】C可在D中燃烧发出苍白色火焰,为氢气与氯气反应生成HCl,可推知C为H、
2
D为Cl、F为HCl,M是日常生活中不可缺少的调味品,由转化关系可知,M的溶液电解
2
生成氢气、氯气与B,可推知M为NaCl、B为NaOH;
【详解】(1)HCl的电子式 ,答案: ;
(2)若A是一种常见的酸性氧化物,且可用于制造玻璃,则A为SiO,E为NaSiO,与
2 2 3
F溶液反应可以制备G为HSiO,E溶液的俗称是水玻璃,答案:水玻璃;
2 3
(3)曲线中,从0.1L~0.3L发生反应NaHCO +HCl=NaCl+CO ↑+H O,该阶段消耗盐酸为
3 2 2
200mL,而开始产生二氧化碳时消耗盐酸为100mL,小于200mL,所以溶液中的溶质成分
NaHCO 、NaCO,答案:NaHCO 、NaCO;
3 2 3 3 2 3
(4)若A是一种常见金属单质,且与NaOH溶液能够反应,则A为Al,E为NaAlO ,则
2
将过量的HCl溶液逐滴加入NaAlO 溶液中,先生成氢氧化铝,而后氢氧化铝溶解,故看到
2
的现象为:溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失,
答案:溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失;
答案第6页,共2页(5)若A是一种化肥,实验室可用A和NaOH反应制取气体E,则E为NH 、A为铵盐,
3
NH 与HCl、NH 与氯气相遇均冒白烟,且利用NH 与氯气的反应检验输送氯气的管道是
3 3 3
否泄漏,则氨气与氯气反应生成氯化铵,同时生成氮气,反应方程式为:
3Cl+8NH=N +6NHCl,答案:3Cl+8NH=N +6NHCl;
2 3 2 4 2 3 2 4
(6)由图可知,开始加入NaOH没有沉淀和气体产生,则一定有H+,一定没有CO2-,后
3
来有沉淀产生且最后消失,则一定没有Mg2+、Fe3+,一定含有Al3+;中间段沉淀的质量不
变,应为NH ++OH-=NH·H O的反应,则含有NH +,由电荷守恒可知一定含有SO 2-,发生
4 3 2 4 4
反应H++OH-=H O,氢离子消耗NaOH溶液的体积为1积,发生反应Al3++3OH-=Al(OH)
2
↓,铝离子消耗NaOH溶液的体积为3体积,发生反应NH ++OH-=NH·H O,铵根消耗氢氧
3 4 3 2
化钠为2体积,则n(H+)∶n(Al3+)∶n(NH +)=1∶1∶2,由电荷守恒可知,n(H+)∶n
4
(Al3+)∶n(NH +)∶n(SO 2-)=1∶1∶2∶3,故c(H+)∶c(Al3+)∶c(NH +)∶c
4 4 4
(SO 2-)=1∶1∶2∶3,答案:c(H+)∶c(Al3+)∶c(NH +)∶c(SO 2-)=1∶1∶2∶3。
4 4 4答案第8页,共2页