文档内容
山海联盟校教学协作体 2024-2025 学年第一学期
高一年级 化学学科 期中考试卷
命题人:吴永木 审题人:邱弘利
分值:100 分 完卷时间:75 分钟
相对原子质量:Na 23 Cu 64 H 1 S 32 O 16 C12 Cl 35.5 N 14
一、单选题(每题3分,共15题,共45分)
1.下列与胶体有关的实验描述正确的是
A.用一束激光照射胶体和溶液都有光亮的通路
B.制备氢氧化铁胶体的方法是饱和氯化铁溶液和氢氧化钠溶液混合
C.向氢氧化铁胶体中加入过量盐酸后出现红褐色沉淀
D.用过滤的方法不能分离氢氧化铁胶体和氯化铁溶液
2.下列物质分类正确的组合是
选项 纯净物 混合物 电解质 非电解质
A 盐酸 空气 硫酸 干冰
B 蒸馏水 蔗糖溶液 氧化铝 二氧化硫
C 胆矾 蒸馏水 铁 碳酸钙
D 水银 澄清石灰水 氯化铜 碳酸钠
A.A B.B C.C D.D
3.成语是我国传统文化的瑰宝。下列成语不涉及氧化还原反应的是
A.死灰复燃 B.水滴石穿 C.百炼成钢 D.火上浇油
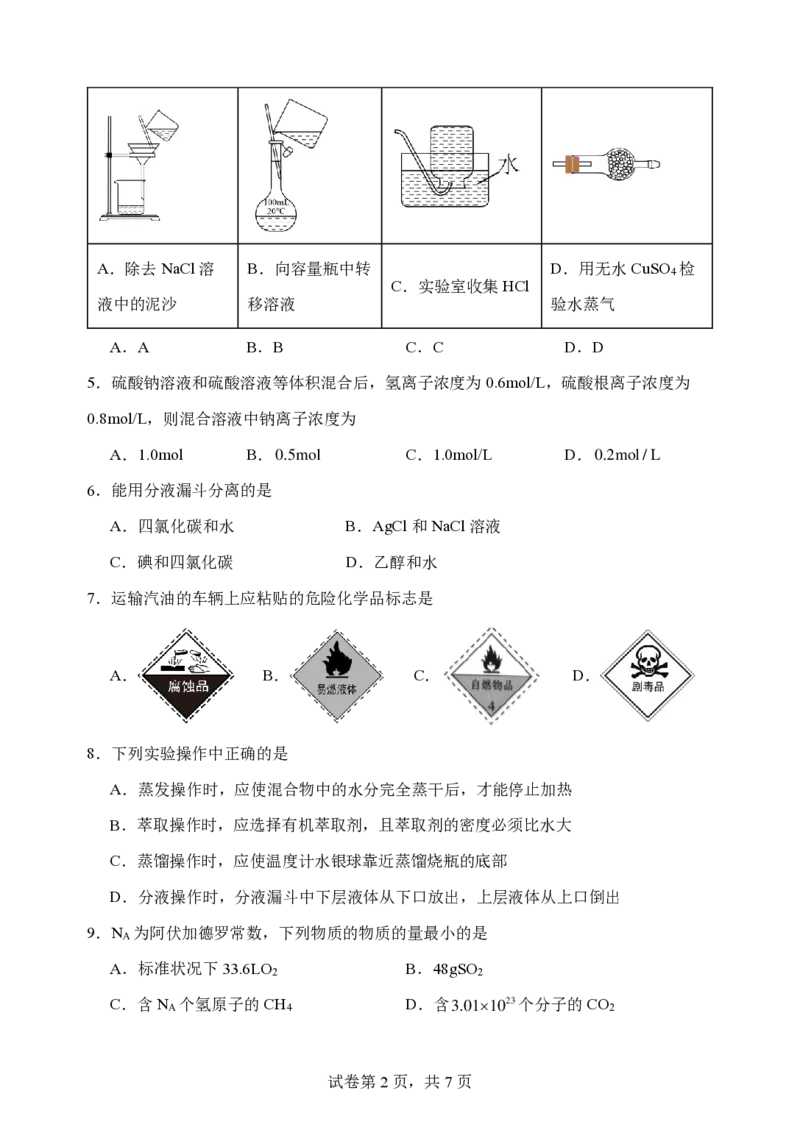
4.下列实验操作或实验目的错误的是
..
试卷第1页,共7页
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}A.除去NaCl溶 B.向容量瓶中转 D.用无水CuSO 检
4
C.实验室收集HCl
液中的泥沙 移溶液 验水蒸气
A.A B.B C.C D.D
5.硫酸钠溶液和硫酸溶液等体积混合后,氢离子浓度为0.6mol/L,硫酸根离子浓度为
0.8mol/L,则混合溶液中钠离子浓度为
A.1.0mol B.0.5mol C.1.0mol/L D.0.2mol/L
6.能用分液漏斗分离的是
A.四氯化碳和水 B.AgCl和NaCl溶液
C.碘和四氯化碳 D.乙醇和水
7.运输汽油的车辆上应粘贴的危险化学品标志是
A. B. C. D.
8.下列实验操作中正确的是
A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热
B.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
C.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的底部
D.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
9.N 为阿伏加德罗常数,下列物质的物质的量最小的是
A
A.标准状况下33.6LO B.48gSO
2 2
C.含N 个氢原子的CH D.含3.011023个分子的CO
A 4 2
试卷第2页,共7页
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}10.有四瓶常用溶液:①BaCl 溶液,②NaCl溶液,③Na SO 溶液,④CuSO 溶液。不
2 2 4 4
用其他试剂,可通过实验方法将它们一一鉴别开来。鉴别出来的先后顺序可能是
A.①④③② B.①④②③ C.④①③② D.①③④②
11.2022年诺贝尔化学奖授予了三位在“点击化学”及其应用方面做出了重大贡献的三位
化学家——卡罗琳·贝尔托西、莫滕桦尔达和巴里·夏普莱斯。卡罗琳·贝尔托西将“点击化
学”运用在生物学领域,并开创了“正交化学”,她的研究中需要对糖类进行示踪和定位。
在很多研究糖类的实验中,会选用具有放射性的
试卷第3页,共7页
14 C 进行示踪研究。以下有关同位素的说
法正确的是
A. 1 4 N
2
、 1 5 N
2
互为同位素
B.同一元素各核素的化学性质几乎完全相同
C. 1 6 O 、 1 8 O 的质子数相同,电子数不同
D.D、T发生核聚变成为其它元素,属于化学反应
12.如图为甲、乙两种微观粒子的结构示意图。下列相关叙述中,正确的是
A.甲粒子是阳离子,乙粒子是原子
B.甲、乙两种粒子都属于金属元素
C.甲粒子没有达到稳定结构,乙粒子已达到稳定结构
D.甲、乙两种粒子可结合形成化合物
13.某溶液可能由Na+、Cu2+、Ba2+、 F e 3 + 、CO2−、SO2−、Cl−中的若干种离子组成。
3 4
现取适量溶液进行如下实验:
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}根据以上实验判断,下列推断错误的是
A.气体1可使澄清石灰水变浑浊
B.原溶液中一定存在
试卷第4页,共7页
N a + ,一定不存在 B a 2 +
C.白色沉淀3为AgCl,原溶液中一定存在 C l −
D.无色溶液说明不存在 C u 2 + 、 F e 3 +
14.标准状况下,将VL A气体(摩尔质量为Mg/mo1)溶于0.1 L水中,所得溶液密度为
ρg/cm3,则此溶液的物质的量浓度(mol/L)为( )
A.
2 2 . 4
M
( V
V
+ 0 . 1 ) ρ
B.
( M
1 0
V
0
+
0
2
V
2
ρ
4 0 )
C.
( M V
V
+
ρ
2 2 4 0 )
D.
(
1
M
0 0
V
0
+
M
2
V
2 4
ρ
0 )
15.在两份相同的Ba(OH) 溶液中,分别滴入物质的量浓度相等的H SO 、NaHSO 溶
2 2 4 4
液,其导电能力随滴入溶液体积变化的曲线如图所示。下列分析不正确的是
A.b点,溶液中大量存在的离子是 N a + 、 O H −
B.①代表滴加H SO 溶液的变化曲线
2 4
C.c点,两溶液中酸碱性不同
D.a、d两点对应的体系具有相同的溶质和滴入溶液的体积
二、填空题(共4题,55分)
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}16.(12分)回答下列问题:
(1)质量相同的SO 和SO 的摩尔质量之比是 ;含氧原子个数比是 。
2 3
(2)标准状况下9.6g某气体体积与0.6g 氢气体积相同,该气体的相对分子质量
是 。
(3)
试卷第5页,共7页
1 .2 0 4 1 0 2 4 个NH 分子所含的氢原子数与 mol CH 含有的氢原子数相同。 3 4
(4)ag H SO 中含有 b个氧原子,则阿伏加德罗常数可以表示为 。
2 4
(5)1.204×10²⁴个CO 分子的摩尔质量是 。
2
17.(13分)中学化学中常见的几种物质:①氢氧化钡固体②铁丝③氯化氢气体④二氧
化碳⑤碳酸钠固体⑥熔融氯化钠,用上述序号填空:
(1)不属于电解质的是 。
(2)属于盐的是 。
(3)写出①在水溶液中的电离方程式: 。
(4)按要求书写下列反应的化学方程式:
②加入③的溶液中 。
⑤的溶液与③的溶液混合 。
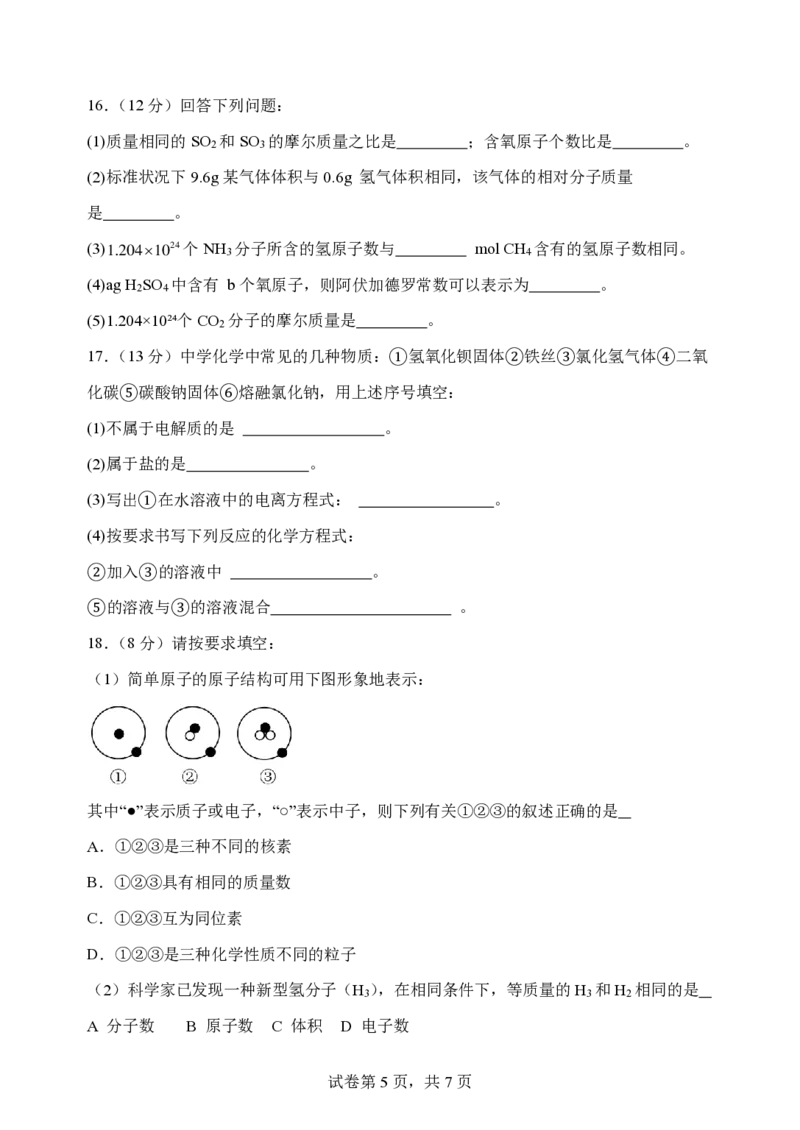
18.(8分)请按要求填空:
(1)简单原子的原子结构可用下图形象地表示:
其中“●”表示质子或电子,“○”表示中子,则下列有关①②③的叙述正确的是
A.①②③是三种不同的核素
B.①②③具有相同的质量数
C.①②③互为同位素
D.①②③是三种化学性质不同的粒子
(2)科学家已发现一种新型氢分子(H ),在相同条件下,等质量的H 和H 相同的是
3 3 2
A 分子数 B 原子数 C 体积 D 电子数
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}(3)微粒A Xn+核外有a个电子,则它的核内中子数为
(4)与10克D O含有相同电子数的NH 在标准状况下的体积是
2 3
19.(22分)I.实验室工作人员现用
试卷第6页,共7页
N a
2
C O
3
1 0 H
2
O 晶体配制 0 .4 m o l L − 1 的 N a
2
C O
3
溶液
230mL。回答下列问题:
(1)配制溶液时下列仪器中:
A.量筒B.托盘天平(带砝码)C.烧杯D.锥形瓶E.药匙F.胶头滴管G.玻璃棒
一定不需要用到的是 (填序号),尚缺的玻璃仪器有 (写名称)。
(2)应称取 N a
2
C O
3
1 0 H
2
O 晶体的质量为 g。
(3)下列主要操作步骤的正确顺序是 (填序号) 。
①称取一定质量的Na CO 10H O晶体,放入烧杯中,用适量蒸馏水溶解;
2 3 2
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻
度线相切;
③用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤将溶液转移到容量瓶中。
(4)根据下列操作对所配溶液的浓度产生的影响,其中引起所配溶液浓度偏低的有 (填
序号)
①Na CO 10H O晶体失去了部分结晶水
2 3 2
②用“左码右物”的称量方法称量晶体(使用游码)
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶内有少量蒸馏水就直接使用
(5)配制过程中向容量瓶中转移溶液时不慎将溶液洒到容量瓶外面,此时的处理方法
是: 。
II.实验室需要0.5molL−1硫酸溶液480mL。回答下列问题:
(6)实验中需要质量分数为98%、密度为1.84gcm−3的浓H SO 溶液 mL,在量
2 4
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}取时宜选用规格为 的量筒(填序号)。
A.10mL B.20mL C.50mL D.100mL
(7)若实验过程中遇到下列情况,对硫酸物质的量浓度有何影响(填“偏高”“偏低”或“无影
响”)。
①未经冷却将溶液注入容量瓶中: ;
②定容时俯视液面: 。
试卷第7页,共7页
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}山海联盟校教学协作体2024-2025学年第一学期
高一年级 化学学科 期中考(答题卡) 18. (8分)
(1)
姓名: 班级:
准考证号
考场/座位号: (2)
注意事项
[0] [0] [0] [0] [0] [0] [0] [0] (3)
[1] [1] [1] [1] [1] [1] [1] [1]
1.答题前请将姓名、班级、考场、准考证号填写清楚。
2.客观题答题,必须使用2B铅笔填涂,修改时用橡皮擦干净。 [2] [2] [2] [2] [2] [2] [2] [2] (4)
3.主观题答题,必须使用黑色签字笔书写。 [3] [3] [3] [3] [3] [3] [3] [3]
4.必须在题号对应的答题区域内作答,超出答题区域书写无效。 [4] [4] [4] [4] [4] [4] [4] [4]
5.保持答卷清洁、完整。 [5] [5] [5] [5] [5] [5] [5] [5]
[6] [6] [6] [6] [6] [6] [6] [6]
19.(22分)
[7] [7] [7] [7] [7] [7] [7] [7]
正确填涂 缺考标记
[8] [8] [8] [8] [8] [8] [8] [8]
(1)
[9] [9] [9] [9] [9] [9] [9] [9]
一、选择题
(2)
1 [A] [B] [C] [D] 6 [A] [B] [C] [D] 11 [A] [B] [C] [D] (3)
2 [A] [B] [C] [D] 7 [A] [B] [C] [D] 12 [A] [B] [C] [D]
3 [A] [B] [C] [D] 8 [A] [B] [C] [D] 13 [A] [B] [C] [D]
(4)
4 [A] [B] [C] [D] 9 [A] [B] [C] [D] 14 [A] [B] [C] [D]
5 [A] [B] [C] [D] 10 [A] [B] [C] [D] 15 [A] [B] [C] [D]
(5)
(6)
二填空题(共55分)
(7)
16. (12分)
(1)
(2)
(3)
(4)
(5)
17. (13分)
(1)
(2)
(3)
(4)
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}山海联盟校教学协作体 2024-2025 学年第一学期
高一年级化学学科半期考试参考答案
说明:
1.本答案及评分说明供阅卷评分时使用,考生若写出其他正确答案,可参
照本说明 给分。
2.化学方程式(包括离子方程式) 中的化学式、离子符号写错,不得分;
化学式、离子符号书写正确,但未配平、“ ↑ ”“ ↓ ”未标、必须书写的反应条
件未写(或写错)等化学用语书写规范错误的,每个化学方程式累计扣 1 分。其中
热化学方程式配平,状态, ∆H 符号、数值、单位有漏写或错误的,均不得分。
3 .化学专用名词书写错误均不得分。
第 I 卷(选择题)
一、选择题(每题只有一个正确选项,每题 3 分,共 15 小题,共 45 分 )
题号 1 2 3 4 5 6 7 8 9 10
答案 D B B C C A B D C C
题号 11 12 13 14 15
答案 B D C B D
第 II 卷(非选择题)
二、填空题(本大题共 4 小题,共 55 分)
16(12分)
(1)4:5(2分) 5:6(2分)
(2)32(2分)
(3)1.5(2分)
(4)
2
4 9 b
2 a
mol-1(2分)
(5)44gmol-1(2分)
17(13分)
(1)②④(2分)
(2)⑤⑥(2分)
(3)Ba(OH) =Ba2++2OH-(3分)
2
(4)Fe+2HCl=FeCl +H ↑ (3分) Na CO +2HCl=H O+CO ↑+2NaCl(3分)
2 2 2 3 2 2
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}18(8分)
(1) AC(2分)
(2) BD(2分)
(3)
2
A - ( a + n ) 或A-a-n(2分)
(4) 11.2L(2分)
19(22分)
(1)D(2分) 250mL容量瓶(2分,容量瓶规格没写不得分)
(2)28.6(2分)
(3)①⑤③②④(3分)
(4)②③(3分,漏选一个得2分,多选不得分)
(5)重新配制(2分)
(6)13.6(2分) B(2分)
(7)偏高(2分) 偏高(2分)
{#{QQABYYSQgggoAAAAAQhCQQHCCgCQkgEAAagOhAAIIAABiQFABAA=}#}