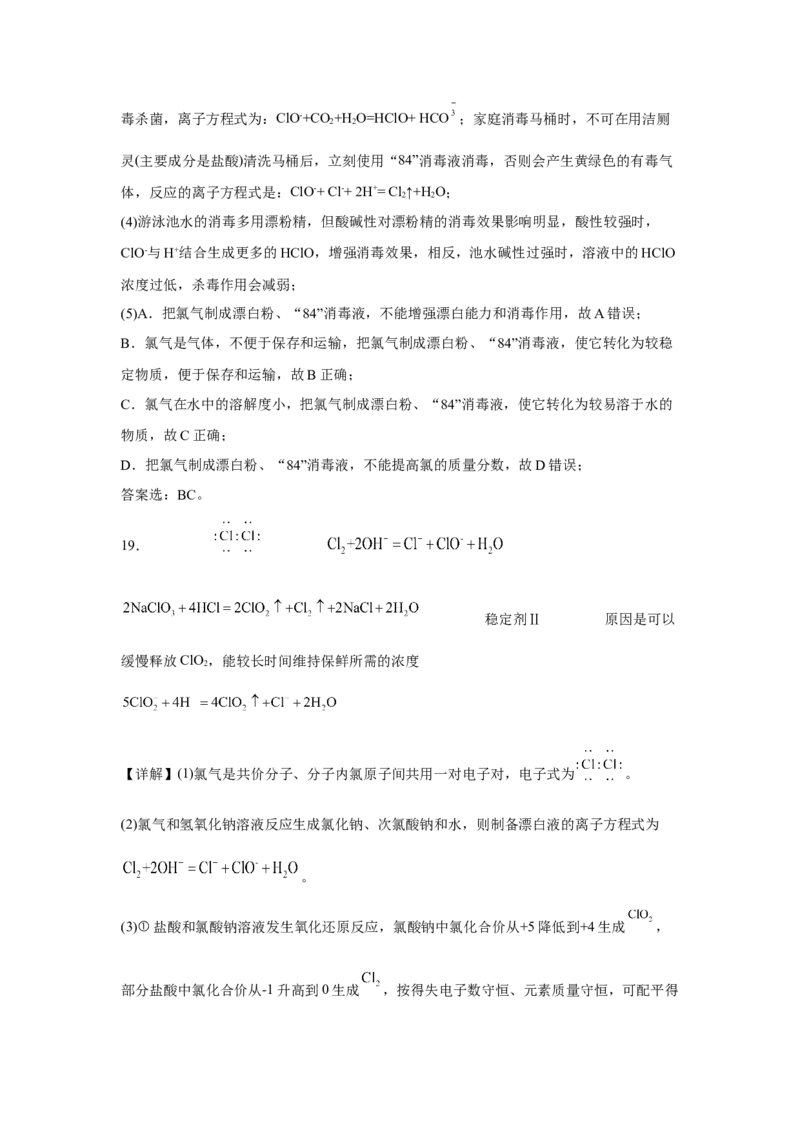文档内容
人教版(2019)必修第一册第二章第二节氯及其化合物
课时训练二
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1. 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应
为 。下列说法错误的是
A.产生22.4L(标准状况) 时,反应中转移
B.反应中氧化剂和还原剂的物质的量之比为11:6
C.可用石灰乳吸收反应产生的 制备漂白粉
D.可用酸化的淀粉碘化钾溶液检验食盐中 的存在
2.化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选
现象或事实 解释
项
A 用热的烧碱溶液洗去油污 NaCO 可直接和油污反应
2 3
漂白粉中的CaCl 与空气中的CO
B 漂白粉在空气中久置变质 2 2
反应生成CaCO
3
施肥时,草木灰(有效成分为KCO)不能 KCO 与NH Cl反应生成氨气会降
C 2 3 2 3 4
与NH Cl混合使用 低肥效
4
FeCl 能从含有Cu2+的溶液中置换出
D FeCl 溶液可用于铜质印刷线路板制作 3
3 铜
A.A B.B C.C D.D
3.新冠肺炎对生产生活带来了巨大冲击。医用酒精、含 的消毒液可用于个人
与环境消毒,但含 的消毒液与医用酒精不可混用,混用会产生有毒气体 ,
发生的主要反应为:① ,②……(后
续反应略)。下列关于氯气和新制氯水的说法正确的是A.足量铁丝在 中燃烧生成
B.向加有淀粉的 溶液中通入少量 后溶液变蓝,说明 的氧化性强于
C. 溶液中滴加新制氯水,溶液变成棕黄色,说明新制氯水中含有
D.用强光照射新制氯水一段时间后,溶液 增大
4.利用数字传感器对氯水的光照实验进行数据采集与分析,下列图示正确的是
A. B.
C. D.
5.在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl
2
B.向氯水中滴加硝酸酸化的AgNO 溶液,产生白色沉淀,说明氯水中含有Cl-
3
C.向氯水中加入NaHCO 粉末,有气泡产生,说明氯水中含有H+
3
D.向FeCl 溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
2
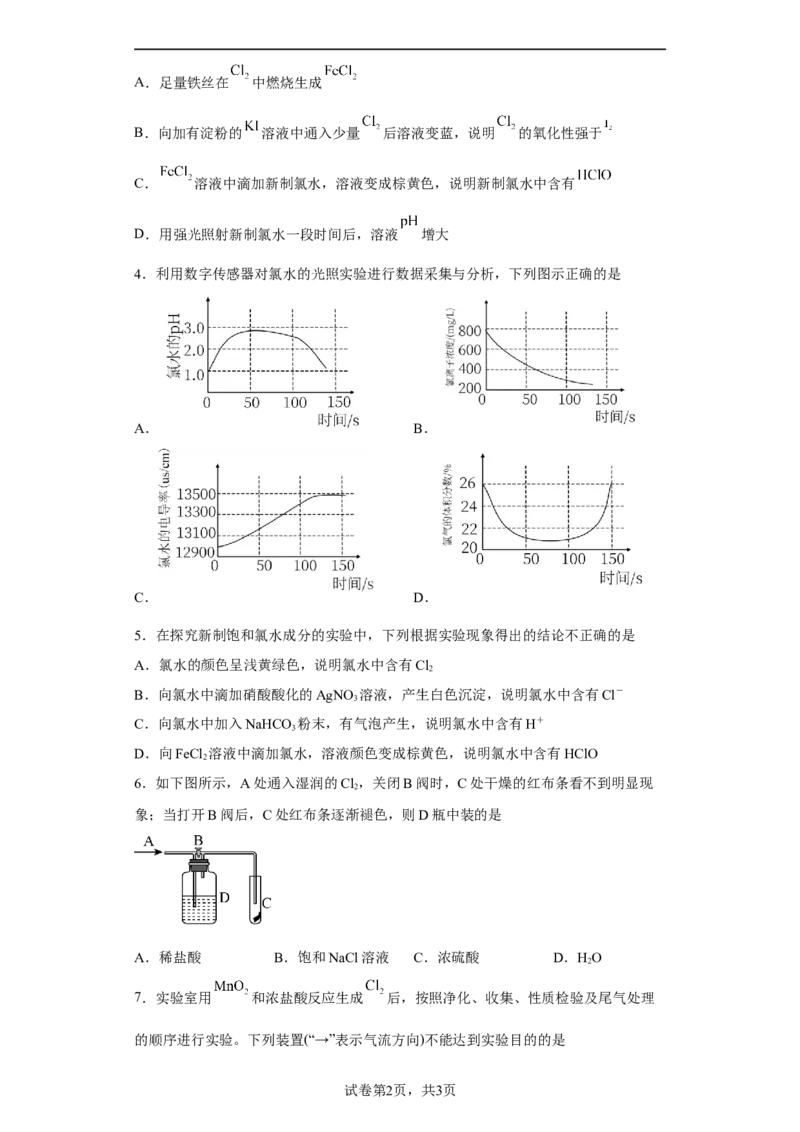
6.如下图所示,A处通入湿润的Cl,关闭B阀时,C处干燥的红布条看不到明显现
2
象;当打开B阀后,C处红布条逐渐褪色,则D瓶中装的是
A.稀盐酸 B.饱和NaCl溶液 C.浓硫酸 D.HO
2
7.实验室用 和浓盐酸反应生成 后,按照净化、收集、性质检验及尾气处理
的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是
试卷第2页,共3页A.A B.B C.C D.D
8.国家卫健委公布的新型冠状病毒肺炎诊疗方案指出,乙醚、75%乙醇、含氯消毒剂、
过氧乙酸(CHCOOOH)、氯仿等均可有效灭活病毒。对于上述化学药品,下列说法错
3
误的是
A.CHCHOH能与水互溶
3 2
B.NaClO通过氧化灭活病毒
C.过氧乙酸相对分子质量为76
D.氯仿的化学名称是四氯化碳
9.盐在生产、生活中有广泛应用。下列盐的性质与用途具有对应关系的是
A.NaClO有强氧化性,可用于消毒杀菌 B.NaHSO 有还原性,可用于漂白纸浆
3
C.NaCl易溶于水,可用于工业电解制备钠 D.NaHCO 受热易分解,可用于制抗酸
3
药物
10.化学在生活中有着广泛的应用,下列对应关系错误的是( )
化学性质 实际应用
A. Al (SO ) 和小苏打反应 泡沫灭火器灭火
2 4 3
B. 铁比铜金属性强 FeCl 腐蚀Cu刻制印刷电路板
3
C. 次氯酸盐具有氧化性 漂白粉漂白织物
D. HF与SiO 反应 氢氟酸在玻璃器皿上刻蚀标记
2
A.A B.B C.C D.D
11.有关氯元素,下列叙述正确的是
A.Cl 的化学性质活泼,与H 混合后会立即发生爆炸
2 2
B.光照下,新制氯水会产生气泡,该气体是Cl
2
C.若发生Cl 泄漏,应立即向高处转移
2
D.漂白粉比HClO稳定,可露置在空气中长期保存
12.在可能含有 、 的溶液中,要检验 是否存在,下列实验方法正确的是
A.取样,加 溶液,有白色沉淀生成,则有B.取样,加足量 溶液,过滤后再加 溶液,有白色沉淀,则有
C.取样,加入足量 溶液,过滤后再加 溶液,有白色沉淀,则有
D.取样,加入 和 混合溶液,有白色沉淀,则有
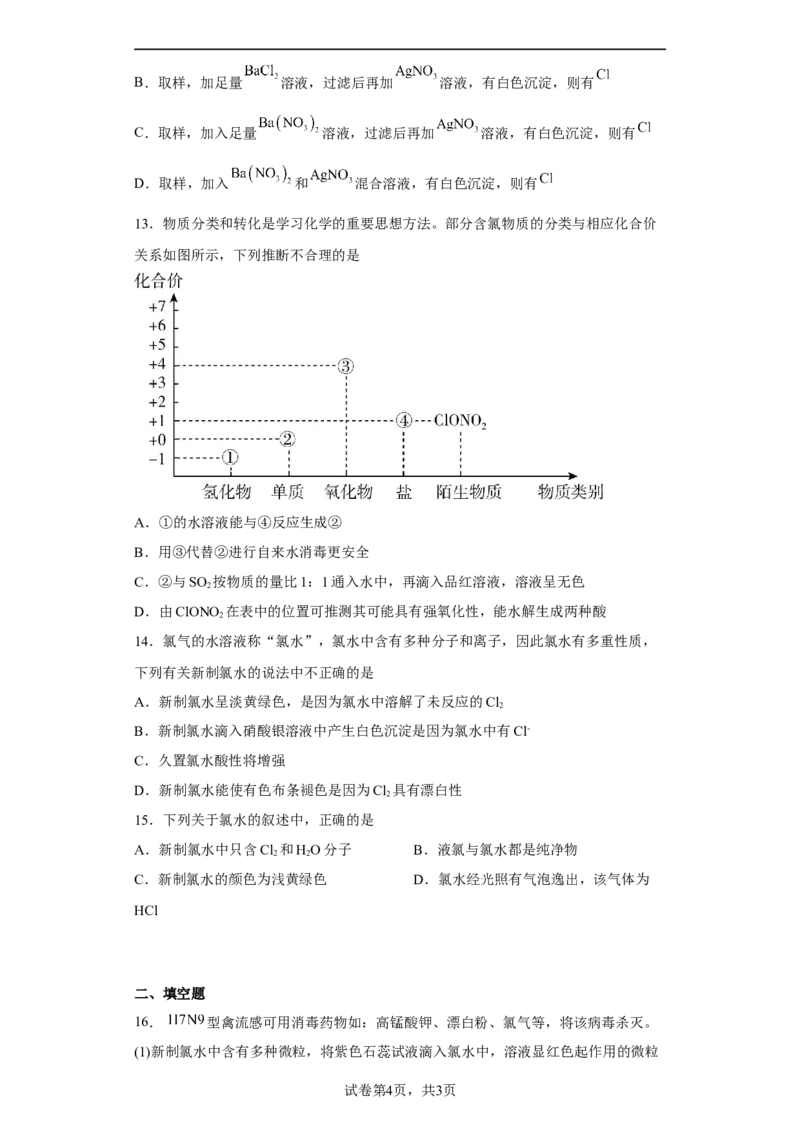
13.物质分类和转化是学习化学的重要思想方法。部分含氯物质的分类与相应化合价
关系如图所示,下列推断不合理的是
A.①的水溶液能与④反应生成②
B.用③代替②进行自来水消毒更安全
C.②与SO 按物质的量比1:1通入水中,再滴入品红溶液,溶液呈无色
2
D.由ClONO 在表中的位置可推测其可能具有强氧化性,能水解生成两种酸
2
14.氯气的水溶液称“氯水”,氯水中含有多种分子和离子,因此氯水有多重性质,
下列有关新制氯水的说法中不正确的是
A.新制氯水呈淡黄绿色,是因为氯水中溶解了未反应的Cl
2
B.新制氯水滴入硝酸银溶液中产生白色沉淀是因为氯水中有Cl-
C.久置氯水酸性将增强
D.新制氯水能使有色布条褪色是因为Cl 具有漂白性
2
15.下列关于氯水的叙述中,正确的是
A.新制氯水中只含Cl 和HO分子 B.液氯与氯水都是纯净物
2 2
C.新制氯水的颜色为浅黄绿色 D.氯水经光照有气泡逸出,该气体为
HCl
二、填空题
16. 型禽流感可用消毒药物如:高锰酸钾、漂白粉、氯气等,将该病毒杀灭。
(1)新制氯水中含有多种微粒,将紫色石蕊试液滴入氯水中,溶液显红色起作用的微粒
试卷第4页,共3页是___________(填化学符号,下同);过一会儿,溶液颜色逐渐褪去,起作用的微粒是
___________。
(2)工业上利用氯气和石灰乳反应制取漂白粉,漂白粉的有效成分为___________(填化
学式)。向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,写出发生反应的离子方程
式___________。
(3)已知高锰酸钾与浓盐酸混合能产生氯气,化学反应方程式为:
,回答下列问题:
①用双线桥标出电子转移的方向和数目_____。
②氧化性强弱: ____ 填“>”,“<”或“=”)。
③反应中氯化氢表现出的性质是___________。(填写字母)
a. 还原性 酸性 氧化性
④若生成标准状况下22.4 L 则转移电子总数是___________。
17.疫情防控期间,含氯消毒剂功不可没,研究消毒剂的性质意义重大。回答下列问
题。
(1)Cl 、HO、ClO (还原产物为Cl-)、84消毒液等物质常被用作消毒剂。等物质的量的
2 2 2 2
上述物质消毒效率最高的是_______(填序号)。
a.Cl b.H O c.ClO d.84消毒液
2 2 2 2
(2)工业上常通过反应KClO+HCl(浓)→KCl+C1 ↑+ 制备氯气,请补充完整并配平
3 2
该化学方程式______,反应中转移电子数为N 时,理论上生成标况下气体体积是
A
______L。
(3)如图是某品牌84消毒液包装上的有关使用说明。
①分析对金属制品有腐蚀作用的原因______。
②需密闭保存的原因______。洁厕灵的主要成分为浓盐酸,家庭室内切不可将两者混
合使用的原因(用离子方程式表示)______。实验室中可用NaClO与浓盐酸反应制取干
燥、纯净的C1 ,装置如图所示。
2上述仪器的连接顺序为: 接 接 接 ,_______,乙装置中盛放
的药品是_______。
18.2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。氯气、漂
白液、漂白粉都是生活中常用的含氯消毒剂。家庭中常常使用的消毒剂主要是“84”消
毒液,可以说化学让生活更美好。图为“84”消毒液说明书。请回答下列问题。
药品名称 84消毒液
主要成分 NaClO,有效氯含量50.00g/L~60.00g/L
注意事项 不可与其他洗涤剂或消毒液混合使用
说明书 稀释后浸泡或洗刷白色衣物,浴缸等1:200水溶
用法用量
液餐饮具,瓜果等1:100水溶液
(1)“84”消毒液的有效氯指的是每升含氯消毒剂的氧化能力(得失电子数)相当于多少克
Cl 的氧化能力(Cl均转化为Cl-)。若该“84”消毒液商品的有效氯按53.25g/L计算,该
2
消毒液的NaClO的物质的量浓度是_______。
(2)常温下用烧碱溶液吸收Cl 制备“84”消毒液。写出该反应的离子方程式_______,若
2
将Cl 通入热的烧碱溶液中,可以得到NaCl、NaClO和NaClO 的混合液。当混合液中
2 3
Cl-和ClO 的个数比为15∶2时,混合液中ClO-和ClO 的个数比为_______,从氧化还
原角度分析Cl 表现了______性。
2
(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要
急于用清水擦拭,要浸泡,这样效果会更好,原因是______(用离子方程式表达)。(已
知:酸性:HCO>HClO>HCO ),家庭消毒马桶时,不可在用洁厕灵(主要成分是盐
2 3
酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气体,其反应
的离子方程式是_______。
(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显。池水碱性过
强,杀毒作用会_______(填“增强”或“减弱”)。
试卷第6页,共3页(5)Cl 可直接用于杀菌消毒,但常常把氯气制成漂白粉、“84”消毒液,主要目的_____。
2
A.增强漂白能力和消毒作用
B.使它转化为较稳定物质,便于保存和运输
C.使它转化为较易溶于水的物质
D.提高氯的质量分数,有利于漂白、消毒
19. 与 的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。
回答下列问题:
(1)氯气的电子式为_______。
(2)氯气和氢氧化钠溶液制备漂白液的离子方程式为_______。
(3)某兴趣小组通过如下装置(夹持装置略)对 制备、吸收、释放和应用进行了研究。
已知:装置C中的药品可以吸收氯气
①打开B的活塞,A中发生反应生成 ,请将化学方程式配平_______
_______ _______ _______ _______ _______ _____
__ 。
②已吸收 气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放 的浓度随时间的变化如下
图所示。若将其用于水果保鲜,你认为效果较好的稳定剂是_______,原因是_______。③关闭B的活塞, 在D中被稳定剂完全吸收生成 ,在酸性条件下
可发生反应生成 并释放出 ,该反应的离子方程式为_______。
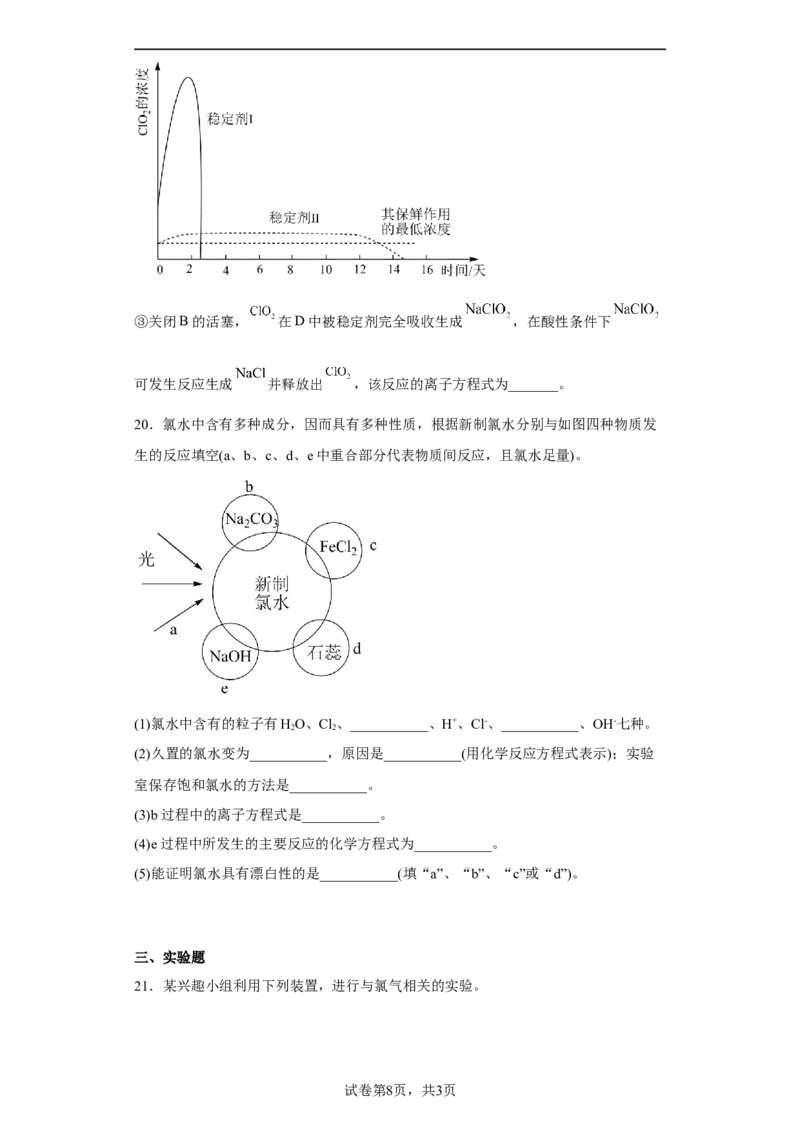
20.氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发
生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。
(1)氯水中含有的粒子有HO、Cl、___________、H+、Cl-、___________、OH-七种。
2 2
(2)久置的氯水变为___________,原因是___________(用化学反应方程式表示);实验
室保存饱和氯水的方法是___________。
(3)b过程中的离子方程式是___________。
(4)e过程中所发生的主要反应的化学方程式为___________。
(5)能证明氯水具有漂白性的是___________(填“a”、“b”、“c”或“d”)。
三、实验题
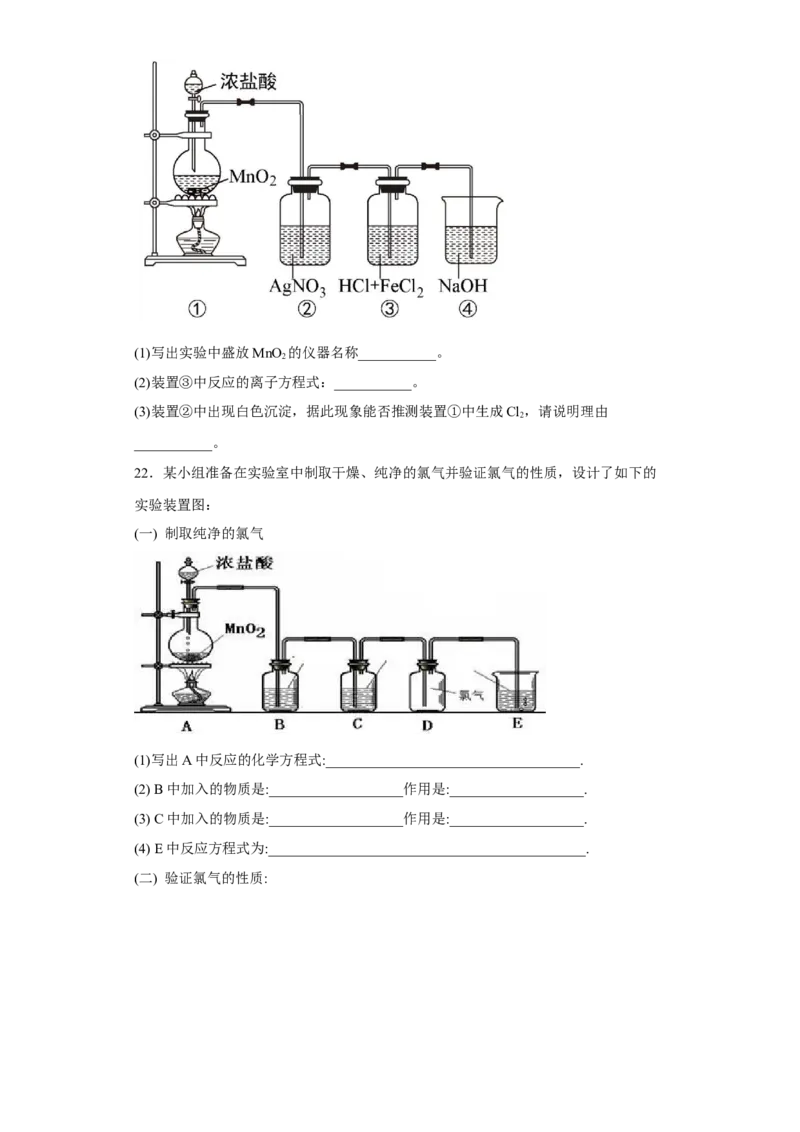
21.某兴趣小组利用下列装置,进行与氯气相关的实验。
试卷第8页,共3页(1)写出实验中盛放MnO 的仪器名称___________。
2
(2)装置③中反应的离子方程式:___________。
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl,请说明理由
2
___________。
22.某小组准备在实验室中制取干燥、纯净的氯气并验证氯气的性质,设计了如下的
实验装置图:
(一) 制取纯净的氯气
(1)写出A中反应的化学方程式:____________________________________.
(2) B中加入的物质是:___________________作用是:___________________.
(3) C中加入的物质是:___________________作用是:___________________.
(4) E中反应方程式为:_____________________________________________.
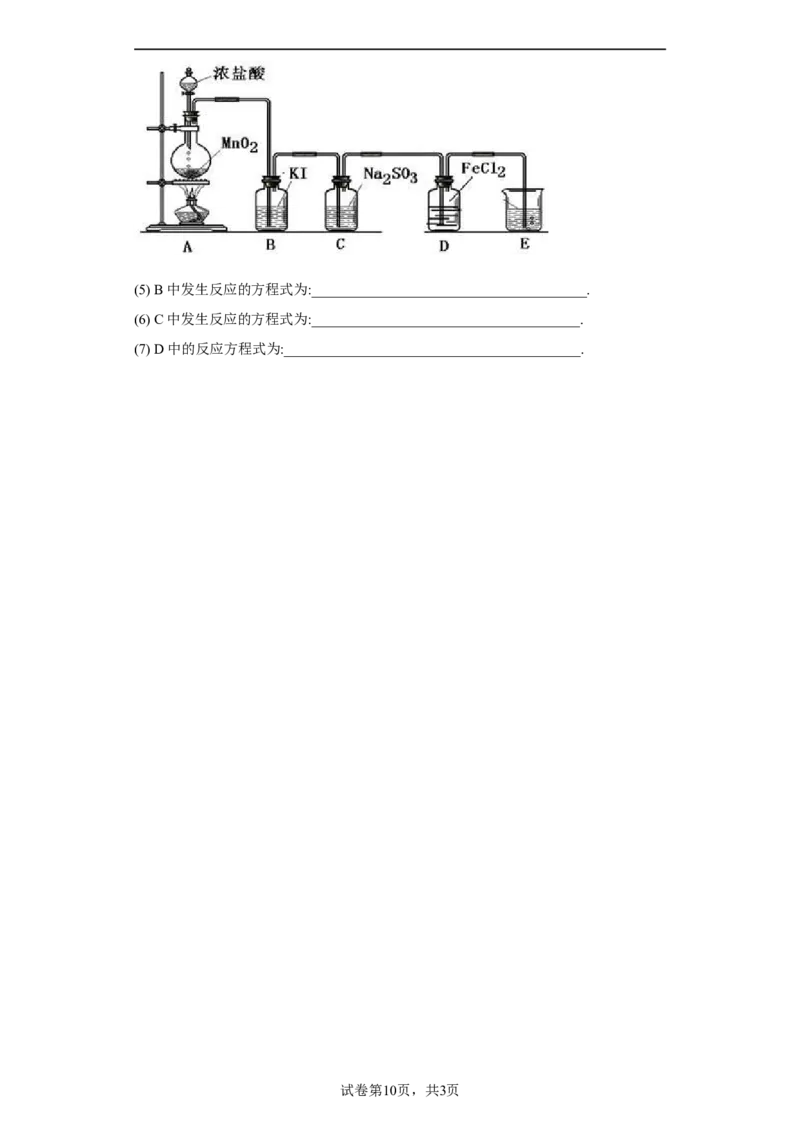
(二) 验证氯气的性质:(5) B中发生反应的方程式为:_______________________________________.
(6) C中发生反应的方程式为:______________________________________.
(7) D中的反应方程式为:__________________________________________.
试卷第10页,共3页参考答案:
1.A
【详解】A.该反应中只有碘元素价态升高,由0价升高至KH(IO) 中+5价,每个碘原子
3 2
升高5价,即6I 60e-,又因方程式中6I 3Cl,故3Cl 60e-,即Cl 20e-,所以产生
2 2 2 2 2
22.4L (标准状况) Cl 即1mol Cl 时,反应中应转移20 mol e-,A错误;
2 2
B.该反应中KClO 中氯元素价态降低,KClO 作氧化剂,I 中碘元素价态升高,I 作还原
3 3 2 2
剂,由该方程式的计量系数可知,11KClO 6I,故该反应的氧化剂和还原剂的物质的量
3 2
之比为11:6,B正确;
C.漂白粉的有效成分是次氯酸钙,工业制漂白粉可用石灰乳与氯气反应,C正确;
D.食盐中 可先与酸化的淀粉碘化钾溶液中的H+、I-发生归中反应
生成I,I 再与淀粉发生特征反应变为蓝色,故可用酸化的淀粉碘
2 2
化钾溶液检验食盐中 的存在,D正确。
故选A。
2.C
【详解】A、盐的水解反应是吸热反应,所以升高温度,促进盐的水解,溶液的碱性更强。
因此用热的纯碱溶液可以洗去油污。并不是碳酸钠可与油污直接反应。错误。
B、漂白粉在空气中久置变质,是因为有效成分Ca(ClO) 会发生反应产生的HClO不稳定,
2
光照分解产生HCl和氧气,错误;
C、当施肥时草木灰(有效成分为KCO)与NH Cl混合使用,则二者的水解作用相互促
2 3 4
进,使N元素以氨气的形式逸出因而肥效会降低。正确;
D、FeCl 溶液可用于铜质印刷线路板的制作,是因为二者发生反应生成氯化亚铁和氯化铜,
3
把多余的Cu腐蚀掉。错误。
答案选C。
3.B
【详解】A. 足量铁丝在 中燃烧生成 ,故A错误;
B. 氧化剂的氧化性大于氧化产物,向加有淀粉的 溶液中通入少量 后溶液变蓝,说明 的氧化性强于 ,故B正确;
C. 溶液中滴加新制氯水,溶液变成棕黄色,氧化FeCl 的主要是Cl,不能说明
2 2
HClO的生成,故C错误;
D. 用强光照射新制氯水一段时间后,氯水最终生成盐酸,pH减小,故D错误;
故选B。
4.C
【详解】A.氯水的光照,次氯酸光照分解生成盐酸和氧气,酸性增强,pH应逐渐减小,
故A错误;
B.氯水的光照,次氯酸光照分解生成盐酸和氧气,氯离子浓度增大,故B错误;
C.氯水的光照,次氯酸是弱酸,次氯酸光照分解生成盐酸和氧气,盐酸是强电解质,因
此电导率增大,故C正确;
D.氯水的光照,次氯酸光照分解生成盐酸和氧气,氧气体积逐渐增大,故D错误。
综上所述,答案为C。
5.D
【详解】A、氯气是黄绿色气体,因此氯水的颜色呈浅绿色,说明氯水中含有Cl,A正确;
2
B、向氯水中滴加硝酸酸化的AgNO 溶液,产生白色沉淀,白色沉淀是氯化银,这说明氯
3
水中含有Cl-,B正确;
C、向氯水中加入NaHCO 粉末,有气泡产生,气体是CO,这说明氯水中含有H+,C正
3 2
确;
D、向FeCl 溶液中滴加氯水,溶液颜色变成棕黄色,说明反应中有氯化铁生成。由于氯气
2
也能把氯化亚铁氧化生成氯化铁,因此不能说明氯水中含有HClO,D不正确。
答案选D。
6.C
【分析】Cl 没有漂白性,Cl 与水反应生成的HClO具有漂白性,打开B阀后,湿润的Cl
2 2 2
能使C处红布条褪色;
【详解】A.若D瓶中装的是稀盐酸,关闭B阀时,湿润的Cl 经过D瓶,导入C处的仍
2
是湿润的Cl,则C处干燥的红布条会褪色,A不符合题意;
2
B.若D瓶中装的是饱和NaCl溶液,关闭B阀时,湿润的Cl 经过D瓶,导入C处的仍是
2
湿润的Cl,则C处干燥的红布条会褪色,B不符合题意;
2
C.若D瓶中装的是浓硫酸,关闭B阀时,湿润的Cl 经过D瓶,氯气被浓硫酸干燥,导入
2
答案第2页,共2页C处的是干燥的Cl,Cl 没有漂白性,C处干燥的红布条不会褪色,C符合题意;
2 2
D.若D瓶中装的是HO,关闭B阀时,湿润的Cl 经过D瓶,导入C处的仍是湿润的
2 2
Cl,则C处干燥的红布条会褪色,D不符合题意;
2
答案选C。
7.D
【详解】A.浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl 可用
2
浓硫酸干燥,A装置能达到实验目的,故A不符合题意;
B.氯气的密度大于空气,用向上排空气法收集,B装置能收集氯气,故B不符合题意;
C.湿润的红布条褪色,干燥的红色布条不褪色,可验证干燥的氯气不具有漂白性,故C
不符合题意;
D.氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,D装置不能达到实验目的,故D
符合题意;
答案选D。
8.D
【详解】A.乙醇分子中有羟基,其与水分子间可以形成氢键,因此乙醇能与水互溶,A说
法正确;
B.次氯酸钠具有强氧化性,其能使蛋白质变性,故其能通过氧化灭活病毒,B说法正确;
C.过氧乙酸的分子式为C HO,故其相对分子质量为76,C说法正确;
2 4 3
D.氯仿的化学名称为三氯甲烷,D说法不正确。
综上所述,故选D。
9.A
【详解】A.NaClO有氧化性,可用于消毒杀菌,消毒杀菌就是利用了NaClO的强氧化性,
A正确;
B.漂白纸浆是利用SO 的漂白性,B错误;
2
C.工业电解熔融的氯化钠来制备金属钠,与氯化钠是否易溶于水无关,C错误;
D.NaHCO 可用于制抗酸药物,是利用了其能和酸反应生成CO,与NaHCO 受热易分解
3 2 3
无关,D错误;
故选A。
10.B
【详解】A、硫酸铝和碳酸氢钠发生反应生成氢氧化铝沉淀、硫酸钠和二氧化碳,能灭火,故说法正确;
B、氯化铁和铜反应生成氯化亚铁和氯化铜,说明铜的还原性强于亚铁离子,不能说明铁
的金属性比铜强,故说法错误;
C、次氯酸具有强氧化性,能漂白,故说法正确;
D、氟化氢和二氧化硅反应生成四氟化硅和水,可以刻蚀玻璃,故说法正确。
故选B。
【点睛】盐类水解在生活中涉及方方面面,如泡沫灭火器、明矾净水等等,泡沫灭火剂原
理就是盐类水解:Al3++3HCO -=Al(OH) ↓+3CO↑。比较金属性的强弱,可以通过置换反
3 3 2
应,利用金属性强的制取置换性弱的,如Fe+Cu2+=Fe2++Cu,说明Fe比Cu金属性强。
11.C
【详解】A.氯气和氢气在光照条件下混合才会产生爆炸,纯净的氯气与氢气点燃时可以
安静的燃烧,故A错误;
B.新制氯水中有HClO,次氯酸光照条件下分解生成盐酸和氧气,故B错误;
C.氯气有毒且密度比空气的大,因此若氯气发生泄漏,应立即用湿毛巾捂住口鼻,并向
高处转移,故C正确;
D.漂白粉不可露置在空气中, ,
,故D错误;
故选C。
12.C
【分析】一般情况下,检验 需要用 溶液和 溶液,但是 的存在会干扰
的检验,所以先用 除去,再检验 ;此时已经没有其他的干扰离子,所以可以省
略 溶液;
【详解】A.直接加入 溶液,生成的白色沉淀可能是 ,也可能是 ,无
法确定是否含有 ,A错误;
答案第4页,共2页B.加足量 溶液,虽然可以除去 ,但是同时也加入了 ,干扰检验,B错误;
C.先加足量 溶液,可除去 ,从而排除 的干扰,过滤后再加 溶
液,产生了白色沉淀,可表明溶液中含有 ,C正确;
D.加入 和 混合溶液,可能生成 、 、 白色沉淀,无
法确定是否含有 ,D错误;
故合理选项为C。
13.C
【分析】由图可知,①是Cl元素-1价的氢化物,则①为HCl,②为Cl元素的单质,则②为
Cl,③为Cl元素+4价的氧化物,则③为ClO ,④为次氯酸盐。
2 2
【详解】A.盐酸和次氯酸钠可以发生反应2HCl+NaClO=Cl ↑+NaCl+HO,生成氯气,故
2 2
A正确;
B. Cl 有毒,ClO 氧化性更强,用ClO 代替Cl 进行自来水消毒程度高且无污染,更安全,
2 2 2 2
故B正确;
C.Cl 与SO 按物质的量比1:1通入水中发生反应Cl+SO+2H O=HSO +2HCl,再滴入品
2 2 2 2 2 2 4
红溶液,品红不会褪色,溶液呈红色,故C错误;
D. ClONO 中Cl为+1价、N为+5价,O为-2价,+1价的Cl和+5价的N都有强氧化性,
2
所以ClONO 具有强氧化性,ClONO 水解可生成硝酸和次氯酸,故D正确;
2 2
答案选C。
14.D
【分析】氯水中含有三分子(HO、Cl、HClO)、四离子(H+、Cl-、ClO-、OH-),因此
2 2
氯水具有漂白性(HClO)、强氧化性(HClO、Cl)、酸性(HCl),久置的氯水中,
2
HClO分解生成HCl和O,HCl溶于水形成盐酸,氯水酸性增强。据此解答。
2
【详解】A.新制氯水中,部分氯气与水反应生成盐酸和次氯酸。未反应完的氯气溶解在
水中,使氯水呈淡黄绿色,故A项正确;
B.新制氯水中存在HCl分子,向新制氯水中滴入硝酸银溶液,Ag+与Cl-反应产生白色沉,
故B项正确;
C.氯水久置后,氯水中的次氯酸分解生成氧气和HCl气体,HCl溶于水形成盐酸,溶液酸性增强,故C项正确;
D.新制氯水能使有色布条褪色,是因为氯气与水反应生成的HClO具有漂白性,故D项
错误。
故答案为:D。
15.C
【详解】A.新制的氯水因其含Cl 而呈淡绿色,其中还含有HClO和HO分子,故A错误;
2 2
B.液氯是纯净物,氯水是混合物,故B错误;
C.新制的氯水因其含Cl 而呈淡绿色,故C正确;
2
D.氯水由于其中的HClO见光易分解:2HClO 2HCl+O↑,所以氯水经光照有O 气
2 2
泡逸出,故D错误。
故选C。
16.(1) H+ HClO
(2) Ca(ClO) Ca2++CO =CaCO ↓
2 3
(3)
> ab 2N
A
【解析】(1)
氯气和水反应生成盐酸和次氯酸,盐酸和次氯酸电离出氢离子而使溶液呈酸性,氢离子能
使紫色石蕊变红色;次氯酸具有漂白性,所以能使溶液褪色的是HClO;
(2)
氯气与氢氧化钙反应制备漂白粉,则漂白粉的主要成分为CaCl 、Ca(ClO) ,有效成分为
2 2
Ca(ClO) ;向漂白粉清液中滴加碳酸钠溶液,有白色沉淀生成,是碳酸钠和溶液中钙离子
2
反应生成碳酸钙沉淀,反应的离子方程式为Ca2++CO =CaCO ;
3
答案第6页,共2页(3)
①高锰酸钾中锰元素由+7价变成+2价,盐酸中氯元素由-1价变成0价,所以双线桥为
;
②实验室用二氧化锰和浓盐酸在加热的情况下生成氯气,而题干中反应制备氯气不需要加
热,故高锰酸钾的氧化性大于二氧化锰;
③反应前后盐酸的化合价-1价升高为0价,化合价升高表现为还原性,反应前后化合价不
变表现为酸性,故选ab;
④由双线桥可知,生成5mol Cl 时,转移10 mol电子,所以生成标准状况下22.4 L Cl,对
2 2
应1mol Cl 时,转移2mol电子,故转移电子总数是2N 。
2 A
17. c KClO+6HCl(浓)=KCl+3C1 ↑+3H O 13.44 NaClO有强氧化性,而
3 2 2
一般金属具有强还原性 消毒液的有效成分NaClO能与空气中的CO 作用,使其
2
变质 ClO-+Cl-+2H+=Cl↑+H O acbe 饱和食盐水
2 2
【分析】(2)根据化合价不交叉的原则,KClO 中+5价的氯元素降为0价,HCl中氯元素升
3
为0价,氯化钾中的氯元素来自盐酸,所以KClO 是氧化剂、部分HCl是还原剂,
3
(3)84消毒液主要成分是NaClO,具有氧化性,能与还原性的金属单质反应,不能与洁厕灵
混合使用,否则会产生有毒气体氯气,制取的氯气中含氯化氢杂质气体,经过装置乙中的
饱和食盐水洗气后,再经过浓硫酸干燥。
【详解】(1)1mol Cl 、HO、ClO 、84消毒液(NaClO)分别消毒时,转移电子依次为
2 2 2 2
2mol、2mol、5mol、2mol,等物质的量的上述物质反应,ClO 转移的电子数最多,消毒效
2
率最高。
(2)根据化合价不交叉的原则,在KClO+HCl→KCl+Cl ↑的反应中,KClO 中+5价的氯元素
3 2 3
降为0价,该氯原子为被还原的氯原子,HCl中氯元素升为0价,该氯原子为被氧化的氯
原子,氯化钾中的氯元素来自盐酸,则被氧化发生氧化反应的Cl为5,只具有酸性的Cl为
1,则HCl前配6,KClO 前配1,再根据原子守恒配平方程式为:
3
KClO+6HCl=KCl+3Cl ↑+3H O,反应中转移5mol电子生成3mol氯气,则转移1mol电子时,
3 2 2
产生标准状况下的Cl 为0.6mol,其体积为13.44 L;
2
(3)①NaClO具有漂白作用,利用了NaClO的氧化性,而金属具有还原性,发生了氧化还原反应,对金属腐蚀;
②消毒液有效成分是次氯酸盐与二氧化碳和水生成了次氯酸,次氯酸不稳定,见光分解,
所以应该密封保存;次氯酸根离子与氯离子发生氧化还原反应生成氯气和水,离子方程式:
Cl-+ClO-+2H+=Cl↑+H O;
2 2
用甲装置制取氯气,用乙除去氯气中的氯化氢气体,用丙吸收水蒸气,仪器的连接顺序为:
acbe,乙装置中盛放的药品是:饱和食盐水。
18. 0.75mol/L Cl +2OH-=Cl-+ClO-+H O 5∶2 氧化性和还原性
2 2
ClO-+CO +H O=HClO+ HCO ClO-+ Cl-+ 2H+= Cl ↑+H O 减弱 BC
2 2 2 2
【详解】
(1) Cl元素转化为Cl-时,1molNaClO和Cl 均得到2mol电子,说明二者物质的量相等,若
2
该“84”消毒液商品的有效氯按53.25g/L计算,设溶液的体积为1L,则Cl 的物质的量为:
2
=0.75mol,该消毒液中NaClO的物质的量浓度是: =0.75mol/L;
(2)常温下用烧碱溶液吸收Cl 制备“84”消毒液时,反应生成氯化钠、次氯酸钠和水,离子
2
方程式为:Cl+2OH-=Cl-+ClO-+H O;若将Cl 通入热的烧碱溶液中,可以得到NaCl、
2 2 2
NaClO和NaClO 的混合液,当混合液中Cl-和ClO 的个数比为15∶2时,设Cl-和ClO 的个
3
数分别为:15、2,生成15个Cl-时得到15个电子,生成2个ClO 时失去10个电子,当生
成1个ClO-时失去1个电子,根据得失电子守恒,生成ClO-的个数为5个,则混合液中
ClO-和ClO 的个数比为5∶2;在该反应中,氯元素的化合价既升高又降低,Cl 既表现了氧
2
化性又表现了还原性;
(3)家庭用“84”消毒液用法强调,做家庭物品消毒时,要做适当的稀释,喷洒后也不要急
于用清水擦拭,要浸泡,这样效果会更好,原因是酸性:HCO>HClO>HCO ,NaClO溶
2 3
液可以和空气中的二氧化碳充分反应生成碳酸氢钠和HClO,HClO具有强氧化性,可以消
答案第8页,共2页毒杀菌,离子方程式为:ClO-+CO +H O=HClO+ HCO ;家庭消毒马桶时,不可在用洁厕
2 2
灵(主要成分是盐酸)清洗马桶后,立刻使用“84”消毒液消毒,否则会产生黄绿色的有毒气
体,反应的离子方程式是:ClO-+ Cl-+ 2H+= Cl ↑+H O;
2 2
(4)游泳池水的消毒多用漂粉精,但酸碱性对漂粉精的消毒效果影响明显,酸性较强时,
ClO-与H+结合生成更多的HClO,增强消毒效果,相反,池水碱性过强时,溶液中的HClO
浓度过低,杀毒作用会减弱;
(5)A.把氯气制成漂白粉、“84”消毒液,不能增强漂白能力和消毒作用,故A错误;
B.氯气是气体,不便于保存和运输,把氯气制成漂白粉、“84”消毒液,使它转化为较稳
定物质,便于保存和运输,故B正确;
C.氯气在水中的溶解度小,把氯气制成漂白粉、“84”消毒液,使它转化为较易溶于水的
物质,故C正确;
D.把氯气制成漂白粉、“84”消毒液,不能提高氯的质量分数,故D错误;
答案选:BC。
19.
稳定剂Ⅱ 原因是可以
缓慢释放ClO ,能较长时间维持保鲜所需的浓度
2
【详解】(1)氯气是共价分子、分子内氯原子间共用一对电子对,电子式为 。
(2)氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,则制备漂白液的离子方程式为
。
(3)①盐酸和氯酸钠溶液发生氧化还原反应,氯酸钠中氯化合价从+5降低到+4生成 ,
部分盐酸中氯化合价从-1升高到0生成 ,按得失电子数守恒、元素质量守恒,可配平得化学方程式为 。②由图知:用于水果保鲜
效果较好的是稳定剂Ⅱ,原因是可以缓慢释放ClO ,能较长时间维持保鲜所需的浓度。③
2
在酸性条件下 可发生反应,部分 中氯化合价从+3降低到-1生成 ,部
分 中氯化合价从+3升高到+4生成 ,按得失电子数守恒、元素质量守恒,可配
平得该反应的离子方程式为 。
20.(1) HClO
(2) 稀HCl 在阴凉处置于棕色试剂瓶中密封保存
(3)
(4) (或 或
)
(5)d
【分析】Cl
2
+H
2
O⇌HCl+HClO是一个可逆反应,盐酸是强酸,次氯酸是弱酸,所以氯水中
含有三种分子:HO、Cl、HClO及四种离子:H+、OH-、Cl-、ClO-;次氯酸具有强氧化性,
2 2
还具有漂白性,还具有不稳定性,见光易分解。
(1)
Cl
2
+H
2
O⇌HCl+HClO是一个可逆反应,盐酸是强酸,次氯酸是弱酸,所以氯水中含有三种
分子:HO、Cl、HClO及四种离子:H+、OH-、Cl-、ClO-;答案为HClO ClO-
2 2
(2)
氯水中含有的HClO见光容易分解生成HCl和O,从而导致氯水最后会全部变为盐酸,故
2
必须盛放在棕色的细口瓶中并放置在阴凉处。答案为稀HCl 在阴凉
答案第10页,共2页处置于棕色试剂瓶中密封保存
(3)
碳酸钠和氯水反应,主要是和盐酸反应生成氯化钠、二氧化碳和水,离子方程式为
故答案为
(4)
氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应方程式为
故答案为
(5)
氯水中的HClO有强氧化性,一般在应用其漂白时,HClO的强氧化性将有色物质氧化成无
色物质,本题中氯水能使石蕊试液先变红,后褪色,故d符合题意,答案为d。
21. 圆底烧瓶 2Fe2++Cl=2Fe3++2Cl- 不能说明,因为浓盐酸挥发出来
2
的氯化氢也会和硝酸银反应,也会产生白色沉淀
【分析】实验室通过加热MnO 和浓盐酸来制备氯气,MnO +4HCl(浓)
2 2
MnCl +Cl↑+2H O,由于浓盐酸会挥发产生HCl气体,生成的氯气中混有氯化氢,Cl 通入
2 2 2 2
硝酸银溶液中会生成白色沉淀,通入③中可以氧化二价铁,Cl 可与NaOH溶液反应,常用
2
NaOH溶液来吸收Cl,防止污染空气,以此解答。
2
【详解】(1)实验中盛放MnO 的仪器名称是圆底烧瓶,故答案为:圆底烧瓶;
2
(2)装置③中氯气把二价铁氧化为三价铁,离子方程式为:2Fe2++Cl=2Fe3++2Cl-,故答案为:
2
2Fe2++Cl=2Fe3++2Cl-;
2
(3)由于浓盐酸会挥发产生HCl气体,HCl气体可以和AgNO 溶液反应产生AgCl白色沉淀,
3
HCl+AgNO =AgCl↓+HNO ,不能说明是Cl 与AgNO 溶液发生了反应。故答案为:不能说
3 3 2 3
明,因为浓盐酸挥发出来的氯化氢也会和硝酸银反应,也会产生白色沉淀。
22. MnO + 4HCl =MnCl +Cl+ H O 饱和食盐水 除去Cl 中混有的
2 2 2 2 2
HCl气体 浓硫酸 干燥Cl 2NaOH + Cl = NaCl+ NaClO +H O
2 2 2
Cl+2KI =2KCl + I Cl +Na SO + H O = Na SO + 2HCl 2FeCl +Cl=2FeCl
2 2 2 2 3 2 2 4 2 2 3
【分析】(一)(1)根据浓盐酸和二氧化锰的性质判断生成物,从而写出反应方程式;
(2)根据混合气体的成分及氯气、氯化氢的性质分析;(3)根据杂质的成分及性质分析;
(4)根据氯气的性质分析;
(二)根据氯气的性质分析。
【详解】(一)(1)浓盐酸有还原性,二氧化锰有氧化性,浓盐酸和二氧化锰能发生氧化还原
反应生成氯化锰、氯气和水,发生反应的化学方程式为MnO +4HCl(浓)
2
MnCl +Cl↑+2H O;
2 2 2
(2)浓盐酸有挥发性,浓盐酸中的水在加热条件下变成水蒸气,所以氯气中混有氯化氢和水
蒸气;氯化氢极易溶于水,氯气能溶于水,且与水反应,Cl+H O=H++Cl-+HClO,食盐水
2 2
溶液中的氯离子抑制氯气的溶解,降低氯气的溶解度,所以可用饱和的食盐水除去HCl气
体;
(3)浓硫酸有吸水性,且不和氯气反应,所以可用浓硫酸干燥氯气;
(4)氯气有毒,污染环境,所以不能直接排空;氯气能和氢氧化钠反应生成氯化钠、次氯酸
钠和水,所以可用氢氧化钠溶液吸收多余的氯气,发生反应的化学方程式为2NaOH+Cl
2
=NaCl+NaClO+H O;
2
(二)(5)氯气有氧化性,能置换出碘化钾中的碘,发生反应的化学方程式为
Cl+2KI=2KCl+I ;
2 2
(6)氯气有氧化性,能把亚硫酸钠中的硫元素氧化成最高价,本身被还原成-1价,发生反应
的化学方程式为Cl+Na SO +H O=Na SO +2HCl;
2 2 3 2 2 4
(7)氯气有氧化性,能把变价金属离子氧化成最高价,本身被还原成-1价,发生反应的化学
方程式为2FeCl +Cl=2FeCl 。
2 2 3
答案第12页,共2页