文档内容
赣州中学 2024-2025 学年高一下学期开学考试
化学试题
可能用到的原子量:H 1 D 2 B 11 O 16 Fe 56 Cl 35.5 S 32 Ba 137
一、选择题:(每小题3分;共42分)
1. 近年来,我国科技成果显著。下列成果所涉及的材料不属于金属材料的是
A. 神舟十九号的耐高温材料——铼合金
B. 超导量子计算机“本源悟空”的芯片材料——铝、铜和铌等
C. 国产大飞机C919发动机的涂层材料——氮化硅
D. 首艘大型邮轮“爱达·魔都号”上层建筑材料——铝合金
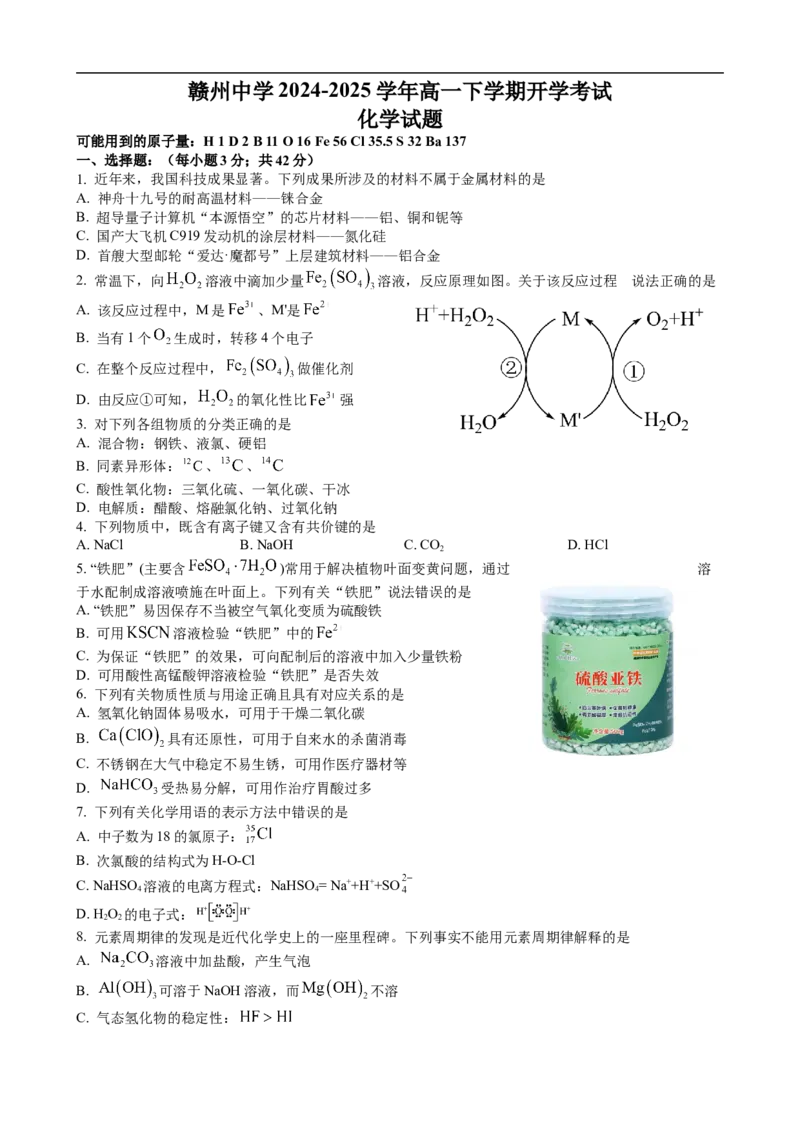
2. 常温下,向 溶液中滴加少量 溶液,反应原理如图。关于该反应过程 的说法正确的是
A. 该反应过程中,M是 、M'是
B. 当有1个 生成时,转移4个电子
C. 在整个反应过程中, 做催化剂
D. 由反应①可知, 的氧化性比 强
3. 对下列各组物质的分类正确的是
A. 混合物:钢铁、液氯、硬铝
B. 同素异形体: 、 、
C. 酸性氧化物:三氧化硫、一氧化碳、干冰
D. 电解质:醋酸、熔融氯化钠、过氧化钠
4. 下列物质中,既含有离子键又含有共价键的是
A. NaCl B. NaOH C. CO D. HCl
2
5. “铁肥”(主要含 )常用于解决植物叶面变黄问题,通过 溶
于水配制成溶液喷施在叶面上。下列有关“铁肥”说法错误的是
A. “铁肥”易因保存不当被空气氧化变质为硫酸铁
B. 可用 溶液检验“铁肥”中的
C. 为保证“铁肥”的效果,可向配制后的溶液中加入少量铁粉
D. 可用酸性高锰酸钾溶液检验“铁肥”是否失效
6. 下列有关物质性质与用途正确且具有对应关系的是
A. 氢氧化钠固体易吸水,可用于干燥二氧化碳
B. 具有还原性,可用于自来水的杀菌消毒
C. 不锈钢在大气中稳定不易生锈,可用作医疗器材等
D. 受热易分解,可用作治疗胃酸过多
7. 下列有关化学用语的表示方法中错误的是
A. 中子数为18的氯原子:
B. 次氯酸的结构式为H-O-Cl
C. NaHSO 溶液的电离方程式:NaHSO= Na++H++SO
4 4
D. H O 的电子式:
2 2
8. 元素周期律的发现是近代化学史上的一座里程碑。下列事实不能用元素周期律解释的是
A. 溶液中加盐酸,产生气泡
B. 可溶于NaOH溶液,而 不溶
C. 气态氢化物的稳定性:D. 从NaBr溶液中置换出
9. 近年来我国航空航天事业取得了很多令世界瞩目的成就。下列说法错误的是
A. 当光束通过空间站热控材料使用的纳米气凝胶时,可以观察到丁达尔效应
B. 由于 碱性强于 ,载人飞船中常用 固体吸收空气中的
C. 钛密度小、耐高温、耐腐蚀,适用于制造火箭发动机壳体、人造卫星壳体
D. 过氧化钠可与水及二氧化碳发生反应生成氧气,常用作航天飞船的供氧剂
10. 配制0.1mol/L的NaOH溶液,下列哪些操作会使实验结果偏高
A. 用滤纸称量NaOH固体 B. 移液前容量瓶内有水珠
C. 摇匀后,液面低于刻度线,再加水至刻度线 D. 定容时,俯视刻度线
11. 下面关于钠及其化合物的描述错误的是
A. 钠单质具有很强的还原性
B. 碳酸氢钠中加入少量水伴随着吸热现象
C. 实验室金属钠需要保存在煤油或石蜡油中
D. 常温下钠在空气中会被氧化为淡黄色固体
12. 下列离子组在指定条件下的溶液中,一定能大量共存的是
A. 含有大量 的溶液:
B. 澄清透明溶液中:
C. 加入 固体的溶液中:
D. 在能溶解 的溶液中:
13. 已知 是阿伏加德罗常数的值,下列说法正确的是
A. 的 中,含有 个中子
B. 和 中含有的质子数均为
C. 与足量水蒸气反应,转移的电子数为
D. 常温常压下, 含共价键数为
14. 短周期主族元素X、Y、Z、W的原子序数依次增大,Y在短周期中原子半径最大,Z是地壳中含量最
高的金属元素,X和W同主族,W的最高正化合价与最低负化合价的代数和为4。下列说法错误的是
A. 简单气态氢化物的稳定性:
B. 原子半径由小到大的顺序:
C. Y、Z、W三元素最高价氧化物对应水化物两两之间均可发生反应
D. X与Y形成的化合物中可能既含离子键,又含共价键
二、填空题:(共58分)
15. (每空2分,共16分)铁和铝是两种重要的金属,它们的单质及其化合物有着各自的性质。
(1)现配制100mL 0.01mol∙L-1 FeCl 溶液,配制过程中需要的玻璃仪器除量筒、胶头滴管、烧杯外,
3
还需要 。
(2)将FeCl 溶液滴入沸水可得到红褐色液体,反应的离子方程式是 。此液体具有的性
3
质是 (填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b. 将该液体进行过滤,可得到红褐色固体
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)在隔绝空气的条件下,用镁条引燃Fe O 粉末和铝粉的均匀混合物,使其充分反应。向充分反应后
3 4
的剩余固体中加入足量的NaOH溶液,有大量气泡产生,所得剩余固体中除铁外还含有的固体物质是
(填化学式)。写出以上过程中涉及到的化学反应方程式,如果是离子反应,用离子反应方程式表示
。(4)“细菌冶金”是利用某些细菌的特殊代谢功能开采金属矿石,例如溶液中氧化亚铁硫杆菌能利用空
气中的氧气将黄铁矿(主要成分FeS)氧化为Fe (SO ),并使溶液酸性增强。
2 2 4 3
①该过程反应的化学方程式为 。
②人们可利用Fe (SO ) 作强氧化剂溶解铜矿石(Cu S),然后加入铁屑进一步得到铜,该过程中发生
2 4 3 2
的离子反应方程式如下,请补充完整并配平:
Cu S+ Fe3++ HO Cu2++ Fe2++ ( )+ SO 2- 。
2 2 4
(5)羟胺(NH OH)是一种还原剂,用25.00 mL 0.049 mol/L羟胺的酸性溶液跟足量的硫酸铁溶液在
2
煮沸条件下反应,生成的Fe2+离子恰好与24.5 mL 0.020 mol/L的KMnO 酸性溶液反应。则在上述反应
4
中,羟胺的氧化产物是 。
16.(每空2分,共16分)研究工业废弃物的处理和防治具有重要的意义。
(1)利用反应CH+2NO N+CO +2H O可消除NO 的污染,该反应中氧化剂是 ,当消耗CH 的
4 2 2 2 2 2 4
体积是11.2 L(标准状况下)时,理论上可处理 molNO 。
2
(2)治理汽车尾气中CO和NO的一种方法是:在汽车排气管中安装一个催化转化装置,该装置能将CO和
NO转化为参与大气循环的无毒气体。该反应的化学方程式为 .
(3)某无色废水中可能含有Fe3+、Al3+、Na+、Cl-、OH-、SO 2-、中的几种离子。分别取三份废水进行如
4
下实验:
I.进行焰色反应实验,火焰为无色。
Ⅱ.取100 mL废水,加入足量的BaCl 溶液,生成2.33g白色沉淀。
2
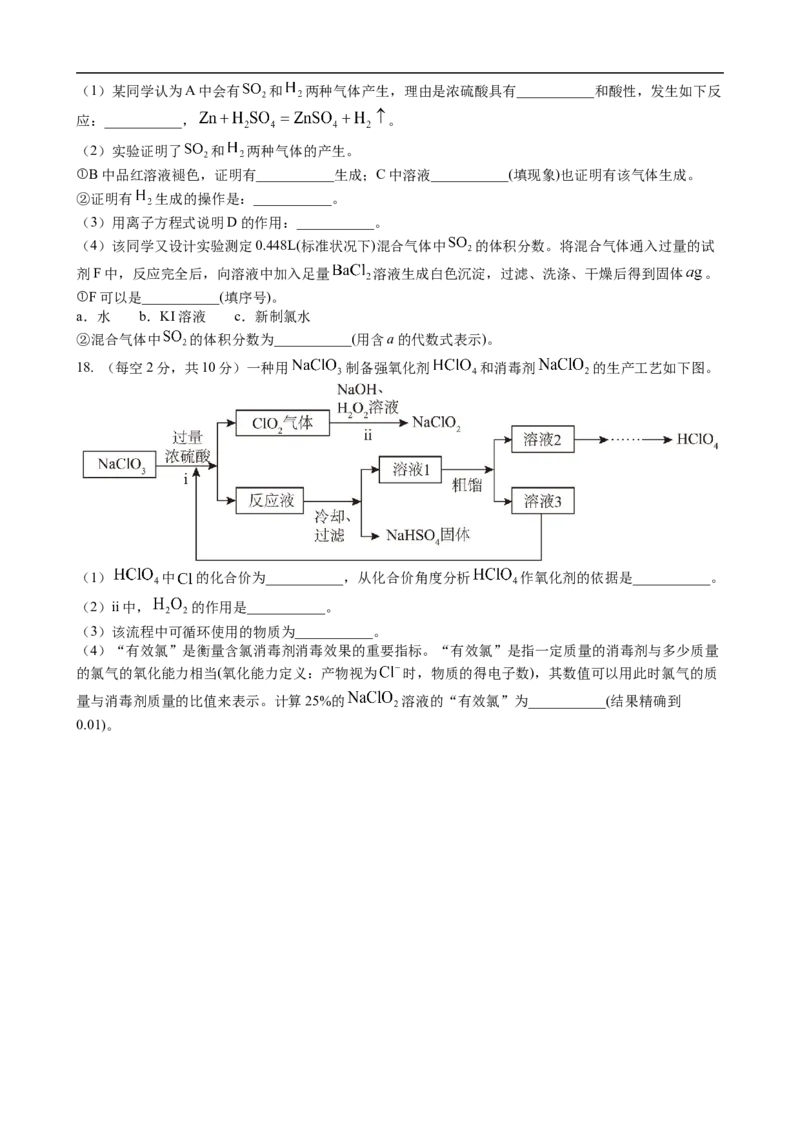
Ⅲ.取100 mL废水,逐滴加入1.0 mol/L的NaOH溶液,消耗NaOH溶液的体积与生成沉淀的质量如下
图所示。
请根据上述信息回答下列问题:、
①该废水中一定不含有的离子是 .
②实验中需配制1.0 mol/L的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、
胶头滴管,还缺少的仪器有 。
③写出图中A→B反应的离子方程式: 。
④通过计算,该废水中 Cl-(填“含有”或“不含有”);若含有,则c(Cl-)= (若不
含有,此问不必作答)。
17. (每空2分,共16分)用下图所示实验对足量的锌与浓硫酸在加热条件下反应产生的气体进行研究
(夹持和加热装置已略去)。(1)某同学认为A中会有 和 两种气体产生,理由是浓硫酸具有___________和酸性,发生如下反
应:___________, 。
(2)实验证明了 和 两种气体的产生。
①B中品红溶液褪色,证明有___________生成;C中溶液___________(填现象)也证明有该气体生成。
②证明有 生成的操作是:___________。
(3)用离子方程式说明D的作用:___________。
(4)该同学又设计实验测定0.448L(标准状况下)混合气体中 的体积分数。将混合气体通入过量的试
剂F中,反应完全后,向溶液中加入足量 溶液生成白色沉淀,过滤、洗涤、干燥后得到固体 。
①F可以是___________(填序号)。
a.水 b.KI溶液 c.新制氯水
②混合气体中 的体积分数为___________(用含a的代数式表示)。
18. (每空2分,共10分)一种用 制备强氧化剂 和消毒剂 的生产工艺如下图。
(1) 中 的化合价为___________,从化合价角度分析 作氧化剂的依据是___________。
(2)ii中, 的作用是___________。
(3)该流程中可循环使用的物质为___________。
(4)“有效氯”是衡量含氯消毒剂消毒效果的重要指标。“有效氯”是指一定质量的消毒剂与多少质量
的氯气的氧化能力相当(氧化能力定义:产物视为 时,物质的得电子数),其数值可以用此时氯气的质
量与消毒剂质量的比值来表示。计算25%的 溶液的“有效氯”为___________(结果精确到
0.01)。参考答案
一、选择题:(每小题3分;共42分)
1. C 2. C 3. D 4. B 5. B 6. C 7. D 8. A 9. B 10. D 11. D 12. B 13. A 14. B。
二、填空题:(每空2分,共58分)
15. 100mL容量瓶、玻璃棒; Fe3++3H O Fe(OH) (胶体)+3H+ ;
2 3
a、d; Al ;Al O ; 2 Al +2OH-+2 H O = 2 AlO +3H ↑ ; Al O +2OH-=2 AlO + H O ;
2 3 2 2 2 3 2
4FeS+15O +2H O2Fe (SO )+2H S O ; 1 10 4 2 10 ; 8H+ ; 1 ;
2 2 2 2 4 3 2 4
NO。
2
16.(1) NO 1
2
(2)2CO+2NO N+2CO
2 2
(3) Fe3+ 、Na+、OH- 100ml容量瓶 Al(OH) +OH-=AlO +2H O 含有 0.1mol/L
3 2
17. (1) ①. 强氧化性 ②.
(2) ①. ②. 出现浑浊 ③. 点燃E中肥皂泡
(3)
(4) ①. c ②.
18. (1) ①. +7 ②. +7价是Cl元素的最高化合价,化合价有降低的趋势,因此HClO 可作氧化
4
剂
(2)
(3)作还原剂,将 还原为
(4)(5)39%