文档内容
2024-2025 学年度上学期月考
高一化学(A)
命题范围:必修一第一章
时间:75分钟 满分:100分
一、单项选择题:每题3分,共60分。
1. 胶体在日常生活中随处可见。下列分散系不属于胶体的是
A. 云 B. 矿泉水
C. 豆浆 D. 滴入沸水中形成的分散系
【答案】B
【解析】
【详解】胶体是一种分散系、分散质微粒直径在1~100nm之间,选项中云、豆浆及 滴入沸水中形成
的分散系即氢氧化铁胶体均属于胶体,矿泉水属于溶液、不属于胶体;
故选B。
2. 下列化学反应基本类型中一定是氧化还原反应的是
A. 化合反应 B. 分解反应 C. 复分解反应 D. 置换反应
【答案】D
【解析】
【详解】凡有元素化合价升降或变化的化学反应就是氧化还原反应,在四大基本类型的反应中,只有置换
反应一定有化合价变化,所以置换反应一定是氧化还原反应,故选D。
3. 溶液、胶体和浊液这三种分散系的根本区别是
A. 是否是大量分子或离子的集合体 B. 分散质粒子直径的大小
C. 是否能透过滤纸 D. 是否为均一、稳定、透明的外观
【答案】B
【解析】
【详解】溶液、胶体和浊液这三种分散系的根本区别是分散质粒子的直径大小,故选B。
4. 下列逻辑关系图示中正确的是A. B. C. D.
【答案】D
【解析】
【详解】A.胶体与气溶胶是包含关系,A错误;
B.氧化还原反应与离子反应属于交叉关系,B错误;
C.钠盐、钾盐与碳酸盐是交叉关系,不是并列关系,C错误;
D.电解质是溶于水或在熔融状态下能够导电的化合物;非电解质是溶于水或在熔融状态下不能够导电的
化合物;混合物含有多种物质,单质为一种元素组成的纯净物;混合物、单质、电解质与非电解质等概念
是并列关系,D正确;
故选D。
5. 下列叙述正确的是
A. 固体氯化钠不导电,所以氯化钠不是电解质
B. 铜丝能导电,所以铜是电解质
C. 氯化氢水溶液能导电,所以氯化氢是电解质
D. CO 溶于水能导电,所以CO 是电解质
2 2
【答案】C
【解析】
【详解】A.固体氯化钠不含自由移动的离子,所以不能导电,但氯化钠的溶液和熔融状态下均能导电,
所以氯化钠是电解质,A错误;
B.铜是金属单质,铜是既不是电解质又不是非电解质,B错误;
C.氯化氢属于化合物,其水溶液能导电,所以氯化氢是电解质,C正确;
D.CO 自身不能电离,所以CO 是非电解质,D错误;
2 2
故选C。
6. 下列物质中属于强电解质且在给定条件下不能导电的是
A. 液态氯化氢 B. 熔融氯化钾 C. 稀硝酸 D. 三氧化硫固体
【答案】A
【解析】
【分析】
【详解】A.液态氯化氢没有自由移动的离子,不能导电,且HCl为强电解质,A符合题意;
B.熔融氯化钾中有自由移动的离子,可以导电,B不符合题意;C.稀硝酸中有自由移动的离子,可以导电,C不符合题意;
D.三氧化硫固体虽然不导电,但三氧化硫不是电解质,D不符合题意;
综上所述答案为A。
7. 下列化学方程式不能用 表示的是
A.
B.
C.
D.
【答案】D
【解析】
【分析】 表示的是强酸和强碱反应且没有沉淀生成的离子方程式;
【详解】A. 中无沉淀生成,离子方程式为 ,选项A不符合;
B. 中无沉淀生成,离子方程式为 ,选项B不符合;
C. 没有沉淀生成,其离子方程式为 ,选项C不
符合;
D. ,无沉淀生成,但有弱电解质参与反应,其离子方程式为
,选项D符合;
答案选D。
8. 下列物质在水中的电离方程式书写正确的是
A. MgCl =Mg2++Cl B. NaHCO =Na++H++CO
2 3
C. HCO H++HCO D. Ba(OH)=Ba2++2(OH)-
2 3 2
【答案】C【解析】
【分析】用化学式和离子符号表示电离过程的式子,称为电离方程式,表示物质溶解于水或熔融状态下电
离成离子的化学方程式。据此解答。
【详解】A.氯化镁完全电离出镁离子和氯离子:MgCl =Mg2++2Cl-,A错误;
2
B.碳酸氢钠是弱酸的酸式盐,完全电离出钠离子和碳酸氢根离子:NaHCO =Na++HCO ,B错误;
3
C.碳酸是二元弱酸,部分电离,以第一步电离为主:HCO H++HCO ,C正确;
2 3
D.氢氧化钡是二元强碱,完全电离出氢氧根离子和钡离子:Ba(OH)=Ba2++2OH-,D错误;
2
答案选C。
9. 分类是科学研究的重要方法,下列物质分类不正确的是
A. 酸性氧化物:干冰、二氧化硫、三氧化硫
B. 同素异形体:活性炭、 、金刚石
.
C 非电解质:乙醇、甲烷、氯气
D. 碱性氧化物:氧化钙、氧化铁、氧化镁
【答案】C
【解析】
【详解】A.酸性氧化物的定义是与碱反应只生成盐和水的氧化物,CO、SO 、SO 都是酸性氧化物,A
2 2 3
正确;
B.同素异形体是同种元素形成的不同单质,活性炭、 、金刚石都是C元素形成的不同单质,B正确;
C.非电解质指在水溶液中和熔融状态下都不电离的化合物,Cl 是单质,既不是电解质,也不是非电解质,
2
C错误;
D.碱性氧化物的定义是与酸反应只生成盐和水的氧化物,氧化钙、氧化铁、氧化镁都是碱性氧化物,D
正确;
故选C。
10. 离子方程式中CO +2H+ = H O+CO↑的CO 不可能来自下列物质中的
2 2
A. KCO B. NaCO C. CaCO D. (NH )CO
2 3 2 3 3 4 2 3
【答案】C
【解析】
【详解】根据离子方程式的书写规则,弱电解质或难溶物在离子方程式中应为化学式,KCO,NaCO,
2 3 2 3(NH )CO,为强电解质,CaCO 为难溶物,所以离子方程式中CO +2H+ = H O+CO↑的CO 不可能来自
4 2 3 3 2 2
CaCO ,故答案选C。
3
11. 下列各组物质不能发生离子反应的是
A. NaCl溶液与AgNO 溶液 B. HSO 溶液与NaOH溶液
3 2 4
C. KNO 溶液与NaOH溶液 D. NaCO 溶液与盐酸
3 2 3
【答案】C
【解析】
【详解】A.NaCl溶液与AgNO 溶液混合生成氯化银沉淀和硝酸钠,属于离子反应,A不符合;
3
B.HSO 溶液与NaOH溶液混合生成硫酸钠和水,属于离子反应,B不符合;
2 4
C.KNO 溶液与NaOH溶液混合不反应,不能发生离子反应,C符合;
3
D.NaCO 溶液与盐酸混合发生离子反应生成氯化钠、二氧化碳和水或生成碳酸氢钠和氯化钠,D不符合;
2 3
答案选C。
12. 下列变化过程中,需要加入氧化剂才能实现的是
A. B. C. D.
【答案】A
【解析】
【详解】A. ,I元素化合价升高,失电子,发生氧化反应,需要加入氧化剂,A正确;
B. ,S元素化合价降低,得电子,发生还原反应,需加入还原剂,B错误;
C. ,化合价不变,不是氧化还原反应,不需要加入氧化剂,C错误;
D. ,化合价降低,发生还原反应,需加入还原剂,D错误;
故选A。
13. 下列关于物质的分类中,正确的是
选
酸 碱 盐 混合物
项
A HClO 纯碱 明矾 CuSO ·5H O
4 2
B HNO 生石灰 NaHSO 盐酸
3 4
C HSO 烧碱 碳酸氢钠 澄清石灰水
2 3D Al(OH) 熟石灰 BaCO 液氯
3 3
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.纯碱不是碱是盐,CuSO ·5H O是纯净物,故A错误;
4 2
B.生石灰是氧化物,故B错误;
C.各种物质分类正确,故C正确;
D. Al(OH) 是碱,液氯是纯净物,故D错误;
3
答案C。
14. 能在稳定人体血液的pH中起作用的离子是( )
A. Na+ B. Cl﹣ C. D. Fe2+
【答案】C
【解析】
【分析】根据稳定人体血液的pH可知,选项中的离子既能与酸反应又能与碱反应才符合题意,以此来解
答。
的
【详解】A.Na+不水解,为强碱阳离子,不能起到调节人体内pH值 作用,故A错误;
B.Cl−不水解,为强酸阴离子,不能起到调节人体内pH值的作用,故B错误;
C.HCO −在溶液中存在两个趋势:HCO −离子电离使得溶液呈酸性,或者HCO −水解使得溶液呈碱性,即
3 3 3
电离呈酸性,降低pH值,水解呈碱性,pH值升高,故C正确;
D.Fe2+水解,为弱碱阳离子,使得溶液水解呈酸性,只能降低pH值,故D错误;
故答案选C。
【点睛】明确稳定pH是解答本题的关键,并熟悉盐类水解的规律及常见离子的水解及酸式酸根离子的性
质来解答。
的
15. 某溶液中只含有Na+、Al3+、Cl-、SO 四种离子,已知前三种离子 个数比为3:2:1,则溶液中Cl-
和SO 的离子个数比为
A. 1:4 B. 3:4 C. 1:2 D. 3:2
【答案】A【解析】
【详解】设Na+、Al3+、Cl-的个数分别为3、2、1,根据电荷守恒:3×1+2×3=1×1+2×N( ),N(
)=4,Cl-和 的个数比为1:4,则故选A。
16. 下列粒子不具有还原性的是
A. B. C. D.
【答案】D
【解析】
【详解】A.O元素化合价处于中间价态,既具有氧化性又具有还原性,故A不符合题意;
B.S元素化合价处于最低价态,具有还原性,故B不符合题意;
C.Cl元素化合价处于最低价态,具有还原性,故C不符合题意;
D.Cu元素的化合价为最高价态,只具有氧化性,故D符合题意;
故选D。
17. 单宁是葡萄酒中存在的一种天然防腐剂,可以避免因氧化作用而使葡萄酒变酸,下列关于其抗氧化反
应的说法不正确的是
A. 在反应中作氧化剂 B. 在反应中失去电子
C. 在反应中被氧化 D. 在反应中有元素化合价升高
【答案】A
【解析】
【详解】单宁为防止葡萄酒被氧化,则单宁还原性比葡萄糖强,在反应中单宁作还原剂,失去电子,元素
的化合价升高,被氧化,故B、C、D正确,A错误;
答案选A。
18. 某饮料的配料表如表所示,下列说法错误的是
配料:水、蔗糖、氯化钠、浓缩果汁、柠檬酸钠、山梨酸钾、苹果酸、维生素C……
A. 苹果酸可以与氢氧化钠反应
B. 维生素C可作抗氧化剂是由于其易被氧化
C. 蔗糖属于电解质
D. 柠檬酸钠属于一种盐
【答案】C【解析】
【详解】A.苹果酸属于酸,可以与氢氧化钠反应,故A正确;
B.维生素C可用作抗氧化剂说明其具有还原性,易被氧化,故B正确;
C.蔗糖属于非电解质,故C错误;
D.柠檬酸钠属于盐类,故D正确;
答案选C。
19. 让天更蓝、山更绿、水更清,化学在行动。废水脱氮中有一种方法是在废水中加入过量 使
完全转化为 ,反应可表示为 。下列有关该反
应的说法错误的是
A. 是还原产物 B. 被氧化
C. 氧化剂与还原剂物质的量之比为 D. 氧化性:
【答案】D
【解析】
【详解】A.由 知,Cl的化合价由+1价降到-1价,故
是还原产物,A正确;
B. 中N的化合价由-3价升高到 中0价,故 被氧化,B正确;
C.由 知,氧化剂为 ,还原剂为 ,氧化剂
的
与还原剂物质 量之比为 ,C正确;
D.由 知,氧化剂为 ,氧化产物为 ,故氧化性:
,D错误;
故选D。
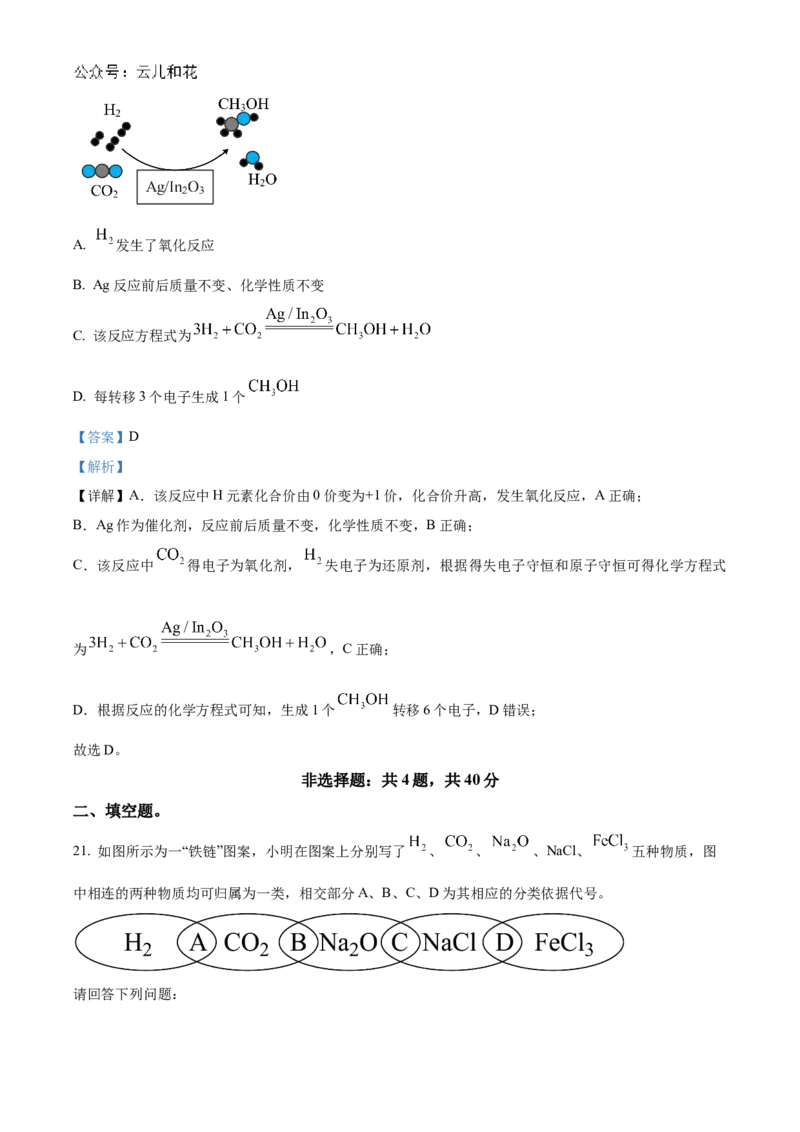
20. 我国化学家用氧化钢( )负载的Ag催化剂实现了 加氢制备 ,原理如图所示。关于该
反应的说法错误的是A. 发生了氧化反应
B. Ag反应前后质量不变、化学性质不变
C. 该反应方程式为
D. 每转移3个电子生成1个
【答案】D
【解析】
【详解】A.该反应中H元素化合价由0价变为+1价,化合价升高,发生氧化反应,A正确;
B.Ag作为催化剂,反应前后质量不变,化学性质不变,B正确;
C.该反应中 得电子为氧化剂, 失电子为还原剂,根据得失电子守恒和原子守恒可得化学方程式
为 ,C正确;
D.根据反应的化学方程式可知,生成1个 转移6个电子,D错误;
故选D。
非选择题:共4题,共40分
二、填空题。
21. 如图所示为一“铁链”图案,小明在图案上分别写了 、 、 、NaCl、 五种物质,图
中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。
请回答下列问题:的
(1)请将分类依据代号填入相应 括号内:
( )两种物质都是钠的化合物。
( )两种物质都是氧化物。
( )两种物质都是盐。
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向沸水中逐滴加入饱和的图中某种物质M的水溶
液,继续煮沸可制得一种红褐色胶体。
①物质M的化学式为___________________。
②证明有红褐色胶体生成的实验操作及现象是___________。
【答案】 ①. C ②. B ③. D ④. ⑤. 用激光照射烧杯内的液体,在光的侧面可观
察到光亮的“通路”
【解析】
【详解】(1)含有钠元素的化合物是氧化钠和氯化钠,C正确;二氧化碳和氧化钠中由两种元素组成,其中
一种是氧元素,属于氧化物,B正确;氯化钠和氯化铁是能电离出酸根阴离子和金属阳离子的化合物,属
于盐类,D正确;答案为C,B,D。
(2)①用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入氯化铁的饱和溶液,继续煮沸
可制得一种红褐色氢氧化铁胶体;答案为FeCl 。
3
②利用胶体的丁达尔现象,可证明胶体的生成,具体操作和实验现象为用激光照射烧杯内的液体,在光的
侧面可观察到光亮的“通路”;答案为用激光照射烧杯内的液体,在光的侧面可观察到光亮的“通路”。
22. I.某化学兴趣小组对下列三组物质进行研究:
A.HCl、HSO 、HCO 、HNO
2 4 2 3 3
B.NaCl溶液、水、泥沙悬浊液、AgI胶体
C.NaCO 、NaNO 、AgNO 、Ba(NO )
2 3 3 3 3 2
请你帮他们完善下列空白:
A B C
(3)
分类标准 含氧酸 分散系
_______
(1)
不属于该类别的物质 (2)_______ NaCO
_______ 2 3
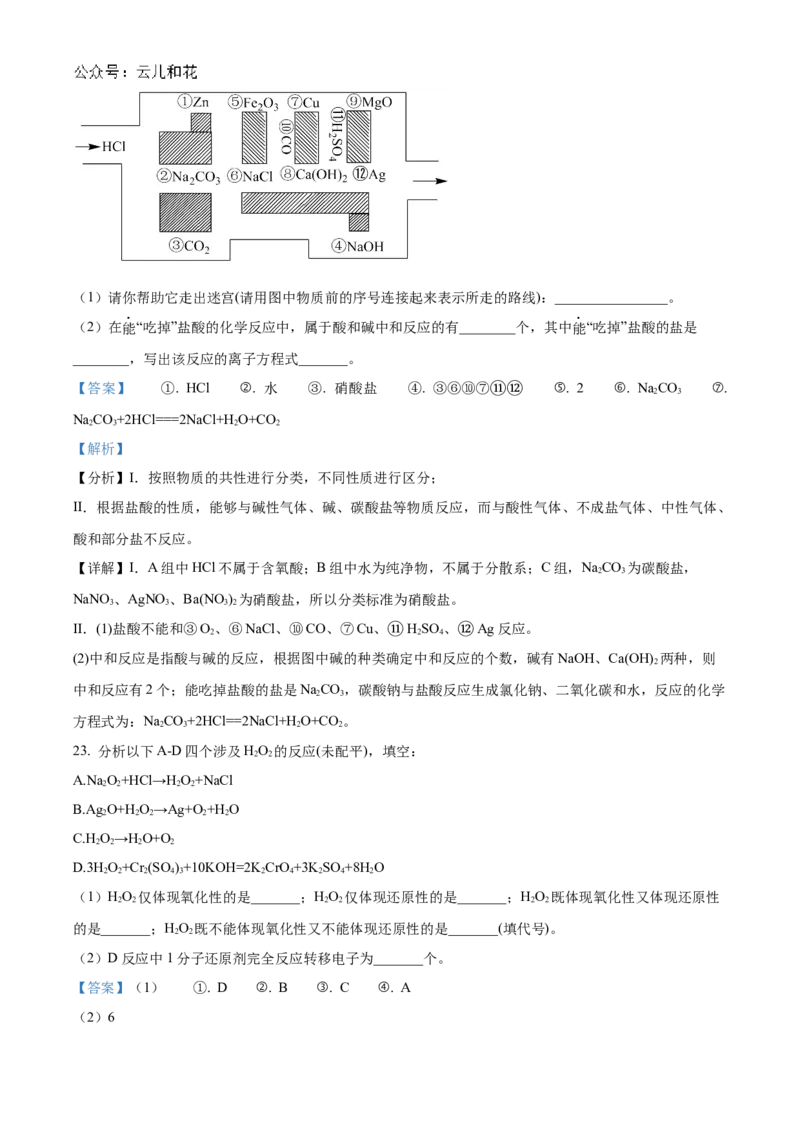
II.“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能
与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。(1)请你帮助它走出迷宫(请用图中物质前的序号连接起来表示所走的路线):________________。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有________个,其中能“吃掉”盐酸的盐是
________,写出该反应的离子方程式_______。
【答案】 ①. HCl ②. 水 ③. 硝酸盐 ④. ③⑥⑩⑦ ⑤. 2 ⑥. NaCO ⑦.
2 3
NaCO+2HCl===2NaCl+H O+CO ⑪⑫
2 3 2 2
【解析】
【分析】I.按照物质的共性进行分类,不同性质进行区分;
II.根据盐酸的性质,能够与碱性气体、碱、碳酸盐等物质反应,而与酸性气体、不成盐气体、中性气体、
酸和部分盐不反应。
【详解】I.A组中HCl不属于含氧酸;B组中水为纯净物,不属于分散系;C组,NaCO 为碳酸盐,
2 3
NaNO 、AgNO、Ba(NO ) 为硝酸盐,所以分类标准为硝酸盐。
3 3 3 2
II.(1)盐酸不能和③O、⑥NaCl、⑩CO、⑦Cu、 HSO 、 Ag反应。
2 2 4
(2)中和反应是指酸与碱的反应,根据图中碱的种类确⑪定中和反应⑫的个数,碱有NaOH、Ca(OH)
2
两种,则
中和反应有2个;能吃掉盐酸的盐是NaCO,碳酸钠与盐酸反应生成氯化钠、二氧化碳和水,反应的化学
2 3
方程式为:NaCO+2HCl==2NaCl+H O+CO。
2 3 2 2
23. 分析以下A-D四个涉及HO 的反应(未配平),填空:
2 2
A.Na O+HCl→H O+NaCl
2 2 2 2
B.Ag O+HO→Ag+O+H O
2 2 2 2 2
C.H O→HO+O
2 2 2 2
D.3HO+Cr (SO )+10KOH=2K CrO+3K SO +8H O
2 2 2 4 3 2 4 2 4 2
(1)HO 仅体现氧化性的是_______;HO 仅体现还原性的是_______;HO 既体现氧化性又体现还原性
2 2 2 2 2 2
的是_______;HO 既不能体现氧化性又不能体现还原性的是_______(填代号)。
2 2
(2)D反应中1分子还原剂完全反应转移电子为_______个。
【答案】(1) ①. D ②. B ③. C ④. A
(2)6【解析】
【分析】HO 仅体现氧化性,则O元素的化合价降低;双氧水仅体现还原性,则双氧水在反应中仅被氧化,
2 2
化合价只升高;HO 既体现氧化性又体现还原性,则O元素的化合价既升高又降低;HO 既不做氧化剂又
2 2 2 2
不做还原剂,说明在反应中双氧水中元素的化合价不发生变化;根据化合价的变化分析判断转移电子,据
此分析。
【小问1详解】
A.NaO+HCl→H O+NaCl,是一个非氧化还原反应,HO 既不是氧化剂,也不是还原剂;
2 2 2 2 2 2
B.Ag O+HO→Ag+O+H O,Ag O被还原成单质银,HO 中氧元素转化为O,表现还原性;
2 2 2 2 2 2 2 2 2
C.HO→HO+O,是一个自身氧化还原反应,HO 既表现了氧化性,又表现了还原性;
2 2 2 2 2 2
D.3HO+Cr (SO )+10KOH=2K CrO+3K SO +8H O,HO 中氧元素化合价由-1变成-2,化合价降低被还
2 2 2 4 3 2 4 2 4 2 2 2
原,表现氧化性;
所以HO 仅体现氧化性的反应是D;HO 仅体现还原性的反应是B;HO 既体现氧化性,又体现还原性的
2 2 2 2 2 2
反应是C;HO 既不做氧化剂又不做还原剂的反应是A,故答案为:D;B;C;A。
2 2
【小问2详解】
3HO+Cr (SO )+10KOH=2K CrO+3K SO +8H O反应中氧化剂为HO,还原剂为Cr (SO ),根据方程式,
2 2 2 4 3 2 4 2 4 2 2 2 2 4 3
1分子还原剂完全反应,Cr由+3价升高为+6价,转移电子的物质的量为3×2=6,故答案为:6。
24. 根据反应 ,回答下列问题。
(1)氧化剂_______。
(2)氧化剂与还原剂的物质的量之比:_______。
(3)用单线桥的方法表示该反应的电子转移情况。_______。
【答案】(1)
(2)3:2 (3)
【解析】
【分析】根据反应方程式可知,N的化合价从-3价变为0价,化合价升高,氨气作还原剂;氯气中氯的化
合价从0价变为-1价,化合价降低,氯气作氧化剂,据此作答:
【小问1详解】
根据分析可知,氧化剂为 ;【小问2详解】
氧化剂为 ,还原剂为NH ,8molNH 中只有2molNH 的化合价发生了变化,故氧化剂与还原剂的物质
3 3 3
的量之比为3:2;
【小问3详解】
1molNH 转移3mole-,故2molNH 转移6mole-,因此单线桥为 。
3 3