文档内容
上学期期中试题
高二化学
一、单选题
1. 某元素X的最高价氧化物为 ,则它的气态氢化物是
A. B. C. D.
【答案】A
【解析】
【分析】
【详解】某元素X的最高价氧化物为 ,则它的最高正价为+7价,最低负价为-1价,
其气态氢化物的化学式是HX,故选A。
2. 下列每组中各物质内既有离子键又有共价键的一组是
A. KOH、HNO、(NH )HPO B. NaO、NaCO、NH HCO
3 4 2 4 2 2 3 4 3
C. NaO、Ba(OH) 、NaSO D. HBr、Al O、CaCl
2 2 2 2 4 2 3 2
【答案】C
【解析】
【分析】
【详解】A.HNO 内只有共价键,A错误;
3
B.中NaO内只有离子键,B错误;
2
C.aO、Ba(OH) 、NaSO 内既有离子键又有共价键,C正确;
2 2 2 2 4
D.中HBr内只有共价键,Al O、CaCl 内只有离子键,D错误;
2 3 2
答案选C。
3. SO 分别通入下列溶液中,溶液都褪成无色,其中体现了二氧化硫漂白性的是
2
A. 橙黄色的溴水 B. 品红溶液
C. 紫红色的KMnO 溶液 D. 滴了酚酞的NaOH溶液
4
【答案】B
【解析】
【分析】
【详解】A. 橙黄色的溴水褪成无色,体现二氧化硫的还原性,故A不符;
B. 品红溶液褪成无色,体现了二氧化硫漂白性,故B符合;
C. 紫红色的KMnO 溶液褪成无色,体现二氧化硫的还原性,故C不符;
4
D. 滴了酚酞的NaOH溶液褪成无色,体现二氧化硫的酸性氧化物的性质,故D不符;
故选B。
4. 下列物质中,不能由单质直接化合生成的是
①Cu S ②FeS ③SO ④HS ⑤FeCl
2 3 2 2
A. ③⑤ B. ①②③⑤ C. ①②④⑤ D. 全部【答案】A
【解析】
【分析】
【详解】①铜与硫共热反应生成硫化亚铜,故不符合题意;
②铁与硫共热反应生成硫化亚铁,故不符合题意;
③硫在氧气中燃烧只能生成二氧化硫,不能生成三氧化硫,故符合题意;
④氢气与硫蒸汽共热反应生成硫化氢气体,故不符合题意;
⑤铁在氯气中燃烧只能生成氯化铁,不能生成氯化亚铁,故符合题意;
③⑤符合题意,故选A。
5. 下列说法正确的是
A. HClO、NaO、SO 都可用于漂白适当的物质,其漂白原理相同
2 2 2
B. 氮的固定都属于氧化还原反应
C. “雷雨发庄稼”的科学道理中,涉及的化学反应,氮元素都是被氧化
D. NH 水溶液能导电,所以 NH 是电解质
3 3
【答案】B
【解析】
【分析】
【详解】A. HClO、NaO 均因具有强氧化性、可用于漂白;SO 使品红等有色物质褪色
2 2 2
的原理是二者结合生成无色不稳定的物质,A错误;
B.氮的固定是游离态氮元素变化为化合态氮元素;则氮的固定都属于氧化还原反应,B正
确;
C. “雷雨发庄稼”的科学道理中,涉及的化学反应, 、
和 , 、
氮元素被氧化, 中氮元素既被氧化又被
还原,C错误;
D.氨气溶于水生成一水合氨,一水合氨电离出氢氧根离子、铵根离子,故其水溶液因含
可自由移动的离子可导电,但氨分子自身不发生电离,故氨气属于非电解质,D错误;
答案选B。
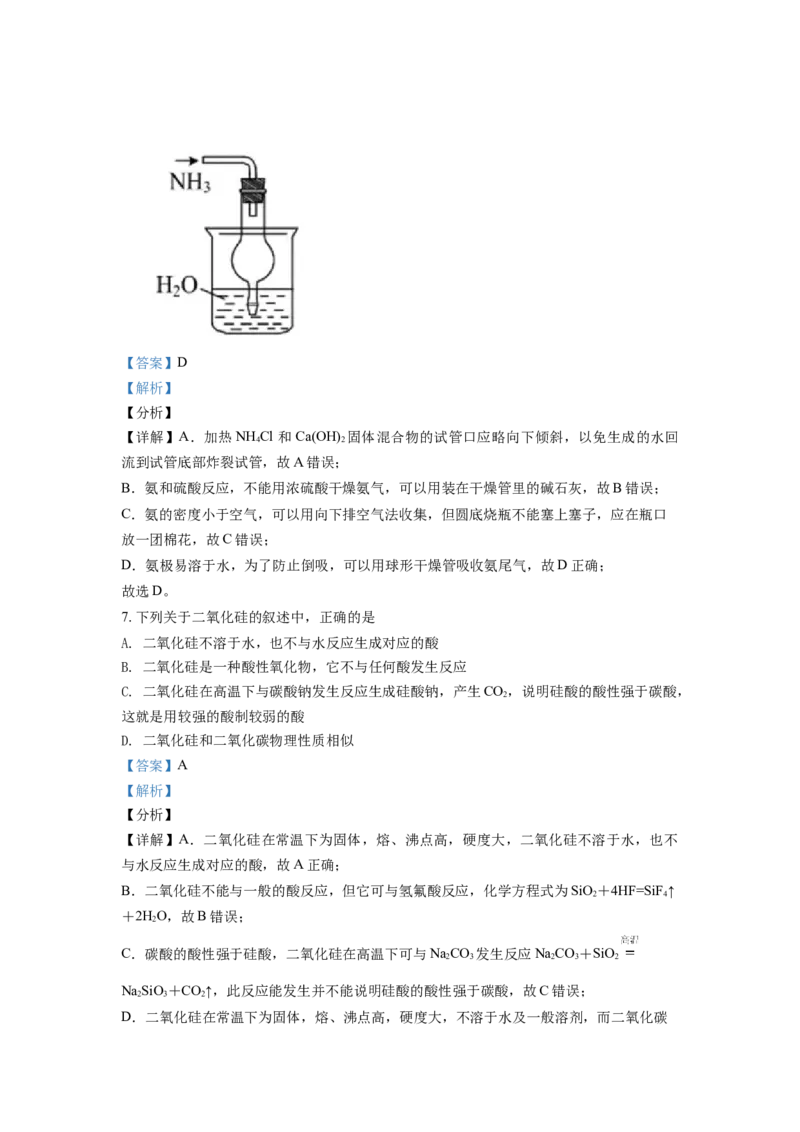
6. 实验室用加热NH Cl 和 Ca(OH) 固体混合物的方法制取少量的氨气,图中装置能达到相
4 2
应的实验目的的是A. 生成NH B. 干燥NH
3 3
C. 收集NH D. 吸收NH 尾气
3 3【答案】D
【解析】
【分析】
【详解】A.加热NH Cl 和 Ca(OH) 固体混合物的试管口应略向下倾斜,以免生成的水回
4 2
流到试管底部炸裂试管,故A错误;
B.氨和硫酸反应,不能用浓硫酸干燥氨气,可以用装在干燥管里的碱石灰,故B错误;
C.氨的密度小于空气,可以用向下排空气法收集,但圆底烧瓶不能塞上塞子,应在瓶口
放一团棉花,故C错误;
D.氨极易溶于水,为了防止倒吸,可以用球形干燥管吸收氨尾气,故D正确;
故选D。
7. 下列关于二氧化硅的叙述中,正确的是
A. 二氧化硅不溶于水,也不与水反应生成对应的酸
B. 二氧化硅是一种酸性氧化物,它不与任何酸发生反应
C. 二氧化硅在高温下与碳酸钠发生反应生成硅酸钠,产生CO,说明硅酸的酸性强于碳酸,
2
这就是用较强的酸制较弱的酸
D. 二氧化硅和二氧化碳物理性质相似
【答案】A
【解析】
【分析】
【详解】A.二氧化硅在常温下为固体,熔、沸点高,硬度大,二氧化硅不溶于水,也不
与水反应生成对应的酸,故A正确;
B.二氧化硅不能与一般的酸反应,但它可与氢氟酸反应,化学方程式为SiO+4HF=SiF↑
2 4
+2HO,故B错误;
2
C.碳酸的酸性强于硅酸,二氧化硅在高温下可与NaCO 发生反应NaCO+SiO
2 3 2 3 2
NaSiO+CO↑,此反应能发生并不能说明硅酸的酸性强于碳酸,故C错误;
2 3 2
D.二氧化硅在常温下为固体,熔、沸点高,硬度大,不溶于水及一般溶剂,而二氧化碳在常温下为气体,熔、沸点低,可溶于水,二氧化硅和二氧化碳物理性质不同,故D错误;
选A。
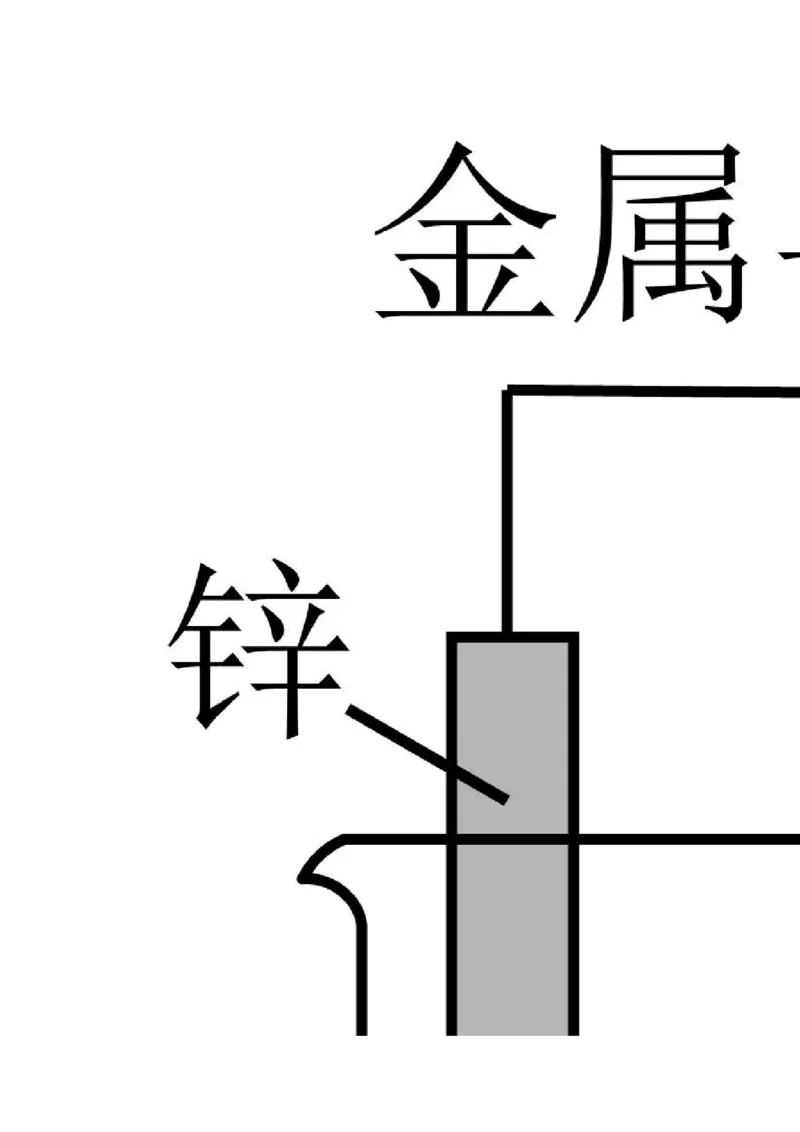
8. 关于如图所示装置的叙述正确的是A. Zn为负极
B. Zn极发生还原反应
C. Cu为负极
D. Cu极发生氧化反应
【答案】A
【解析】
【分析】
【详解】如图所示为原电池,较活泼 的金属为负极,则Zn为负极,Cu为正极,负极失电
子发生氧化反应,正极得电子发生还原反应,综上所述故选A。
9. 某反应过程中能量变化如图,下列说法正确的是
A. 反应是吸热反应
B. 该反应的反应物总能量比生成物的总能量低
C. 使用适当催化剂可改变该反应的反应速率
D. 该反应一定在加热条件下才能进行
【答案】C
【解析】
【分析】
【详解】A.该反应的反应物总能量比生成物的总能量高,反应是放热反应,故A错误;
B.该反应的反应物总能量比生成物的总能量高,故B错误;
C.使用适当催化剂可改变该反应的反应速率,故C正确;
D.该反应不一定在加热条件下才能进行,放热反应与反应需不需要加热无关,故D错误。
综上所述,答案为C。
10. 下列关于化学平衡状态的叙述错误的是
A. 化学平衡是所有可逆反应都存在的一种状态
B. 达到平衡时,正、逆反应速率均为零
C. 达到平衡时,反应物和生成物的浓度不再发生变化
D. 在给定条件下,达到平衡时可逆反应完成程度达到最大【答案】B
【解析】
【分析】
【详解】A.化学平衡状态是可逆反应在一定条件下建立的一种动态平衡状态,故A正确
B.达到平衡时,正、逆反应速率相等但不为0,故B错误;
C.化学反应达到平衡状态时反应物和生成物的浓度均不在发生改变,故C正确;
D.在一定条件下,化学平衡状态是反应所能达到的最大限度,故D正确;
故选:B。
11. 下列措施中,不能增大化学反应速率的是
A. Zn与稀硫酸反应制取H 时,加入硫酸钠溶液
2
B. Al在O 中燃烧生成Al O,用铝粉代替铝片
2 2 3
C. CaCO 与稀盐酸反应生成CO 时,适当升高温度
3 2
D. KClO 分解制取O 时,添加少量MnO
3 2 2
【答案】A
【解析】
【分析】
【详解】A.加入硫酸钠溶液,相当于稀释溶液,化学反应速率减慢,故A符合题意;
B.用铝粉代替铝片,增大反应物的接触面积,化学反应速率加快,故B不符合题意;
C.升高温度化学反应速率加快,故C不符合题意;
D.KClO 分解制取O 时,添加少量MnO 起催化作用,化学反应速率加快,故D不符合
3 2 2
题意;
。
答案选A
12. 在2A(g)+B(g)=3C(g)+4D(g)反应中,表示该反应速率最快的是
A. v(A)=0.5mol/(L·s) B. v(B)=0.3mol/(L·s)
C. v(C)=0.8mol/(L·s) D. v(D)=1.0mol/(L·s)
【答案】B
【解析】
【分析】根据反应速率之比等于各物质的计量数之比,将不同物质表示的速率利用此关系
转化成相同的物质进行比较速率的快慢。
【详解】根据反应速率和系数之间的关系: ,对A、B、C、D
四个选项中的不同速率进行转化:A: ,B: ,C: ,D:
;故答案B表示的速率最快,故选B。
【点睛】速率比较大小简便方法是将各物质的速率比各物质的系数利用比值的大小进行判
断。13. 下列化学用语正确的是
A. 硫原子结构示意图: B. 中子数为8的氮原子:
C. 乙烯的结构简式:CHCH D. 乙烯分子的球棍模型:
2 2
【答案】D
【解析】
【分析】
【详解】A.硫原子的核电荷数、核外电子总数都是16,硫原子的结构示意图为 ,
故A错误;
B.中子数为8的氮原子表达式为 ,故B错误;
C.乙烯的结构简式为 ,其中碳碳双键不能省略,故C错误;
D.乙烯分子的球棍模型为 ,故D正确;
故答案选D。
14. 下列物质的沸点由高到低排列的顺序是
①CH(CH)CH②CH(CH)CH③(CH)CH④(CH)CHCH CH
3 2 2 3 3 2 3 3 3 3 3 2 2 3
A. ②④①③ B. ④②①③ C. ④②③① D.
②④③①
【答案】A
【解析】
【分析】
【详解】②④中均含5个C原子,但④中含支链,则沸点为②>④,①③中均含4个C原
子,但③中含支链,则沸点为①>③,相对分子质量越大,沸点越高,所以沸点由高到低
排列为②④①③;
答案选A。
15. 下列关于乙烯与聚乙烯的说法,正确的是
A. 乙烯与聚乙烯都是纯净物
B. 乙烯通过加成聚合反应得到聚乙烯,聚乙烯也可以通过降解得到乙烯
C. 相同质量的乙烯与聚乙烯,完全燃烧所需要的氧气质量也相同D. 乙烯与聚乙烯,都能使酸性KMnO 溶液褪色
4
【答案】C
【解析】
【分析】
【详解】A. 乙烯是纯净物,聚乙烯是高分子化合物,高分子化合物都属于混合物,A错
误;
B. 乙烯通过加成聚合反应得到聚乙烯,聚乙烯中是饱和碳原子、碳碳单键性质稳定、难
以降解,B错误;
C.乙烯与聚乙烯的最简式均为CH,相同质量的乙烯与聚乙烯,完全燃烧所需要的氧气质
2
量也相同,C正确;
D. 乙烯含碳碳双键、能被酸性KMnO 溶液氧化而使之褪色;聚乙烯中是饱和碳原子、碳
4
碳单键性质稳定、不能使酸性KMnO 溶液褪色,D错误;
4
答案选C。
16. 下列反应属于取代反应的是
A. CH+2O CO+H O
4 2 2 2
B. CH=CH +H O CHCHOH
2 2 2 3 2
C. CHCl+Cl CHCl+HCl
3 2 2 2
.
D Fe+2HCl=FeCl +H↑
2 2
【答案】C
【解析】
【分析】
【详解】取代反应是指化合物或有机物分子中任何一个原子或原子团被试剂中同类型的其
它原子或原子团所替代的反应。
A.CH+2O CO+H O属于氧化反应,故A不选;
4 2 2 2
B.CH=CH +H O CHCHOH属于加成反应,故B不选;
2 2 2 3 2
C.CHCl+Cl CHCl+HCl反应过程中CHCl中1个H原子被Cl 中Cl原子取代,
3 2 2 2 3 2
属于取代反应,故C选;
D.Fe+2HCl=FeCl +H↑为置换反应,故D不选;
2 2
综上所述,答案为C。
17. 下列说法中,正确的是
A. 苯、乙醇和乙酸都能发生取代反应
B. CHCHCHCH 的二氯取代产物只有5种结构
3 2 2 3
C. CHCO18OH和C HOH在一定条件下酯化产物是CHCO18OC H
3 2 5 3 2 5D. 使用酸性KMnO 溶液除去乙烷中混有的乙烯
4
【答案】A
【解析】
【分析】
【详解】A.苯环与浓硝酸、浓硫酸在加热的条件下发生取代反应;乙醇可与乙酸之间发
生取代反应,故A正确;
B.通过“定一移二”法,可得二氯取代产物有6种
故B错误;
C.CHCO18OH和C HOH在一定条件下酯化,酸脱羟基醇脱氢, 18O应该在生成的产物水
3 2 5
中,故C错误;
D.乙烷不能与酸性KMnO 溶液反应,乙烯能被KMnO 溶液氧化成二氧化碳,所以又会
4 4
带入新的杂质二氧化碳,故D错误;
故答案选A。
18. 下列物质转化常通过加成反应实现的是( )
A. → B. CHCHOH→CH CHO
3 2 3
.
C CH→CHCl D. CH=CH →CHCHBr
4 3 2 2 3 2
【答案】D【解析】
【详解】A.通过取代反应转化,故A错误;
B.通过氧化反应转化,故B错误;
C.通过取代反应转化,故C错误;
D.有双键可通过加成反应转化,故D正确。
故答案为D。
19. 下列化学方程式书写错误的是
A. 乙醇的催化氧化:
B. 乙酸乙酯的制备:
C. 实验室用液溴和苯在催化剂作用下制溴苯: +Br
2
+HBr
D. 三氯甲烷与液氯混合后,强光照射,发生反应:
【答案】B
【解析】
【分析】
【详解】A.CHCHOH在Cu或Ag的催化下发生催化氧化反应生成乙醛,方程式为:
3 2
2CHCHOH+O 2CHCHO+2HO,故A正确;
3 2 2 3 2
B.羧酸与醇发生酯化反应,羧基脱去−OH, 羟基脱去−OH中的−H,相互结合生成水,该
反应可逆为反应,化学方程式为:CHCOOH+CH CH18OH
3 3 2
CHCO18OCH CH+H O,故B错误;
3 2 3 2
C.液溴和苯在溴化铁催化作用下反应,化学方程式为:
,故C正确;
D.三氯甲烷与液氯混合后,强光照射,发生取代反应,方程式为:
,故D正确;
故答案选D。20. 下列物质中不属于天然高分子化合物的是
A. 淀粉 B. 蛋白质 C. 油脂 D. 纤维素
【答案】C
【解析】
【分析】
【详解】淀粉、纤维素和蛋白质均是天然有机高分子化合物,油脂是高级脂肪酸和甘油形
成的酯类,不属于高分子化合物,故C正确;
故选C。
二、填空题
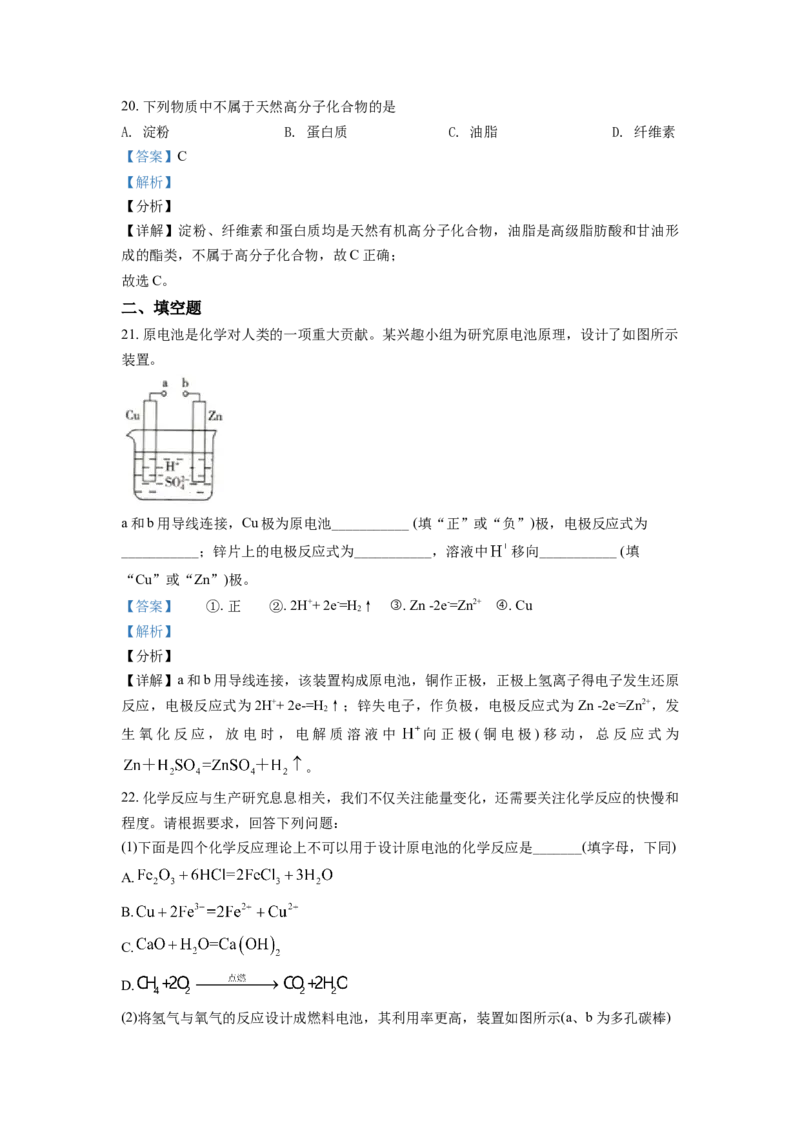
21. 原电池是化学对人类的一项重大贡献。某兴趣小组为研究原电池原理,设计了如图所示
装置。
a和b用导线连接,Cu极为原电池___________ (填“正”或“负”)极,电极反应式为
___________;锌片上的电极反应式为___________,溶液中 移向___________ (填
“Cu”或“Zn”)极。
【答案】 ①. 正 ②. 2H++ 2e-=H ↑ ③. Zn -2e-=Zn2+ ④. Cu
2
【解析】
【分析】
【详解】a和b用导线连接,该装置构成原电池,铜作正极,正极上氢离子得电子发生还原
反应,电极反应式为2H++ 2e-=H ↑;锌失电子,作负极,电极反应式为Zn -2e-=Zn2+,发
2
生氧化反应,放电时,电解质溶液中 向正极(铜电极)移动,总反应式为
。
22. 化学反应与生产研究息息相关,我们不仅关注能量变化,还需要关注化学反应的快慢和
程度。请根据要求,回答下列问题:
(1)下面是四个化学反应理论上不可以用于设计原电池的化学反应是_______(填字母,下同)
A.
B.
C.
D.
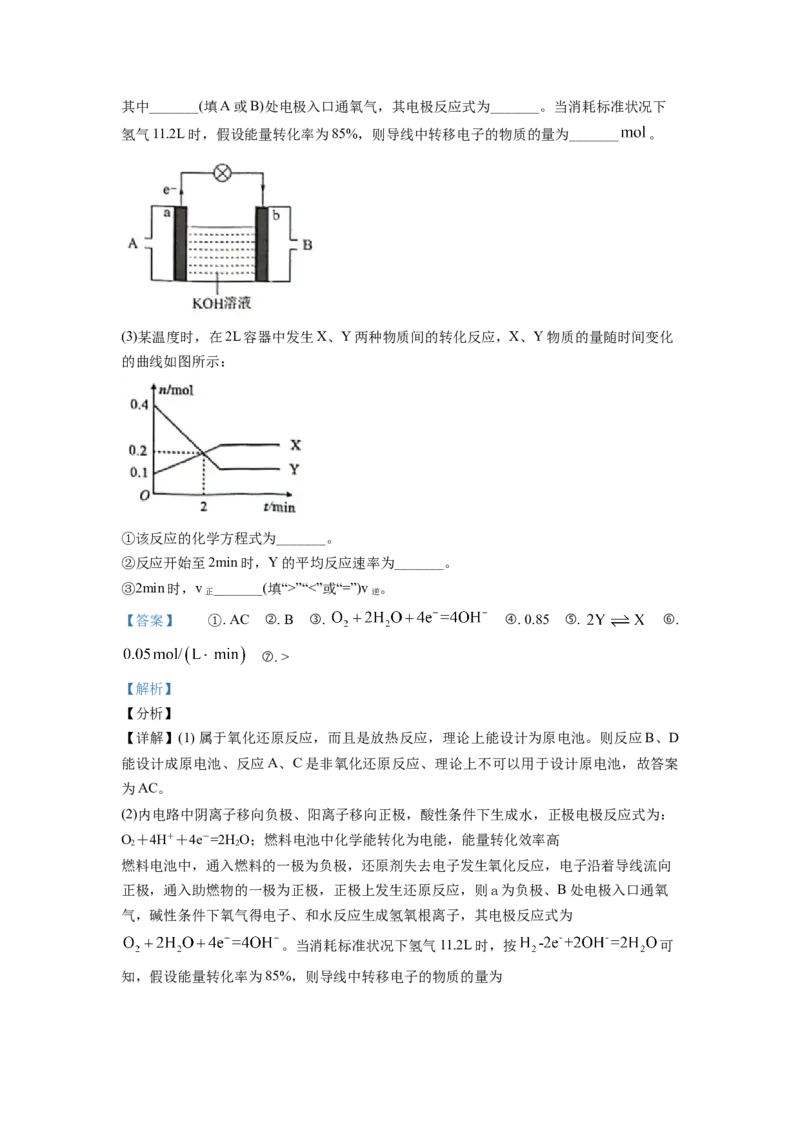
(2)将氢气与氧气的反应设计成燃料电池,其利用率更高,装置如图所示(a、b为多孔碳棒)其中_______(填A或B)处电极入口通氧气,其电极反应式为_______。当消耗标准状况下
氢气11.2L时,假设能量转化率为85%,则导线中转移电子的物质的量为_______ 。
(3)某温度时,在2L容器中发生X、Y两种物质间的转化反应,X、Y物质的量随时间变化
的曲线如图所示:
①该反应的化学方程式为_______。
②反应开始至2min时,Y的平均反应速率为_______。
③2min时,v _______(填“>”“<”或“=”)v 。
正 逆
【答案】 ①. AC ②. B ③. ④. 0.85 ⑤. ⑥.
⑦. >
【解析】
【分析】
【详解】(1) 属于氧化还原反应,而且是放热反应,理论上能设计为原电池。则反应B、D
能设计成原电池、反应A、C是非氧化还原反应、理论上不可以用于设计原电池,故答案
为AC。
(2)内电路中阴离子移向负极、阳离子移向正极,酸性条件下生成水,正极电极反应式为:
O+4H++4e-=2H O;燃料电池中化学能转化为电能,能量转化效率高
2 2
燃料电池中,通入燃料的一极为负极,还原剂失去电子发生氧化反应,电子沿着导线流向
正极,通入助燃物的一极为正极,正极上发生还原反应,则a为负极、B处电极入口通氧
气,碱性条件下氧气得电子、和水反应生成氢氧根离子,其电极反应式为
。当消耗标准状况下氢气11.2L时,按 可
知,假设能量转化率为85%,则导线中转移电子的物质的量为。
(3)①X的物质的量增加、Y的物质的量减小,所以Y是反应物、X是生成物,物质的量变
化值之比等与化学计量数之比,即Y与X的化学计量数之比为(0.4-0.2):(0.2-0.1)=2:1,故该
反应的化学方程式为 。
②反应开始至2min时,Y的平均反应速率为
。
③2min时,平衡还未建立,体系处于从正反应建立平衡的途中,故v v 。
正 逆
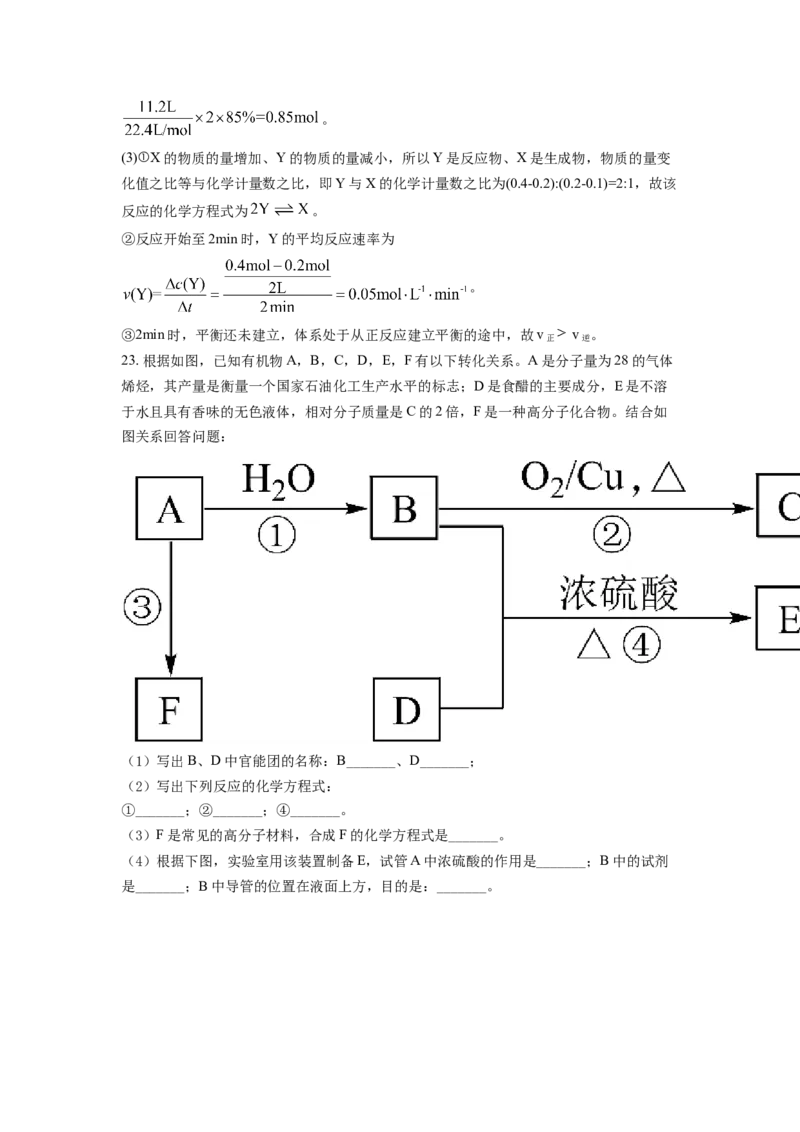
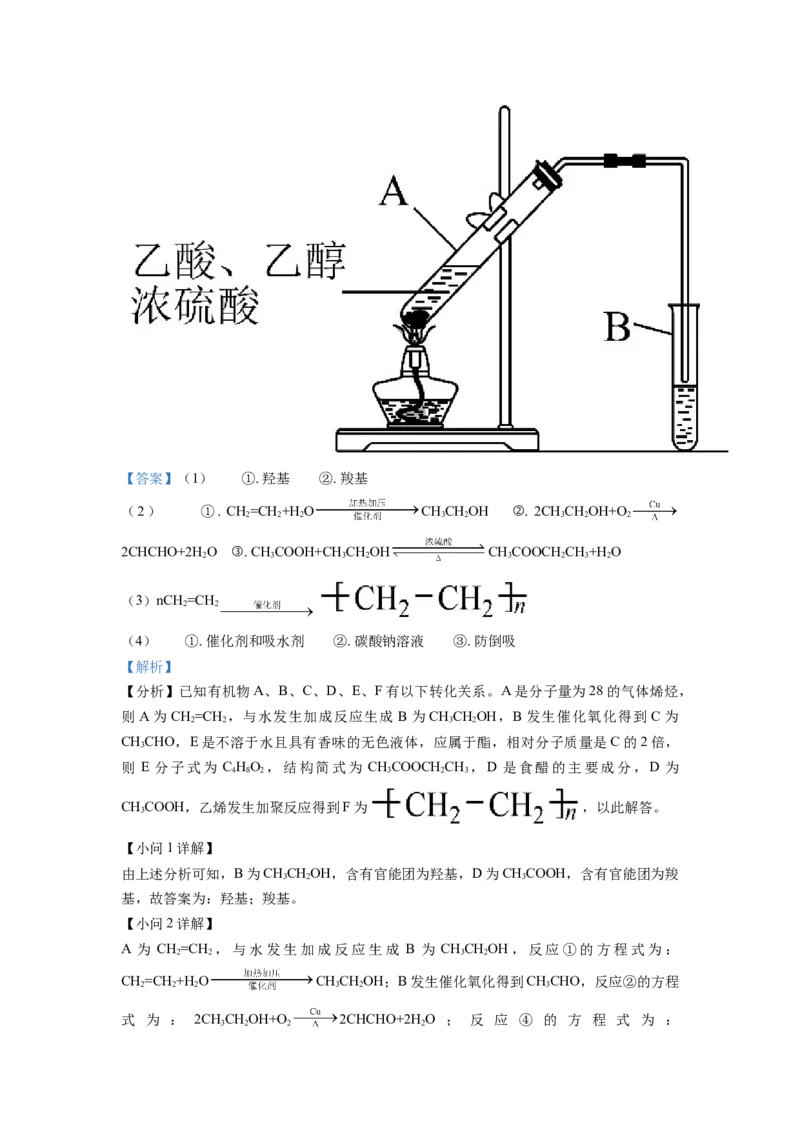
23. 根据如图,已知有机物A,B,C,D,E,F有以下转化关系。A是分子量为28的气体
烯烃,其产量是衡量一个国家石油化工生产水平的标志;D是食醋的主要成分,E是不溶
于水且具有香味的无色液体,相对分子质量是C的2倍,F是一种高分子化合物。结合如
图关系回答问题:
(1)写出B、D中官能团的名称:B_______、D_______;
(2)写出下列反应的化学方程式:
①_______;②_______;④_______。
(3)F是常见的高分子材料,合成F的化学方程式是_______。
(4)根据下图,实验室用该装置制备E,试管A中浓硫酸的作用是_______;B中的试剂
是_______;B中导管的位置在液面上方,目的是:_______。【答案】(1) ①. 羟基 ②. 羧基
(2) ①. CH=CH +H O CHCHOH ②. 2CHCHOH+O
2 2 2 3 2 3 2 2
2CHCHO+2H O ③. CHCOOH+CH CHOH CHCOOCH CH+H O
2 3 3 2 3 2 3 2
(3)nCH=CH
2 2
(4) ①. 催化剂和吸水剂 ②. 碳酸钠溶液 ③. 防倒吸
【解析】
【分析】已知有机物A、B、C、D、E、F有以下转化关系。A是分子量为28的气体烯烃,
则A为CH=CH ,与水发生加成反应生成 B为CHCHOH,B发生催化氧化得到 C为
2 2 3 2
CHCHO,E是不溶于水且具有香味的无色液体,应属于酯,相对分子质量是C的2倍,
3
则 E 分子式为 C HO ,结构简式为 CHCOOCH CH ,D 是食醋的主要成分,D 为
4 8 2 3 2 3
CHCOOH,乙烯发生加聚反应得到F为 ,以此解答。
3
【小问1详解】
由上述分析可知,B为CHCHOH,含有官能团为羟基,D为CHCOOH,含有官能团为羧
3 2 3
基,故答案为:羟基;羧基。
【小问2详解】
A 为 CH=CH ,与水发生加成反应生成 B 为 CHCHOH,反应①的方程式为:
2 2 3 2
CH=CH +H O CHCHOH;B发生催化氧化得到CHCHO,反应②的方程
2 2 2 3 2 3
式 为 : 2CHCHOH+O 2CHCHO+2H O ; 反 应 ④ 的 方 程 式 为 :
3 2 2 2CHCOOH+CH CHOH CHCOOCH CH+H O,故答案为:CH=CH +H O
3 3 2 3 2 3 2 2 2 2
CHCHOH ; 2CHCHOH+O 2CHCHO+2H O ;
3 2 3 2 2 2
CHCOOH+CH CHOH CHCOOCH CH+H O。
3 3 2 3 2 3 2
【小问3详解】
乙烯发生加聚反应得 ,化学方程式为:nCH=CH
2 2
,故答案为:nCH=CH
2 2
。
【小问4详解】
试管A中浓硫酸的作用是催化剂和吸水剂,B中的试剂是碳酸钠溶液,B中导管的位置在
液面上方,目的是防倒吸,故答案为:催化剂和吸水剂;碳酸钠溶液;防倒吸。