文档内容
2025-2026 学年第一学期期中七校联合调研试题
高一化学
可能用到的相对原子质量:H 1 C 12 O 16 Na23
一、选择题:共16题,每题3分,共48分。每题只有一个选项最符合题意。
1. 化学与生产、生活、科技等方面密切相关,下列说法正确的是
A.NaCO 可用于制玻璃、肥皂、造纸、纺织等工业
2 3
B.我国十大科技成果之一的“纳米氮化镓(GaN)”是一种胶体
C.实现“碳中和”具有直接贡献的一种措施:研发催化剂将CO 转化为甲醇(CHOH,其中碳元素化
2 3
合价为-2价),该过程中CO 发生了氧化反应
2
D.维生素C又称“抗坏血酸”,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,
这说明维生素C具有氧化性
2.分类是科学研究的重要方法,下列物质分类正确的是
A.化合物:干冰、石灰石 B.混合物:盐酸、矿泉水
C.酸性氧化物:CO、CO D.电解质:硫酸、液氯
2
3.现有一种制备氯气方法:KClO + 6HCl(浓) =KCl + 3Cl ↑+ 3H O,下列表达不正确的是
3 2 2
A.氯离子的结构示意图:
B.KClO 的电离方程式:KClO =K++ClO -
3 3 3
的
C.常温下氯气与铁不反应,液氯可以保存在干燥 钢瓶中
D.双线桥可表示为
4. 下列说法正确的是
A.将足量的NaO 加到酚酞溶液中,最终溶液为红色
2 2
B.可用pH试纸测氯水的pH值
C.相同条件下NaCO 和NaHCO 在水中的溶解度,NaCO 更大
2 3 3 2 3
D.相同质量NaCO 和NaHCO 两种固体中分别滴入几滴水,二者产生的热效应相同
2 3 3
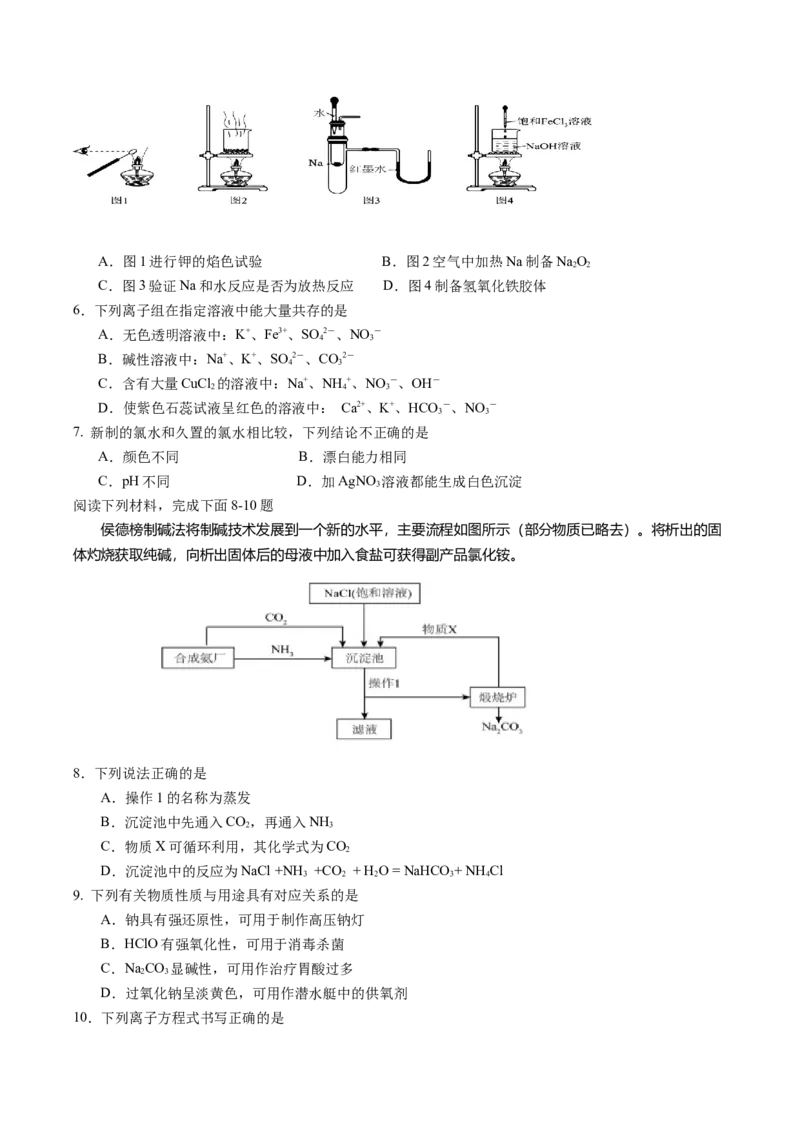
5.用下列装置或操作进行相应实验,能达到实验目的的是A.图1进行钾的焰色试验 B.图2空气中加热Na制备NaO
2 2
C.图3验证Na和水反应是否为放热反应 D.图4制备氢氧化铁胶体
6.下列离子组在指定溶液中能大量共存的是
A.无色透明溶液中:K+、Fe3+、SO 2-、NO -
4 3
B.碱性溶液中:Na+、K+、SO 2-、CO2-
4 3
C.含有大量CuCl 的溶液中:Na+、NH +、NO -、OH-
2 4 3
D.使紫色石蕊试液呈红色的溶液中: Ca2+、K+、HCO -、NO -
3 3
7. 新制的氯水和久置的氯水相比较,下列结论不正确的是
A.颜色不同 B.漂白能力相同
C.pH不同 D.加AgNO 溶液都能生成白色沉淀
3
阅读下列材料,完成下面8-10题
侯德榜制碱法将制碱技术发展到一个新的水平,主要流程如图所示(部分物质已略去)。将析出的固
体灼烧获取纯碱,向析出固体后的母液中加入食盐可获得副产品氯化铵。
8.下列说法正确的是
A.操作1的名称为蒸发
B.沉淀池中先通入CO,再通入NH
2 3
C.物质X可循环利用,其化学式为CO
2
D.沉淀池中的反应为NaCl +NH +CO + H O = NaHCO + NH Cl
3 2 2 3 4
9. 下列有关物质性质与用途具有对应关系的是
A.钠具有强还原性,可用于制作高压钠灯
B.HClO有强氧化性,可用于消毒杀菌
C.NaCO 显碱性,可用作治疗胃酸过多
2 3
D.过氧化钠呈淡黄色,可用作潜水艇中的供氧剂
10.下列离子方程式书写正确的是A.NaHCO 与稀盐酸发生反应:CO2-+2H+ = HO+CO↑
3 3 2 2
B.向澄清石灰水中滴加少量小苏打溶液:
Ca2++2OH−+2HCO −=CaCO ↓+CO 2-+2H O
3 3 3 2
C.氯气和水的反应:Cl 2 + H 2 O ⇌ 2H++Cl-+ ClO-
D.实验室制取氯气:MnO +4H++2Cl-=====Mn2++Cl↑+2HO
2 2 2
11.下列物质的转化在给定条件下能实现的是
A.
B.NaCl(aq) 漂白粉
C.
D.
12.高铁酸钠(NaFeO )是一种新型绿色消毒剂。工业上制备高铁酸钠的反应原理为:
4
3ClO-+2Fe3++10OH-=2FeO2-+3Cl-+5HO,下列有关说法正确的是
4 2
A.反应物中氧化剂是Fe3+ B.Cl-是氧化产物
C.氧化性:ClO->FeO2- D.反应中消耗3个ClO-,转移3个电子
4
13. 在酸性溶液中,下列物质氧化KI时,自身发生如下变化:Fe3+→Fe2+;MnO -→Mn2+;Cl→Cl-;
4 2
ClO -→Cl-。如果分别用相等数目的这些微粒氧化足量的KI,得到I 最少是
3 2
A.Fe3+ B.MnO - C.Cl D.ClO -
4 2 3
14.下列实验方案能达到实验目的的是
选项 实验目的 实验方案
向等浓度等体积的盐酸中分别逐滴滴加等浓度的
A 鉴别NaCO 和NaHCO 溶液
2 3 3 NaCO 和NaHCO 溶液,观察产生气泡的快慢
2 3 3
B 除去Cl 中的HCl气体 通入盛有饱和NaHCO 溶液的洗瓶
2 3
C 除去 FeSO 溶液中的 CuSO 加入过量铁粉并过滤
4 4
D 除去NaCl固体中的NaHCO 加热
3
A.A B.B C.C D.D
15.利用NaClO和尿素[CO(NH)](氮元素化合价为-3价)反应制备NH·H O (水合肼)的实验流程如图所
2 2 2 4 2
示:
已知:①氯气与烧碱溶液的反应是放热反应;
②N H·H O有强还原性,能与NaClO剧烈反应生成N。
2 4 2 2下列说法不正确的是
A.步骤I中为避免温度过高,可采用冰水浴
B.步骤I制备NaClO溶液时,若溶液中NaClO与副产物NaClO 的个数之比为5∶1,则参与反应的氧
3
化剂与还原剂的个数之比为5∶3
C.步骤II生成水合肼反应中NaClO作为氧化剂
D.步骤II中可将尿素水溶液逐滴滴入NaClO碱性溶液中
16.天然气是应用广泛的燃料,但含有少量HS等气体。在酸性溶液中利用硫杆菌可实
2
现天然气的催化脱硫,其原理如图所示。下列说法不正确的是
A.该脱硫过程需要不断添加Fe (SO ) 溶液
2 4 3
B.过程甲中氧化产物与还原产物的化学计量数之比为1:2
C.过程乙发生反应的离子方程式为:
4Fe2++O+4H+ = 4Fe3++2HO
2 2
D.脱硫过程的总反应为2HS+O=2S↓+2H O(反应条件省略)
2 2 2
二、非选择题:共3题,共52分。
17.Ⅰ.分类是研究物质性质的重要方法,图中对某些物质进行分类。回答下列问题:
(1) Ba(OH) 在水溶液中的电离方程式为 ▲ 。
2
(2)已知MgO不能与碱反应。它与稀HSO 反应的离子方程式为 ▲ ;由此可推断MgO
2 4
为 ▲ (填“酸性”或“碱性”)氧化物。
(3)NaH PO 属于 ▲ (选填“正盐”或“酸式盐”)。
2 2
Ⅱ.过氧化钙(CaO)广泛应用于水产养殖、污水处理,是优良的供氧剂。
2
(1)取适量过氧化钙放入试管中加适量水,写出该反应的化学方程式: ▲ 。
(2)此供氧剂长期暴露在空气中,会变质生成CaCO ,为检验此供氧剂是否变质,可向其中加入稀盐酸,若
3
观察到有气泡生成,则此供氧剂已变质。有同学不认同上述方案理由
是 ▲ 。
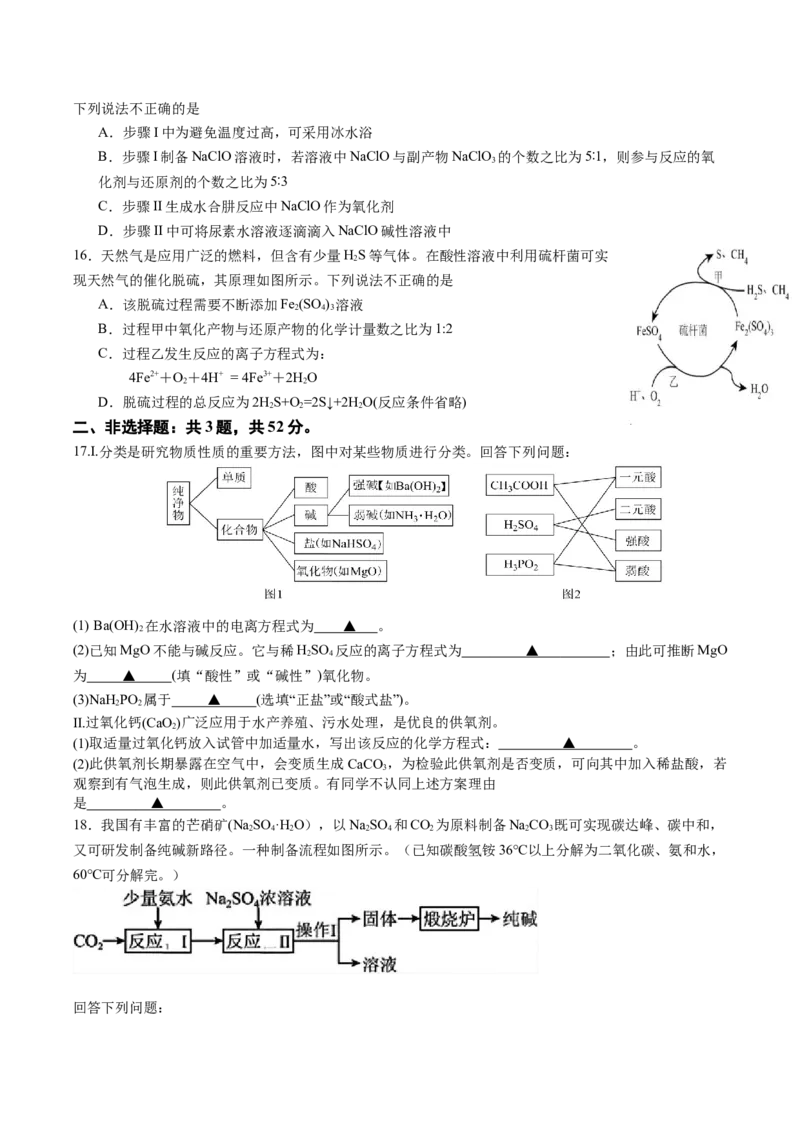
18.我国有丰富的芒硝矿(NaSO ·H O),以NaSO 和CO 为原料制备NaCO 既可实现碳达峰、碳中和,
2 4 2 2 4 2 2 3
又可研发制备纯碱新路径。一种制备流程如图所示。(已知碳酸氢铵36℃以上分解为二氧化碳、氨和水,
60℃可分解完。)
回答下列问题:(1)反应Ⅰ生成NH HCO 的离子方程式为 ▲ 。
4 3
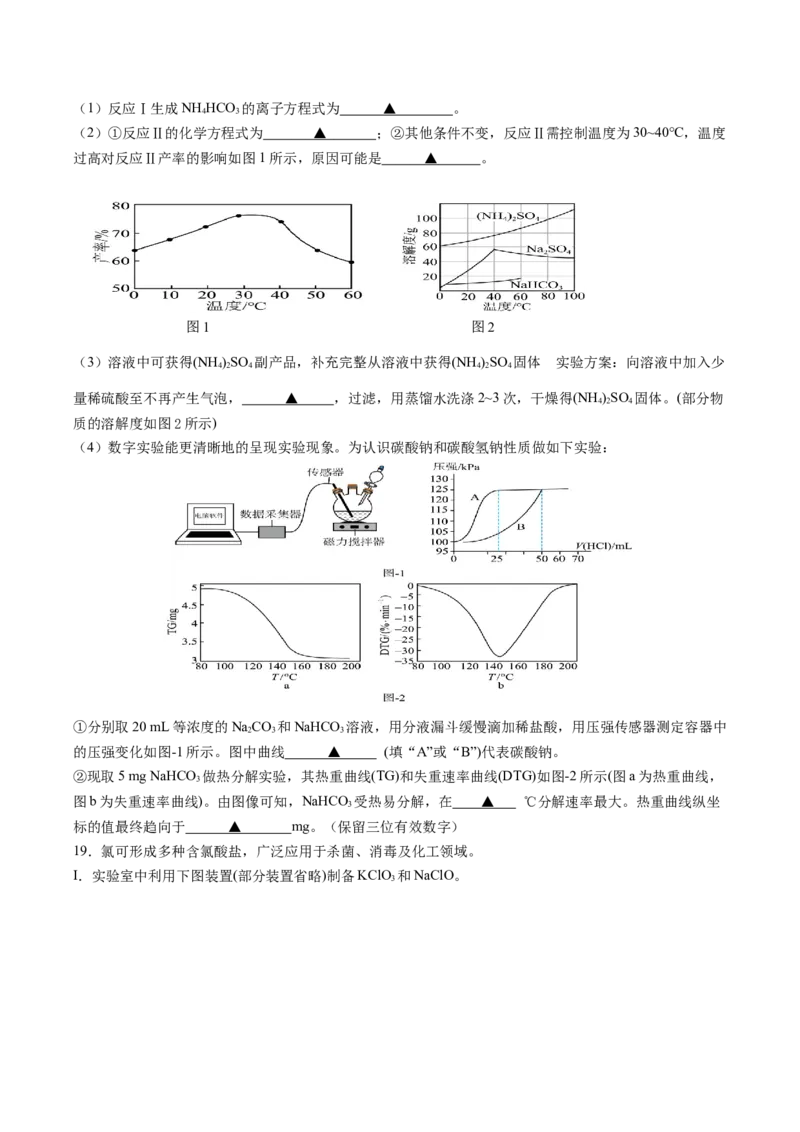
(2)①反应Ⅱ的化学方程式为 ▲ ;②其他条件不变,反应Ⅱ需控制温度为30~40℃,温度
过高对反应Ⅱ产率的影响如图1所示,原因可能是 ▲ 。
图1 图2
的
(3)溶液中可获得(NH )SO 副产品,补充完整从溶液中获得(NH )SO 固体 实验方案:向溶液中加入少
4 2 4 4 2 4
量稀硫酸至不再产生气泡, ▲ ,过滤,用蒸馏水洗涤2~3次,干燥得(NH )SO 固体。(部分物
4 2 4
质的溶解度如图2所示)
(4)数字实验能更清晰地的呈现实验现象。为认识碳酸钠和碳酸氢钠性质做如下实验:
①分别取20 mL等浓度的NaCO 和NaHCO 溶液,用分液漏斗缓慢滴加稀盐酸,用压强传感器测定容器中
2 3 3
的压强变化如图-1所示。图中曲线 ▲ (填“A”或“B”)代表碳酸钠。
②现取5 mg NaHCO 做热分解实验,其热重曲线(TG)和失重速率曲线(DTG)如图-2所示(图a为热重曲线,
3
图b为失重速率曲线)。由图像可知,NaHCO 受热易分解,在 ▲ ℃分解速率最大。热重曲线纵坐
3
标的值最终趋向于 ▲ mg。(保留三位有效数字)
19.氯可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。
I.实验室中利用下图装置(部分装置省略)制备KClO 和NaClO。
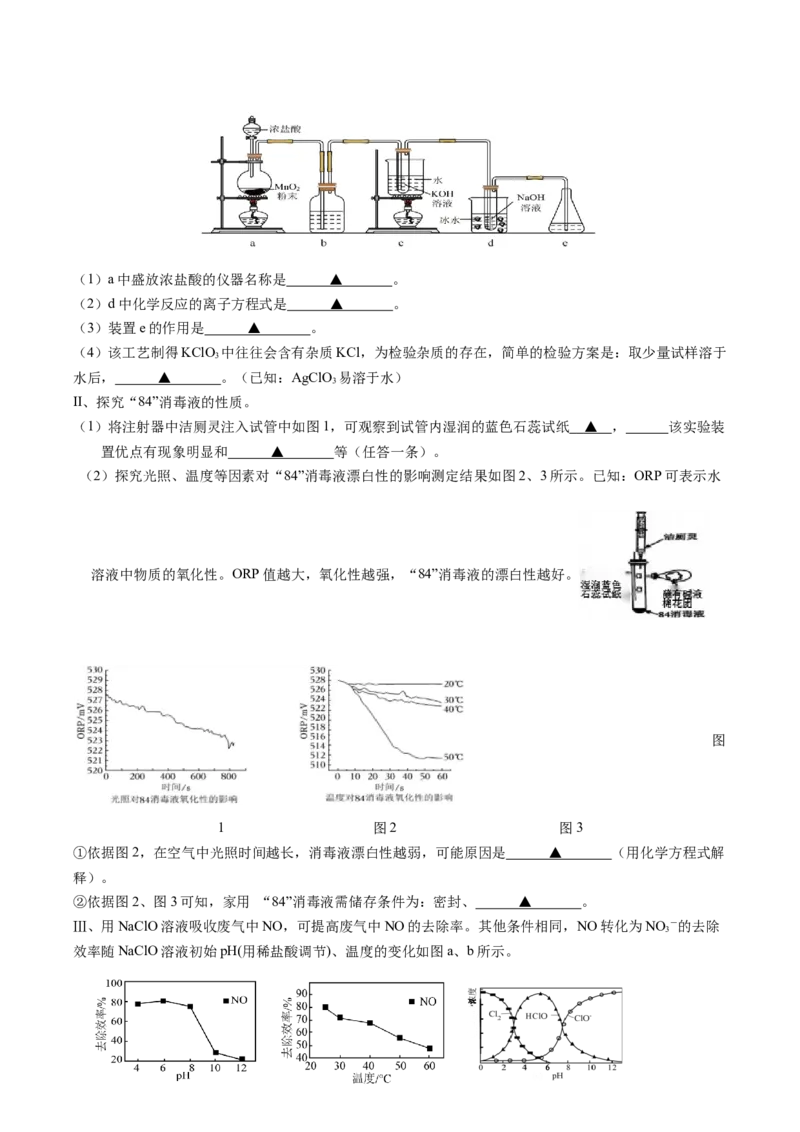
3(1)a中盛放浓盐酸的仪器名称是 ▲ 。
(2)d中化学反应的离子方程式是 ▲ 。
(3)装置e的作用是 ▲ 。
(4)该工艺制得KClO 中往往会含有杂质KCl,为检验杂质的存在,简单的检验方案是:取少量试样溶于
3
水后, ▲ 。(已知:AgClO 易溶于水)
3
Ⅱ、探究“84”消毒液的性质。
(1)将注射器中洁厕灵注入试管中如图1,可观察到试管内湿润的蓝色石蕊试纸 ▲ , 该实验装
置优点有现象明显和 ▲ 等(任答一条)。
(2)探究光照、温度等因素对“84”消毒液漂白性的影响测定结果如图2、3所示。已知:ORP可表示水
溶液中物质的氧化性。ORP值越大,氧化性越强,“84”消毒液的漂白性越好。
图
1 图2 图3
①依据图2,在空气中光照时间越长,消毒液漂白性越弱,可能原因是 ▲ (用化学方程式解
释)。
②依据图2、图3可知,家用 “84”消毒液需储存条件为:密封、 ▲ 。
Ⅲ、用NaClO溶液吸收废气中NO,可提高废气中NO的去除率。其他条件相同,NO转化为NO -的去除
3
效率随NaClO溶液初始pH(用稀盐酸调节)、温度的变化如图a、b所示。图a 图b 图c
已知:次氯酸盐溶解在水中有三种不同的存在形式,分别是Cl、ClO-和HClO,其含量与pH的关系如图
2
c所示。HClO的氧化性大于ClO- 。
(1)在酸性的NaClO溶液中,HClO氧化NO生成Cl-和NO - ,其离子方程式
3
为 ▲ 。
的
(2)当NaClO溶液 初始pH>6,NO去除率下降的原因可能是 ▲ 。
(3)当温度高于25℃,NO去除率下降的原因可能是 ▲ 。1 2 3 4 5 6 7 8
A B D C C B B C
9 10 11 12 13 14 15 16
B D B C A C D A
化学方程式2分:反应物和产物写对得1分,其它条件1分(反应条件、↑、↓)
化学方程式3分:反应物和产物写对得2分,其它条件1分(反应条件、↑、↓)
17(12分)
I(1)Ba(OH) =Ba2++2OH-(2分) (2) MgO+2H+=Mg2++H O(2分) 碱性(2分)
2 2
(3) 正盐(2分)
II(1)2CaO+2HO===2Ca(OH) +O↑ (2分)
2 2 2 2
(2)因为稀盐酸(或稀盐酸中的水)能和过氧化钙反应生成氧气,无法判断供氧剂是否变质(答案合理即可)
(2分)
18.(16分)
(1) NH ·H O+CO =NH++HCO−(3分)
3 2 2 4 3
(2)①NaSO +2NHHCO = 2NaHCO ↓+(NH) SO (3分)
2 4 4 3 3 4 2 4
②温度过高,NaHCO (1分)和NH HCO (1分)受热易分解,使产率降低
3 4 3
(3)蒸发浓缩(1分),降温至40℃结晶(1分,不写40℃不得分)
(4)①B(2分) ②140 (2分) 3.15(2分)
19.(24分)
I(1)分液漏斗 (2分) (2)Cl+2OH− =Cl−+ClO-+H O(3分)
2 2
(3) 吸收尾气Cl (1分),防止污染空气(1分)
2
(4) 加适量的稀硝酸,再加硝酸银(1分),若产生白色沉淀,则含有KCl(1分)
II(1)①先变红后褪色 (2分)
② 节约试剂, 产生氯气的量可控制,密闭体系无污染。(合理即得分)(2分)
(2)①2HClO2HCl+O↑(2分) ②避光、低温(2分)
2
III(1)3HClO+2NO+HO =3Cl−+2NO -+5H+(3分)
2 3
(2)随溶液的pH增大,溶液中HClO的浓度减小(1分) ,氧化能力减弱,NO的去除率下降(1分)