文档内容
关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
主题一 物质的化学变化
专题 03 质量守恒定律 化学方程式
01模拟基础练
【题型一】质量守恒定律
【题型二】化学方程式
【题型三】根据化学方程式进行简单计算
02重难创新练
03真题实战练
题型一 质量守恒定律
1.下列说法中正确的是
A.5g铁粉和5g铜粉混合,总质量为10g,符合质量守恒定律
B.煤燃烧后剩余的煤渣减轻,因此不符合质量守恒定律
C.10g水全部蒸发变成10g水蒸气,因此符合质量守恒定律
D.高锰酸钾分解后固体质量变小,符合质量守恒定律
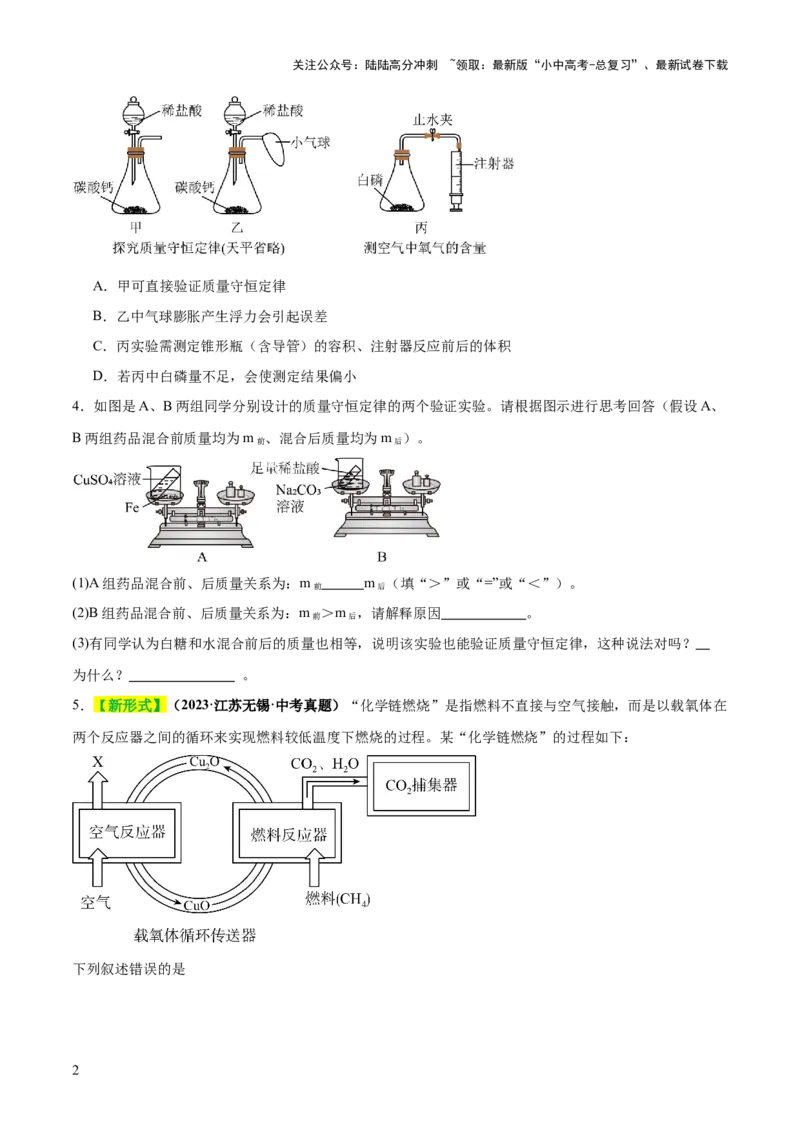
2.【新考向】某小组同学通过铜与氧气反应验证质量守恒定律(图a所示),锥形瓶中固体部分变为黑色,
实验过程中瓶内物质或元素质量变化与图b相符的是
A.铜粉的质量 B.氮气的质量 C.氧元素的质量 D.固态物质的质量
3.【新考向】(2024·陕西咸阳·一模)对下列有关实验的分析不正确的是
1关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
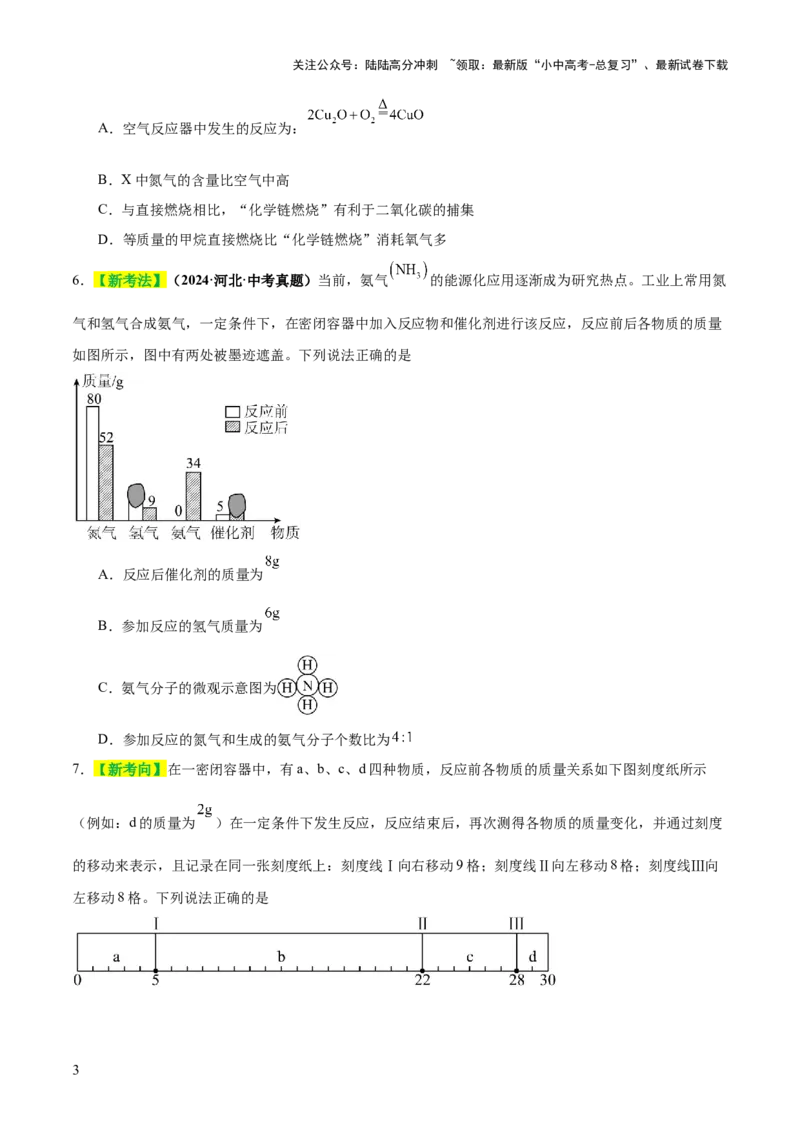
A.甲可直接验证质量守恒定律
B.乙中气球膨胀产生浮力会引起误差
C.丙实验需测定锥形瓶(含导管)的容积、注射器反应前后的体积
D.若丙中白磷量不足,会使测定结果偏小
4.如图是A、B两组同学分别设计的质量守恒定律的两个验证实验。请根据图示进行思考回答(假设A、
B两组药品混合前质量均为m 、混合后质量均为m )。
前 后
(1)A组药品混合前、后质量关系为:m m (填“>”或“=”或“<”)。
前 后
(2)B组药品混合前、后质量关系为:m >m ,请解释原因 。
前 后
(3)有同学认为白糖和水混合前后的质量也相等,说明该实验也能验证质量守恒定律,这种说法对吗?
为什么? 。
5.【新形式】(2023·江苏无锡·中考真题)“化学链燃烧”是指燃料不直接与空气接触,而是以载氧体在
两个反应器之间的循环来实现燃料较低温度下燃烧的过程。某“化学链燃烧”的过程如下:
下列叙述错误的是
2关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.空气反应器中发生的反应为:
B.X中氮气的含量比空气中高
C.与直接燃烧相比,“化学链燃烧”有利于二氧化碳的捕集
D.等质量的甲烷直接燃烧比“化学链燃烧”消耗氧气多
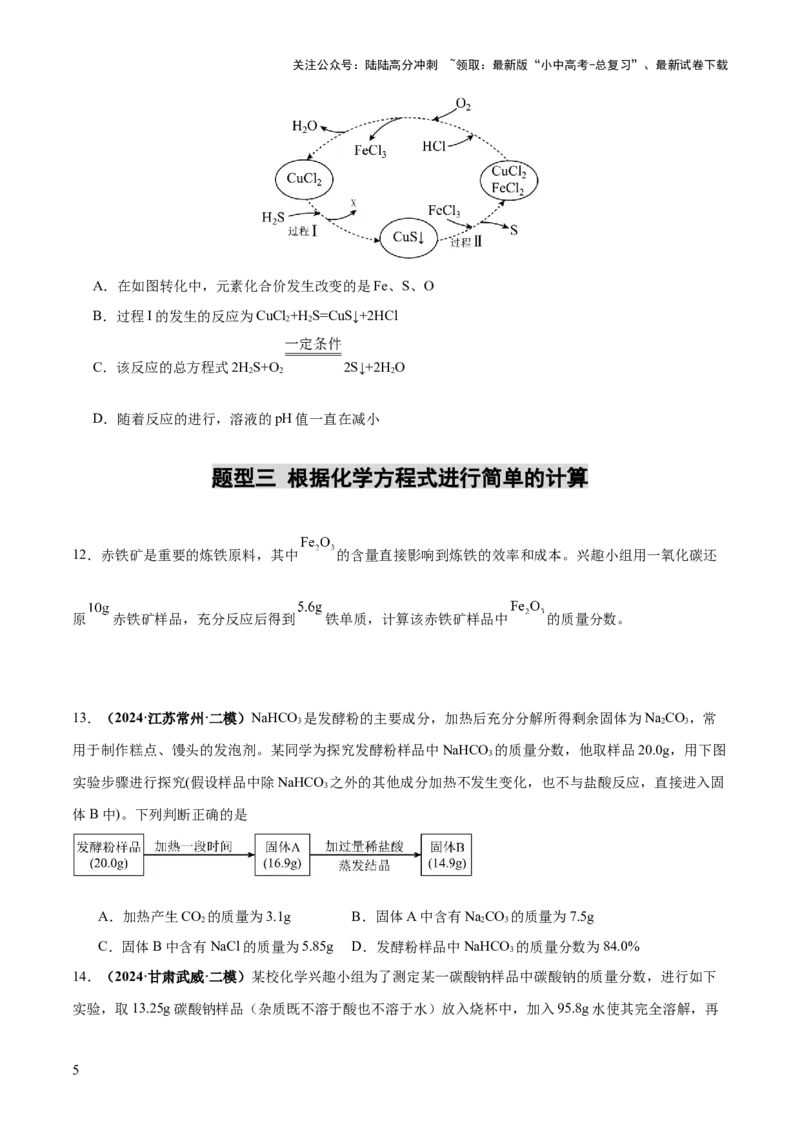
6.【新考法】(2024·河北·中考真题)当前,氨气 的能源化应用逐渐成为研究热点。工业上常用氮
气和氢气合成氨气,一定条件下,在密闭容器中加入反应物和催化剂进行该反应,反应前后各物质的质量
如图所示,图中有两处被墨迹遮盖。下列说法正确的是
A.反应后催化剂的质量为
B.参加反应的氢气质量为
C.氨气分子的微观示意图为
D.参加反应的氮气和生成的氨气分子个数比为
7.【新考向】在一密闭容器中,有a、b、c、d四种物质,反应前各物质的质量关系如下图刻度纸所示
(例如:d的质量为 )在一定条件下发生反应,反应结束后,再次测得各物质的质量变化,并通过刻度
的移动来表示,且记录在同一张刻度纸上:刻度线Ⅰ向右移动9格;刻度线Ⅱ向左移动8格;刻度线Ⅲ向
左移动8格。下列说法正确的是
3关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.反应结束后c的质量为
B.该反应为化合反应
C.a、b变化的质量比一定为
D.a、d的相对分子质量之比一定为
8.(2024·四川达州·一模)将10g碳酸钙固体高温煅烧一段时间后,停止加热,冷却后称得固体质量为
8g,再向剩余固体中加入足量稀盐酸,充分反应后,蒸发,得到固体的质量为
A.11.1g B.15.9g C.33.3g D.44.4g
题型二 化学方程式
9.【原创题】通过电能驱动的电化学固氮被认为是一种可持续发展的绿色合成氨技术。氧化铌电催化氮
气还原合成氨具备巨大潜力,反应的微观示意图如图,下列说法正确的是
A.反应前后原子和分子总数都不变
B.该反应的化学方程式为
C.反应前后三种元素的化合价均发生变化
D.参加反应的“ ”和“ ”的化学计量数之比为1:2,
10.(2024·黑龙江大庆·中考真题)下列化学方程式书写正确的是
A.氧化铝溶于稀硫酸:Al O+2H SO =2AlSO+2H O
2 3 2 4 4 2
B.铁溶于稀盐酸:2Fe+6HCl=2FeCl +3H ↑
3 2
C.氢气还原氧化铜:CuO+H=Cu+H O
2 2
D.向硫酸铜溶液中滴加少量氢氧化钠溶液:CuSO +2NaOH=Cu(OH) ↓+Na SO
4 2 2 4
11.【新考向】(2024·江苏常州·二模)HS气体剧毒,可用FeCl 、FeCl 、CuCl 的混合液处理(如图)并得
2 3 2 2
到化工原料S。下列说法不正确的是
4关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.在如图转化中,元素化合价发生改变的是Fe、S、O
B.过程I的发生的反应为CuCl +H S=CuS↓+2HCl
2 2
C.该反应的总方程式2HS+O 2S↓+2HO
2 2 2
D.随着反应的进行,溶液的pH值一直在减小
题型三 根据化学方程式进行简单的计算
12.赤铁矿是重要的炼铁原料,其中 的含量直接影响到炼铁的效率和成本。兴趣小组用一氧化碳还
原 赤铁矿样品,充分反应后得到 铁单质,计算该赤铁矿样品中 的质量分数。
13.(2024·江苏常州·二模)NaHCO 是发酵粉的主要成分,加热后充分分解所得剩余固体为NaCO,常
3 2 3
用于制作糕点、馒头的发泡剂。某同学为探究发酵粉样品中NaHCO 的质量分数,他取样品20.0g,用下图
3
实验步骤进行探究(假设样品中除NaHCO 之外的其他成分加热不发生变化,也不与盐酸反应,直接进入固
3
体B中)。下列判断正确的是
A.加热产生CO 的质量为3.1g B.固体A中含有NaCO 的质量为7.5g
2 2 3
C.固体B中含有NaCl的质量为5.85g D.发酵粉样品中NaHCO 的质量分数为84.0%
3
14.(2024·甘肃武威·二模)某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下
实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再
5关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
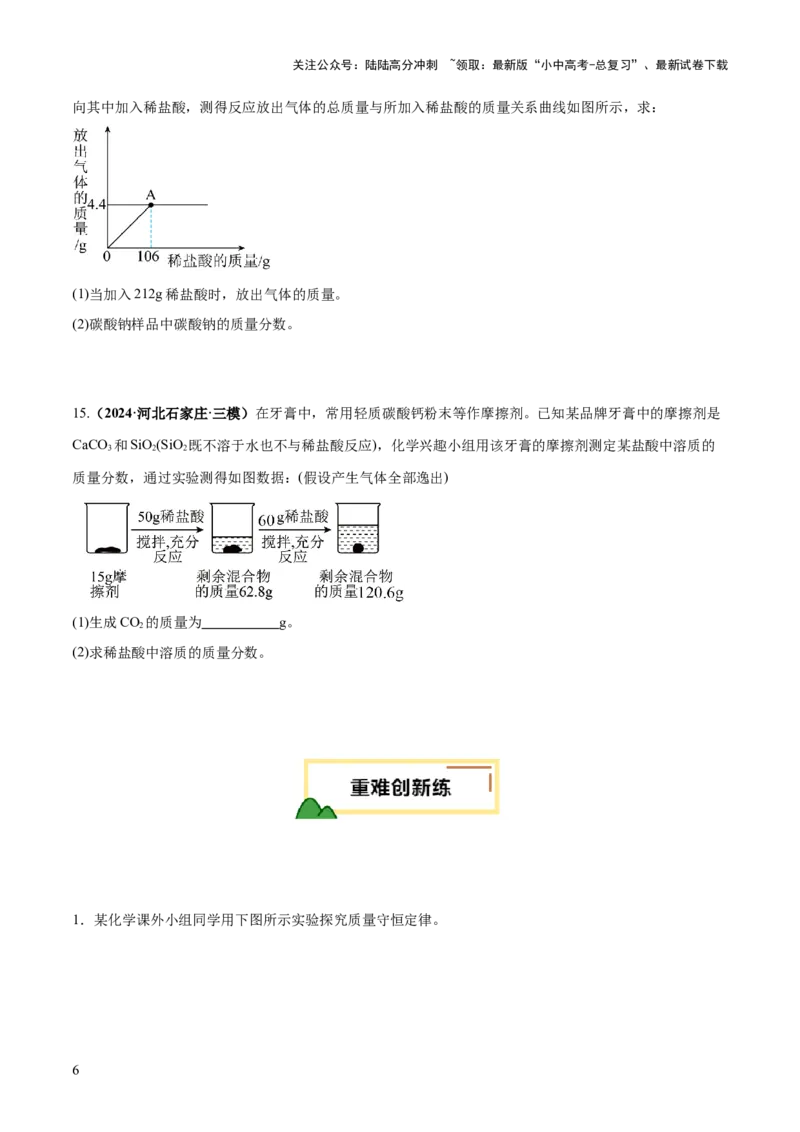
向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如图所示,求:
(1)当加入212g稀盐酸时,放出气体的质量。
(2)碳酸钠样品中碳酸钠的质量分数。
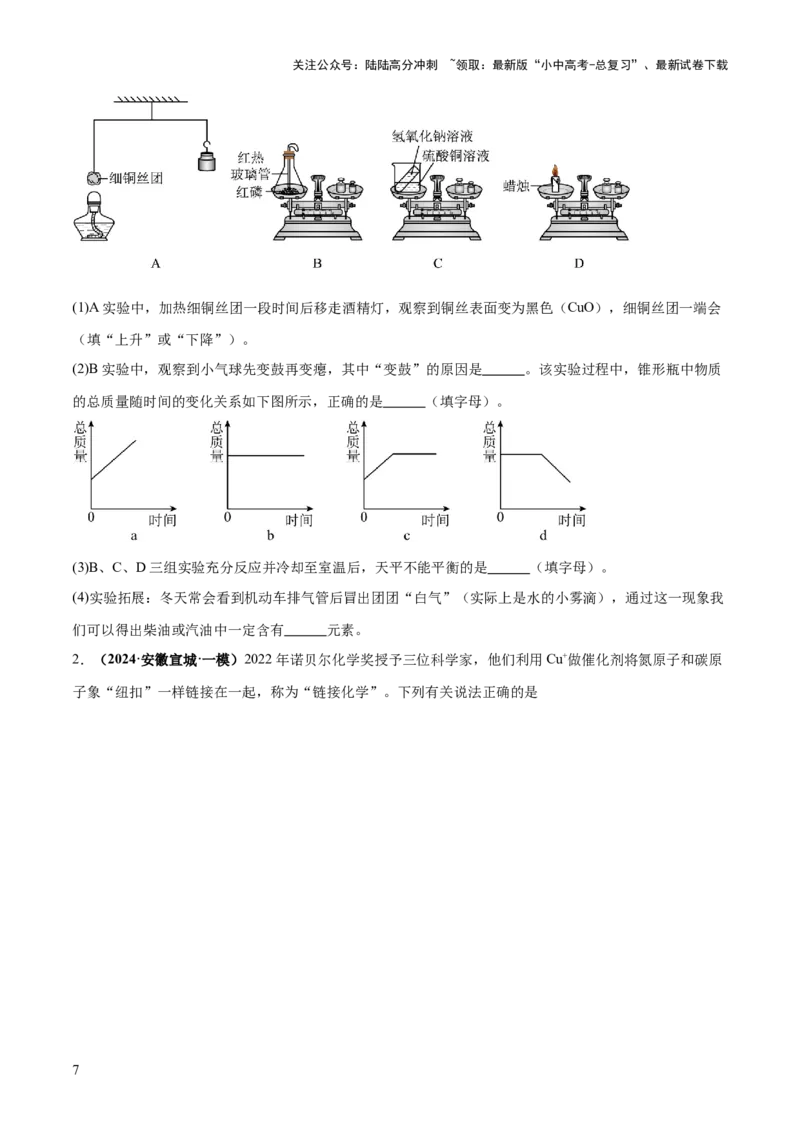
15.(2024·河北石家庄·三模)在牙膏中,常用轻质碳酸钙粉末等作摩擦剂。已知某品牌牙膏中的摩擦剂是
CaCO 和SiO(SiO 既不溶于水也不与稀盐酸反应),化学兴趣小组用该牙膏的摩擦剂测定某盐酸中溶质的
3 2 2
质量分数,通过实验测得如图数据:(假设产生气体全部逸出)
(1)生成CO 的质量为 g。
2
(2)求稀盐酸中溶质的质量分数。
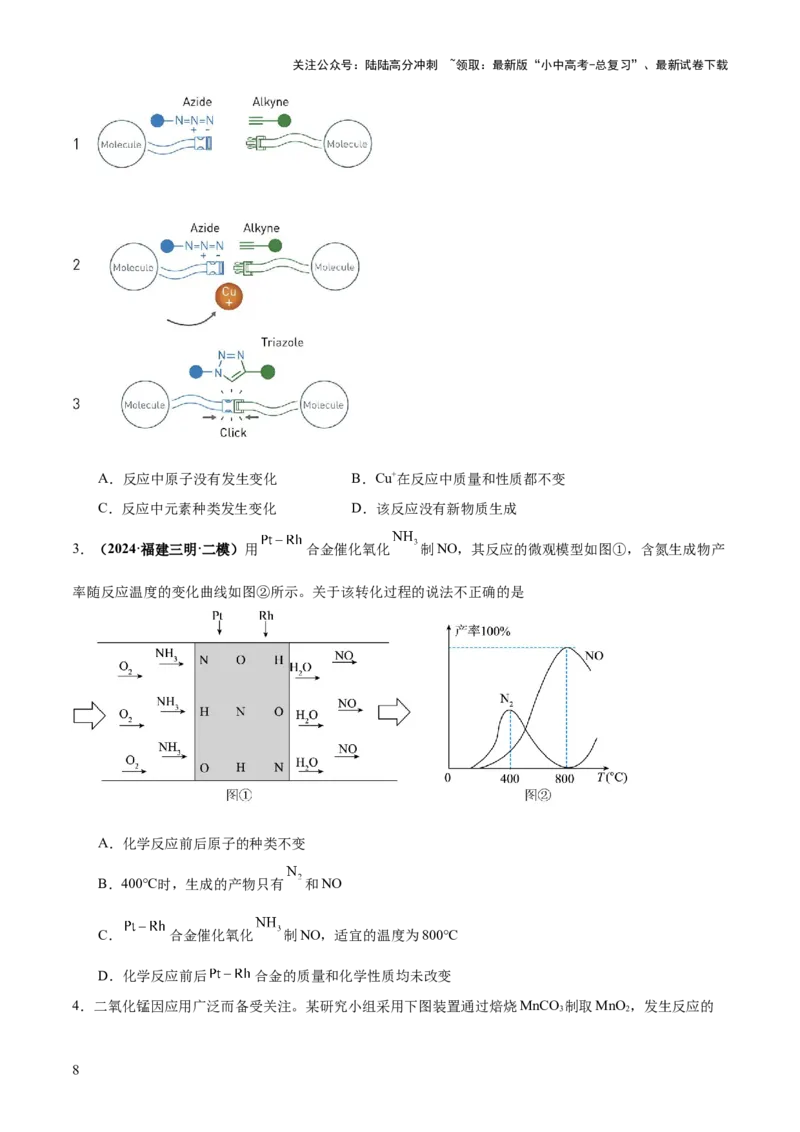
1.某化学课外小组同学用下图所示实验探究质量守恒定律。
6关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
(1)A实验中,加热细铜丝团一段时间后移走酒精灯,观察到铜丝表面变为黑色(CuO),细铜丝团一端会
(填“上升”或“下降”)。
(2)B实验中,观察到小气球先变鼓再变瘪,其中“变鼓”的原因是 。该实验过程中,锥形瓶中物质
的总质量随时间的变化关系如下图所示,正确的是 (填字母)。
(3)B、C、D三组实验充分反应并冷却至室温后,天平不能平衡的是 (填字母)。
(4)实验拓展:冬天常会看到机动车排气管后冒出团团“白气”(实际上是水的小雾滴),通过这一现象我
们可以得出柴油或汽油中一定含有 元素。
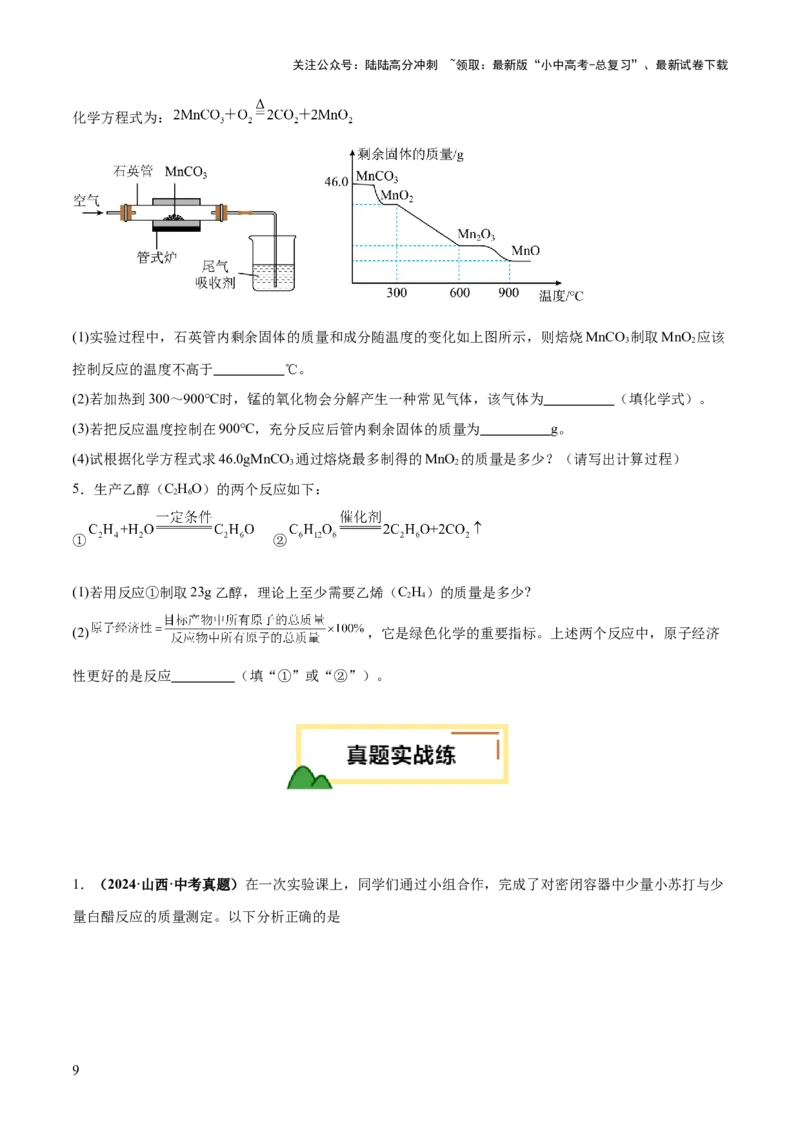
2.(2024·安徽宣城·一模)2022年诺贝尔化学奖授予三位科学家,他们利用Cu+做催化剂将氮原子和碳原
子象“纽扣”一样链接在一起,称为“链接化学”。下列有关说法正确的是
7关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.反应中原子没有发生变化 B.Cu+在反应中质量和性质都不变
C.反应中元素种类发生变化 D.该反应没有新物质生成
3.(2024·福建三明·二模)用 合金催化氧化 制NO,其反应的微观模型如图①,含氮生成物产
率随反应温度的变化曲线如图②所示。关于该转化过程的说法不正确的是
A.化学反应前后原子的种类不变
B.400℃时,生成的产物只有 和NO
C. 合金催化氧化 制NO,适宜的温度为800℃
D.化学反应前后 合金的质量和化学性质均未改变
4.二氧化锰因应用广泛而备受关注。某研究小组采用下图装置通过焙烧MnCO 制取MnO ,发生反应的
3 2
8关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
化学方程式为:
(1)实验过程中,石英管内剩余固体的质量和成分随温度的变化如上图所示,则焙烧MnCO 制取MnO 应该
3 2
控制反应的温度不高于 ℃。
(2)若加热到300~900℃时,锰的氧化物会分解产生一种常见气体,该气体为 (填化学式)。
(3)若把反应温度控制在900℃,充分反应后管内剩余固体的质量为 g。
(4)试根据化学方程式求46.0gMnCO 通过熔烧最多制得的MnO 的质量是多少?(请写出计算过程)
3 2
5.生产乙醇(C HO)的两个反应如下:
2 6
① ②
(1)若用反应①制取23g乙醇,理论上至少需要乙烯(C H)的质量是多少?
2 4
(2) ,它是绿色化学的重要指标。上述两个反应中,原子经济
性更好的是反应 (填“①”或“②”)。
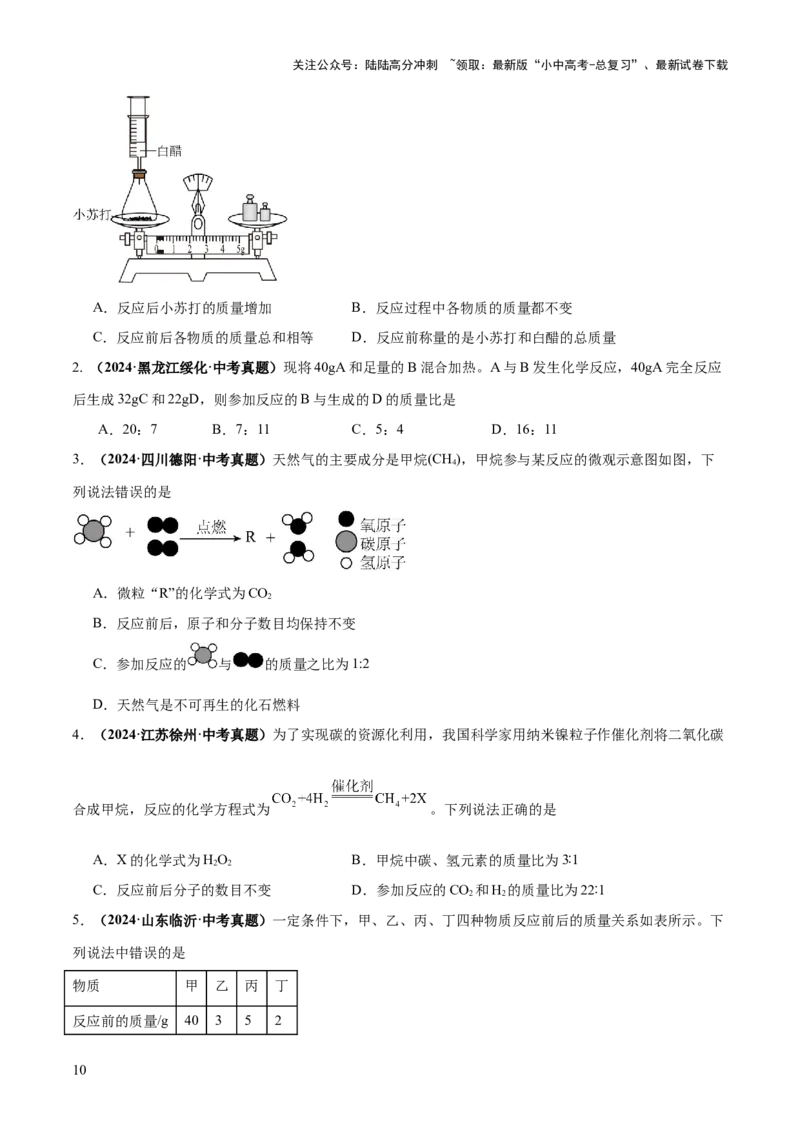
1.(2024·山西·中考真题)在一次实验课上,同学们通过小组合作,完成了对密闭容器中少量小苏打与少
量白醋反应的质量测定。以下分析正确的是
9关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
A.反应后小苏打的质量增加 B.反应过程中各物质的质量都不变
C.反应前后各物质的质量总和相等 D.反应前称量的是小苏打和白醋的总质量
2. (2024·黑龙江绥化·中考真题)现将40gA和足量的B混合加热。A与B发生化学反应,40gA完全反应
后生成32gC和22gD,则参加反应的B与生成的D的质量比是
A.20:7 B.7:11 C.5:4 D.16:11
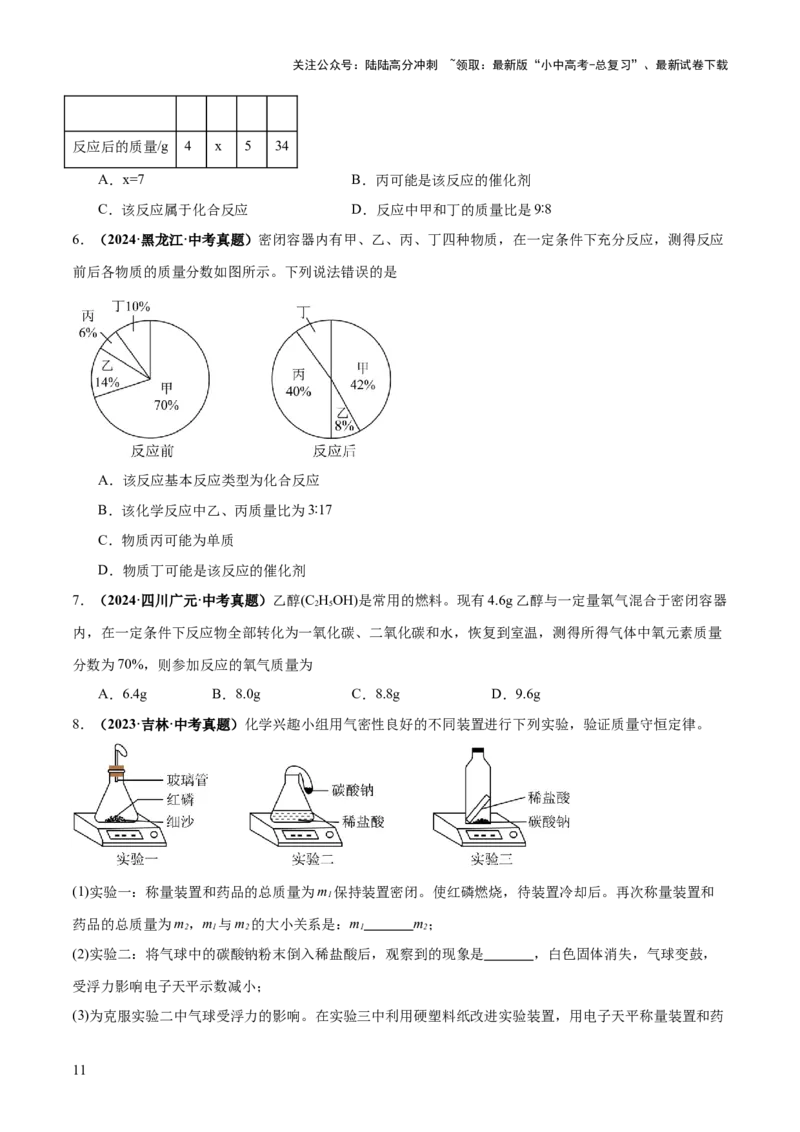
3.(2024·四川德阳·中考真题)天然气的主要成分是甲烷(CH),甲烷参与某反应的微观示意图如图,下
4
列说法错误的是
A.微粒“R”的化学式为CO
2
B.反应前后,原子和分子数目均保持不变
C.参加反应的 与 的质量之比为1:2
D.天然气是不可再生的化石燃料
4.(2024·江苏徐州·中考真题)为了实现碳的资源化利用,我国科学家用纳米镍粒子作催化剂将二氧化碳
合成甲烷,反应的化学方程式为 。下列说法正确的是
A.X的化学式为HO B.甲烷中碳、氢元素的质量比为3∶1
2 2
C.反应前后分子的数目不变 D.参加反应的CO 和H 的质量比为22∶1
2 2
5.(2024·山东临沂·中考真题)一定条件下,甲、乙、丙、丁四种物质反应前后的质量关系如表所示。下
列说法中错误的是
物质 甲 乙 丙 丁
反应前的质量/g 40 3 5 2
10关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
反应后的质量/g 4 x 5 34
A.x=7 B.丙可能是该反应的催化剂
C.该反应属于化合反应 D.反应中甲和丁的质量比是9∶8
6.(2024·黑龙江·中考真题)密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应
前后各物质的质量分数如图所示。下列说法错误的是
A.该反应基本反应类型为化合反应
B.该化学反应中乙、丙质量比为3∶17
C.物质丙可能为单质
D.物质丁可能是该反应的催化剂
7.(2024·四川广元·中考真题)乙醇(C HOH)是常用的燃料。现有4.6g乙醇与一定量氧气混合于密闭容器
2 5
内,在一定条件下反应物全部转化为一氧化碳、二氧化碳和水,恢复到室温,测得所得气体中氧元素质量
分数为70%,则参加反应的氧气质量为
A.6.4g B.8.0g C.8.8g D.9.6g
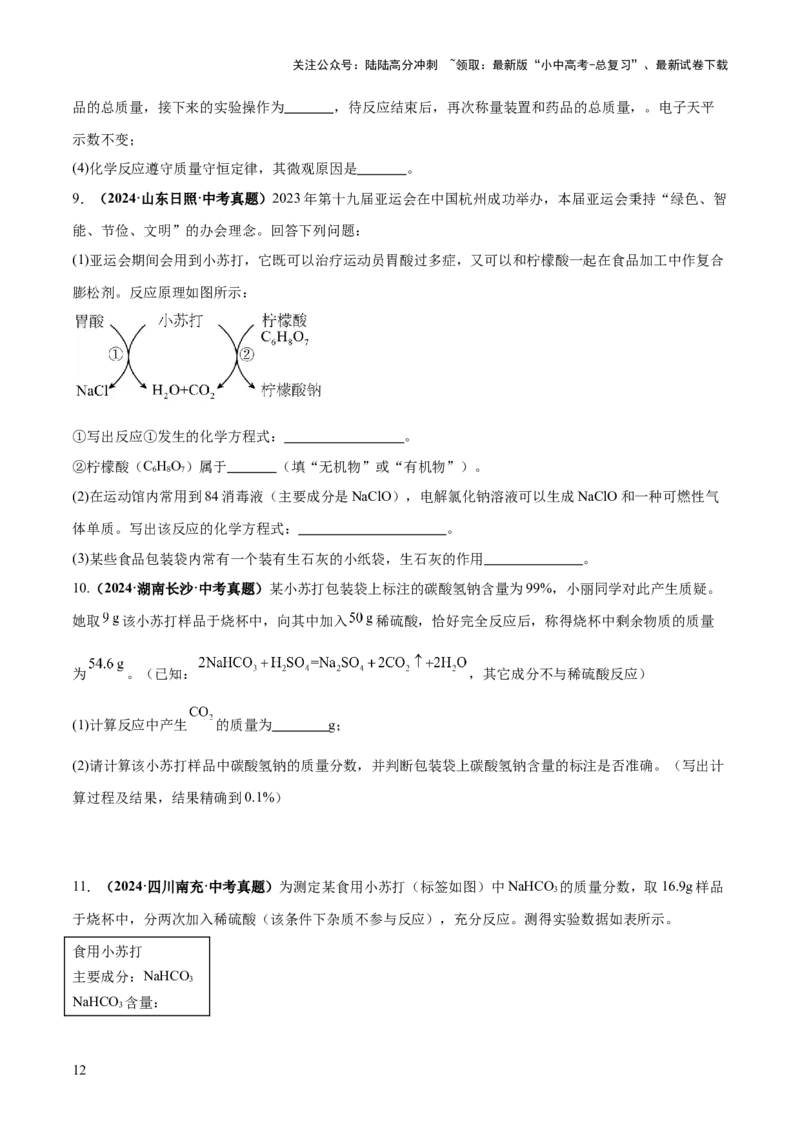
8.(2023·吉林·中考真题)化学兴趣小组用气密性良好的不同装置进行下列实验,验证质量守恒定律。
(1)实验一:称量装置和药品的总质量为m 保持装置密闭。使红磷燃烧,待装置冷却后。再次称量装置和
1
药品的总质量为m,m 与m 的大小关系是:m m;
2 1 2 1 2
(2)实验二:将气球中的碳酸钠粉末倒入稀盐酸后,观察到的现象是 ,白色固体消失,气球变鼓,
受浮力影响电子天平示数减小;
(3)为克服实验二中气球受浮力的影响。在实验三中利用硬塑料纸改进实验装置,用电子天平称量装置和药
11关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
品的总质量,接下来的实验操作为 ,待反应结束后,再次称量装置和药品的总质量,。电子天平
示数不变;
(4)化学反应遵守质量守恒定律,其微观原因是 。
9.(2024·山东日照·中考真题)2023年第十九届亚运会在中国杭州成功举办,本届亚运会秉持“绿色、智
能、节俭、文明”的办会理念。回答下列问题:
(1)亚运会期间会用到小苏打,它既可以治疗运动员胃酸过多症,又可以和柠檬酸一起在食品加工中作复合
膨松剂。反应原理如图所示:
①写出反应①发生的化学方程式: 。
②柠檬酸(C HO)属于 (填“无机物”或“有机物”)。
6 8 7
(2)在运动馆内常用到84消毒液(主要成分是NaClO),电解氯化钠溶液可以生成NaClO和一种可燃性气
体单质。写出该反应的化学方程式: 。
(3)某些食品包装袋内常有一个装有生石灰的小纸袋,生石灰的作用 。
10.(2024·湖南长沙·中考真题)某小苏打包装袋上标注的碳酸氢钠含量为99%,小丽同学对此产生质疑。
她取 该小苏打样品于烧杯中,向其中加入 稀硫酸,恰好完全反应后,称得烧杯中剩余物质的质量
为 。(已知: ,其它成分不与稀硫酸反应)
(1)计算反应中产生 的质量为 g;
(2)请计算该小苏打样品中碳酸氢钠的质量分数,并判断包装袋上碳酸氢钠含量的标注是否准确。(写出计
算过程及结果,结果精确到0.1%)
11.(2024·四川南充·中考真题)为测定某食用小苏打(标签如图)中NaHCO 的质量分数,取16.9g样品
3
于烧杯中,分两次加入稀硫酸(该条件下杂质不参与反应),充分反应。测得实验数据如表所示。
食用小苏打
主要成分:NaHCO
3
NaHCO 含量:
3
12关注公众号:陆陆高分冲刺 ~领取:最新版“小中高考-总复习”、最新试卷下载
≥99%
加入稀硫酸的次数 第一次 第二次
加入稀硫酸的质量/g 50.0 50.0
生成气体的质量/g 5.0 3.8
(1)两次加稀硫酸后,生成二氧化碳的总质量是 g。
(2)通过计算说明样品中NaHCO 含量与标签是否相符(写出计算过程)。(反应的化学方程式为:
3
)
13