文档内容
D.甲增加0.1 mol H ,乙增加0.1 mol I
2009 年北京市高考化学试卷 2 2
6.(5分)甲、乙、丙、丁4中物质分别含2种或3种元素,它们的分子中各含18个电子.甲是
一、选择题(共8小题,每小题5分,满分40分)
气态氢化物,在水中分步电离出两种阴离子.下列推断合理的是( )
1.(5分)化学与人类生活密切相关.下列说法正确的是( )
A.某钠盐溶液含甲电离出的阴离子,则该溶液显碱性,只能与酸反应
A.苯酚有一定毒性,不能作消毒剂和防腐剂
B.乙与氧气的摩尔质量相同,则乙一定含有极性键和非极性键
B.白磷着火点高且无毒,可用于制造安全火柴
C.丙中含有二周期IVA族的元素,则丙一定是甲烷的同系物
C.油脂皂化生成的高级脂肪酸钠是肥皂的有效成分
D.丁和甲中各元素质量比相同,则丁中一定含有﹣1价的元素
D.用食醋去除水壶中的水垢时所发生的是水解反应
7.(5分)有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①CH COONa与HCl;
3
2.(5分)下列叙述不正确的是( )
②CH COONa与NaOH;③CH COONa与NaCl;④CH COONa与NaClO 下列各项排序正确的是(
3 3 3
A.铁表面镀锌,铁作阳极
)
B.船底镶嵌锌块,锌作负极,以防船体被腐蚀
A.pH:②>③>④>① B.c(CH COO﹣):②>④>③>①
3
C.钢铁吸氧腐蚀的正极反应:O +2H O+4e﹣=4OH﹣
2 2 C.溶液中c(H+):①>③>②>④ D.c(CH COOH):①>④>③>②
3
D.工业上电解饱和食盐水的阳极反应:2Cl﹣﹣2e﹣=Cl
2 8.(5分)由短周期元素组成的中学常见无机物 A、B、C、D、E、X 存在如在右图转化关系(部
3.(5分)W、X、Y、Z均为短周期元素,W的最外层电子数与核外电子总数之比为 7:17;X与
分生成物和反应条件略去)下列推断不正确的是( )
W同主族;Y的原子序数是W和X的原子序数之和的一半;含 Z元素的物质焰色反应为黄色.
下列判断正确的是( )
A.金属性:Y>Z B.氢化物的沸点:X>W
C.离子的还原性:X>W D.原子及离子半径:Z>Y>X
A.若X是Na CO ,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应
2 3
4.(5分)下列叙述正确的是( )
B.若A是单质,B和D的反应是OH﹣+HCO ﹣=H O+CO 2,则E一定能还原Fe O
3 2 3 2 3
A.将CO 通入BaCl 溶液中至饱和,无沉淀产生;再通入SO ,产生沉淀
2 2 2
C.若D为CO,C能和E反应,则A一定为Na O ,其电子式是
2 2
B.在稀硫酸中加入铜粉,铜粉不溶解;再加入Cu(NO ) 固体,铜粉仍不溶
3 2
C.向AlCl 溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO 溶液,沉淀消失 D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
3 4
D.纯锌与稀硫酸反应产生氢气的速率较慢;再加入少量CuSO 固体,速率不改变
4
5.(5分)已知:H (g)+I (g) 2HI(g);△H<0.有相同容积的定容密闭容器甲和乙,甲
2 2
中加入H 和I 各0.1mol,乙中加入HI 0.2mol,相同温度下分别达到平衡。欲使甲中 HI的平衡
2 2 ⇌
浓度大于乙中HI的平衡浓度,应采取的措施是( )
A.甲、乙提高相同温度
B.甲中加入0.1 mol He,乙不变
C.甲降低温度,乙不变二、解答题(共4小题,满分60分) Ⅱ.将FeSO •7H O配制成溶液.
4 2
9.(16分)丙烯可用于合成杀除根瘤线虫的农药(分子式为C H Br Cl)和应用广泛的DAP树脂: Ⅲ.FeSO 溶液与稍过量的NH HCO 溶液混合,得到含FeCO 的浊液.
3 5 2 4 4 3 3
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到FeCO 固体.
3
V.煅烧FeCO ,得到Fe O 固体.
3 2 3
已知:NH HC0 在热水中分解.
4 3
(1)Ⅰ中,加足量的铁屑除去废液中的Fe3+,该反应的离子方程式是 .
(2)Ⅱ中,需加一定量硫酸.运用化学平衡原理简述硫酸的作用 .
(3)Ⅲ中,生成FeCO 的离子方程式是 .若FeCO 浊液长时间暴露在空气中,会有部分固
3 3
体表面变为红褐色,该变化的化学方程式是 .
已知酯与醇可发生如下酯交换反应:
(4)IV中,通过检验SO 2﹣来判断沉淀是否洗涤干净.检验SO 2的操作是 .
4 4
RCOOR′+R″OH RCOOR″+R′OH (R、R′、R″代表烃基)
(5)已知煅烧FeCO 的化学方程式是 4FeCO +O 2Fe O +4CO .现煅烧464.0kg的FeCO ,
3 3 2 2 3 2 3
(1)农药分子C H Br Cl中每个碳原子上均连有卤原子.
3 5 2
得到316.8kg 产品.若产品中杂质只有 FeO,则该产品中 Fe O 的质量是 Kg.(摩尔质
2 3
①A的结构简式是 ,A含有的官能团名称是 ;
量/g•mol﹣1:FeC0 116 Fe 0 160 Fe0 72)
②由丙烯生成A的反应类型是 . 3 2 3
11.(14分)某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器
(2)A水解可得到D,该水解反应的化学方程式是 .
已略去).实验表明浓硝酸能将NO氧化成NO ,而稀硝酸不能氧化NO.由此得出的结论是浓
2
(3)C蒸气密度是相同状态下甲烷密度的 6.25倍,C中各元素的质量分数分别为:碳 60%,氢
硝酸的氧化性强于稀硝酸.
8%,氧32%.C的结构简式是 .
(4)下列说法正确的是(选填序号字母) .
a.C能发生聚合反应、还原反应和氧化反应
b.C含有2个甲基的羧酸类同分异构体有4个
c.D催化加氢的产物与B具有相同的相对分子质量
d.E具有芳香气味,易溶于乙醇
(5)E的水解产物经分离最终得到甲醇和B,二者均可循环利用于DAP树脂的制备.其中将甲醇
与H分离的操作方法是 .
(6)F的分子式为C H O .DAP单体为苯的二元取代物,且两个取代基不处于对位,该单体苯环
10 10 4
可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
上的一溴取代物只有两种.D和F反应生成DAP单体的化学方程式是 .
已知:氢氧化钠溶液不与NO反应,能与NO 反应2NO +2NaOH=NaNO +NaNO +H O
2 2 3 2 2
10.(15分)以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
Ⅰ.从废液中提纯并结晶出FeSO •7H O.
4 2
(2)滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后(3)装置①中发生反应的化学方程式是 ①SO 既可作为生产硫酸的原料循环再利用,也可用于工业制溴过程中吸收潮湿空气中的 Br .SO
2 2 2
(4)装置②的作用是 ,发生反应的化学方程式是 吸收Br 的离子方程式是 .
2
(5)该小组得出的结论依据的试验现象是 ②为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到 50.00mL相同浓度的NaOH
(6)试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色.甲同学认为是该溶液中硝酸铜 溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解),该气体经干燥后用浓硫酸吸收
的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体.同学们分别涉及了一下 4 完全,测定浓硫酸增加的质量.
个试验来判断两种看法是否正确.这些方案中可行的是 (填序号字母,多选不给分) 部分测定结果:
a)加热该绿色溶液,观察颜色变化 铵盐质量为10.00g和20.00g时,浓硫酸增加的质量相同;
b)加水稀释绿色溶液,观察颜色变化 铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变.
c)向该绿色溶液中通入氮气,观察颜色变化 计算:该铵盐中氮元素的质量分数是 %;若铵盐质量为l5.00g,浓硫酸增加的质量为 .
d)向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化. (计算结果保留两位小数)
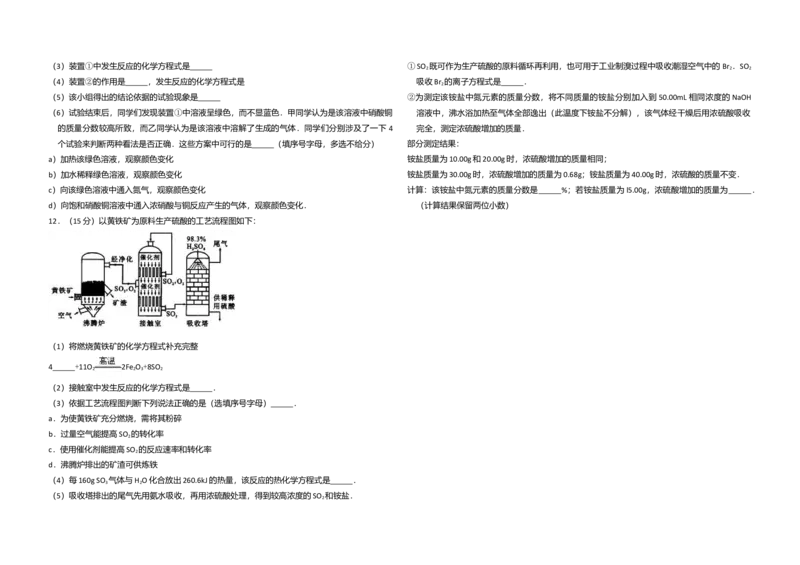
12.(15分)以黄铁矿为原料生产硫酸的工艺流程图如下:
(1)将燃烧黄铁矿的化学方程式补充完整
4 +11O 2Fe O +8SO
2 2 3 2
(2)接触室中发生反应的化学方程式是 .
(3)依据工艺流程图判断下列说法正确的是(选填序号字母) .
a.为使黄铁矿充分燃烧,需将其粉碎
b.过量空气能提高SO 的转化率
2
c.使用催化剂能提高SO 的反应速率和转化率
2
d.沸腾炉排出的矿渣可供炼铁
(4)每160g SO 气体与H O化合放出260.6kJ的热量,该反应的热化学方程式是 .
3 2
(5)吸收塔排出的尾气先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO 和铵盐.
2