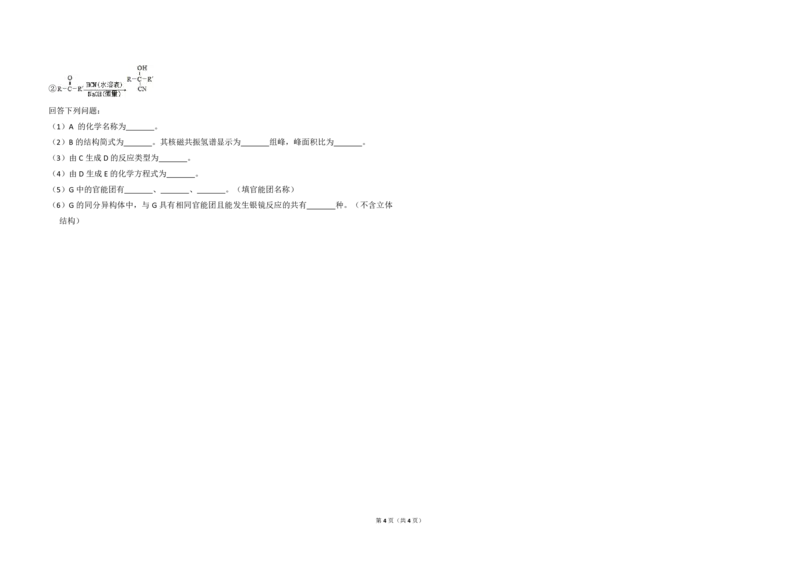文档内容
2016 年全国统一高考化学试卷(新课标Ⅱ) A.NaHCO 3 、Al(OH) 3 B.AgCl、NaHCO 3
C.Na SO 、BaCO D.Na CO 、CuSO
一、选择题:本大题共 7小题,每小题 6分.在每小题给出的四个选项中,只有一项是符合题目 2 3 3 2 3 4
7.(6分)下列实验操作能达到实验目的是( )
要求的.
实验目的 实验操作
1.(6分)下列关于燃料的说法错误的是( )
A.燃料燃烧产物 CO 是温室气体之一
A. 制备Fe(OH)
3
胶体 将NaOH浓溶液滴加到饱和FeCl
3
溶液中
2
B.化石燃料完全燃烧不会造成大气污染 B. 由MgCl 溶液制备无水 将MgCl 溶液加热蒸干
2 2
C.以液化石油气代替燃油可减少大气污染 MgCl
2
D.燃料不完全燃烧排放的CO 是大气污染物之一 C. 除去Cu 粉中混有的CuO 加入稀硝酸溶液,过滤、洗涤、干燥
2.(6分)下列各组中的物质均能发生加成反应的是( )
D. 比较水与乙醇中氢的活泼性 分别将少量钠投入到盛有水和乙醇的烧杯中
A.乙烯和乙醇 B.苯和氯乙烯 C.乙酸和溴乙烷 D.丙烯和丙烷
A.A B.B C.C D.D
3.(6分)a、b、c、d 为短周期元素,a的原子中只有 1个电子,b2﹣和 c+的电子层结构相同,d
与b 同族.下列叙述错误的是( )
三、非选择题:包括必考题和选考题两部分.第 22题~第 32题为必考题,每个试题考生都必须
A.a与其他三种元素形成的二元化合物中其化合价均为+1
作答.第 33题~第 40题为选考题,考生根据要求作答.(一)必考题(共 129分)
B.b 与其他三种元素均可形成至少两种二元化合物
8.(14分)联氨(又称肼,N H ,无色液体)是一种应用广泛的化工原料,可用作火箭燃
2 4
C.c的原子半径是这些元素中最大的
料.回答下列问题:
D.d 与a 形成的化合物的溶液呈弱酸性
(1)联氨分子的电子式为 ,其中氮的化合价为 .
4.(6分)分子式为C H Cl 的有机物共有(不含立体异构)( )
4 8 2 (2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 .
A.7种 B.8种 C.9种 D.10种
(3)①2O (g)+N (g)═N O (l)△H
2 2 2 4 1
5.(6分)Mg﹣AgCl 电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是( )
②N (g)+2H (g)═N H (l)△H
2 2 2 4 2
A.负极反应式为 Mg﹣2e﹣=Mg2+
③O (g)+2H (g)═2H O(g)△H
2 2 2 3
B.正极反应式为 Ag++e﹣=Ag
④2N H (l)+N O (l)═3N (g)+4H O(g)△H =﹣1048.9kJ•mol﹣1
2 4 2 4 2 2 4
C.电池放电时 Cl﹣由正极向负极迁移
上述反应热效应之间的关系式为△H = ,联氨和 N O 可作为火箭推进剂的主要原因
4 2 4
D.负极会发生副反应 Mg+2H O=Mg(OH) +H ↑
2 2 2 为 .
6.(6分)某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
(4)联氨为二元弱碱,在水中的电离方式与氨相似.联氨第一步电离反应的平衡常数值为
①取少量样品加入足量水仍有部分固体未溶解:再加入足量稀盐酸,有气泡产生,固体全部溶
(已知:N H +H+⇌N H +的 K=8.7×107;K =1.0×10﹣14).联氨与硫酸形成的酸式盐的化学式
2 4 2 5 w
解;
为 .
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在.
(5)联氨是一种常用的还原剂.向装有少量 AgBr的试管中加入联氨溶液,观察到的现象
该白色粉末可能为( )
第1页(共4页)是 .联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀.理论上 1kg 的联氨可除去 (2)甲组同学取 2mLFeCl 溶液.加入几滴氯水,再加入 1滴 KSCN溶液,溶液变红,说明 Cl 可
2 2
水中溶解的O kg;与使用Na SO 处理水中溶解的O 相比,联氨的优点是 . 将Fe2+氧化.FeCl 溶液与氯水反应的离子方程式为 .
2 2 3 2 2
9.(14分)丙烯腈(CH =CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产。主 (3)乙组同学认为甲组的实验不够严谨,该组同学在 2mLFeCl 溶液中先加入 0.5mL 煤油,再于
2 2
要副产物有丙烯醛(CH =CHCHO)和乙腈(CH CN)等。回答下列问题: 液面下依次加入几滴氯水和 l 滴KSCN溶液,溶液变红,煤油的作用是 .
2 3
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C H N)和副产物丙烯醛(C H O) (4)丙组同学取 10mL0.1mol/LKI溶液,加入 6mL0.1mol/LFeCl 溶液混合.分别取 2mL 此溶液于 3
3 3 3 4 3
的热化学方程式如下: 支试管中进行如下实验:
①C
3
H
6
(g)+NH
3
(g)+ O
2
(g)═C
3
H
3
N(g)+3H
2
O(g)△H=﹣515kJ•mol﹣1 ①第一支试管中加入1mLCCl
4
充分振荡、静置,CCl
4
层呈紫色;
②第二只试管中加入1滴K [Fe(CN) ]溶液,生成蓝色沉淀;
②C H (g)+O (g)═C H O(g)+H O(g)△H=﹣353kJ•mol﹣1 3 6
3 6 2 3 4 2
③第三支试管中加入1滴KSCN溶液,溶液变红.
两个反应在热力学上趋势均很大,其原因是 ;有利于提高丙烯腈平衡产率的反应条件
实验②检验的离子是 (填离子符号);实验①和③说明:在 I﹣过量的情况下,溶液中仍含
是 ;提高丙烯腈反应选择性的关键因素是 。
有 (填离子符号),由此可以证明该氧化还原反应为 .
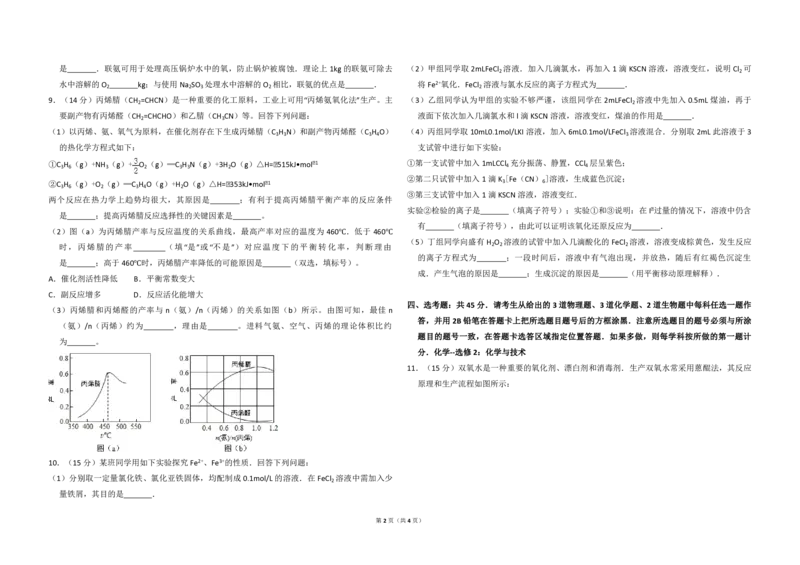
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应的温度为 460℃.低于 460℃
(5)丁组同学向盛有 H O 溶液的试管中加入几滴酸化的 FeCl 溶液,溶液变成棕黄色,发生反应
时,丙烯腈的产率 (填“是”或“不是”)对应温度下的平衡转化率,判断理由 2 2 2
的离子方程式为 ;一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生
是 ;高于460℃时,丙烯腈产率降低的可能原因是 (双选,填标号)。
成.产生气泡的原因是 ;生成沉淀的原因是 (用平衡移动原理解释).
A.催化剂活性降低 B.平衡常数变大
C.副反应增多 D.反应活化能增大
四、选考题:共 45分.请考生从给出的 3道物理题、3道化学题、2道生物题中每科任选一题作
(3)丙烯腈和丙烯醛的产率与 n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳 n
答,并用 2B铅笔在答题卡上把所选题目题号后的方框涂黑.注意所选题目的题号必须与所涂
(氨)/n(丙烯)约为 ,理由是 。进料气氨、空气、丙烯的理论体积比约
题目的题号一致,在答题卡选答区域指定位置答题.如果多做,则每学科按所做的第一题计
为 。
分.化学--选修 2:化学与技术
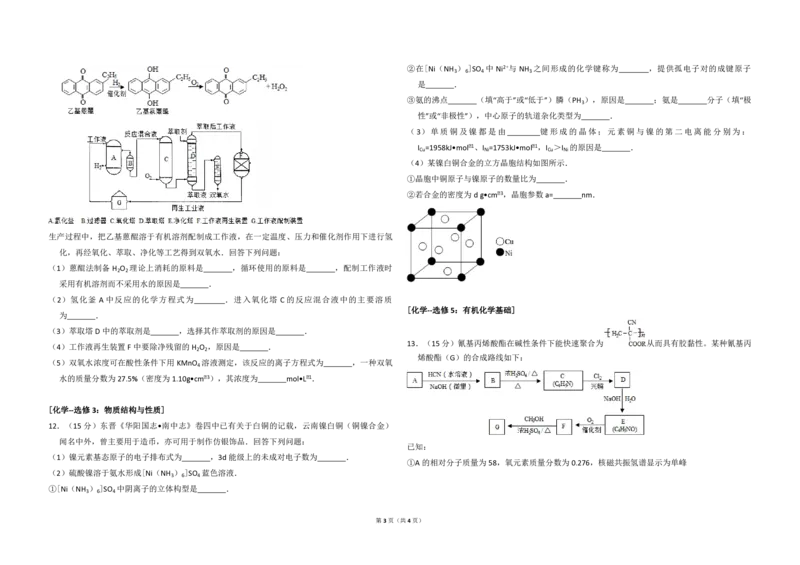
11.(15分)双氧水是一种重要的氧化剂、漂白剂和消毒剂.生产双氧水常采用蒽醌法,其反应
原理和生产流程如图所示:
10.(15分)某班同学用如下实验探究 Fe2+、Fe3+的性质.回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成 0.1mol/L 的溶液.在 FeCl 溶液中需加入少
2
量铁屑,其目的是 .
第2页(共4页)②在[Ni(NH ) ]SO 中 Ni2+与 NH 之间形成的化学键称为 ,提供孤电子对的成键原子
3 6 4 3
是 .
③氨的沸点 (填“高于”或“低于”)膦(PH ),原因是 ;氨是 分子(填“极
3
性”或“非极性”),中心原子的轨道杂化类型为 .
(3)单质铜及镍都是由 键形成的晶体;元素铜与镍的第二电离能分别为:
I =1958kJ•mol﹣1、I =1753kJ•mol﹣1,I >I 的原因是 .
Cu Ni Cu Ni
(4)某镍白铜合金的立方晶胞结构如图所示.
①晶胞中铜原子与镍原子的数量比为 .
②若合金的密度为d g•cm﹣3,晶胞参数a= nm.
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定温度、压力和催化剂作用下进行氢
化,再经氧化、萃取、净化等工艺得到双氧水.回答下列问题:
(1)蒽醌法制备 H O 理论上消耗的原料是 ,循环使用的原料是 ,配制工作液时
2 2
采用有机溶剂而不采用水的原因是 .
(2)氢化釜 A中反应的化学方程式为 .进入氧化塔 C 的反应混合液中的主要溶质
[化学--选修 5:有机化学基础]
为 .
(3)萃取塔D 中的萃取剂是 ,选择其作萃取剂的原因是 .
13.(15分)氰基丙烯酸酯在碱性条件下能快速聚合为 从而具有胶黏性。某种氰基丙
(4)工作液再生装置F 中要除净残留的H O ,原因是 .
2 2
烯酸酯(G)的合成路线如下:
(5)双氧水浓度可在酸性条件下用 KMnO 溶液测定,该反应的离子方程式为 ,一种双氧
4
水的质量分数为27.5%(密度为 1.10g•cm﹣3),其浓度为 mol•L﹣1.
[化学--选修 3:物质结构与性质]
12.(15分)东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)
闻名中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:
已知:
(1)镍元素基态原子的电子排布式为 ,3d 能级上的未成对电子数为 .
①A的相对分子质量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
(2)硫酸镍溶于氨水形成[Ni(NH ) ]SO 蓝色溶液.
3 6 4
①[Ni(NH ) ]SO 中阴离子的立体构型是 .
3 6 4
第3页(共4页)②
回答下列问题:
(1)A 的化学名称为 。
(2)B的结构简式为 。其核磁共振氢谱显示为 组峰,峰面积比为 。
(3)由C 生成 D 的反应类型为 。
(4)由D 生成E 的化学方程式为 。
(5)G中的官能团有 、 、 。(填官能团名称)
(6)G的同分异构体中,与 G具有相同官能团且能发生银镜反应的共有 种。(不含立体
结构)
第4页(共4页)