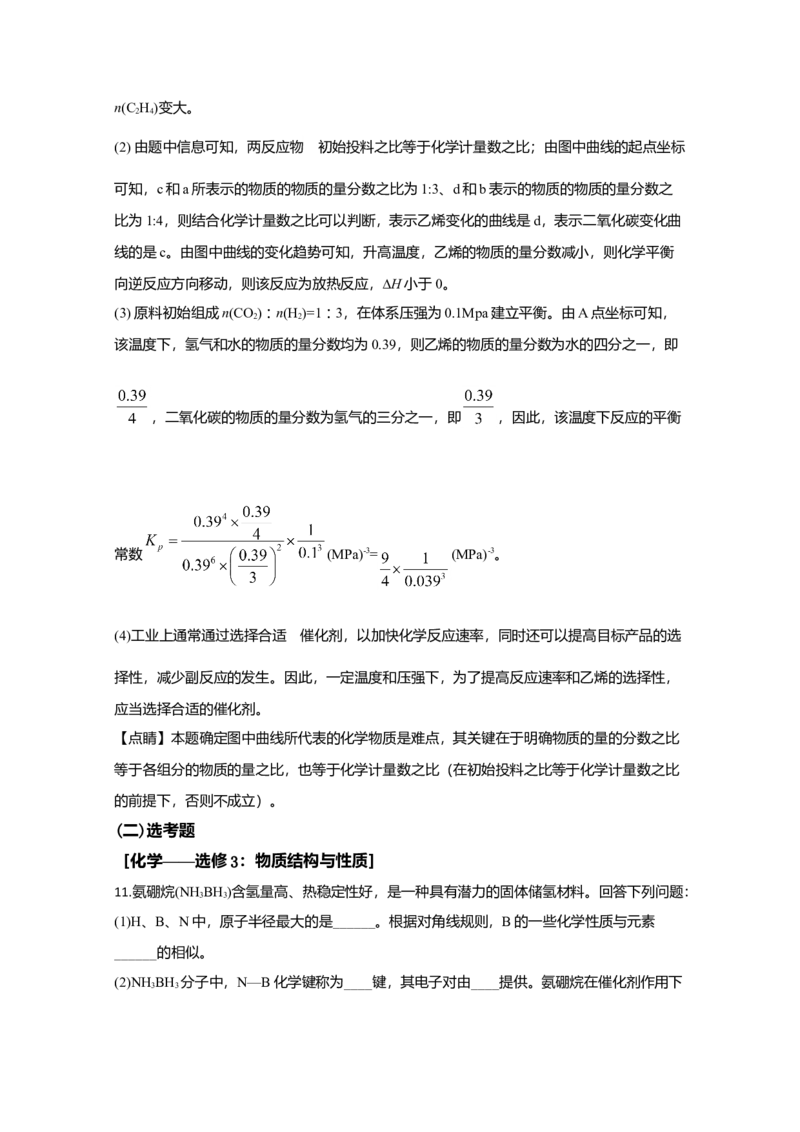文档内容
2020 年普通高等学校招生全国统一考试
理科综合能力测试 化学
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mg 24 S 32 Fe 56 Cu
64
一、选择题:在每小题给出的四个选项中,只有一项是符合题目要求的。
1.宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀
石颜料(主要成分为Cu(OH) ·CuCO),青色来自蓝铜矿颜料(主要成分为Cu(OH) ·2CuCO)。
2 3 2 3
下列说法错误的是
A. 保存《千里江山图》需控制温度和湿度
B. 孔雀石、蓝铜矿颜料不易被空气氧化
C. 孔雀石、蓝铜矿颜料耐酸耐碱
D. Cu(OH) ·CuCO 中铜的质量分数高于Cu(OH) ·2CuCO
2 3 2 3
【答案】C
【解析】
【详解】A.字画主要由纸张和绢、绫、锦等织物构成,为防止受潮和氧化,保存古代字画
的
时要特别注意控制适宜 温度和湿度,A说法正确;
B.由孔雀石和蓝铜矿的化学成分可知,其中的铜元素、碳元素和氢元素均处于最高价,其
均为自然界较稳定的化学物质,因此,用其所制作的颜料不易被空气氧化,B说法正确;
C.孔雀石和蓝铜矿的主要成分均可与酸反应生成相应的铜盐,因此,用其制作的颜料不耐
酸腐蚀,C说法错误;
D.因为氢氧化铜中铜元素的质量分数高于碳酸铜,所以Cu(OH) ∙CuCO 中铜的质量分数高
2 3
于Cu(OH) ∙2CuCO ,D说法正确。
2 3
综上所述,相关说法错误的是C,故本题答案为C。
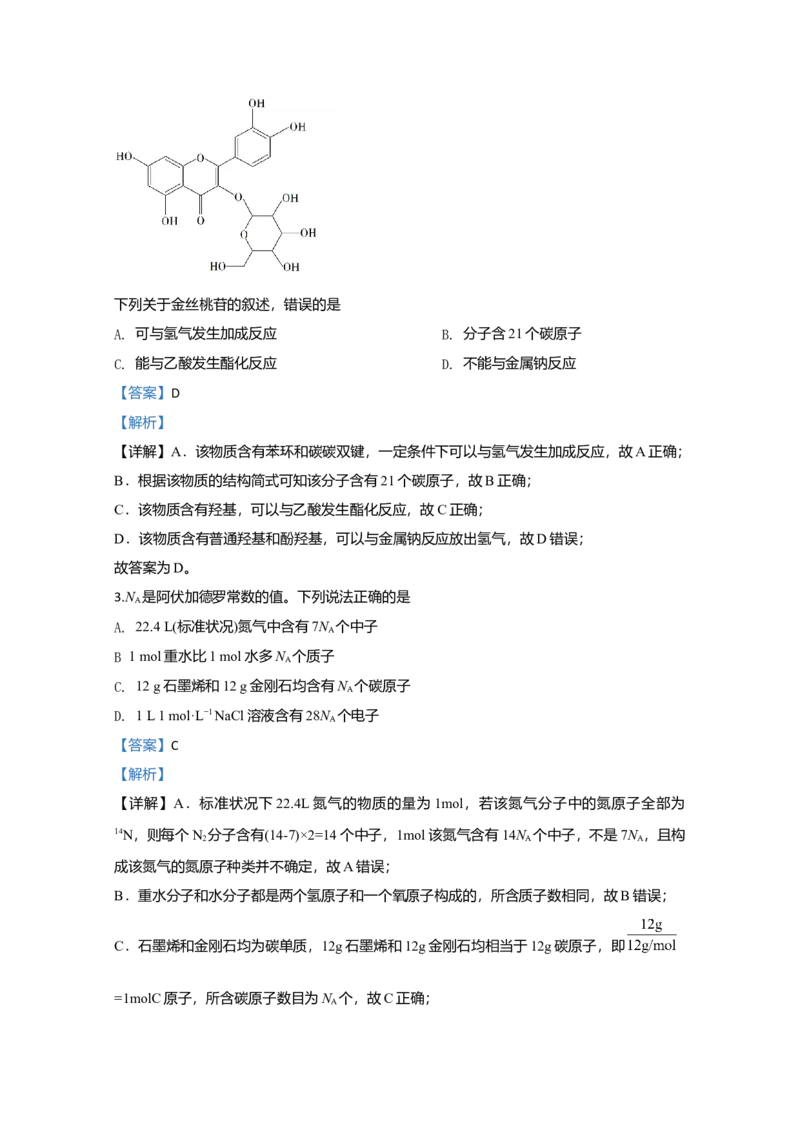
2.金丝桃苷是从中药材中提取的一种具有抗病毒作用的黄酮类化合物,结构式如下:下列关于金丝桃苷的叙述,错误的是
A. 可与氢气发生加成反应 B. 分子含21个碳原子
C. 能与乙酸发生酯化反应 D. 不能与金属钠反应
【答案】D
【解析】
【详解】A.该物质含有苯环和碳碳双键,一定条件下可以与氢气发生加成反应,故A正确;
B.根据该物质的结构简式可知该分子含有21个碳原子,故B正确;
C.该物质含有羟基,可以与乙酸发生酯化反应,故C正确;
D.该物质含有普通羟基和酚羟基,可以与金属钠反应放出氢气,故D错误;
故答案为D。
3.N 是阿伏加德罗常数的值。下列说法正确的是
A
A. 22.4 L(标准状况)氮气中含有7N 个中子
A
B 1 mol重水比1 mol水多N 个质子
A
C. 12 g石墨烯和12 g金刚石均含有N 个碳原子
A
D. 1 L 1 mol·L−1 NaCl溶液含有28N 个电子
A
【答案】C
【解析】
【详解】A.标准状况下22.4L氮气的物质的量为1mol,若该氮气分子中的氮原子全部为
14N,则每个N 分子含有(14-7)×2=14个中子,1mol该氮气含有14N 个中子,不是7N ,且构
2 A A
成该氮气的氮原子种类并不确定,故A错误;
B.重水分子和水分子都是两个氢原子和一个氧原子构成的,所含质子数相同,故B错误;
C.石墨烯和金刚石均为碳单质,12g石墨烯和12g金刚石均相当于12g碳原子,即
=1molC原子,所含碳原子数目为N 个,故C正确;
AD.1molNaCl中含有28N 个电子,但该溶液中除NaCl外,水分子中也含有电子,故D错误;
A
故答案为C。
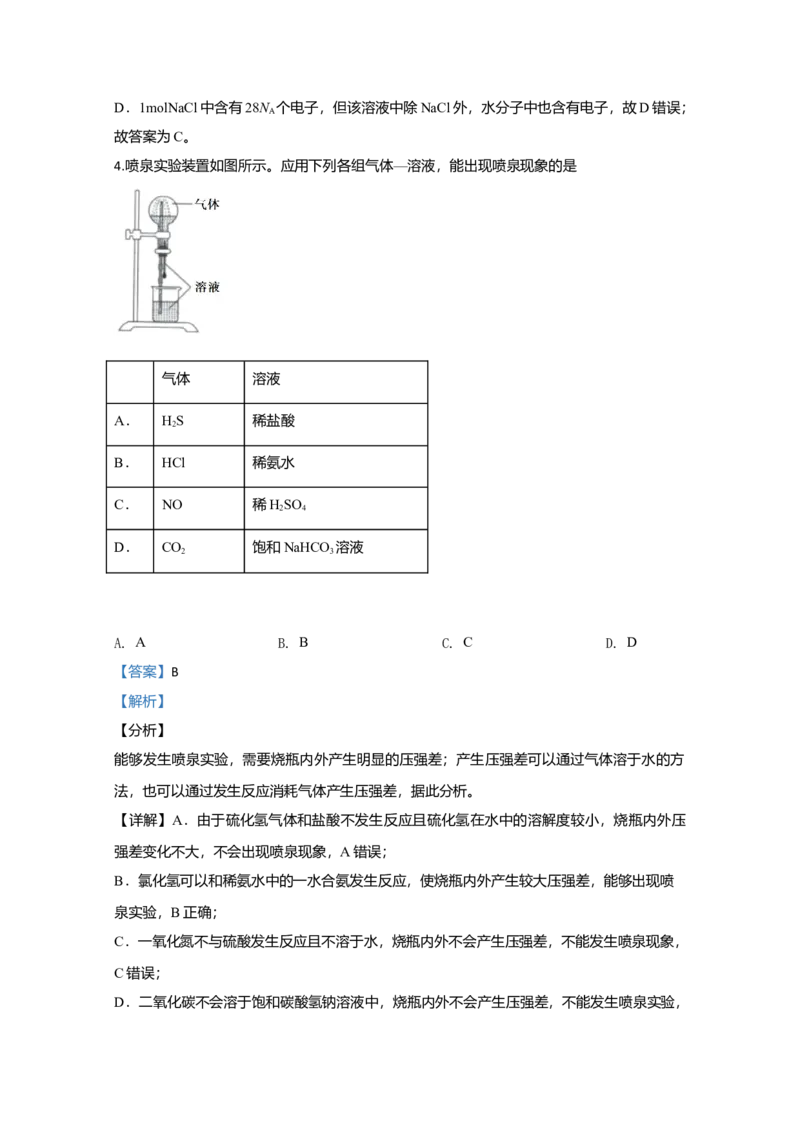
4.喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉现象的是
气体 溶液
A. HS 稀盐酸
2
B. HCl 稀氨水
C. NO 稀HSO
2 4
D. CO 饱和NaHCO 溶液
2 3
A. A B. B C. C D. D
【答案】B
【解析】
【分析】
能够发生喷泉实验,需要烧瓶内外产生明显的压强差;产生压强差可以通过气体溶于水的方
法,也可以通过发生反应消耗气体产生压强差,据此分析。
【详解】A.由于硫化氢气体和盐酸不发生反应且硫化氢在水中的溶解度较小,烧瓶内外压
强差变化不大,不会出现喷泉现象,A错误;
B.氯化氢可以和稀氨水中的一水合氨发生反应,使烧瓶内外产生较大压强差,能够出现喷
泉实验,B正确;
C.一氧化氮不与硫酸发生反应且不溶于水,烧瓶内外不会产生压强差,不能发生喷泉现象,
C错误;
D.二氧化碳不会溶于饱和碳酸氢钠溶液中,烧瓶内外不会产生压强差,不能发生喷泉实验,D错误;
故选B。
5.对于下列实验,能正确描述其反应的离子方程式是
A. 用NaSO 溶液吸收少量Cl:
2 3 2
B. 向CaCl 溶液中通入CO:
2 2
C. 向HO 溶液中滴加少量FeCl :
2 2 3
D. 同浓度同体积NH HSO 溶液与NaOH溶液混合:
4 4
【答案】A
【解析】
【详解】A.用NaSO 溶液吸收少量的Cl ,Cl 具有强氧化性,可将部分 氧化为 ,
2 3 2 2
同时产生的氢离子与剩余部分 结合生成 ,Cl 被还原为Cl-,反应的离子反应方程
2
式为:3 +Cl+H O=2 +2Cl-+ ,A选项正确;
2 2
B.向CaCl 溶液中通入CO,HCO 是弱酸,HCl是强酸,弱酸不能制强酸,故不发生反应,
2 2 2 3
B选项错误;
C.向HO 中滴加少量的FeCl ,Fe3+的氧化性弱于HO,不能氧化HO,但Fe3+能催化HO
2 2 3 2 2 2 2 2 2
的分解,正确的离子方程式应为2HO 2HO+O↑,C选项错误;
2 2 2 2
D.NH HSO 电离出的H+优先和NaOH溶液反应,同浓度同体积的NH HSO 溶液与NaOH溶
4 4 4 4
液混合,氢离子和氢氧根恰好完全反应,正确的离子反应方程式应为:H++OHˉ=HO,D选
2
项错误;
答案选A。
【点睛】B选项为易错点,在解答时容易忽略HCO 是弱酸,HCl是强酸,弱酸不能制强酸
2 3
这一知识点。
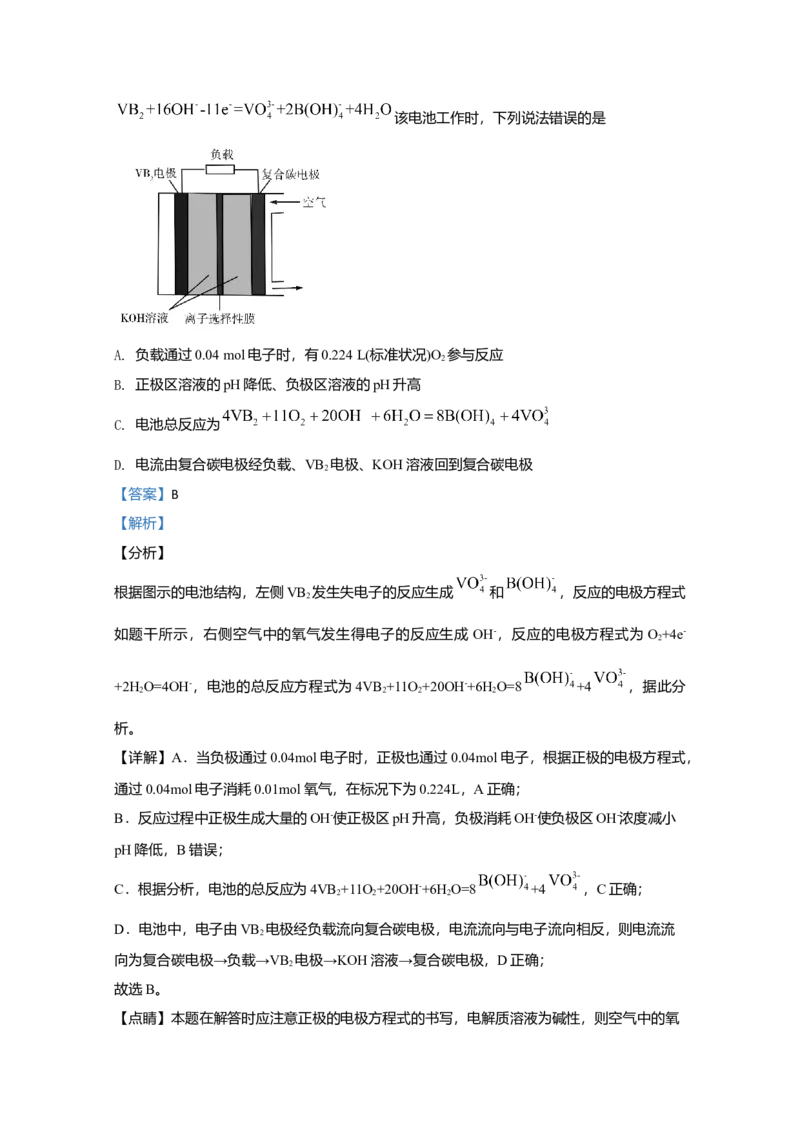
6.一种高性能的碱性硼化钒(VB )—空气电池如下图所示,其中在VB 电极发生反应:
2 2该电池工作时,下列说法错误的是
A. 负载通过0.04 mol电子时,有0.224 L(标准状况)O 参与反应
2
B. 正极区溶液的pH降低、负极区溶液的pH升高
C. 电池总反应为
D. 电流由复合碳电极经负载、VB 电极、KOH溶液回到复合碳电极
2
【答案】B
【解析】
【分析】
根据图示的电池结构,左侧VB 发生失电子的反应生成 和 ,反应的电极方程式
2
如题干所示,右侧空气中的氧气发生得电子的反应生成 OH-,反应的电极方程式为O+4e-
2
+2H O=4OH-,电池的总反应方程式为4VB +11O +20OH-+6H O=8 +4 ,据此分
2 2 2 2
析。
【详解】A.当负极通过0.04mol电子时,正极也通过0.04mol电子,根据正极的电极方程式,
通过0.04mol电子消耗0.01mol氧气,在标况下为0.224L,A正确;
B.反应过程中正极生成大量的OH-使正极区pH升高,负极消耗OH-使负极区OH-浓度减小
pH降低,B错误;
C.根据分析,电池的总反应为4VB +11O +20OH-+6H O=8 +4 ,C正确;
2 2 2
D.电池中,电子由VB 电极经负载流向复合碳电极,电流流向与电子流向相反,则电流流
2
向为复合碳电极→负载→VB 电极→KOH溶液→复合碳电极,D正确;
2
故选B。
【点睛】本题在解答时应注意正极的电极方程式的书写,电解质溶液为碱性,则空气中的氧气得电子生成氢氧根;在判断电池中电流流向时,电流流向与电子流向相反。
7.W、X、Y、Z为原子序数依次增大的短周期元素,四种元素的核外电子总数满足
X+Y=W+Z;化合物XW 与WZ相遇会产生白烟。下列叙述正确的是
3
A. 非金属性:W> X>Y> Z B. 原子半径:Z>Y>X>W
C. 元素X的含氧酸均为强酸 D. Y的氧化物水化物为强碱
【答案】D
【解析】
【分析】
根据题干信息可知,W、X、Y、Z为原子序数依次增大的短周期元素,化合物XW 与WZ相
3
遇会产生白烟,则WX 为NH ,WZ为HCl,所以W为H元素,X为N元素,Z为Cl元素,
3 3
又四种元素的核外电子总数满足X+Y=W+Z,则Y的核外电子总数为11,Y为Na元素,据
此分析解答。
【详解】根据上述分析可知,W为H元素,X为N元素,Y为Na元素,Z为Cl元素,则
A.Na为金属元素,非金属性最弱,非金属性Y<Z,A选项错误;
B.同周期元素从左至右原子半径依次减小,同主族元素至上而下原子半径依次增大,则原
子半径:Na>Cl>N>H,B选项错误;
C.N元素的含氧酸不一定全是强酸,如HNO 为弱酸,C选项错误;
2
D.Y的氧化物水化物为NaOH,属于强碱,D选项正确;
答案选D。
二、非选择题
(一)必考题
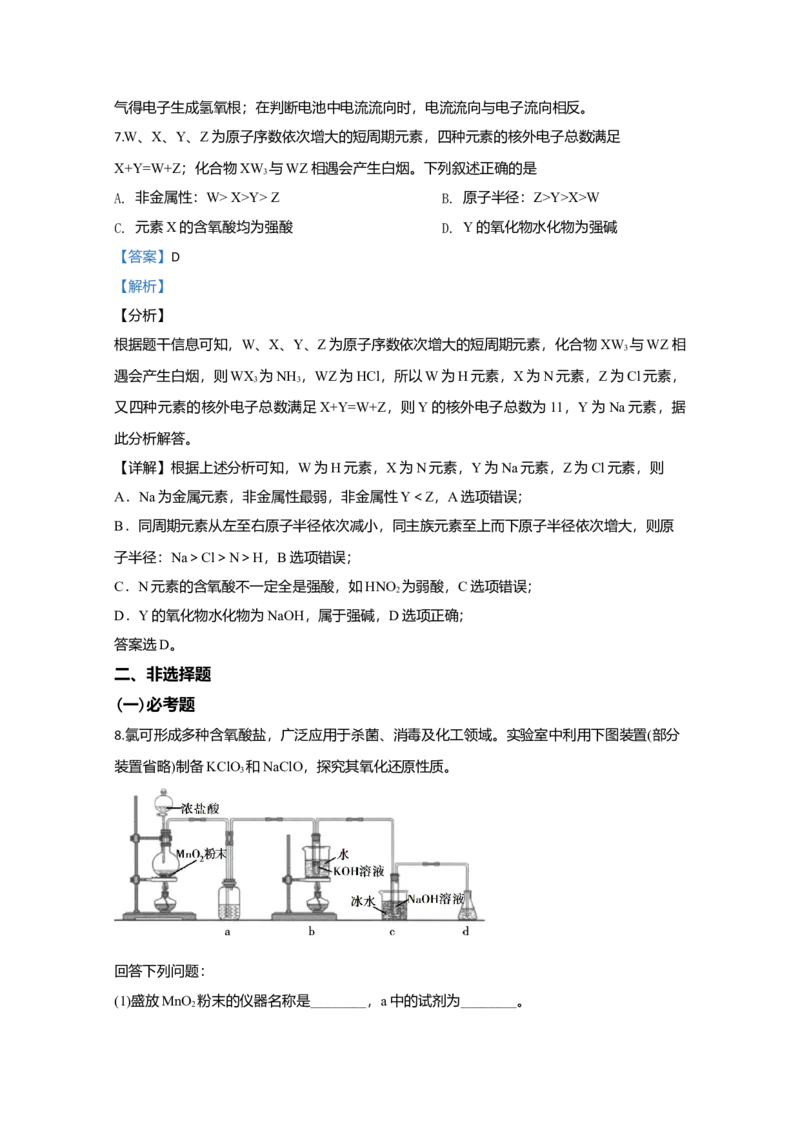
8.氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分
装置省略)制备KClO 和NaClO,探究其氧化还原性质。
3
回答下列问题:
(1)盛放MnO 粉末的仪器名称是________,a中的试剂为________。
2(2)b中采用的加热方式是_________,c中化学反应的离子方程式是________________,采用
冰水浴冷却的目的是____________。
(3)d的作用是________,可选用试剂________(填标号)。
A.NaS B.NaCl C.Ca(OH) D.HSO
2 2 2 4
(4)反应结束后,取出b中试管,经冷却结晶,________,__________,干燥,得到KClO 晶
3
体。
(5)取少量KClO 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液
3
颜色不变。2号试管溶液变为棕色,加入CCl 振荡,静置后CCl 层显____色。可知该条件下
4 4
KClO 的氧化能力____NaClO(填“大于”或“小于”)。
3
【答案】 (1). 圆底烧瓶 (2). 饱和食盐水 (3). 水浴加热 (4). Cl+2OH−=ClO−+Cl−+H O (5).
2 2
避免生成NaClO (6). 吸收尾气(Cl ) (7). AC (8). 过滤 (9). 少量(冷)水洗涤 (10). 紫 (11).
3 2
小于
【解析】
【分析】
本实验目的是制备KClO 和NaClO,并探究其氧化还原性质;首先利用浓盐酸和 MnO 粉末
3 2
共热制取氯气,生成的氯气中混有HCl气体,可在装置a中盛放饱和食盐水中将HCl气体除
去;之后氯气与KOH溶液在水浴加热的条件发生反应制备KClO,再与NaOH溶液在冰水浴
3
中反应制备NaClO;氯气有毒会污染空气,所以需要d装置吸收未反应的氯气。
【详解】(1)根据盛放MnO 粉末的仪器结构可知该仪器为圆底烧瓶;a中盛放饱和食盐水除
2
去氯气中混有的HCl气体;
(2)根据装置图可知盛有KOH溶液的试管放在盛有水的大烧杯中加热,该加热方式为水浴加
热;c中氯气在NaOH溶液中发生歧化反应生成氯化钠和次氯酸钠,结合元素守恒可得离子
方程式为Cl+2OHˉ=ClOˉ+Clˉ+H O;根据氯气与KOH溶液的反应可知,加热条件下氯气可
2 2
以和强碱溶液反应生成氯酸盐,所以冰水浴的目的是避免生成NaClO;
3
(3)氯气有毒,所以d装置的作用是吸收尾气(Cl );
2
A.NaS可以将氯气还原成氯离子,可以吸收氯气,故A可选;
2
B.氯气在NaCl溶液中溶解度很小,无法吸收氯气,故B不可选;
C.氯气可以Ca(OH) 或浊液反应生成氯化钙和次氯酸钙,故C可选;
2
D.氯气与硫酸不反应,且硫酸溶液中存在大量氢离子会降低氯气的溶解度,故D不可选;
综上所述可选用试剂AC;
(4)b中试管为KClO 和KCl的混合溶液,KClO 的溶解度受温度影响更大,所以将试管b中
3 3混合溶液冷却结晶、过滤、少量(冷)水洗涤、干燥,得到KClO 晶体;
3
(5)1号试管溶液颜色不变,2号试管溶液变为棕色,说明1号试管中氯酸钾没有将碘离子氧化,
2号试管中次氯酸钠将碘离子氧化成碘单质,即该条件下KClO 的氧化能力小于NaClO;碘
3
单质更易溶于CCl ,所以加入CCl 振荡,静置后CCl 层显紫色。
4 4 4
【点睛】第3小题为本题易错点,要注意氯气除了可以用碱液吸收之外,氯气还具有氧化性,
可以用还原性的物质吸收。
9.某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶
性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO ·7H O):
4 2
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2+ Al3+ Fe3+ Fe2+
开始沉淀时(c=0.01 mol·L−1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10−5 mol·L−1)的pH 8.7 4.7 3.2 9.0
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是______________。为回收金属,用稀硫酸将“滤液①”调
为中性,生成沉淀。写出该反应的离子方程式______________。
(2)“滤液②”中含有的金属离子是______________。
(3)“转化”中可替代HO 的物质是______________。若工艺流程改为先“调pH”后“转化”,即
2 2
“滤液③”中可能含有的杂质离子为______________。
(4)利用上述表格数据,计算Ni(OH) 的K =______________(列出计算式)。如果“转化”后的溶
2 sp
液中Ni2+浓度为1.0 mol·L−1,则“调pH”应控制的pH范围是______________。(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出
该反应的离子方程式______________。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______________。
【答案】 (1). 除去油脂、溶解铝及其氧化物 (2). +H++H O=Al(OH) ↓或
2 3
+H+=Al(OH) ↓+H O (3). Ni2+ 、 Fe2+ 、 Fe3+ (4). O 或 空 气 (5). Fe3+ (6).
3 2 2
(7). 3.2~6.2 (8). 2Ni2++ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H O
2
(9). 提高镍回收率
【解析】
【分析】
由工艺流程分析可得,向废镍催化剂中加入NaOH溶液进行碱浸,可除去油脂,并发生反应
2Al+2NaOH+2H O=2NaAlO +3H ↑、2Al O+4NaOH=4NaAlO +2H O将Al及其氧化物溶解,
2 2 2 2 3 2 2
得到的滤液①含有NaAlO ,滤饼①为Ni、Fe及其氧化物和少量其他不溶性杂质,加稀
2
HSO 酸浸后得到含有Ni2+、Fe2+、Fe3+的滤液②,Fe2+经HO 氧化为Fe3+后,加入NaOH调节
2 4 2 2
pH使Fe3+转化为Fe(OH) 沉淀除去,再控制pH浓缩结晶得到硫酸镍的晶体,据此分析解答
3
问题。
【详解】(1)根据分析可知,向废镍催化剂中加入NaOH溶液进行碱浸,可除去油脂,并将Al
及其氧化物溶解,滤液①中含有NaAlO (或Na[Al(OH)]),加入稀硫酸可发生反应 +H+
2 4
+H O=Al(OH) ↓或 +H+=Al(OH) ↓+H O,故答案为:除去油脂、溶解铝及其氧化物;
2 3 3 2
+H++H O=Al(OH) ↓或 +H+=Al(OH) ↓+H O;
2 3 3 2
(2)加入稀硫酸酸浸,Ni、Fe及其氧化物溶解,所以“滤液②”中含有的金属离子是Ni2+、
Fe2+、Fe3+,故答案为:Ni2+、Fe2+、Fe3+;
(3)“转化”在HO 的作用是将Fe2+氧化为Fe3+,可用O 或空气替代;若将工艺流程改为先“调
2 2 2
pH”后“转化”,会使调pH过滤后的溶液中含有Fe2+,则滤液③中可能含有转化生成的Fe3+,
故答案为:O 或空气;Fe3+;
2
(4)由上述表格可知,Ni2+完全沉淀时的pH=8.7,此时c(Ni2+)=1.0×10-5mol·L-1,c(H+)=1.0×10-8.7mol·L-1,则c(OH-)= ,则Ni(OH) 的
2
;或者当Ni2+开始沉淀时pH=7.2,此时
c(Ni2+)=0.01mol·L-1,c(H+)=1.0×10-7.2mol·L-1,则c(OH-)= ,则
Ni(OH) 的 ;如果“转化”后的溶液中Ni2+浓度为
2
1.0mol·L-1,为避免镍离子沉淀,此时 ,
则 ,即pH=6.2;Fe3+完全沉淀的pH为3.2,因此“调节pH”应
控制的pH范围是3.2~6.2,故答案为: ;3.2~6.2;
(5)由题干信息,硫酸镍在强碱中被NaClO氧化得到NiOOH沉淀,即反应中Ni2+被氧化为
NiOOH沉淀,ClOˉ被还原为Clˉ,则根据氧化还原得失电子守恒可得离子方程式为2Ni2+
+ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H O,故答案为:2Ni2++ClOˉ+4OHˉ=2NiOOH↓+Clˉ+H O;
2 2
(6)分离出硫酸镍晶体后的母液中还含有Ni2+,可将其收集、循环使用,从而提高镍的回收率,
故答案为:提高镍的回收率。
【点睛】本题主要考查金属及其化合物的性质、沉淀溶解平衡常数Ksp的计算、氧化还原离
子反应方程式的书写等知识点,需要学生具有很好的综合迁移能力,解答关键在于正确分析
出工艺流程原理,难点在于Ksp的计算及“调pH”时pH的范围确定。
10.二氧化碳催化加氢合成乙烯是综合利用CO 的热点研究领域。回答下列问题:
2
(1)CO 催化加氢生成乙烯和水的反应中,产物的物质的量之比
2
n(C H)∶n(H O)=__________。当反应达到平衡时,若增大压强,则n(C H)___________(填
2 4 2 2 4
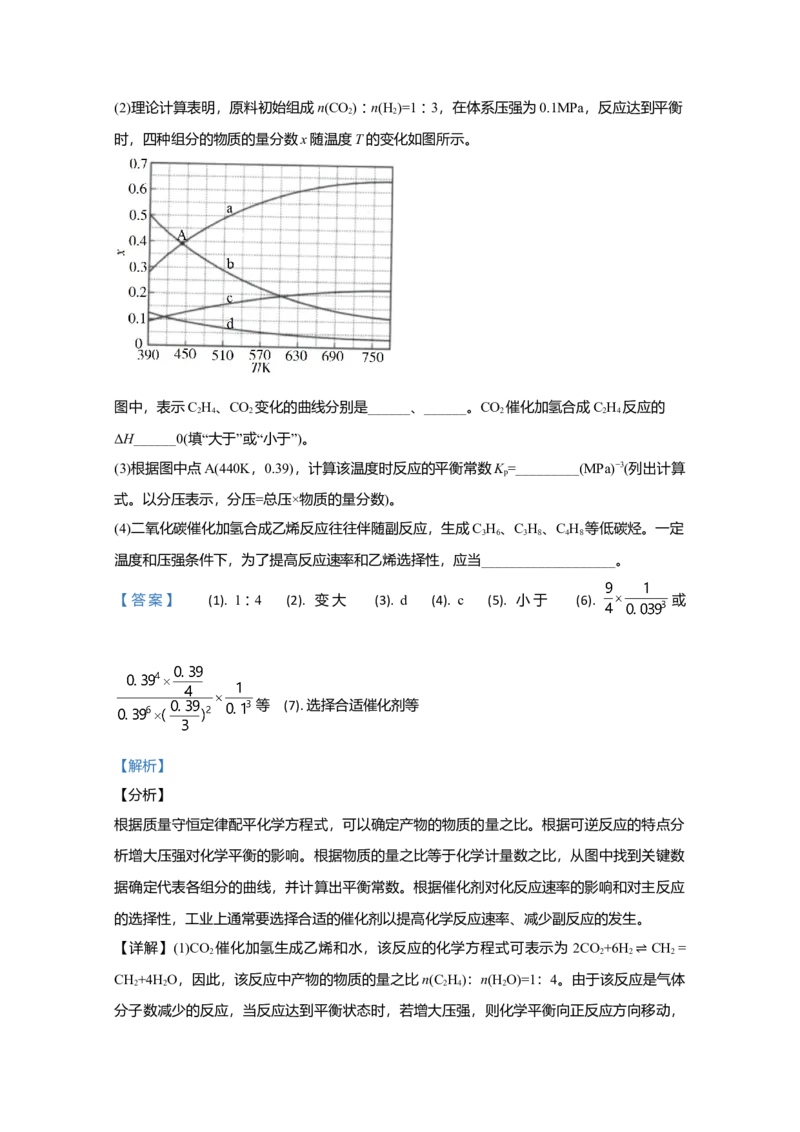
“变大”“变小”或“不变”)。(2)理论计算表明,原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1MPa,反应达到平衡
2 2
时,四种组分的物质的量分数x随温度T的变化如图所示。
图中,表示C H、CO 变化的曲线分别是______、______。CO 催化加氢合成C H 反应的
2 4 2 2 2 4
ΔH______0(填“大于”或“小于”)。
(3)根据图中点A(440K,0.39),计算该温度时反应的平衡常数K =_________(MPa)−3(列出计算
p
式。以分压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C H、C H、C H 等低碳烃。一定
3 6 3 8 4 8
温度和压强条件下,为了提高反应速率和乙烯选择性,应当___________________。
【答案】 (1). 1∶4 (2). 变大 (3). d (4). c (5). 小于 (6). 或
等 (7). 选择合适催化剂等
【解析】
【分析】
根据质量守恒定律配平化学方程式,可以确定产物的物质的量之比。根据可逆反应的特点分
析增大压强对化学平衡的影响。根据物质的量之比等于化学计量数之比,从图中找到关键数
据确定代表各组分的曲线,并计算出平衡常数。根据催化剂对化反应速率的影响和对主反应
的选择性,工业上通常要选择合适的催化剂以提高化学反应速率、减少副反应的发生。
【详解】(1)CO 催化加氢生成乙烯和水,该反应的化学方程式可表示为 2CO+6H CH =
2 2 2 2
CH+4H O,因此,该反应中产物的物质的量之比n(C H):n(H O)=1:4。由于该反应⇌是气体
2 2 2 4 2
分子数减少的反应,当反应达到平衡状态时,若增大压强,则化学平衡向正反应方向移动,n(C H)变大。
2 4
的
(2) 由题中信息可知,两反应物 初始投料之比等于化学计量数之比;由图中曲线的起点坐标
可知,c和a所表示的物质的物质的量分数之比为1:3、d和b表示的物质的物质的量分数之
比为1:4,则结合化学计量数之比可以判断,表示乙烯变化的曲线是d,表示二氧化碳变化曲
线的是c。由图中曲线的变化趋势可知,升高温度,乙烯的物质的量分数减小,则化学平衡
向逆反应方向移动,则该反应为放热反应,∆H小于0。
(3) 原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1Mpa建立平衡。由A点坐标可知,
2 2
该温度下,氢气和水的物质的量分数均为0.39,则乙烯的物质的量分数为水的四分之一,即
,二氧化碳的物质的量分数为氢气的三分之一,即 ,因此,该温度下反应的平衡
常数 (MPa)-3= (MPa)-3。
的
(4)工业上通常通过选择合适 催化剂,以加快化学反应速率,同时还可以提高目标产品的选
择性,减少副反应的发生。因此,一定温度和压强下,为了提高反应速率和乙烯的选择性,
应当选择合适的催化剂。
【点睛】本题确定图中曲线所代表的化学物质是难点,其关键在于明确物质的量的分数之比
等于各组分的物质的量之比,也等于化学计量数之比(在初始投料之比等于化学计量数之比
的前提下,否则不成立)。
(二)选考题
[化学——选修3:物质结构与性质]
11.氨硼烷(NH BH)含氢量高、热稳定性好,是一种具有潜力的固体储氢材料。回答下列问题:
3 3
(1)H、B、N中,原子半径最大的是______。根据对角线规则,B的一些化学性质与元素
______的相似。
(2)NH BH 分子中,N—B化学键称为____键,其电子对由____提供。氨硼烷在催化剂作用下
3 3水解释放氢气:3NH BH+6H O=3NH + +9H , 的结构如图所示:
3 3 2 3 2
在该反应中,B原子的杂化轨道类型由______变为______。
(3)NH BH 分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),电
3 3
负性大小顺序是__________。与NH BH 原子总数相等的等电子体是_________(写分子式),
3 3
其熔点比NH BH____________(填“高”或“低”),原因是在NH BH 分子之间,存在
3 3 3 3
____________________,也称“双氢键”。
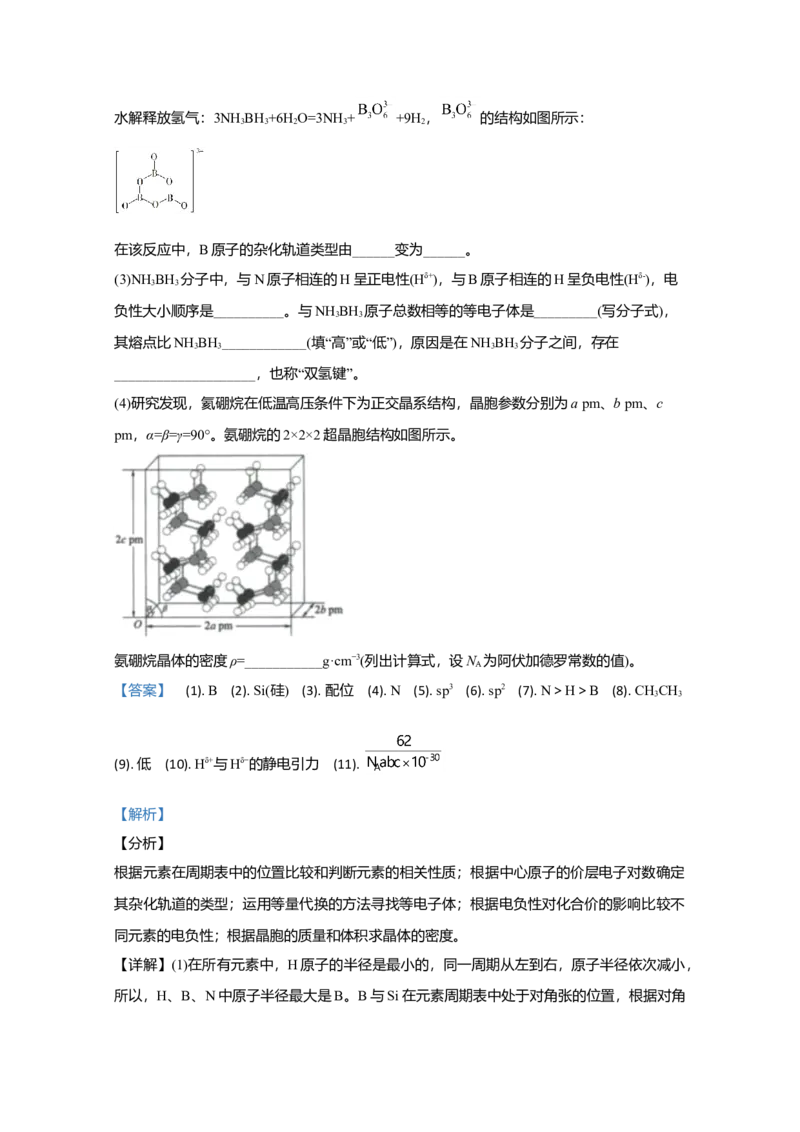
(4)研究发现,氦硼烷在低温高压条件下为正交晶系结构,晶胞参数分别为a pm、b pm、c
pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞结构如图所示。
氨硼烷晶体的密度ρ=___________g·cm−3(列出计算式,设N 为阿伏加德罗常数的值)。
A
【答案】 (1). B (2). Si(硅) (3). 配位 (4). N (5). sp3 (6). sp2 (7). N>H>B (8). CHCH
3 3
(9). 低 (10). Hδ+与Hδ−的静电引力 (11).
【解析】
【分析】
根据元素在周期表中的位置比较和判断元素的相关性质;根据中心原子的价层电子对数确定
其杂化轨道的类型;运用等量代换的方法寻找等电子体;根据电负性对化合价的影响比较不
同元素的电负性;根据晶胞的质量和体积求晶体的密度。
【详解】(1)在所有元素中,H原子的半径是最小的,同一周期从左到右,原子半径依次减小,
所以,H、B、N中原子半径最大是B。B与Si在元素周期表中处于对角张的位置,根据对角线规则,B的一些化学性质与Si元素相似。
(2)B原子最外层有3个电子,其与3个H原子形成共价键后,其价层电子对只有3对,还有
一个空轨道;在NH 中,N原子有一对孤对电子,故在NH BH 分子中,N—B键为配位键,
3 3 3
其电子对由N原子提供。NH BH 分子中,B原子的价层电子对数为4,故其杂化方式为
3 3
sp3。NH BH 在催化剂的作用下水解生成氢气和B O3-,由图中信息可知,B O3-中每个B原
3 3 3 6 3 6
子只形成3个σ键,其中的B原子的杂化方式为sp2,因此,B原子的杂化轨道类型由sp3变
为sp2。
(3) NHBH 分子中,与N原子相连的H呈正电性,说明N的电负性大于H;与B原子相连的
3 3
H呈负电性,说明H的电负性大于B,因此3种元素电负性由大到小的顺序为N>H>B。
NH BH 分子中有8个原子,其价电子总数为14,N和B的价电子数的平均值为4,依据等量
3 3
代换的原则,可以找到其等电子体为CHCH。由于NH BH 分子属于极性分子,而CHCH
3 3 3 3 3 3
属于非极性分子,两者相对分子质量接近,但是极性分子的分子间作用力较大,故CHCH
3 3
熔点比NH BH 低。NH BH 分子间存在“双氢键”,类比氢键的形成原理,说明其分子间存在
3 3 3 3
Hδ+与Hδ-的静电引力。
(4)在氨硼烷的222的超晶胞结构中,共有16个氨硼烷分子,晶胞的长、宽、高分别为
2apm、2bpm、2cpm,若将其平均分为8份可以得到8个小长方体,则平均每个小长方体中
占有2个氨硼烷分子,小长方体的长、宽、高分别为apm、bpm、cpm,则小长方体的质量为
,小长方体的体积为 ,因此,氨硼烷晶体的密度为
g∙cm-3。
【点睛】本题最后有关晶体密度的计算是难点,要求考生能读懂题意,通过观察晶胞结构,
确定超晶胞结构中的分子数,并能合理分成8份,从而简化计算。
[化学——选修5:有机化学基础]
12.苯基环丁烯酮( PCBO)是一种十分活泼的反应物,可利用它的开环反应合
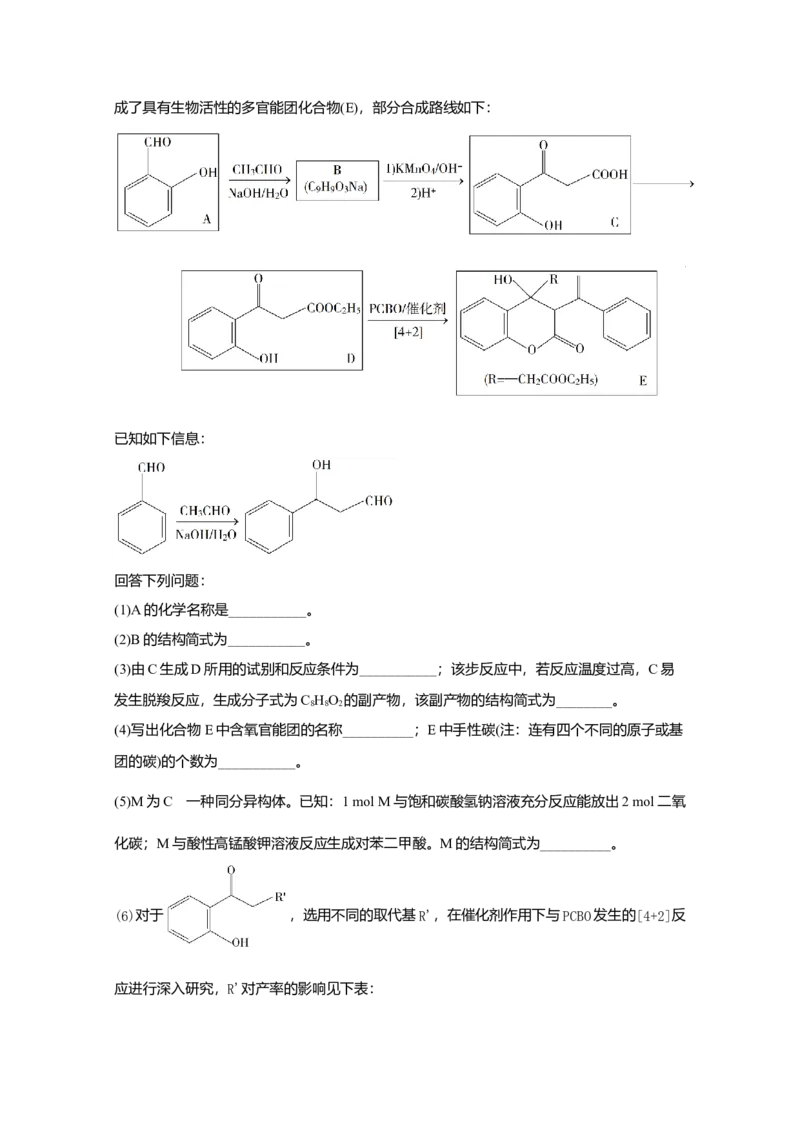
成一系列多官能团化合物。近期我国科学家报道用PCBO与醛或酮发生[4+2]环加成反应,合成了具有生物活性的多官能团化合物(E),部分合成路线如下:
已知如下信息:
回答下列问题:
(1)A的化学名称是___________。
(2)B的结构简式为___________。
(3)由C生成D所用的试别和反应条件为___________;该步反应中,若反应温度过高,C易
发生脱羧反应,生成分子式为C HO 的副产物,该副产物的结构简式为________。
8 8 2
(4)写出化合物E中含氧官能团的名称__________;E中手性碳(注:连有四个不同的原子或基
团的碳)的个数为___________。
的
(5)M为C 一种同分异构体。已知:1 mol M与饱和碳酸氢钠溶液充分反应能放出2 mol二氧
化碳;M与酸性高锰酸钾溶液反应生成对苯二甲酸。M的结构简式为__________。
(6)对于 ,选用不同的取代基R',在催化剂作用下与PCBO发生的[4+2]反
应进行深入研究,R'对产率的影响见下表:R' —CH —C H —CHCHC H
3 2 5 2 2 6 5
产率/% 91 80 63
请找出规律,并解释原因___________。
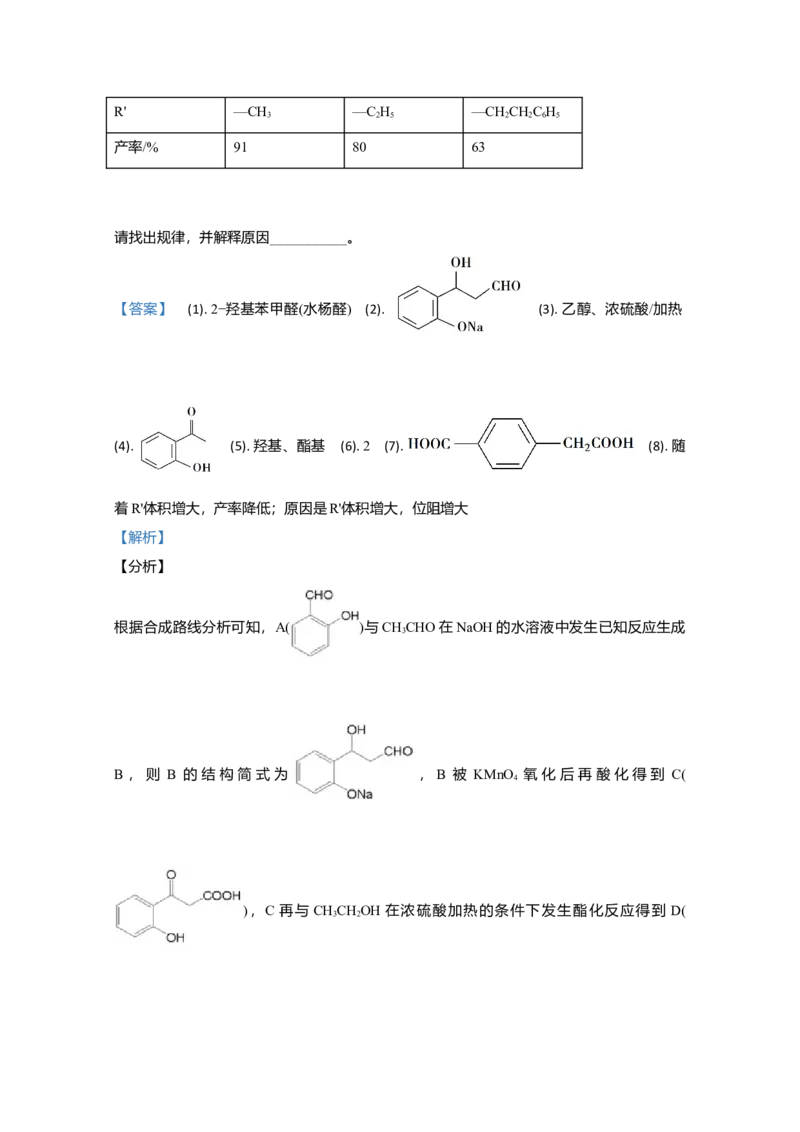
【答案】 (1). 2−羟基苯甲醛(水杨醛) (2). (3). 乙醇、浓硫酸/加热
(4). (5). 羟基、酯基 (6). 2 (7). (8). 随
着R'体积增大,产率降低;原因是R'体积增大,位阻增大
【解析】
【分析】
根据合成路线分析可知,A( )与CHCHO在NaOH的水溶液中发生已知反应生成
3
B ,则 B 的结构简式为 ,B 被 KMnO 氧化 后再 酸化 得到 C(
4
),C 再与 CHCHOH 在浓硫酸加热的条件下发生酯化反应得到 D(
3 2),D再反应得到 E( ),据此分
析解答问题。
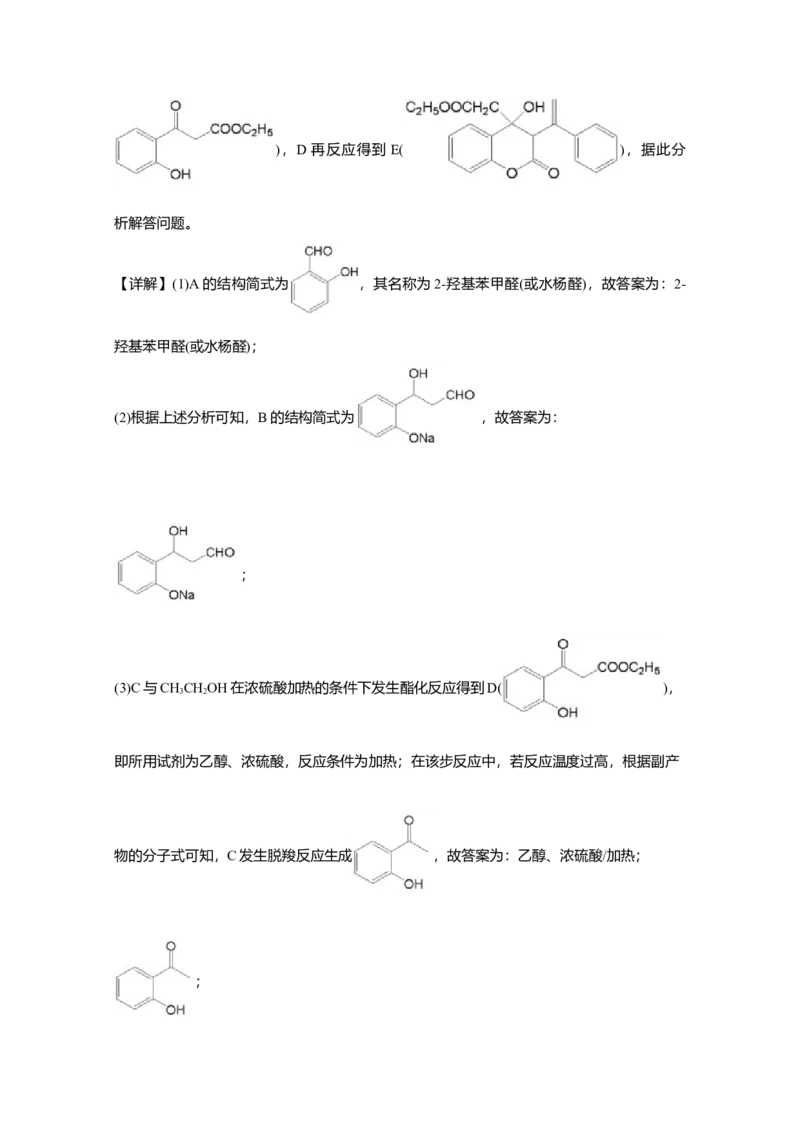
【详解】(1)A的结构简式为 ,其名称为2-羟基苯甲醛(或水杨醛),故答案为:2-
羟基苯甲醛(或水杨醛);
(2)根据上述分析可知,B的结构简式为 ,故答案为:
;
(3)C与CHCHOH在浓硫酸加热的条件下发生酯化反应得到D( ),
3 2
即所用试剂为乙醇、浓硫酸,反应条件为加热;在该步反应中,若反应温度过高,根据副产
物的分子式可知,C发生脱羧反应生成 ,故答案为:乙醇、浓硫酸/加热;
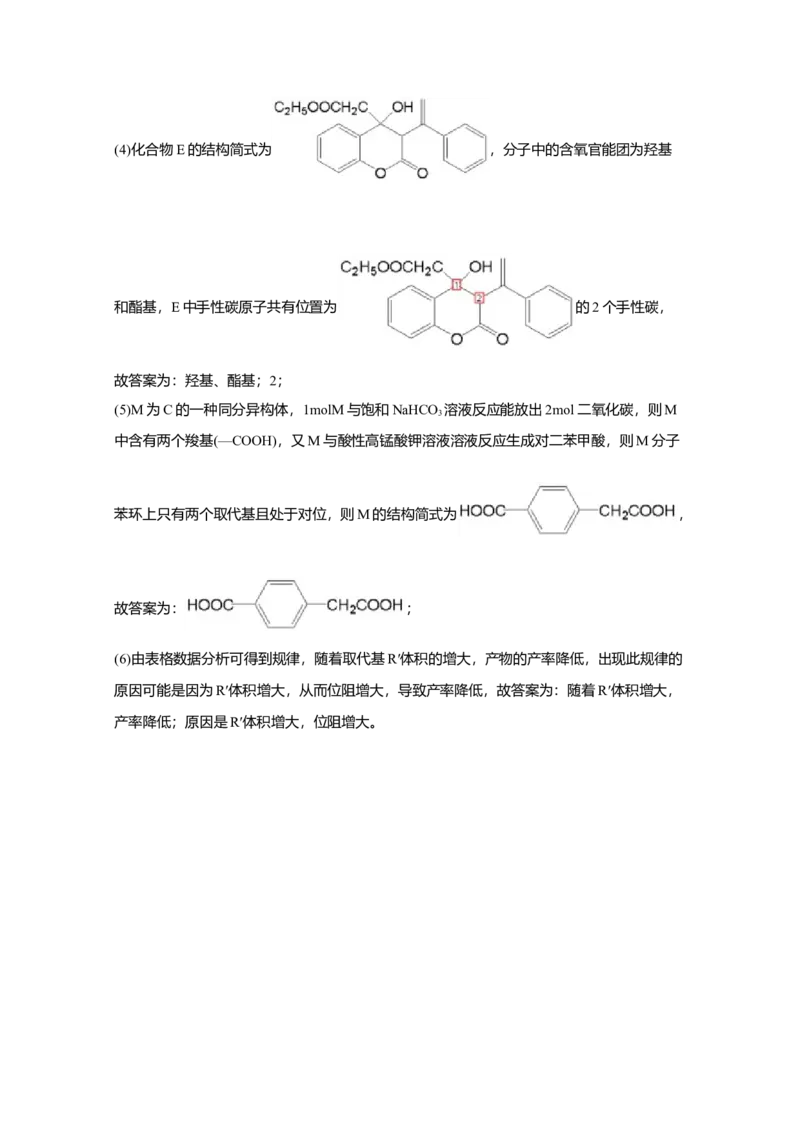
;(4)化合物E的结构简式为 ,分子中的含氧官能团为羟基
和酯基,E中手性碳原子共有位置为 的2个手性碳,
故答案为:羟基、酯基;2;
(5)M为C的一种同分异构体,1molM与饱和NaHCO 溶液反应能放出2mol二氧化碳,则M
3
中含有两个羧基(—COOH),又M与酸性高锰酸钾溶液溶液反应生成对二苯甲酸,则M分子
苯环上只有两个取代基且处于对位,则M的结构简式为 ,
故答案为: ;
(6)由表格数据分析可得到规律,随着取代基R′体积的增大,产物的产率降低,出现此规律的
原因可能是因为R′体积增大,从而位阻增大,导致产率降低,故答案为:随着R′体积增大,
产率降低;原因是R′体积增大,位阻增大。