文档内容
2024 年高三基础测试
化学 试题卷
(2024.9)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 K-39 Mn-55
一、选择题(本大题共16小题,每小题3分,共48分。每小题列出的四个备选项中只有
一个是符合题目要求的,不选、多选、错选均不得分)
1.按物质组成或性质分类,Na[Al(OH) ]属于
4
A.碱 B.酸 C.碱式盐 D.强电解质
2.下列说法不正确的是
...
A.活性炭具有吸附性,可用于分解净化室内甲醛
B.甲烷具有还原性,可用于制作燃料电池
C.次氯酸钠具有氧化性,可用于衣物漂白
D.石灰乳具有碱性,可用于除去废气中的二氧化硫
3.下列化学用语或表述正确的是
A.O 分子的球棍模型:
3
B.PH 3 的电子式:H· · · P · · ·H
H
C.用电子云轮廓图示意“p-p”π键的形成:
H CH
3
⟍ ⟋
D.顺-2-丁烯的结构简式: C=C
⟋ ⟍
CH H
3
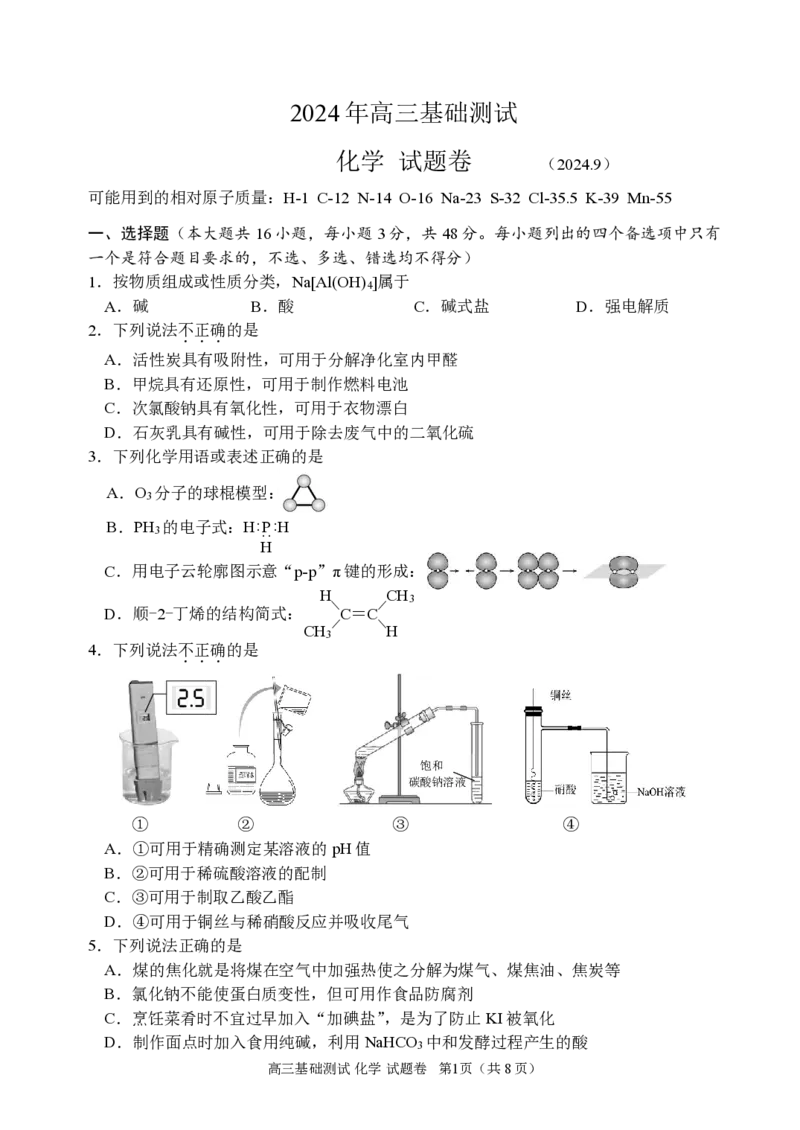
4.下列说法不正确的是
...
饱和
碳酸钠溶液
① ② ③ ④
A.①可用于精确测定某溶液的pH值
B.②可用于稀硫酸溶液的配制
C.③可用于制取乙酸乙酯
D.④可用于铜丝与稀硝酸反应并吸收尾气
5.下列说法正确的是
A.煤的焦化就是将煤在空气中加强热使之分解为煤气、煤焦油、焦炭等
B.氯化钠不能使蛋白质变性,但可用作食品防腐剂
C.烹饪菜肴时不宜过早加入“加碘盐”,是为了防止KI被氧化
D.制作面点时加入食用纯碱,利用NaHCO 中和发酵过程产生的酸
3
高三基础测试 化学 试题卷 第1页(共8页)
{#{QQABIYAEoggIQJBAARgCAwWICAAQkACCASgORBAIIAIBwQNABAA=}#}6.宇航装置中常用超氧化钾(KO )作 CO 吸收剂和供氧剂,反应方程式(未配平)为:
2 2
KO +CO →K CO +O ,N 为阿伏加德罗常数的值。下列说法不正确的是
2 2 2 3 2 A ...
A.7.1gKO 晶体中离子的数目为0.2N
2 A
B.可用Na O 代替宇航装置中的KO
2 2 2
C.氧化剂与还原剂的物质的量之比为3:1
D.该反应生成11.2L(标准状况下)O 时转移0.5N 个电子
2 A
7.物质微观结构决定宏观性质,进而影响用途。下列结构或性质不能解释其用途的是
..
选项 结构或性质 用途
在碳素钢里适量加入铬和镍后形成的不锈钢 可制成医疗器材、厨房用具和地
A
不易生锈,具有很强的抗腐蚀能力 铁列车的车体等
石墨层内未杂化的p轨道重叠使电子可在整
B 石墨可作润滑剂
个碳原子层平面内运动
高铁酸钠具有氧化性,氢氧化铁胶体具有 高铁酸钠可用于水体的消毒、
C
吸附性 净化
CH3
H3C O O 能有效作用于疟原虫体内的膜蛋
D 青蒿素( )中含有过氧键
O 白,从而起到治疗疟疾的效果
O
CH3
O
8.下列离子方程式或化学方程式正确的是
A.向含有1mol明矾的溶液中滴加Ba(OH) 溶液至铝离子完全沉淀:
2
Al3++2SO2−+2Ba2++3OH−=Al(OH) ↓+2BaSO ↓
4 3 4
B.含氟牙膏防治龋齿:Ca 5 (PO 4 ) 3 (OH)(s)+F−(aq) ⇌ Ca 5 (PO 4 ) 3 F(s)+OH−(aq)
OH
| Cu
C.2-丙醇的催化氧化:2CH CHCH +O -—→ 2CH CH CHO+2H O
3 3 2 3 2 2
△
D.用氢氟酸刻蚀玻璃:SiO +4F−+4H+=SiF ↑+2H O
2 4 2
9.某种用于制作镜片的聚碳酸酯 X 制备原理如下,若将有毒的光气改成碳酸二甲酯
(CH OCOOCH ),也可与A反应制得X。以下说法不正确的是
3 3 ...
CH3 O
‖
光气(COCl )+原料A -—→ -[O O-C-]
2 H H n
CH3
(X)
A.光气水解产生氯化氢和二氧化碳
B.原料A为一种二酚类物质
C.原料A与足量H 加成后的产物分子中含4个手性碳原子
2
D.碳酸二甲酯和A反应的产物中有甲醇
高三基础测试 化学 试题卷 第2页(共8页)
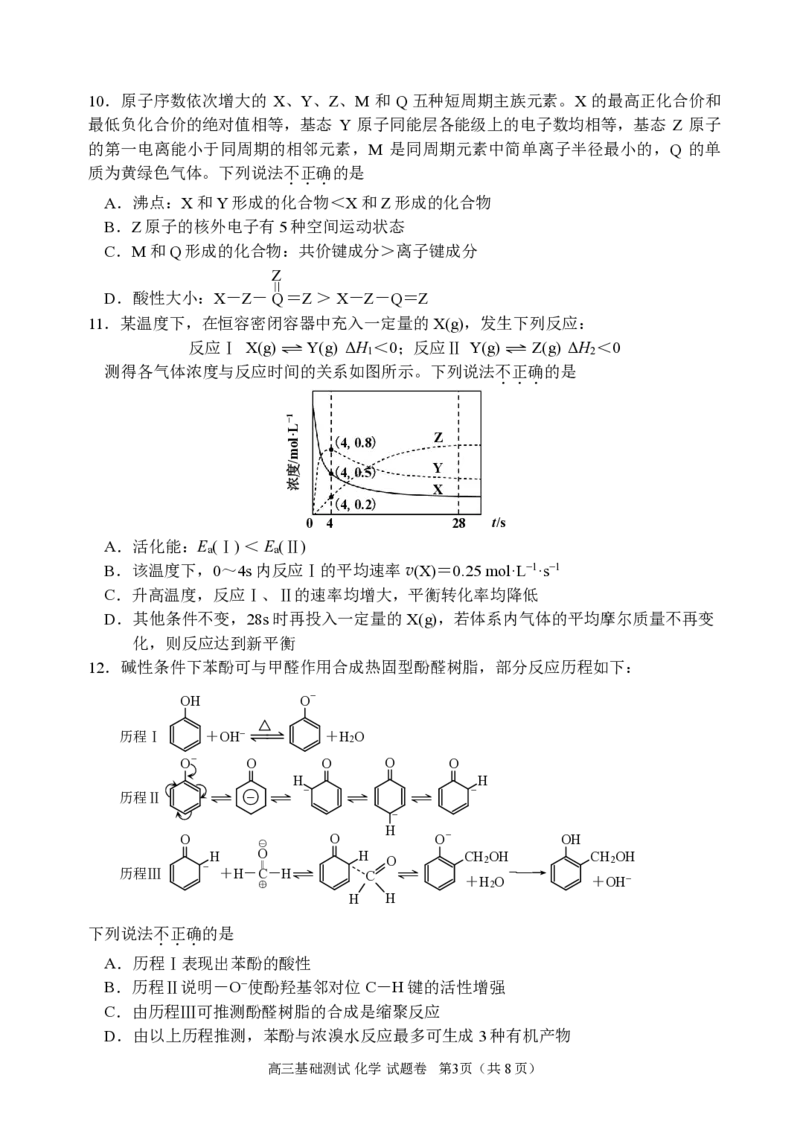
{#{QQABIYAEoggIQJBAARgCAwWICAAQkACCASgORBAIIAIBwQNABAA=}#}10.原子序数依次增大的 X、Y、Z、M和 Q五种短周期主族元素。X的最高正化合价和
最低负化合价的绝对值相等,基态 Y 原子同能层各能级上的电子数均相等,基态 Z 原子
的第一电离能小于同周期的相邻元素,M 是同周期元素中简单离子半径最小的,Q 的单
质为黄绿色气体。下列说法不正确的是
...
A.沸点:X和Y形成的化合物<X和Z形成的化合物
B.Z原子的核外电子有5种空间运动状态
C.M和Q形成的化合物:共价键成分>离子键成分
Z
‖
D.酸性大小:X-Z-Q=Z > X-Z-Q=Z
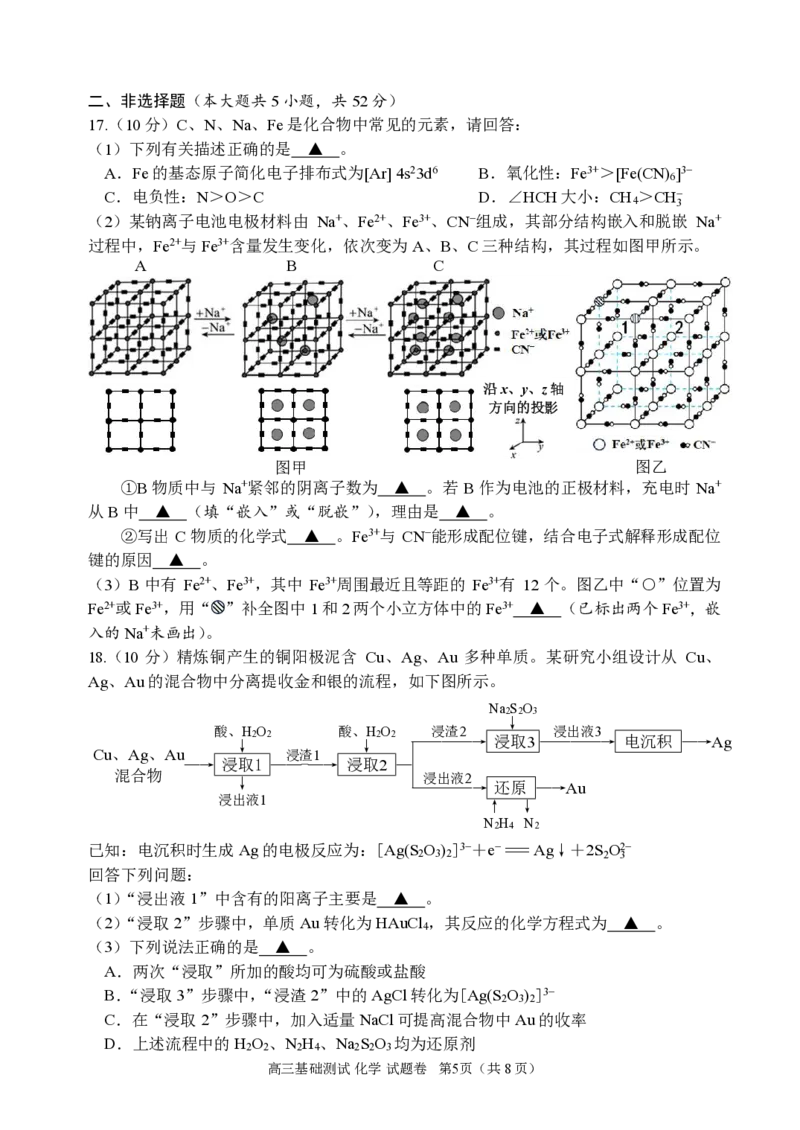
11.某温度下,在恒容密闭容器中充入一定量的X(g),发生下列反应:
反应Ⅰ X(g) ⇌ Y(g) ΔH 1 <0;反应Ⅱ Y(g) ⇌ Z(g) ΔH 2 <0
测得各气体浓度与反应时间的关系如图所示。下列说法不正确的是
...
A.活化能:E (Ⅰ) < E (Ⅱ)
a a
B.该温度下,0~4s内反应Ⅰ的平均速率v(X)=0.25 mol·L−1·s−1
C.升高温度,反应Ⅰ、Ⅱ的速率均增大,平衡转化率均降低
D.其他条件不变,28s时再投入一定量的X(g),若体系内气体的平均摩尔质量不再变
化,则反应达到新平衡
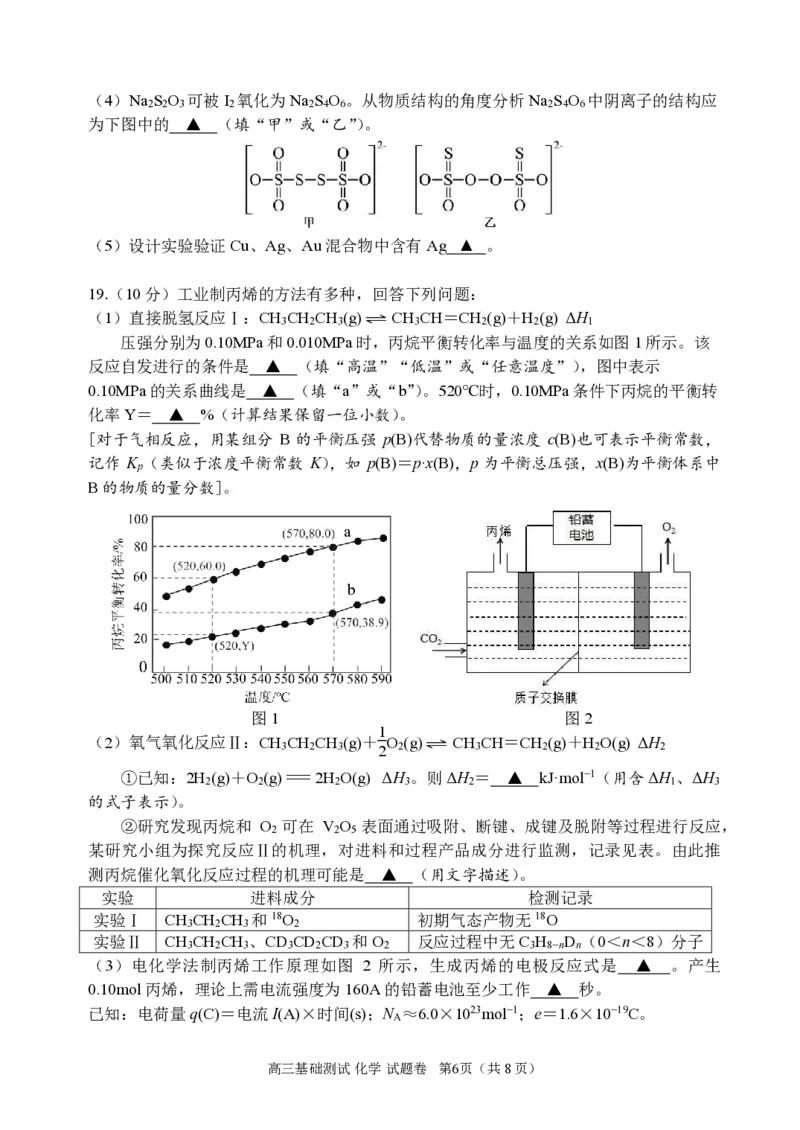
12.碱性条件下苯酚可与甲醛作用合成热固型酚醛树脂,部分反应历程如下:
OH O−
△
历程Ⅰ +OH− ⥫⥬ +H2O
O− O O O O
H H
历程Ⅱ ⇌ ○ − ⇌ − ⇌ ⇌ −
−
H
O O O− OH
○−
历程Ⅲ − H +H- ○ ‖ O + C-H⇌ H C O ⇌ C + H H 2O 2O H -—→ C + H O 2O H H −
H H
下列说法不正确的是
...
A.历程Ⅰ表现出苯酚的酸性
B.历程Ⅱ说明-O−使酚羟基邻对位C-H键的活性增强
C.由历程Ⅲ可推测酚醛树脂的合成是缩聚反应
D.由以上历程推测,苯酚与浓溴水反应最多可生成3种有机产物
高三基础测试 化学 试题卷 第3页(共8页)
1−L·lom/度浓
(4,0.8) Z
(4,0.5) Y
X
(4,0.2)
0 4 28 t/s
{#{QQABIYAEoggIQJBAARgCAwWICAAQkACCASgORBAIIAIBwQNABAA=}#}13.以Pt为电极,一定浓度的NaBr溶液为电解液,
采用电解和催化相结合的循环方式,可实现高效制
H 和O ,装置如图所示。下列说法不正确的是
2 2 ...
A.X为H ,Y为NaBr,Z为O
2 2
B.电极b连接电源正极
电解
C.电解总反应式为Br−+3H O ==== BrO−+3H ↑
2 3 2
D.催化阶段反应产物物质的量之比n(Z):n(Br−)=3:2
14.镓(Ga)常用作半导体的原料,能形成化合物 Ga I ,研究表明该物质由离子构成,
6 6
其阴离子[Ga I ]2−中所有原子的价层均有8个电子。以下说法不正确的是
2 6 ...
A.镓和碘均位于元素周期表的p区
B.化合物 Ga I 中镓的化合价不止一种
6 6
I
⟍ ↙
I
⟍ ⟋
I 2−
C.[Ga 2 I 6 ]2−的结构可以表示为 I⟋ Ga ⟍I ↗ Ga ⟍I
D.[Ga I ]2−中Ga原子的杂化方式为sp3
2 6
15.25℃时,草酸(H C O )的电离常数为K =5.0×10−2,K =5.4×10−5;CaC O 的
2 2 4 a1 a2 2 4
K =2.5×10−9;lg5≈0.7。常温下,下列说法不正确的是
sp ...
A.0.1 mol·L−1的KHC O 溶液呈酸性
2 4
B.若某溶液中c(H C O )=c(HC O−),溶液的pH约为1.3
2 2 4 2 4
C.草酸钙饱和溶液中c(C O2−) > c(HC O−)
2 4 2 4
D.Na C O 溶液中粒子浓度关系:c(OH−)-c(H+) < c(H C O )+c(HC O−)
2 2 4 2 2 4 2 4
16.下列实验方案设计和结论都正确的是
方案设计 现象 结论
向恒温恒容密闭玻璃容器中充入 对于反应前后气体分子
A 100mL HI 气体,分解达到平衡后再 气体颜色不变 数不变的可逆反应,改
充入100mL Ar 变压强平衡不移动
将一支盛有 2 mL 0.5mol·L−1 CuCl
B 溶液的试管水浴加热片刻,取出置 2 溶液颜色由蓝变黄 [Cu(H 2 O) 4 ]2++4Cl− ⇌
绿后再变蓝 [CuCl ]2−+4H O ΔH>0
于冷水中 4 2
向盛有等体积等物质的量浓度的
溶液中存在
C FeCl 和 KSCN 混合溶液的试管中加 溶液颜色变浅
入少
3
量铁粉
Fe3++3SCN−⇌Fe(SCN)
3
分别向两支盛有 1mL 5%H O 水溶
2 2
液的试管中滴 3 滴 0.05mol·L−1 的 滴加 AgNO 溶液 对 H O 分解反应,Ag+
3 2 2
D
CuSO 溶液和 0.05mol·L−1AgNO 溶 的试管产生气泡快 的催化能力优于Cu2+
4 3
液
高三基础测试 化学 试题卷 第4页(共8页)
{#{QQABIYAEoggIQJBAARgCAwWICAAQkACCASgORBAIIAIBwQNABAA=}#}二、非选择题(本大题共5小题,共52分)
17.(10分)C、N、Na、Fe是化合物中常见的元素,请回答:
(1)下列有关描述正确的是 ▲ 。
A.Fe的基态原子简化电子排布式为[Ar] 4s23d6 B.氧化性:Fe3+>[Fe(CN) ]3−
6
C.电负性:N>O>C D.∠HCH大小:CH >CH−
4 3
(2)某钠离子电池电极材料由 Na+、Fe2+、Fe3+、CN−组成,其部分结构嵌入和脱嵌 Na+
过程中,Fe2+与Fe3+含量发生变化,依次变为A、B、C三种结构,其过程如图甲所示。
A B C
沿x、y、z轴
方向的投影
图甲 图乙
①B物质中与 Na+紧邻的阴离子数为 ▲ 。若 B作为电池的正极材料,充电时 Na+
从B中 ▲ (填“嵌入”或“脱嵌”),理由是 ▲ 。
②写出 C物质的化学式 ▲ 。Fe3+与 CN−能形成配位键,结合电子式解释形成配位
键的原因 ▲ 。
(3)B 中有 Fe2+、Fe3+,其中 Fe3+周围最近且等距的 Fe3+有 12 个。图乙中“○”位置为
Fe2+或Fe3+,用“ ”补全图中1和2两个小立方体中的Fe3+ ▲ (已标出两个Fe3+,嵌
入的Na+未画出)。
18.(10 分)精炼铜产生的铜阳极泥含 Cu、Ag、Au 多种单质。某研究小组设计从 Cu、
Ag、Au的混合物中分离提收金和银的流程,如下图所示。
Na2S2O3
↓
酸、
↓
H2O2 酸、
↓
H2O2
——
浸
—
渣
—
2
→ 浸取3 —
浸
—
出
—
液
—
3
→ 电沉积 —→Ag
Cu、Ag、Au 浸渣1
—→ 浸取1 ——-—→ 浸取2 —
混合物 ↓ — 浸 — 出 — 液 — 2 → 还原 —→Au
浸出液1
↑ ↓
N2H4 N2
已知:电沉积时生成Ag的电极反应为:[Ag(S O ) ]3−+e−=Ag↓+2S O2−
2 3 2 2 3
回答下列问题:
(1)“浸出液1”中含有的阳离子主要是 ▲ 。
(2)“浸取2”步骤中,单质Au转化为HAuCl ,其反应的化学方程式为 ▲ 。
4
(3)下列说法正确的是 ▲ 。
A.两次“浸取”所加的酸均可为硫酸或盐酸
B.“浸取3”步骤中,“浸渣2”中的AgCl转化为[Ag(S O ) ]3−
2 3 2
C.在“浸取2”步骤中,加入适量NaCl可提高混合物中Au的收率
D.上述流程中的H O 、N H 、Na S O 均为还原剂
2 2 2 4 2 2 3
高三基础测试 化学 试题卷 第5页(共8页)
{#{QQABIYAEoggIQJBAARgCAwWICAAQkACCASgORBAIIAIBwQNABAA=}#}(4)Na S O 可被I 氧化为Na S O 。从物质结构的角度分析Na S O 中阴离子的结构应
2 2 3 2 2 4 6 2 4 6
为下图中的 ▲ (填“甲”或“乙”)。
(5)设计实验验证Cu、Ag、Au混合物中含有Ag ▲ 。
19.(10分)工业制丙烯的方法有多种,回答下列问题:
(1)直接脱氢反应Ⅰ:CH 3 CH 2 CH 3 (g) ⇌ CH 3 CH=CH 2 (g)+H 2 (g) ΔH 1
压强分别为0.10MPa和0.010MPa时,丙烷平衡转化率与温度的关系如图1所示。该
反应自发进行的条件是 ▲ (填“高温”“低温”或“任意温度”),图中表示
0.10MPa的关系曲线是 ▲ (填“a”或“b”)。520℃时,0.10MPa条件下丙烷的平衡转
化率Y= ▲ %(计算结果保留一位小数)。
[对于气相反应,用某组分 B 的平衡压强 p(B)代替物质的量浓度 c(B)也可表示平衡常数,
记作 K (类似于浓度平衡常数 K),如 p(B)=p·x(B),p为平衡总压强,x(B)为平衡体系中
p
B的物质的量分数]。
a
b
图1 图2
1
(2)氧气氧化反应Ⅱ:CH 3 CH 2 CH 3 (g)+ 2 O 2 (g) ⇌ CH 3 CH=CH 2 (g)+H 2 O(g) ΔH 2
①已知:2H (g)+O (g)=2H O(g) ΔH 。则ΔH = ▲ kJ·mol−1(用含ΔH 、ΔH
2 2 2 3 2 1 3
的式子表示)。
②研究发现丙烷和 O 可在 V O 表面通过吸附、断键、成键及脱附等过程进行反应,
2 2 5
某研究小组为探究反应Ⅱ的机理,对进料和过程产品成分进行监测,记录见表。由此推
测丙烷催化氧化反应过程的机理可能是 ▲ (用文字描述)。
实验 进料成分 检测记录
实验Ⅰ CH CH CH 和18O 初期气态产物无18O
3 2 3 2
实验Ⅱ CH CH CH 、CD CD CD 和O 反应过程中无C H D (0<n<8)分子
3 2 3 3 2 3 2 3 8−n n
(3)电化学法制丙烯工作原理如图 2 所示,生成丙烯的电极反应式是 ▲ 。产生
0.10mol丙烯,理论上需电流强度为160A的铅蓄电池至少工作 ▲ 秒。
已知:电荷量q(C)=电流I(A)×时间(s);N ≈6.0×1023mol−1;e=1.6×10−19C。
A
高三基础测试 化学 试题卷 第6页(共8页)
{#{QQABIYAEoggIQJBAARgCAwWICAAQkACCASgORBAIIAIBwQNABAA=}#}20.(10分)利用 MnO 和 H SO 生成 MnS O 进而制备连二硫酸钠晶体(Na S O ·2H O)。
2 2 3 2 6 2 2 6 2
相关物质性质见下表。
物质(化学式) MnS O Na S O ·2H O
2 6 2 2 6 2
摩尔质量(g·mol−1) 215 242
空气中易分解 空气中不易变质
主要性质
均可溶于水,pH<2.5时会释放出SO 气体
2
操作流程如下:
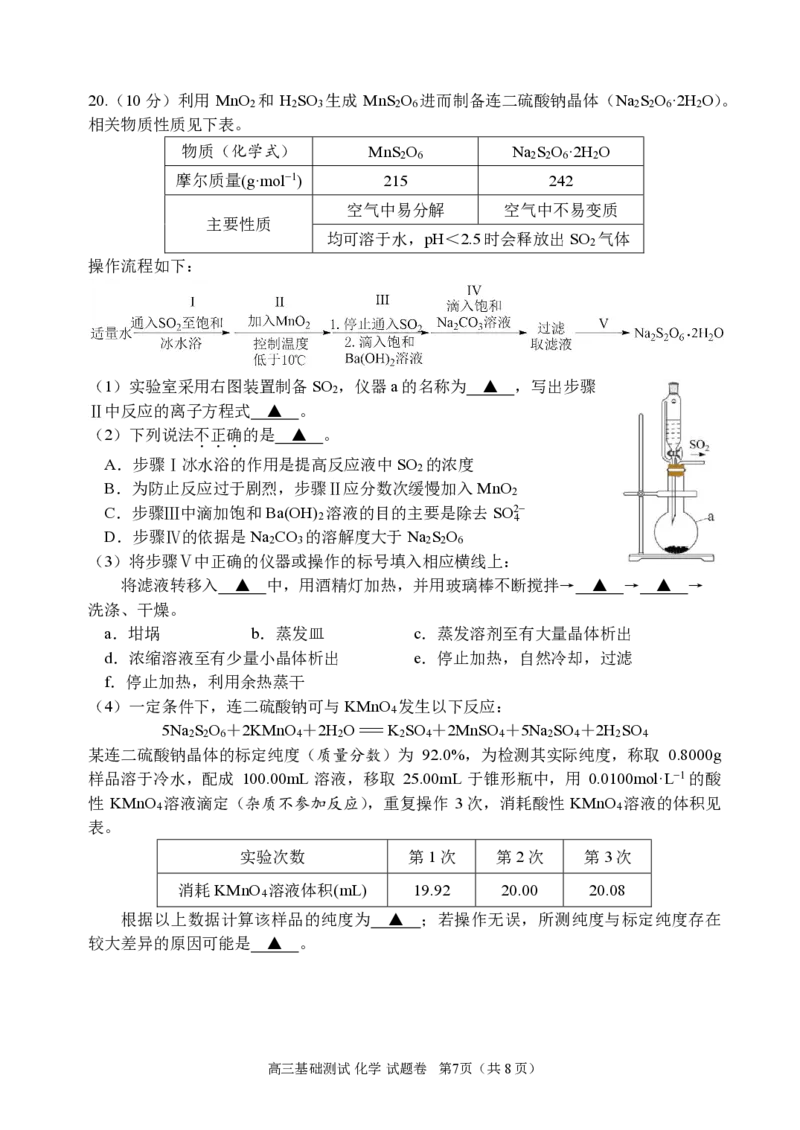
(1)实验室采用右图装置制备SO ,仪器a的名称为 ▲ ,写出步骤
2
Ⅱ中反应的离子方程式 ▲ 。
(2)下列说法不正确的是 ▲ 。
...
A.步骤Ⅰ冰水浴的作用是提高反应液中SO 的浓度
2
B.为防止反应过于剧烈,步骤Ⅱ应分数次缓慢加入MnO
2
C.步骤Ⅲ中滴加饱和Ba(OH) 溶液的目的主要是除去SO2−
2 4
D.步骤Ⅳ的依据是Na CO 的溶解度大于Na S O
2 3 2 2 6
(3)将步骤Ⅴ中正确的仪器或操作的标号填入相应横线上:
将滤液转移入 ▲ 中,用酒精灯加热,并用玻璃棒不断搅拌→ ▲ → ▲ →
洗涤、干燥。
a.坩埚 b.蒸发皿 c.蒸发溶剂至有大量晶体析出
d.浓缩溶液至有少量小晶体析出 e.停止加热,自然冷却,过滤
f.停止加热,利用余热蒸干
(4)一定条件下,连二硫酸钠可与KMnO 发生以下反应:
4
5Na S O +2KMnO +2H O=K SO +2MnSO +5Na SO +2H SO
2 2 6 4 2 2 4 4 2 4 2 4
某连二硫酸钠晶体的标定纯度(质量分数)为 92.0%,为检测其实际纯度,称取 0.8000g
样品溶于冷水,配成 100.00mL 溶液,移取 25.00mL 于锥形瓶中,用 0.0100mol·L−1的酸
性 KMnO 溶液滴定(杂质不参加反应),重复操作 3次,消耗酸性 KMnO 溶液的体积见
4 4
表。
实验次数 第1次 第2次 第3次
消耗KMnO 溶液体积(mL) 19.92 20.00 20.08
4
根据以上数据计算该样品的纯度为 ▲ ;若操作无误,所测纯度与标定纯度存在
较大差异的原因可能是 ▲ 。
高三基础测试 化学 试题卷 第7页(共8页)
{#{QQABIYAEoggIQJBAARgCAwWICAAQkACCASgORBAIIAIBwQNABAA=}#}21.(12分)G是合成一种治疗胃食管反流疾病药物的关键中间体,其合成过程如下:
O
HN — C — HB — r(C — H — O) →2
H
N
O
H H
HN N
N
A B —→H O H — (C — H —3C — O — )2O →
HO
O N
O O
C H —→……—→ O H
2 4 H
D
O
C
O
C 20 H 20 N 2 O 4 — 1) — N - aO -- H - 溶 -— 液 — /△ → C 16 H 14 N 2 O 3 - 1 - ) - S -— OC - l -2—→ H N N
E 2)H+ F 2)NH(CH3)2 H N H
OH
G
O
H H
N N
已知:①R-COOH+ —
(
—
CH —3C
—
O) —2O
→
R
N N
② O不稳定,能快速异构化为 OH
H
NaCN
③R-X———→ R-CN
请回答:
(1)CHBr(CHO) 中含氧官能团的名称是 ▲ 。
2
(2)写出B+C→D的化学方程式 ▲ 。
(3)下列说法不正确的是 ▲ 。
...
A.在气态下,NH(CH ) 的碱性强于CH NH
3 2 3 2
B.A→B的过程只有取代反应
C.F→G中SOCl 的作用是将-COOH变为-COCl,更易与NH(CH ) 反应
2 3 2
D.G的分子式为C H N O
16 13 3 2
(4)化合物E的结构简式为 ▲ 。
(5)设计以乙烯为原料合成C的路线(用流程图表示,无机试剂任选) ▲ 。
(6)写出4种同时符合下列条件的化合物A的同分异构体的结构简式 ▲ 。
①核磁共振氢谱图显示有5组峰;红外光谱图显示没有氮氮单键。
②除苯环外没有其他环且苯环上有三个取代基。
高三基础测试 化学 试题卷 第8页(共8页)
{#{QQABIYAEoggIQJBAARgCAwWICAAQkACCASgORBAIIAIBwQNABAA=}#}