文档内容
第 04 讲 化学平衡状态 化学平衡常数
模块一 思维导图串知识 1.知道可逆反应概念,认识化学平衡状态的特征,理解化学平
模块二 基础知识全梳理 衡的判断方法。
模块三 重点难点必掌握 2.认识化学平衡常数是表示反应限度的物理量,知道化学平衡
模块四 核心考点精准练 常数的含义并能进行有关计算。
模块五 小试牛刀过关测 3.了解浓度商和化学平衡常数的相对大小与反应方向间的联
系。
一.可逆反应
概念 在相同条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应
双向性 可逆反应分为方向相反的两个反应方向:正反应方向和逆反应方向
三特征 双同性 正、逆反应是在同一条件下,同时进行
共存性 反应物与生成物共存(反应物的转化率小于 100%)
二.化学平衡
1.概念
在一定条件下的可逆反应体系中,当正、逆反应速率相等时,反应物和生成物的浓度均保持不变,即体系
的组成不随时间而改变,表明该反应中物质的转化达到了“限度”,这时的状态称之为化学平衡状态,简
称化学平衡。
2.化学平衡的建立
条件 ①可逆反应;②封闭体系中;③一定的反应条件(温度、压强等)
化学平衡
①可加入反应物,从正反应开始;②可加入生成物,从逆反应开始;③也可同时
状态的建立 途径
加入反应物和生成物,从正、逆向同时开始
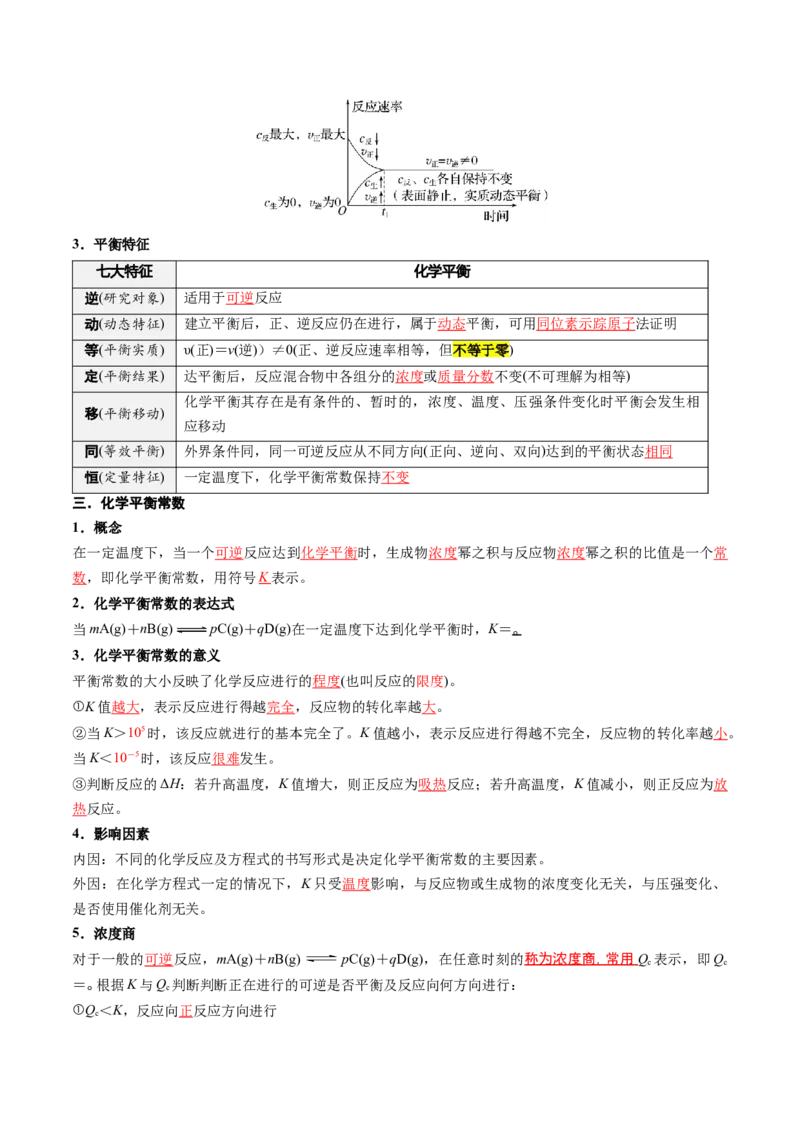
绘制“反应速率-时间”图像,表示从正反应开始建立化学平衡状态的过程。3.平衡特征
七大特征 化学平衡
逆(研究对象) 适用于可逆反应
动(动态特征) 建立平衡后,正、逆反应仍在进行,属于动态平衡,可用同位素示踪原子法证明
等(平衡实质) υ(正)=v(逆))≠0(正、逆反应速率相等,但不等于零)
定(平衡结果) 达平衡后,反应混合物中各组分的浓度或质量分数不变(不可理解为相等)
化学平衡其存在是有条件的、暂时的,浓度、温度、压强条件变化时平衡会发生相
移(平衡移动)
应移动
同(等效平衡) 外界条件同,同一可逆反应从不同方向(正向、逆向、双向)达到的平衡状态相同
恒(定量特征) 一定温度下,化学平衡常数保持不变
三.化学平衡常数
1.概念
在一定温度下,当一个可逆反应达到化学平衡时,生成物浓度幂之积与反应物浓度幂之积的比值是一个常
数,即化学平衡常数,用符号K 表示。
2.化学平衡常数的表达式
当mA(g)+nB(g) pC(g)+qD(g)在一定温度下达到化学平衡时,K=。
3.化学平衡常数的意义
平衡常数的大小反映了化学反应进行的程度(也叫反应的限度)。
①K值越大,表示反应进行得越完全,反应物的转化率越大。
②当K>105时,该反应就进行的基本完全了。K值越小,表示反应进行得越不完全,反应物的转化率越小。
当K<10-5时,该反应很难发生。
③判断反应的ΔH:若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放
热反应。
4.影响因素
内因:不同的化学反应及方程式的书写形式是决定化学平衡常数的主要因素。
外因:在化学方程式一定的情况下,K只受温度影响,与反应物或生成物的浓度变化无关,与压强变化、
是否使用催化剂无关。
5.浓度商
对于一般的可逆反应,mA(g)+nB(g) pC(g)+qD(g),在任意时刻的称为浓度商,常用 Q 表示,即Q
c c
=。根据K与Q 判断判断正在进行的可逆是否平衡及反应向何方向进行:
c
①Q<K,反应向正反应方向进行
c②Q=K,反应处于平衡状态
c
③Q>K,反应向逆反应方向进行
c
1.平衡常数K的书写
①固体或纯液体和液态水不列入平衡常数的表达式中(注意有机反应中的HO则应写入)。
2
②平衡常数的表达式与化学方程式的书写方式有关,如N+3H 2NH ,K=a,则有:
2 2 3
2NH N+3H,K′=;N+H NH ,K″=。
3 2 2 2 2 3
③对于给定的化学方程式,正逆反应的平衡常数互为倒数。
2.K值的大小只能预示着某种可逆反应向某方向进行的最大程度,但不能预示反应达到平衡所需时间。
1.化学平衡状态的判断方法
(1)本质标志
正逆反应速率相等、各组分的量保持不变。
项目 mA(g)+nB(g) pC(g)+qD(g) 是否平衡
在单位时间内消耗了m mol A的同时生成了m mol A √
正反应速率逆 在单位时间内消耗了n mol B的同时消耗了p mol C √
反应速率关系 在单位时间内生成了n mol B的同时消耗了q mol D ×
v (A)∶v (B)=m∶n √
正 逆
(2)等价标志
项目 mA(g)+nB(g) pC(g)+qD(g)[只有A为有色气体] 是否平衡
各物质的物质的量或物质的量的分数一定 √
各物质的质量或质量分数一定 √
混合体系中 各气体的体积或体积分数一定 √
各组分的含量 总物质的量一定 不一定
A物质断裂的化学键与A物质形成的化学键的物质的量相等 √
气体的颜色不变 √
任何化学反应都伴随着能量变化,在其他条件不变时,体系温度
温度 √
一定时
(3)特殊标志
项目 mA(g)+nB(g) pC(g)+qD(g) 是否平衡
当m+n≠p+q时,总压强一定(其它条件一定) √
压强
当m+n=p+q时,总压强一定(其它条件一定) 不一定
混合气体的平均 当m+n=p+q时,M 一定 不一定
相对分子质量 当m+n≠p+q时,M 一定 √
密度 C(s)+CO 2 (g) 2CO(g) (ρ一定) √N(g)+3H(g) 2NH (g) (ρ一定) 不一定
2 2 3
(体积不变)
H(g)+I(g) 2HI(g) (ρ一定) 不一定
2 2
❶审题时,一看题干条件:恒温恒容或恒温恒压或绝热容器;二看化学反应特点(物质状态、气体计量系
数):全部是气体参与,是等体积反应还是非等体积反应。
❷判断可逆反应是否达到平衡时,容易犯以下错误:①若反应前后气体体积不变,则混合气体总体积、总压
强、总物质的量、混合气体平均相对分子质量保持定值不能说明反应达到平衡状态;②若反应物和生成物的
物质的量之比等于化学计算数之比,不能说明达到平衡状态;③若反应前后气体的密度一定,不能说明一定
达到平衡状态。
2.化学平衡常数的计算
“三段式法”是有效解答化学平衡计算题的“万能钥匙”。解题时,要注意准确地列出起始量、变化量、
平衡量,按题目要求进行计算,同时还要注意单位的统一。
分析三个量:起始量、变化量、平衡量。
(1)明确三个关系
①对于同一反应物,起始量-变化量=平衡量。
②对于同一生成物,起始量+变化量=平衡量。
③各物质的转化量之比等于各物质的化学计量数之比。
(2)计算模式
对以下反应:mA(g)+nB(g) pC(g)+qD(g),令A、B起始物质的量分别为a、b,达到平衡后,A的
消耗量为mx mol,容器容积为V L。
mA(g)+nB(g) pC(g)+qD(g)
起始/mol a b 0 0
变化/mol mx nx p x qx
平衡/mol a-mx b-nx px qx
则有①平衡常数:K=。
②A的平衡浓度:c(A)= mol·L-1。
③A的转化率:α(A)=×100%,α(A)∶α(B)=∶=。
④A的体积分数:φ(A)=×100%。
⑤平衡压强与起始压强之比:=。
⑥混合气体的平均密度(混)= g·L-1。
⑦混合气体的平均摩尔质量= g·mol-1。
⑧生成物的产率:实际产量(指生成物)占理论产量的百分数,即产率=×100%。
一般来讲,转化率越大,原料利用率越高,产率越大。
考点一:化学平衡1.(23-24高二上·安徽马鞍山·阶段练习)恒温恒容条件,进行如下反应: ,已知
、 、 的起始浓度分别为 、 、 ,总压强为 ,在一定条件下,当反应达
到平衡时,各物质的物质的量浓度或分压有可能是
A. 的分压为 B. 的浓度为
C. 的分压为 D.Z的浓度为
【答案】B
【解析】 、 、 的起始浓度分别为 、 、 ,由于反应物和生成物都加入,
不能确定向哪个方向建立平衡,进行极端情况讨论:
①假设正向彻底进行,则 、 、 的起始浓度分别为 、 、 ;
②假设逆向彻底进行,则 、 、 的起始浓度分别为 、 、 ;
实际平衡时的数据在上述两种极端情况之间,但达不到极端值;
A.第①种极端值 的分压为 ,不能达到,故A不选;
B. 的浓度为 ,在上述两种极端情况之间,可能达到,故B选;
C.第②种极端值 的分压为 ,不能达到,故C不选;
D.Z的浓度为 为第①种极端值,不能达到,故D不选。
答案选B。
2.(23-24高二下·山东青岛·期中)一定温度下,向1L恒容密闭容器中充入2mol NO与2mol CO发生反应:
。下列说法正确的是
A.气体的平均相对分子质量不再变化时说明反应已达平衡状态
B.反应达平衡后,降低温度, 增大, 减小,平衡正向移动
C.反应达平衡时, 与 一定满足
D.及时分离出产物 ,既能增大平衡转化率又能加快反应速率
【答案】A
【解析】A.反应前后质量守恒,但反应气体体积数减小,说明反应后气体平均相对分子量会增大,故气
体的平均相对分子质量不再变化时说明反应已达平衡状态,A正确;
B.降低温度,正逆反应速率都减小,B错误;
C.同一反应各物质表示的反应速率之比等于化学计量数之比,故v (CO)=2v (N ),反应到平衡时,有v
正 正 2
(N )=v (N ),故v (CO)=2v (N ),C错误;
正 2 逆 2 正 逆 2
D.根据勒夏特列原理,及时分离出CO,使生成物CO 浓度减小,平衡正向移动,平衡转化率增大,但
2 2
是生成物物浓度减小无法加快反应速率,D错误;本题选A。
3.(23-24高二下·湖南长沙·期中)对燃油尾气污染物进行脱硝处理有助于减少空气污染,可使用氨将氮
氧化物 转化为无害气体,发生的反应为 。下列说法正确的是
A.标准状况下, 的体积约为
B. 可用作食品的保护气,原因是 的化学性质不活泼
C.该反应中, 与足量的 反应,理论上可得到
D.该反应中,每断裂 键,同时转移电子的物质的量为
【答案】A
【解析】A. 的物质的量为 =0.2mol,标准状况下, 的体积约为22.4L/
mol×0.2mol= ,A正确;
B. 可用作食品的保护气,原因是常温下 的化学性质不活泼,B错误;
C.该反应是可逆反应,该反应中, 与足量的 反应,理论上可得到 的物质的
量小于0.6mol,C错误;
D.该反应中,N元素由-3价上升到0价,又由+2价下降到0价,每断裂1.2molN-H键,同时转移电子的
物质的量为1.2mol,D错误;
故选A。
4.(23-24高二下·北京·开学考试)恒温恒压条件下,在一个容积可变的容器中发生可逆反应:
,不能作为该反应达到平衡状态的标志的是
A.容器内硫元素的质量分数不变
B. 的消耗速率和 的消耗速率之比为1:1
C.混合气体的密度不变
D.混合气体的平均摩尔质量不变
【答案】A
【解析】A.根据元素守恒可判断容器内硫元素的质量分数始终不变,不能据此判断反应达到平衡状态,A
选;
B. 的消耗速率和 的消耗速率之比为1:1,根据方程式可知正逆反应速率相等,达到平衡状态,B
不选;
C.反应前后混合气体的质量不变,容器容积是变化的,即密度是变化的,所以混合气体的密度不变,说
明反应达到平衡状态,C不选;
D.反应前后混合气体的质量不变,物质的量是变化的,因此平均摩尔质量是变化的,则混合气体的平均
摩尔质量不变,说明反应达到平衡状态,D不选;
答案选A。5.(22-23高二上·北京·期中)在5L密闭容器中进行反应2SO (g)+O(g) 2SO (g),30秒后,SO 的物质
2 2 3 3
的量增加了0.3mol。下列叙述不正确的是
A.v(SO )=0.002 mol·L-1.s-1
3
B.v(O )=0.001 mol·L-1.s-1
2
C.当容器内气体密度不再变化时,反应达到平衡
D.当容器内的SO 的浓度不再增加时,反应达到平衡
3
【答案】C
【解析】A. ,故A正确;
B. ,故B正确;
C. ,密度始终不变,当容器内气体密度不再变化时,不能判断反应达到平衡,故C错误;
D. 一直在变化,当容器内的SO 的浓度不再增加时,反应达到平衡,故D正确;
3
故答案为C。
6.(23-24高二上·北京海淀·期中)在恒容密闭容器中反应 该反应达平衡的标志是
①混合气颜色不随时间的变化
②数值上v(NO 生成)=2v(NO 消耗)
2 2 4
③混合气体的密度不随时间的变化
④压强不随时间的变化而变化
⑤混合气的平均分子量不变
A.②⑤④ B.①④⑤ C.①③④ D.①②③
【答案】B
【解析】①二氧化氮是红棕色气体,四氧化二氮是无色气体,当混合气体颜色不随时间变化说明各组分含
量不再变化,正确;
②数值上v(NO 生成)=2v(NO 消耗),对于任意时刻恒成立,错误;
2 2 4
③恒容容器,反应物和生成物都是气体,气体的质量和体积恒定,密度是个恒定值,无法判断平衡,错误;
④正向体积减小,恒容容器中压强不再变化,说明各组分含量不再改变,正确;
⑤正向体积减小,气体的物质的量变化,质量恒定,平均相对分子量是个变值,不再变化说明各组分含量
不再改变,正确;
综上所述,①④⑤符合题意,故选B。
考点二:化学平衡常数
7.(23-24高二下·上海·期中)只改变一个影响因素,平衡常数 与化学平衡移动的关系叙述正确的是
A. 变化,平衡可能不移动 B. 变化,平衡一定移动
C.平衡不移动, 可能变化 D.平衡移动, 一定变化
【答案】B【分析】化学平衡常数K只受温度影响,K发生变化,证明温度发生改变,温度改变,化学平衡一定发生
移动;反之,平衡移动受很多因素影响,平衡不移动,K一定不变,平衡移动,K不一定变化,由此分析
回答;
【解析】A.由分析可知, 变化,平衡一定移动,A错误;
B.由分析可知, 变化,平衡一定移动,B正确;
C.由分析可知,平衡不移动,温度没变,K不可能变化,C错误;
D.由分析可知,平衡移动, 不一定变化,D错误;
故选B。
8.(23-24高二下·北京·开学考试)向恒容密闭容器中加入1 mol 和一定量的 ,发生反应:
。不同投料比 时, 的平衡转化率随温度的变化
曲线如图所示。下列说法不正确的是
A.
B.该反应为吸热反应
C.点a、b、c对应的平衡常数:
D.投料比固定,当容器内压强不再改变时,反应达到平衡状态
【答案】D
【解析】A.x增大,CO 的量增加,平衡正向移动,根据勒夏特列原理CO 的转化率减小,因此,A正确;
2 2
B.由图像,温度升高,CO 平衡转化率增大,说明平衡正向移动,吸热反应升温有利于平衡正向移动,B
2
正确;
C.b、c两点温度相同,同一反应的K只受温度影响,故Kc=Kb,a点平衡转化率更低,说明反应平衡时
正向程度小,Ka更小,故Ka