文档内容
19 化学反应速率、平衡原理在物质制备中的调控作
用
1.化学反应方向的判定
(1)自发反应
在一定条件下无需外界帮助就能自发进行的反应称为自发反应。
(2)熵和熵变的含义
①熵的含义
熵是衡量一个体系混乱度的物理量。用符号S 表示。同一条件下,不同物质有不同的熵值,
同一物质在不同状态下熵值也不同,一般规律是S(g)>S(l)>S(s)。
②熵变的含义
熵变是反应前后体系熵的变化,用 Δ S 表示,化学反应的ΔS越大,越有利于反应自发进行。
(3)判断化学反应方向的判据
ΔG=ΔH-TΔS
ΔG<0时,反应能自发进行;
ΔG=0时,反应达到平衡状态;
ΔG>0时,反应不能自发进行。
2.控制反应条件的目的
(1)促进有利的化学反应:通过控制反应条件,可以加快化学反应速率,提高反应物的转化
率,从而促进有利的化学反应进行。
(2)抑制有害的化学反应:通过控制反应条件,也可以减缓化学反应速率,减少甚至消除有
害物质的产生或控制副反应的发生,从而抑制有害的化学反应继续进行。
3.控制反应条件的基本措施
(1)控制化学反应速率的措施
通过改变反应体系的温度、溶液的浓度、气体的压强(或浓度)、固体的表面积以及使用催化
剂等途径调控反应速率。
(2)提高转化率的措施
通过改变可逆反应体系的温度、溶液的浓度、气体的压强(或浓度)等改变可逆反应的限度,
从而提高转化率。
如:
以工业合成氨为例,理解运用化学反应原理选择化工生产中的适宜条件
①反应原理:N(g)+3H(g)2NH (g) ΔH=-92.4 kJ·mol-1。
2 2 3②
③从反应快慢和反应限度两个角度选择反应条件
④综合考虑——选择适宜的生产条件
a.温度:400~500 ℃
b.压强:10~30 MPa
c.投料比:=
d.以铁触媒作催化剂
e.采用循环操作提高原料利用率
1.二氧化碳是一种宝贵的碳氧资源。以CO 和NH 为原料合成尿素是固定和利用CO 的成
2 3 2
功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH (g)+CO(g)NH COONH(s) ΔH=-159.47 kJ·mol-1
3 2 2 4 1
反应Ⅱ:NH COONH(s)CO(NH)(s)+HO(g) ΔH=+72.49 kJ·mol-1
2 4 2 2 2 2
请回答下列问题:
(1)写出CO 和NH 为原料生成尿素和气态水的热化学方程式:_______________________,
2 3
反应Ⅱ自发进行的条件是______________________________________________________。
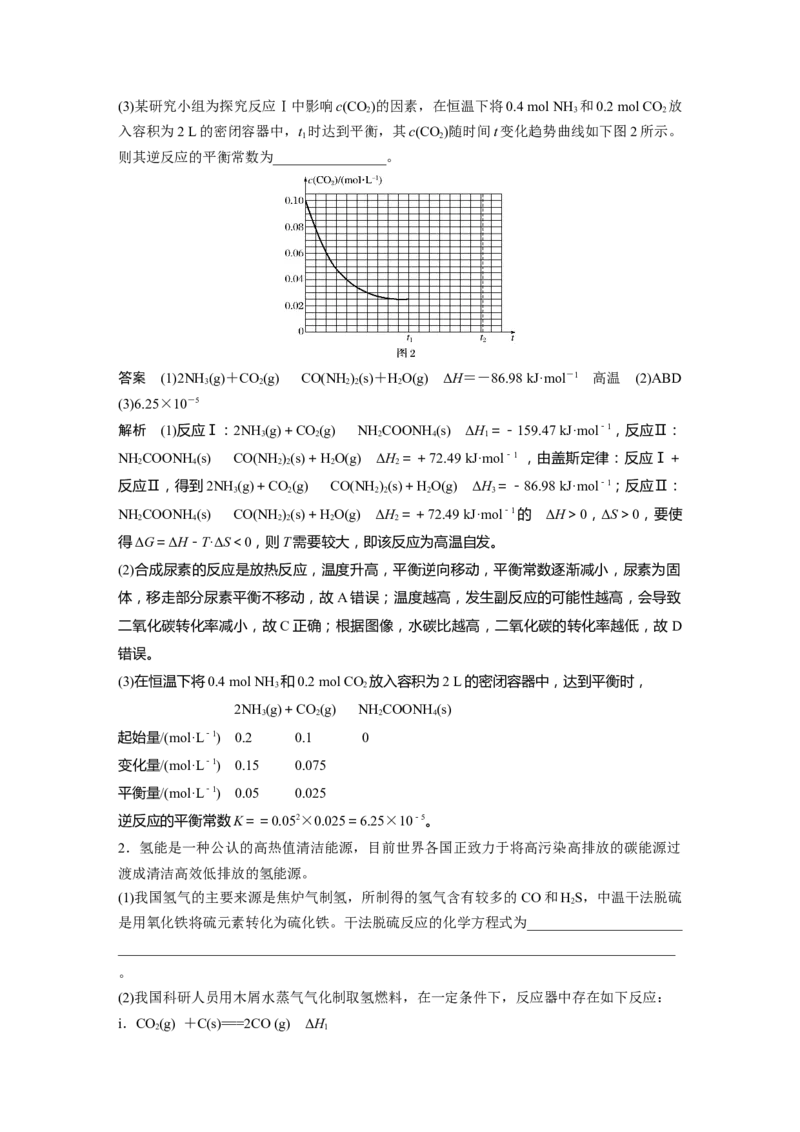
(2)CO 和NH 为原料合成尿素的反应中影响CO 转化率的因素很多,图1为某特定条件下,
2 3 2
不同水碳比和温度影响CO 转化率变化的趋势曲线。
2
下列说法不正确的是________(填字母)。
A.温度升高该反应平衡常数逐渐减小,移走部分尿素平衡向正方向移动
B.当温度低于190 ℃,随温度升高CO 转化率逐渐增大,其原因可能是温度升高平衡向正
2
方向移动
C.当温度高于190 ℃后,随温度升高CO 转化率逐渐减小,其原因可能是温度升高发生了
2
副反应
D.其他条件相同时,为提高CO 的转化率,生产中可以采取的措施是提高水碳比
2(3)某研究小组为探究反应Ⅰ中影响c(CO)的因素,在恒温下将0.4 mol NH 和0.2 mol CO 放
2 3 2
入容积为2 L的密闭容器中,t 时达到平衡,其c(CO)随时间t变化趋势曲线如下图2所示。
1 2
则其逆反应的平衡常数为________________。
答案 (1)2NH (g)+CO(g)CO(NH)(s)+HO(g) ΔH=-86.98 kJ·mol-1 高温 (2)ABD
3 2 2 2 2
(3)6.25×10-5
解析 (1)反应Ⅰ:2NH (g)+CO(g)NH COONH(s) ΔH =-159.47 kJ·mol-1,反应Ⅱ:
3 2 2 4 1
NH COONH(s)CO(NH)(s)+HO(g) ΔH =+72.49 kJ·mol-1 ,由盖斯定律:反应Ⅰ+
2 4 2 2 2 2
反应Ⅱ,得到2NH (g)+CO(g)CO(NH)(s)+HO(g) ΔH =-86.98 kJ·mol-1;反应Ⅱ:
3 2 2 2 2 3
NH COONH(s)CO(NH)(s)+HO(g) ΔH =+72.49 kJ·mol-1的 ΔH>0,ΔS>0,要使
2 4 2 2 2 2
得ΔG=ΔH-T·ΔS<0,则T需要较大,即该反应为高温自发。
(2)合成尿素的反应是放热反应,温度升高,平衡逆向移动,平衡常数逐渐减小,尿素为固
体,移走部分尿素平衡不移动,故 A错误;温度越高,发生副反应的可能性越高,会导致
二氧化碳转化率减小,故C正确;根据图像,水碳比越高,二氧化碳的转化率越低,故 D
错误。
(3)在恒温下将0.4 mol NH 和0.2 mol CO 放入容积为2 L的密闭容器中,达到平衡时,
3 2
2NH (g)+CO(g)NH COONH(s)
3 2 2 4
起始量/mol·L-1 0.2 0.1 0
变化量/mol·L-1 0.15 0.075
平衡量/mol·L-1 0.05 0.025
逆反应的平衡常数K==0.052×0.025=6.25×10-5。
2.氢能是一种公认的高热值清洁能源,目前世界各国正致力于将高污染高排放的碳能源过
渡成清洁高效低排放的氢能源。
(1)我国氢气的主要来源是焦炉气制氢,所制得的氢气含有较多的 CO和HS,中温干法脱硫
2
是用氧化铁将硫元素转化为硫化铁。干法脱硫反应的化学方程式为______________________
_______________________________________________________________________________
。
(2)我国科研人员用木屑水蒸气气化制取氢燃料,在一定条件下,反应器中存在如下反应:
i.CO(g) +C(s)===2CO (g) ΔH
2 1ii.C(s)+HO(g)===CO(g)+H(g) ΔH
2 2 2
iii.C(s)+2H(g)===CH(g) ΔH
2 4 3
iv.CO(g)+HO(g)===CO(g)+H(g) ΔH
2 2 2 4
v.CH(g)+2HO(g)===CO(g)+4H(g) ΔH
4 2 2 2 5
①ΔH=________(用含ΔH、ΔH、ΔH 或ΔH 的式子表示)。
5 1 2 3 4
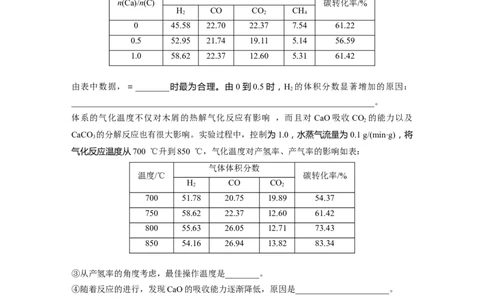
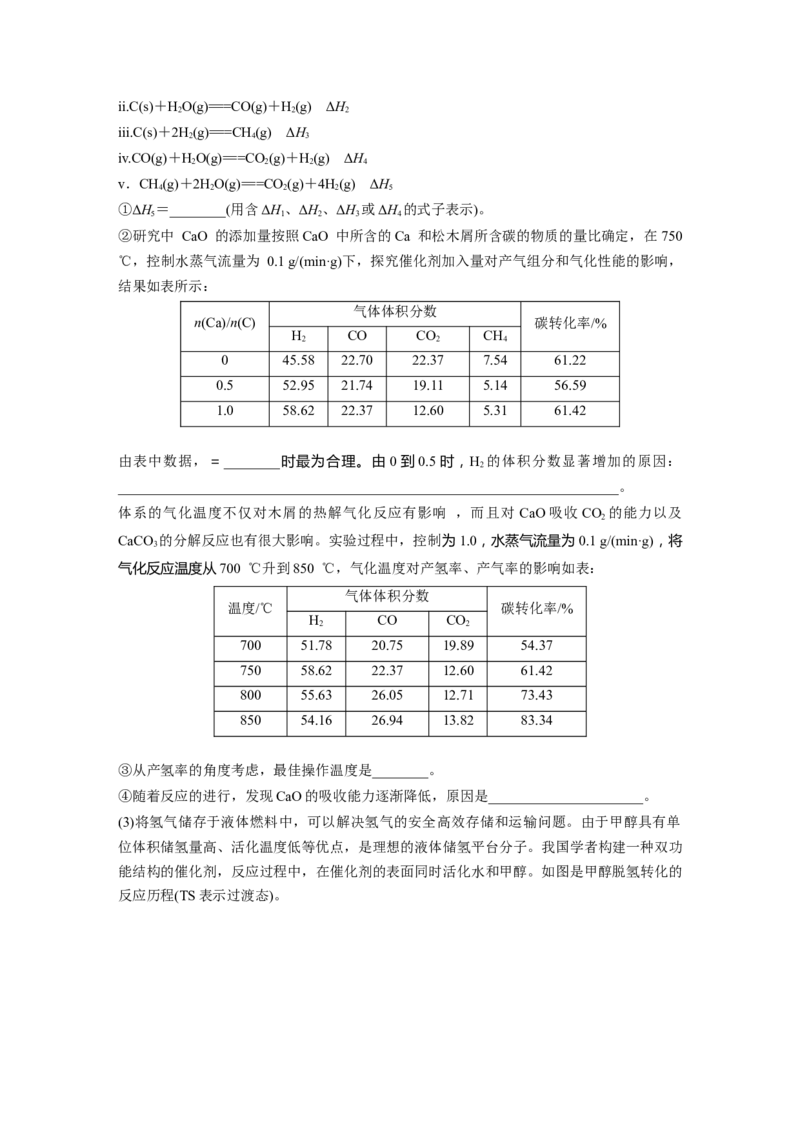
②研究中 CaO 的添加量按照CaO 中所含的Ca 和松木屑所含碳的物质的量比确定,在750
℃,控制水蒸气流量为 0.1 g/(min·g)下,探究催化剂加入量对产气组分和气化性能的影响,
结果如表所示:
气体体积分数
n(Ca)/n(C) 碳转化率/%
H CO CO CH
2 2 4
0 45.58 22.70 22.37 7.54 61.22
0.5 52.95 21.74 19.11 5.14 56.59
1.0 58.62 22.37 12.60 5.31 61.42
由表中数据,=________时最为合理。由 0到0.5时,H 的体积分数显著增加的原因:
2
_______________________________________________________________________。
体系的气化温度不仅对木屑的热解气化反应有影响 ,而且对 CaO吸收CO 的能力以及
2
CaCO 的分解反应也有很大影响。实验过程中,控制为1.0,水蒸气流量为0.1 g/(min·g),将
3
气化反应温度从700 ℃升到850 ℃,气化温度对产氢率、产气率的影响如表:
气体体积分数
温度/℃ 碳转化率/%
H CO CO
2 2
700 51.78 20.75 19.89 54.37
750 58.62 22.37 12.60 61.42
800 55.63 26.05 12.71 73.43
850 54.16 26.94 13.82 83.34
③从产氢率的角度考虑,最佳操作温度是________。
④随着反应的进行,发现CaO的吸收能力逐渐降低,原因是______________________。
(3)将氢气储存于液体燃料中,可以解决氢气的安全高效存储和运输问题。由于甲醇具有单
位体积储氢量高、活化温度低等优点,是理想的液体储氢平台分子。我国学者构建一种双功
能结构的催化剂,反应过程中,在催化剂的表面同时活化水和甲醇。如图是甲醇脱氢转化的
反应历程(TS表示过渡态)。根据图像判断甲醇脱氢反应中断裂的化学键是______,该反应的ΔH________( 填“大于”
“等于”或“小于”)0。
答案 (1)Fe O +3HS===Fe S +3HO (2)①2ΔH -ΔH -ΔH(或2ΔH -ΔH +ΔH 或ΔH
2 3 2 2 3 2 2 1 3 4 3 1 2
+ΔH -ΔH) ②1.0 CaO作为CO 的吸收剂,使产气中CO 分压降低,从而使水煤气变
4 3 2 2
换反应平衡向生成H 的方向移动 ③750 ℃ ④CaO吸收CO 产生的CaCO 附着在CaO
2 2 3
的表面,阻止了CaO对CO 的进一步吸收
2
(3)O—H和C—H 小于
解析 (1)根据题干可知,该反应为氧化铁与HS反应,生成硫化铁和水,反应的化学方程
2
式为:Fe O+3HS ===Fe S+3HO。
2 3 2 2 3 2
(2)①根据盖斯定律v=2×ii- i- iii=2×iv-iii+i=ii+iv-iii,则ΔH =2ΔH -ΔH -
5 2 1
ΔH=2ΔH-ΔH+ΔH=ΔH+ΔH-ΔH。
3 4 3 1 2 4 3
②根据表格中产氢率,=1.0时最高;由0到0.5时,H 的体积分数显著增加的原因是CaO
2
作为CO 的吸收剂,使产气中CO 分压降低,从而使水煤气变换反应平衡向生成H 的方
2 2 2
向移动。③根据表格可知750 ℃时,产氢率最高。
④CaO与二氧化碳反应生成碳酸钙,附着在CaO的表面,阻止了CaO对CO 的进一步吸收。
2
(3)甲醇的结构简式为CHOH,脱氢反应中断裂的化学键是O—H和C—H;该反应的相对能
3
量降低,反应放热。
3.碳、氮能形成多种氧化物、氢化物。
(1)已知:①2NO(g)N(g)+O(g) ΔH=-180.5 kJ·mol-1
2 2 1
②CO(g)+O(g)CO(g) ΔH=-283 kJ·mol-1
2 2 2
则NO与CO反应生成两种无毒气体的热化学方程式为________________________________。
(2)使用高效催化剂可大大减少汽车尾气排放出的NO 含量,某研究所的科研人员探究了T
x 1
℃时等质量的三种催化剂对CO还原NO的催化效果(其他条件相同),所得结果如图1所示。
①如果不考虑催化剂价格,则使用催化剂________(填“Ⅰ”“Ⅱ”或“Ⅲ”)最好;A、B两状态下,生成CO 的速率大小关系是________。
2
②若容器容积为2 L,开始时加入0.5 mol NO、0.5 mol CO,在催化剂Ⅰ的作用下达到如图1
所示平衡,则反应 2NO(g)+2CO(g)N(g)+2CO(g)在该温度下的平衡常数 K=
2 2
________。
③在图2坐标系中画出使用催化剂Ⅰ(其他条件相同)时,25 s时容器内反应的脱氮率(NO转
化率)与温度的关系图。
答案 (1)2CO(g)+2NO(g)2CO(g)+N(g) ΔH=-746.5 kJ·mol-1 (2)①Ⅰ v(A)>v(B)
2 2
②640 ③
解析 (1)NO与CO反应生成两种无毒气体,应为 CO 和N ,化学方程式应为2CO(g)+
2 2
2NO(g)2CO(g)+N(g);由已知:①2NO(g)N(g)+O(g) ΔH =-180.5 kJ·mol-1;
2 2 2 2 1
②CO(g)+O(g)CO(g) ΔH=-283 kJ·mol-1;
2 2 2
根据盖斯定律可知①+②×2可得2CO(g)+2NO(g)2CO(g)+N(g) ΔH=-180.5 kJ·mol-
2 2
1+(-283 kJ·mol-1)×2=-746.5 kJ·mol-1。
(2)①据图可知相同时间内使用催化剂Ⅰ的反应最先达到平衡,所以使用催化剂Ⅰ最好;据
图可知A点曲线的斜率更大,反应速率更快。
②据图可知25 s时氮气的物质的量不再改变说明反应达到平衡,此时n(N )=0.2 mol,根据
2
方程式可知此时容器中n(CO)=0.4 mol,Δn(NO)=Δn(CO)=0.4 mol,初始投料为0.5 mol
2
CO和0.5 mol NO,所以平衡时容器内n(NO)=n(CO)=0.1 mol,容器的容积为2 L,所以K
==640。