文档内容
顺义区 2023 届高三第一次统练
化学试卷
可能用到的相对原子质量:H-1 C-12 O-16 K-39 Mg-24 Fe-56
第I部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一
项。
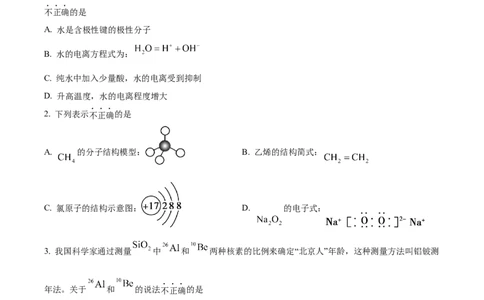
1. 最近《科学》杂志评出“十大科技突破”,其中“火星上‘找’到水的影子”名列第一、下列关于水的说法中
不正确的是
A. 水是含极性键的极性分子
B. 水的电离方程式为:
C. 纯水中加入少量酸,水的电离受到抑制
D. 升高温度,水的电离程度增大
2. 下列表示不正确的是
A. 的分子结构模型: B. 乙烯的结构简式:
C. 氯原子的结构示意图: D. 的电子式:
3. 我国科学家通过测量 中 和 两种核素的比例来确定“北京人”年龄,这种测量方法叫铝铍测
年法。关于 和 的说法不正确的是
A. 和 化学性质完全不同 B. 的原子核内中子数比质子数多
C. 可用质谱法区分 和 D. 和 的质子数和中子数都不相同
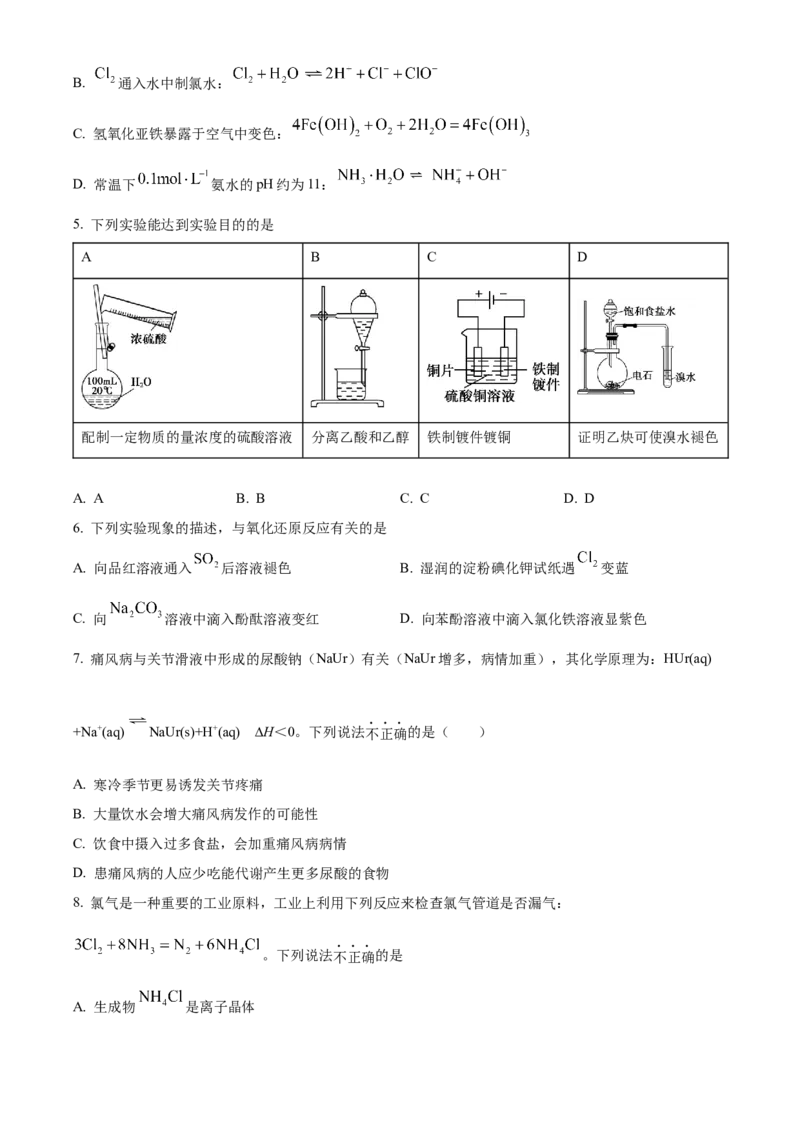
4. 下列方程式与所给事实不相符的是
A. 用碳酸钠溶液处理锅炉水垢:B. 通入水中制氯水:
C. 氢氧化亚铁暴露于空气中变色:
D. 常温下 氨水的pH约为11:
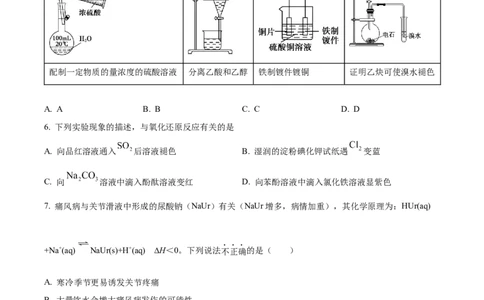
5. 下列实验能达到实验目的的是
A B C D
配制一定物质的量浓度的硫酸溶液 分离乙酸和乙醇 铁制镀件镀铜 证明乙炔可使溴水褪色
A. A B. B C. C D. D
6. 下列实验现象的描述,与氧化还原反应有关的是
A. 向品红溶液通入 后溶液褪色 B. 湿润的淀粉碘化钾试纸遇 变蓝
C. 向 溶液中滴入酚酞溶液变红 D. 向苯酚溶液中滴入氯化铁溶液显紫色
7. 痛风病与关节滑液中形成的尿酸钠(NaUr)有关(NaUr增多,病情加重),其化学原理为:HUr(aq)
+Na+(aq) NaUr(s)+H+(aq) ∆H<0。下列说法不正确的是( )
A. 寒冷季节更易诱发关节疼痛
B. 大量饮水会增大痛风病发作的可能性
C. 饮食中摄入过多食盐,会加重痛风病病情
D. 患痛风病的人应少吃能代谢产生更多尿酸的食物
8. 氯气是一种重要的工业原料,工业上利用下列反应来检查氯气管道是否漏气:
。下列说法不正确的是
A. 生成物 是离子晶体B. 的结构式为 , 分子中含有 键和 键
C. 可通过原电池将 与 反应的化学能转化为电能
D. 该反应氧化剂和还原剂的物质的量之比为3:8
9. 如表为元素周期表的一部分,其中X、Y、W、Z为短周期元素,W的单质常温下为黄绿色气体。下列
说法不正确的是
Y Z
X W
R T
A. X、Y的单质均存在同素异形体
B. Y、Z的简单氢化物的稳定性依次递增
C. R的单质可用于制造半导体材料
D. 工业上电解NaW溶液得W 可使用阴离子交换膜
2
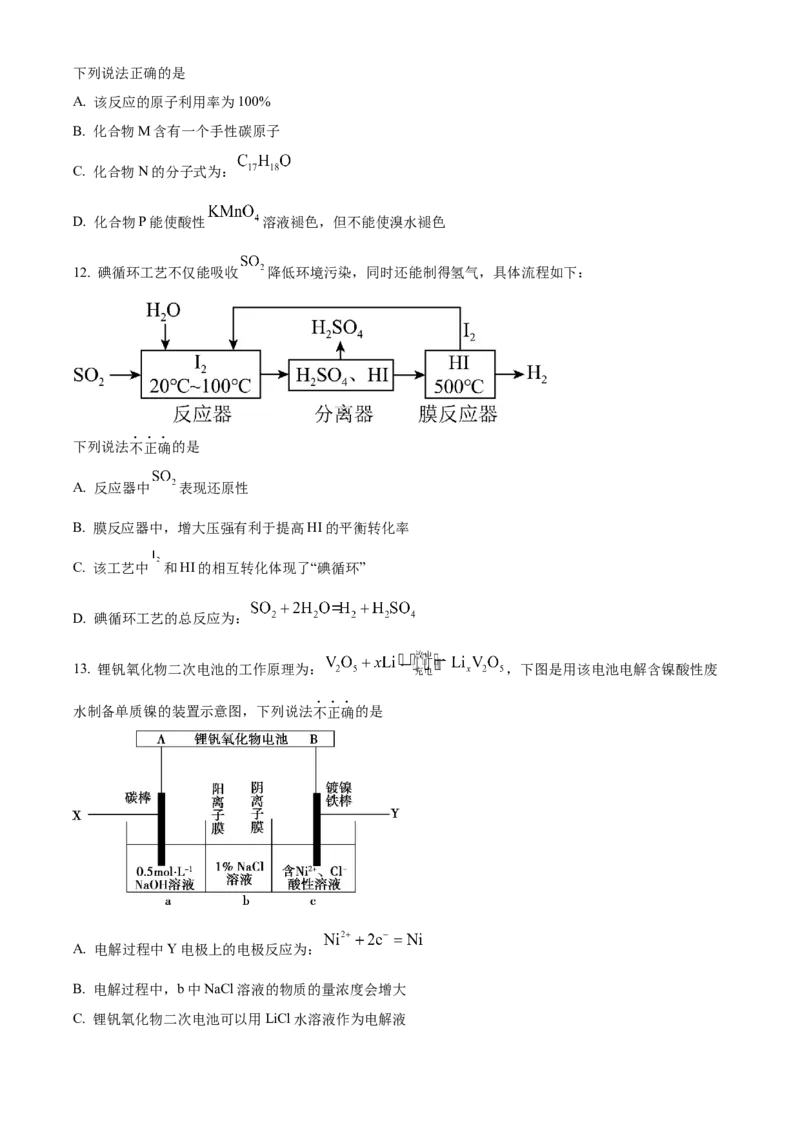
10. 锦纶100具有许多优异的性能,如机械强度高、很好的弹性,高韧性以及耐磨性等,下图是锦纶100
结构的一部分,下列说法不正确的是
A. 合成锦纶100的反应为缩聚反应
B. 氢键对锦纶100的性能有影响
C. 锦纶100很稳定,不能发生水解反应
D. 合成锦纶100的原料主要是癸二酸和癸二胺
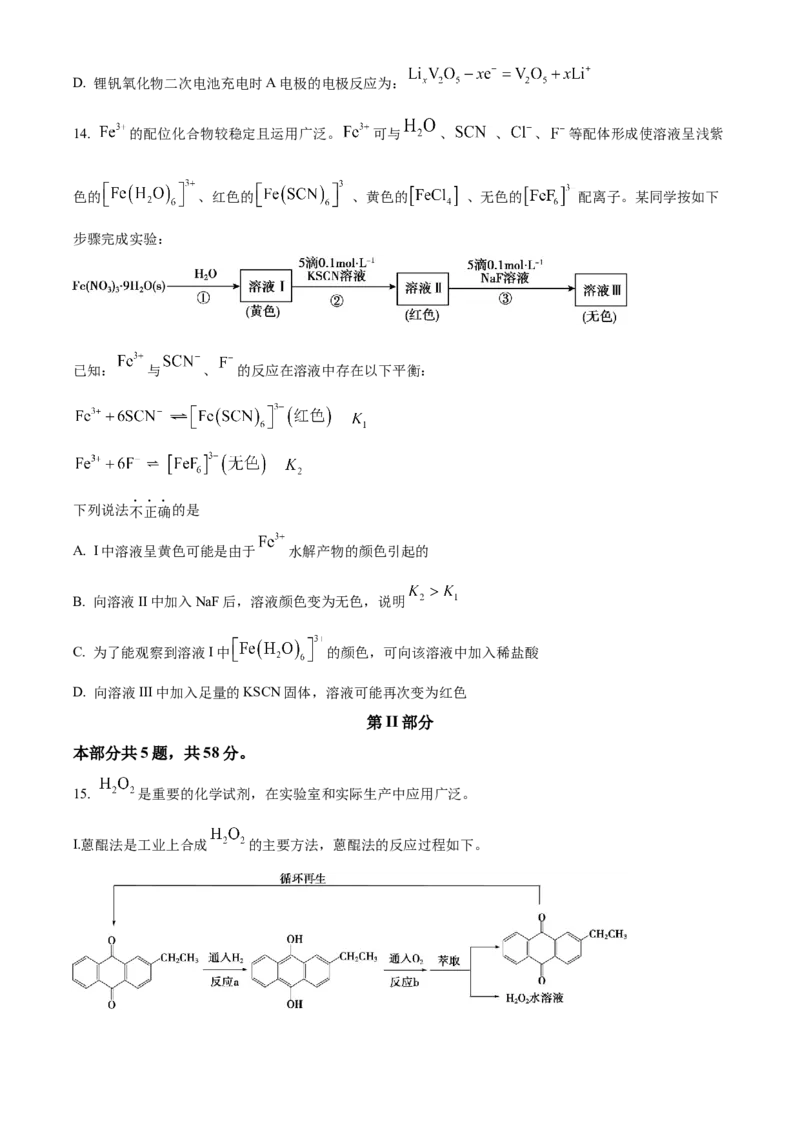
11. 一篇关于合成“纳米小人”的文章成为有机化学史上最受欢迎的文章之一,其中涉及的一个转化关系为:下列说法正确的是
A. 该反应的原子利用率为100%
B. 化合物M含有一个手性碳原子
C. 化合物N的分子式为:
D. 化合物P能使酸性 溶液褪色,但不能使溴水褪色
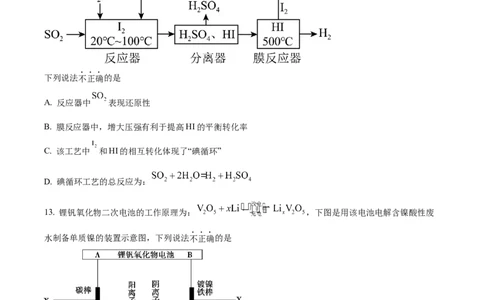
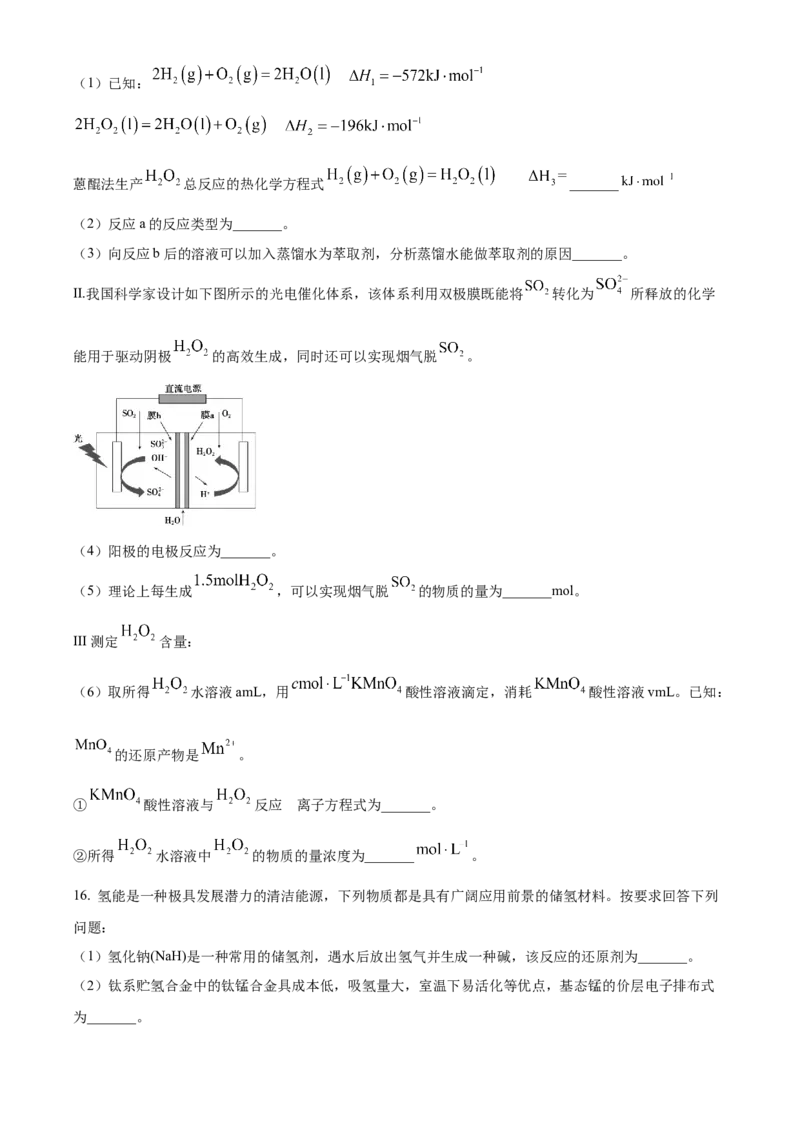
12. 碘循环工艺不仅能吸收 降低环境污染,同时还能制得氢气,具体流程如下:
下列说法不正确的是
A. 反应器中 表现还原性
B. 膜反应器中,增大压强有利于提高HI的平衡转化率
C. 该工艺中 和HI的相互转化体现了“碘循环”
D. 碘循环工艺的总反应为:
13. 锂钒氧化物二次电池的工作原理为: ,下图是用该电池电解含镍酸性废
水制备单质镍的装置示意图,下列说法不正确的是
A. 电解过程中Y电极上的电极反应为:
B. 电解过程中,b中NaCl溶液的物质的量浓度会增大
C. 锂钒氧化物二次电池可以用LiCl水溶液作为电解液D. 锂钒氧化物二次电池充电时A电极的电极反应为:
14. 的配位化合物较稳定且运用广泛。 可与 、 、 、 等配体形成使溶液呈浅紫
色的 、红色的 、黄色的 、无色的 配离子。某同学按如下
步骤完成实验:
已知: 与 、 的反应在溶液中存在以下平衡:
下列说法不正确的是
A. I中溶液呈黄色可能是由于 水解产物的颜色引起的
B. 向溶液II中加入NaF后,溶液颜色变为无色,说明
C. 为了能观察到溶液I中 的颜色,可向该溶液中加入稀盐酸
D. 向溶液III中加入足量的KSCN固体,溶液可能再次变为红色
第II部分
本部分共5题,共58分。
15. 是重要的化学试剂,在实验室和实际生产中应用广泛。
I.蒽醌法是工业上合成 的主要方法,蒽醌法的反应过程如下。(1)已知:
蒽醌法生产 总反应的热化学方程式 _______
(2)反应a的反应类型为_______。
(3)向反应b后的溶液可以加入蒸馏水为萃取剂,分析蒸馏水能做萃取剂的原因_______。
II.我国科学家设计如下图所示的光电催化体系,该体系利用双极膜既能将 转化为 所释放的化学
能用于驱动阴极 的高效生成,同时还可以实现烟气脱 。
(4)阳极的电极反应为_______。
(5)理论上每生成 ,可以实现烟气脱 的物质的量为_______mol。
.
III测定 含量:
(6)取所得 水溶液amL,用 酸性溶液滴定,消耗 酸性溶液vmL。已知:
的还原产物是 。
的
① 酸性溶液与 反应 离子方程式为_______。
②所得 水溶液中 的物质的量浓度为_______ 。
16. 氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。按要求回答下列
问题:
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂为_______。
(2)钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态锰的价层电子排布式
为_______。(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃)而成为颇具潜力的化学储氢材料
之一,它可通过环硼氮烷、 与 进行合成。
①上述涉及的元素H、B、C、N、O电负性最大的是_______。
②键角: _______ (填“>”或“<”),原因是_______。
(4)咔唑( )是一种新型新型有机液体储氢材料,它的沸点比( )的高,其主要原因
是_______。
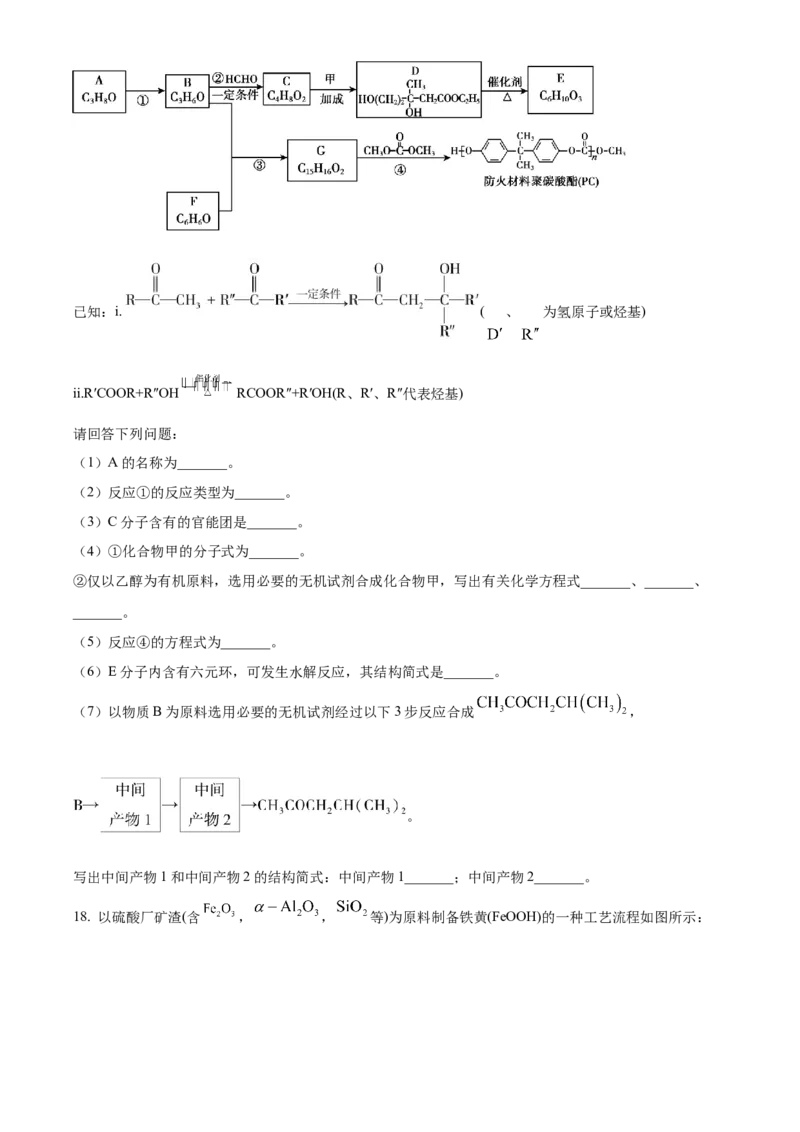
(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,
其晶胞结构如图所示。
的
①距离Mg原子最近 Fe原子个数是_______。
②铁镁合金的化学式为_______。
③若该晶胞的晶胞边长为dnm,阿伏加德罗常数为 ,则该合金的密度为_______ (
)。
④若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
的体积约为_______L。
17. A为重要的有机化工原料,B分子的核磁共振氢谱图中只有一个吸收峰,下列是合成防火材料聚碳酸
酯(PC)和有广泛用途的内酯E的路线:已知:i. ( 、 为氢原子或烃基)
ii.R′COOR+R″OH RCOOR″+R′OH(R、R′、R″代表烃基)
请回答下列问题:
(1)A的名称为_______。
(2)反应①的反应类型为_______。
(3)C分子含有的官能团是_______。
(4)①化合物甲的分子式为_______。
②仅以乙醇为有机原料,选用必要的无机试剂合成化合物甲,写出有关化学方程式_______、_______、
_______。
(5)反应④的方程式为_______。
(6)E分子内含有六元环,可发生水解反应,其结构简式是_______。
(7)以物质B为原料选用必要的无机试剂经过以下3步反应合成 ,
。
写出中间产物1和中间产物2的结构简式:中间产物1_______;中间产物2_______。
18. 以硫酸厂矿渣(含 , , 等)为原料制备铁黄(FeOOH)的一种工艺流程如图所示:资料:i. 化学性质极不活泼,不溶于水也不溶于酸或碱。
ii. ; 。
回答下列问题:
(1)为了提高“酸浸”的效率可以采用的措施有_______。
(2)“还原”过程中的离子方程式为_______。
(3)“滤渣”中主要成分为(填化学式)_______。
的
(4)①“沉铁”过程中有 气体产生,反应 离子方程式为_______。
②“沉铁”过程中往往有副产物 生成,分析原因是_______。
③若用 “沉铁”,则无副产物 产生,当反应完成时,溶液中 _______。
(5)写出氧化过程生成铁黄的化学方程式为_______。
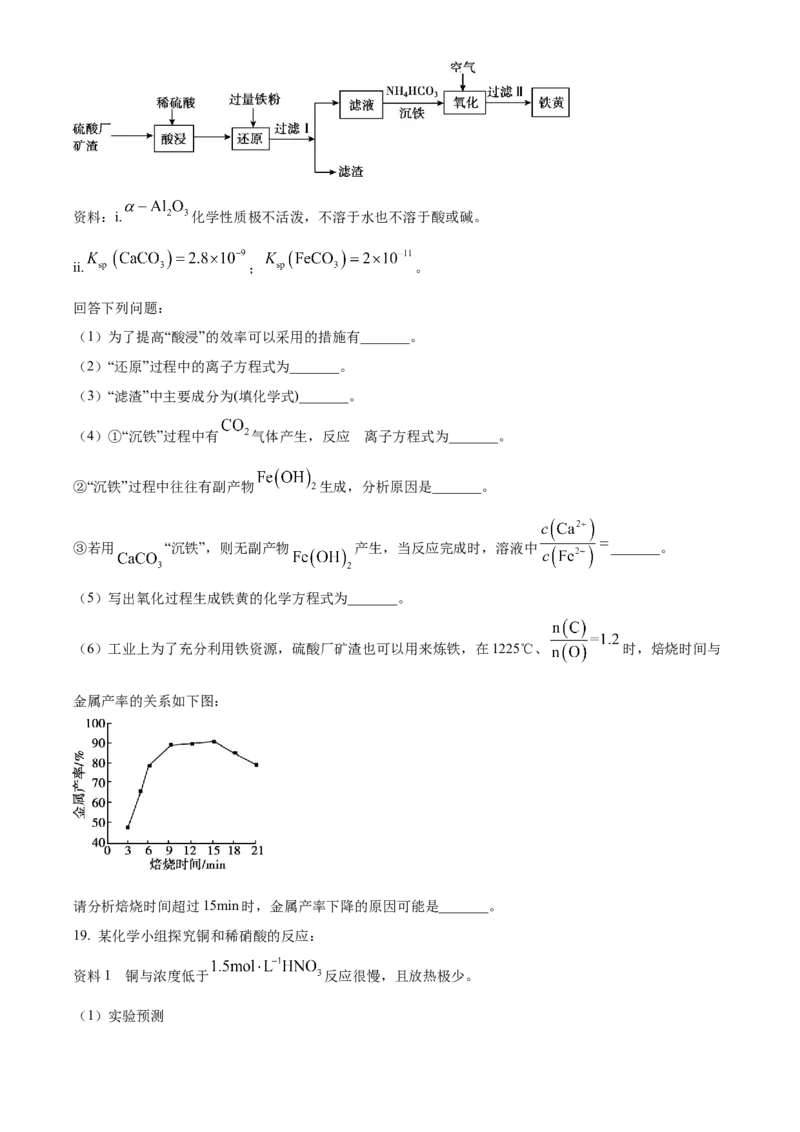
(6)工业上为了充分利用铁资源,硫酸厂矿渣也可以用来炼铁,在1225℃、 时,焙烧时间与
金属产率的关系如下图:
请分析焙烧时间超过15min时,金属产率下降的原因可能是_______。
19. 某化学小组探究铜和稀硝酸的反应:
资料1 铜与浓度低于 反应很慢,且放热极少。
(1)实验预测①铜与稀 反应的离子方程式为_______。
②小组同学预测铜与稀 的反应速率应逐渐减慢,其理论依据是_______。
(2)实验实施
实验I:铜丝与 反应。
实验装置 实验操作 实验现象
反应较慢阶段A:反应前90min几
在洁净的注射器中装入已活化铜丝2.3g,再
乎没有现象,90min左右才有很少
用注射器抽取 ,同 气泡产生(该气体遇空气变成红棕
时排尽注射器中的空气,关闭注射器止水开 色),溶液为浅蓝色;反应较快阶
段B:之后溶液逐渐变为绿色;最
关,以保证铜丝与稀 反应体系处于无
后阶段C:在反应结束前15min左
氧环境中。
右时,体系溶液为深蓝色。
实验II:探究Cu与稀 在无氧环境下反应所得溶液显绿色的原因:
操作及 实验现象
现象 取不同阶段的溶液进行实
验操作
实验序号 阶段A溶液 阶段B溶液 阶段C溶液
滴加 酸性
褪色,滴6滴后 褪色,但滴20滴后 褪色,滴10滴后
1
溶液 溶液不褪色 溶液仍然褪色 溶液不再褪色
2 滴加3% 溶液 无明显现象 少量淡黄色沉淀 较多黄色沉淀
3 滴加稀 溶液 无明显现象 变蓝色 无明显现象
资料2:
i.上述溶液中均不存在-3价的氮; 为淡黄色沉淀。
ii. 是一种弱酸, ;
①通过上述实验,证明铜与稀 反应过程中可能有 生成,理由是_______。
②分析阶段B溶液呈绿色的原因_______。
③从平衡角度分析实验II中,阶段B溶液中滴加稀硫酸溶液由绿色变蓝的原因_______。
④写出铜和稀 反应的生成 的化学方程式_______。
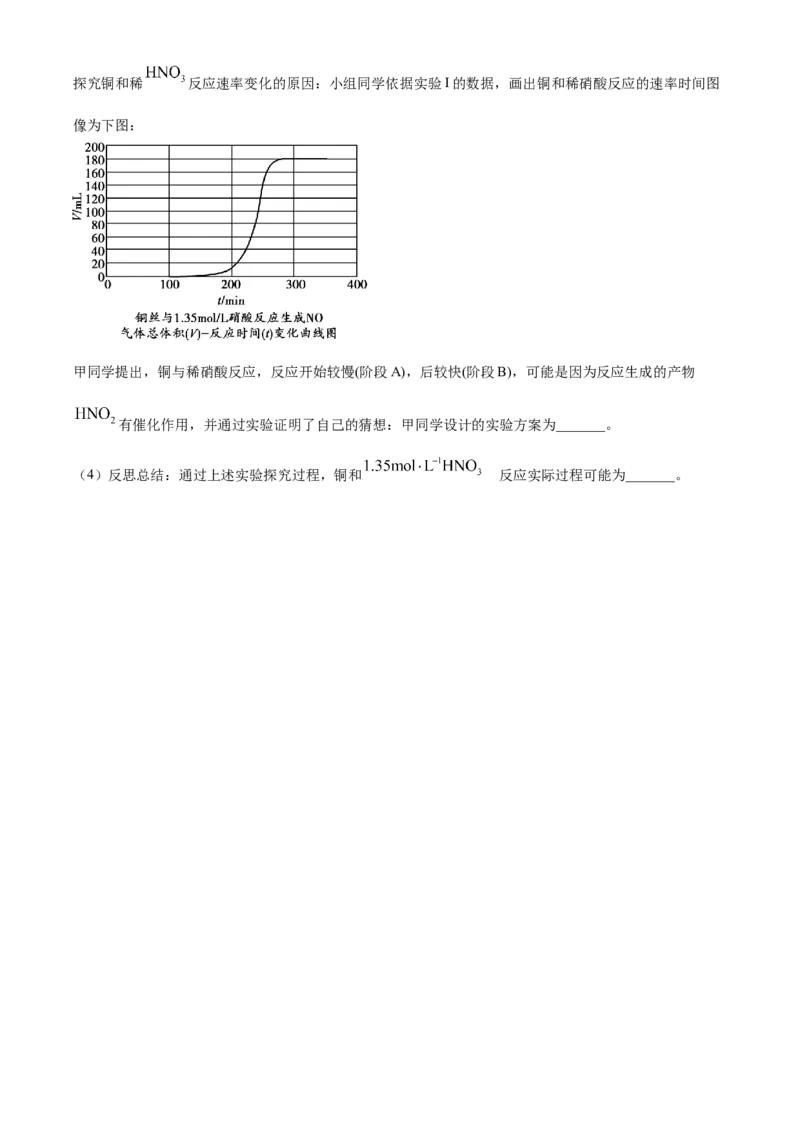
(3)继续探究:探究铜和稀 反应速率变化的原因:小组同学依据实验I的数据,画出铜和稀硝酸反应的速率时间图
像为下图:
甲同学提出,铜与稀硝酸反应,反应开始较慢(阶段A),后较快(阶段B),可能是因为反应生成的产物
有催化作用,并通过实验证明了自己的猜想:甲同学设计的实验方案为_______。
的
(4)反思总结:通过上述实验探究过程,铜和 反应实际过程可能为_______。