文档内容
单元检测十 水溶液中的离子反应与平衡
一、选择题(本题包括15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
1.化学在日常生活和生产中有着重要的应用。下列说法不正确的是( )
A.明矾水解形成的Al(OH) 胶体能吸附水中悬浮物,可用于水的净化
3
B.某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为溶液中的SO发生水解
C.将饱和FeCl 溶液滴入沸水中可制备Fe(OH) 胶体,利用的是盐类水解原理
3 3
D.纯碱溶液呈碱性的原因是CO+HO HCO+OH-
2
2.下列实验操作错误,但不会对实验结果产生影响的是( )
A.用酸碱中和滴定法测待测液浓度时,装标准液的滴定管水洗后未用标准液润洗
B.用酸碱中和滴定法测待测液浓度时,装待测液的锥形瓶水洗后用待测液润洗2~3次
C.测定中和反应的反应热时,将碱溶液缓慢倒入酸溶液中
D.用蒸馏水润湿的pH试纸测定硫酸钠溶液的pH
3.实验室采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe O 、SiO 、Al O ,不考虑其他杂
2 3 2 2 3
质)制取七水合硫酸亚铁(FeSO ·7H O),其流程如图所示:
4 2
已知:25 ℃,K [Fe(OH) ]=8.0×10-16,K [Fe(OH) ]=4.0×10-38,K [Al(OH) ]=1.0×10-
sp 2 sp 3 sp 3
33。下列说法正确的是( )
A.检验溶液1中是否含有Fe3+,可用NH SCN溶液
4
B.加试剂X和加NaOH溶液控制pH,两步顺序可以互换
C.操作①、②用到的玻璃仪器为烧杯、玻璃棒、分液漏斗
D.操作③为将溶液2加热至有大量晶体析出时,停止加热,利用余热蒸干
4.下列说法不正确的是( )
A.25 ℃时,pH=3的一元酸HA溶液与pH=11的NaOH溶液等体积混合后pH≥7
B.相同物质的量浓度的(NH )Fe(SO ) 溶液和FeSO 溶液,c(Fe2+)前者大于后者
4 2 4 2 4
C.25 ℃时,10 mL pH=4的NH Cl溶液稀释至1 000 mL,溶液pH<6
4
D.恒温时,向NH HSO 溶液中逐滴加入过量的NaOH溶液,n(NH)始终减小
4 4
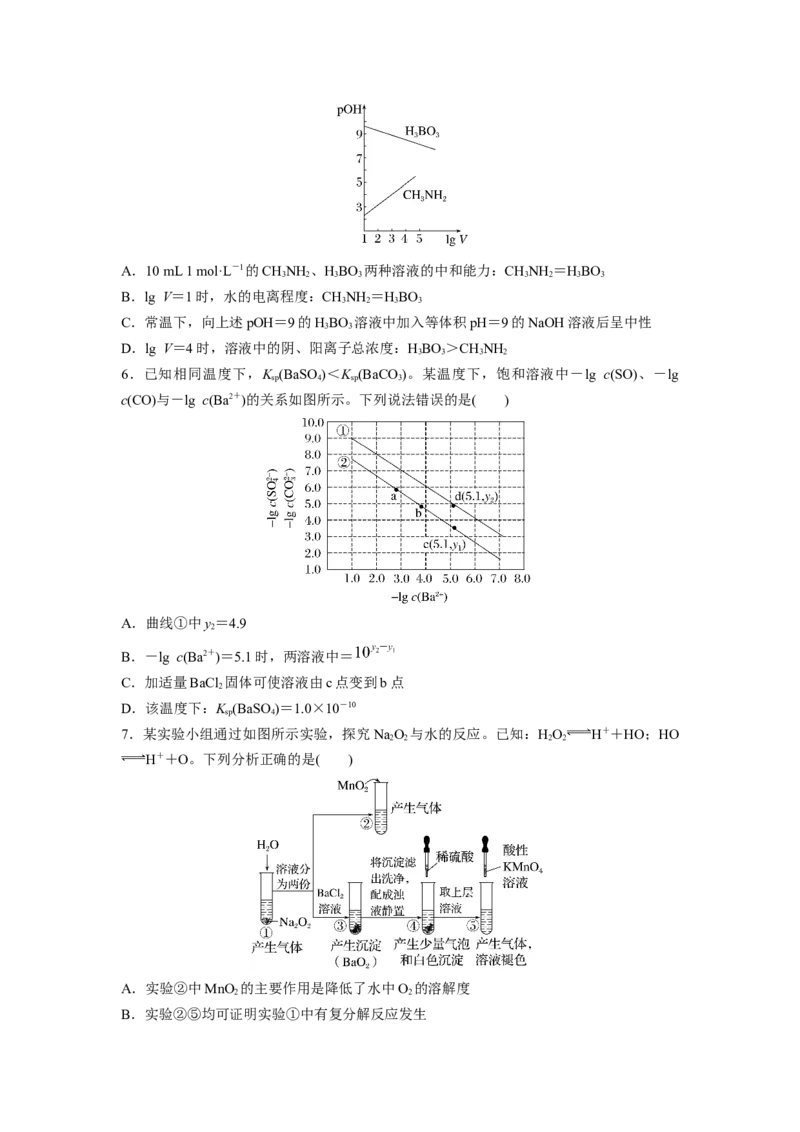
5.已知:CHNH 、HBO 分别为一元弱碱和一元弱酸,二者在水中的电离方程式分别为
3 2 3 3
CHNH +HO CHNH+OH-;HBO +HO [B(OH) ]-+H+。25 ℃时,将10 mL浓
3 2 2 3 3 3 2 4
度均为1 mol·L-1的CHNH 、HBO 两种溶液分别加水稀释,曲线如图所示,V是溶液体
3 2 3 3
积(mL)。 pOH=-lg c(OH-)。下列说法正确的是( )A.10 mL 1 mol·L-1的CHNH 、HBO 两种溶液的中和能力:CHNH =HBO
3 2 3 3 3 2 3 3
B.lg V=1时,水的电离程度:CHNH =HBO
3 2 3 3
C.常温下,向上述pOH=9的HBO 溶液中加入等体积pH=9的NaOH溶液后呈中性
3 3
D.lg V=4时,溶液中的阴、阳离子总浓度:HBO>CHNH
3 3 3 2
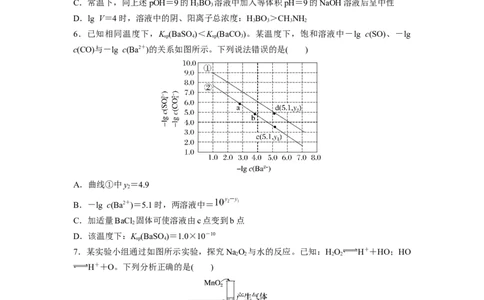
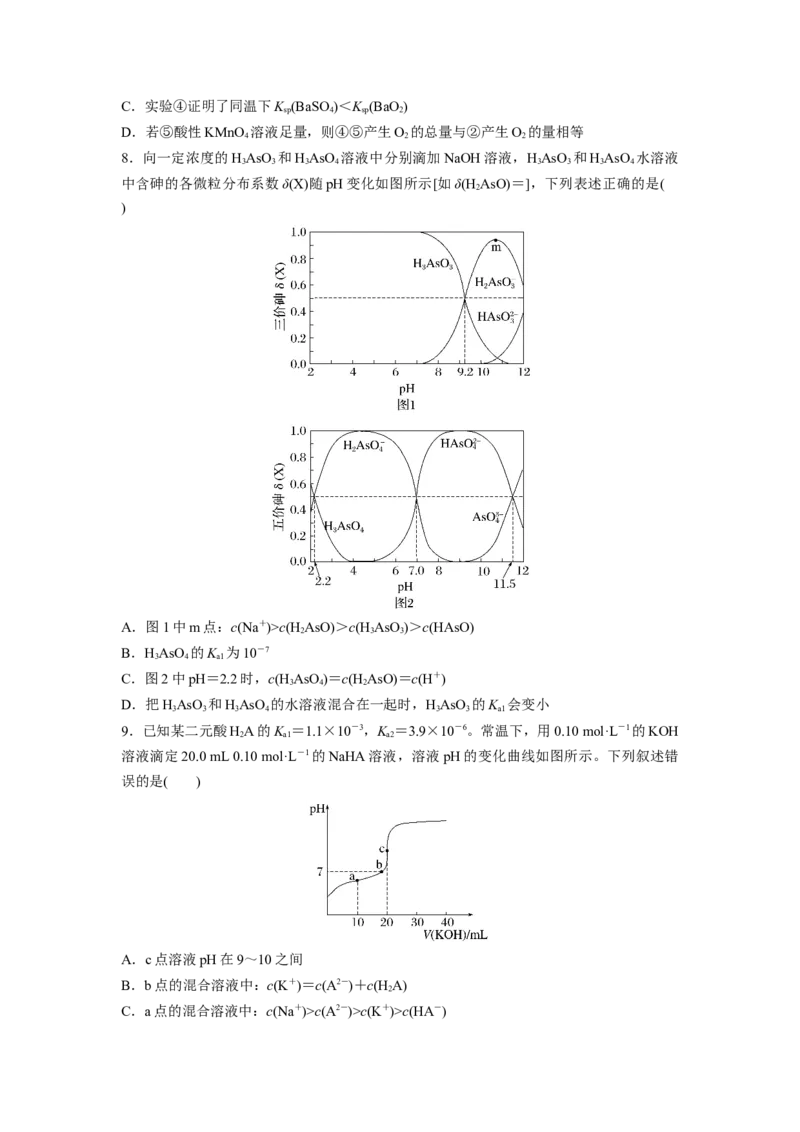
6.已知相同温度下,K (BaSO)<K (BaCO)。某温度下,饱和溶液中-lg c(SO)、-lg
sp 4 sp 3
c(CO)与-lg c(Ba2+)的关系如图所示。下列说法错误的是( )
A.曲线①中y=4.9
2
B.-lg c(Ba2+)=5.1时,两溶液中=
C.加适量BaCl 固体可使溶液由c点变到b点
2
D.该温度下:K (BaSO)=1.0×10-10
sp 4
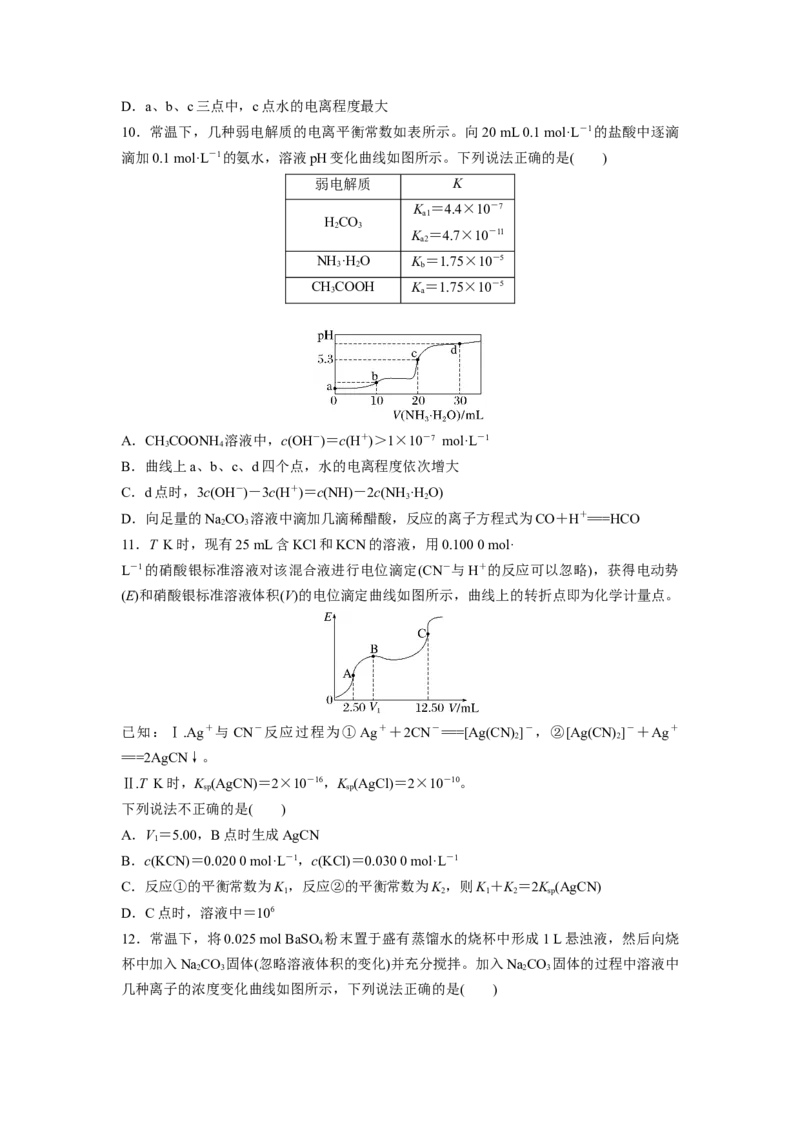
7.某实验小组通过如图所示实验,探究NaO 与水的反应。已知:HO H++HO;HO
2 2 2 2
H++O。下列分析正确的是( )
A.实验②中MnO 的主要作用是降低了水中O 的溶解度
2 2
B.实验②⑤均可证明实验①中有复分解反应发生C.实验④证明了同温下K (BaSO)<K (BaO)
sp 4 sp 2
D.若⑤酸性KMnO 溶液足量,则④⑤产生O 的总量与②产生O 的量相等
4 2 2
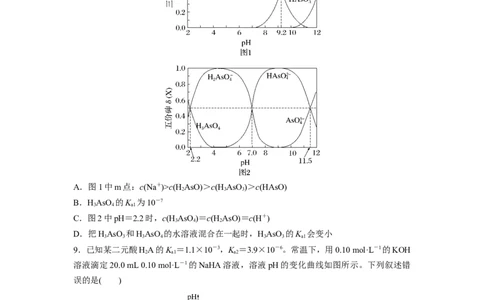
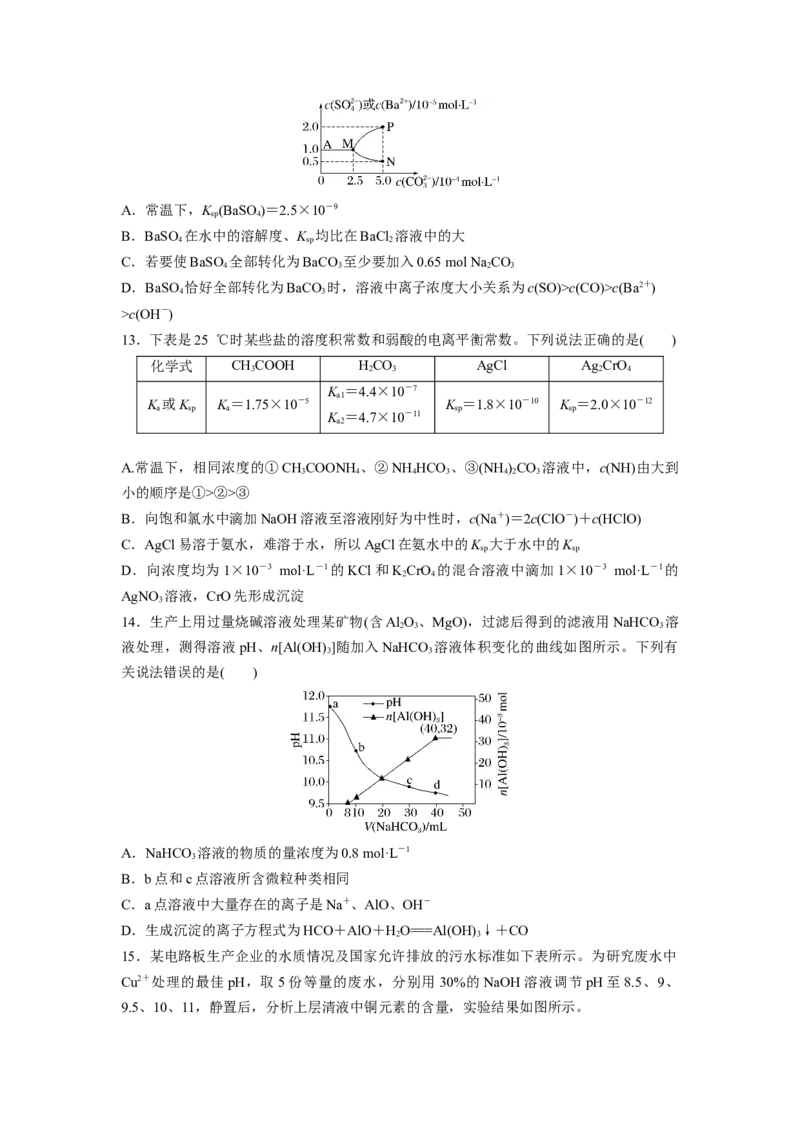
8.向一定浓度的HAsO 和HAsO 溶液中分别滴加NaOH溶液,HAsO 和HAsO 水溶液
3 3 3 4 3 3 3 4
中含砷的各微粒分布系数δ(X)随pH变化如图所示[如δ(H AsO)=],下列表述正确的是(
2
)
A.图1中m点:c(Na+)>c(H AsO)>c(H AsO )>c(HAsO)
2 3 3
B.HAsO 的K 为10-7
3 4 a1
C.图2中pH=2.2时,c(H AsO )=c(H AsO)=c(H+)
3 4 2
D.把HAsO 和HAsO 的水溶液混合在一起时,HAsO 的K 会变小
3 3 3 4 3 3 a1
9.已知某二元酸HA的K =1.1×10-3,K =3.9×10-6。常温下,用0.10 mol·L-1的KOH
2 a1 a2
溶液滴定20.0 mL 0.10 mol·L-1的NaHA溶液,溶液pH的变化曲线如图所示。下列叙述错
误的是( )
A.c点溶液pH在9~10之间
B.b点的混合溶液中:c(K+)=c(A2-)+c(H A)
2
C.a点的混合溶液中:c(Na+)>c(A2-)>c(K+)>c(HA-)D.a、b、c三点中,c点水的电离程度最大
10.常温下,几种弱电解质的电离平衡常数如表所示。向20 mL 0.1 mol·L-1的盐酸中逐滴
滴加0.1 mol·L-1的氨水,溶液pH变化曲线如图所示。下列说法正确的是( )
弱电解质 K
K =4.4×10-7
a1
HCO
2 3
K =4.7×10-11
a2
NH ·H O K =1.75×10-5
3 2 b
CHCOOH K=1.75×10-5
3 a
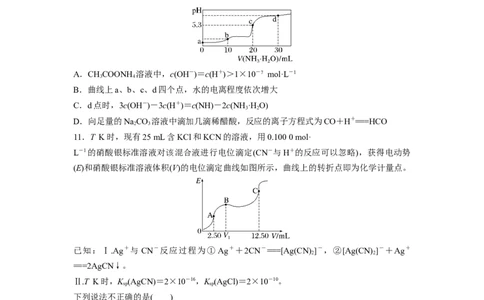
A.CHCOONH 溶液中,c(OH-)=c(H+)>1×10-7 mol·L-1
3 4
B.曲线上a、b、c、d四个点,水的电离程度依次增大
C.d点时,3c(OH-)-3c(H+)=c(NH)-2c(NH ·H O)
3 2
D.向足量的NaCO 溶液中滴加几滴稀醋酸,反应的离子方程式为CO+H+===HCO
2 3
11.T K时,现有25 mL含KCl和KCN的溶液,用0.100 0 mol·
L-1的硝酸银标准溶液对该混合液进行电位滴定(CN-与H+的反应可以忽略),获得电动势
(E)和硝酸银标准溶液体积(V)的电位滴定曲线如图所示,曲线上的转折点即为化学计量点。
已知:Ⅰ.Ag+与 CN-反应过程为① Ag++2CN-===[Ag(CN) ]-,②[Ag(CN) ]-+Ag+
2 2
===2AgCN↓。
Ⅱ.T K时,K (AgCN)=2×10-16,K (AgCl)=2×10-10。
sp sp
下列说法不正确的是( )
A.V=5.00,B点时生成AgCN
1
B.c(KCN)=0.020 0 mol·L-1,c(KCl)=0.030 0 mol·L-1
C.反应①的平衡常数为K ,反应②的平衡常数为K ,则K +K =2K (AgCN)
1 2 1 2 sp
D.C点时,溶液中=106
12.常温下,将0.025 mol BaSO 粉末置于盛有蒸馏水的烧杯中形成1 L悬浊液,然后向烧
4
杯中加入NaCO 固体(忽略溶液体积的变化)并充分搅拌。加入NaCO 固体的过程中溶液中
2 3 2 3
几种离子的浓度变化曲线如图所示,下列说法正确的是( )A.常温下,K (BaSO)=2.5×10-9
sp 4
B.BaSO 在水中的溶解度、K 均比在BaCl 溶液中的大
4 sp 2
C.若要使BaSO 全部转化为BaCO 至少要加入0.65 mol Na CO
4 3 2 3
D.BaSO 恰好全部转化为BaCO 时,溶液中离子浓度大小关系为c(SO)>c(CO)>c(Ba2+)
4 3
>c(OH-)
13.下表是25 ℃时某些盐的溶度积常数和弱酸的电离平衡常数。下列说法正确的是( )
化学式 CHCOOH HCO AgCl Ag CrO
3 2 3 2 4
K =4.4×10-7
a1
K 或K K=1.75×10-5 K =1.8×10-10 K =2.0×10-12
a sp a sp sp
K =4.7×10-11
a2
A.常温下,相同浓度的①CHCOONH 、②NH HCO 、③(NH )CO 溶液中,c(NH)由大到
3 4 4 3 4 2 3
小的顺序是①>②>③
B.向饱和氯水中滴加NaOH溶液至溶液刚好为中性时,c(Na+)=2c(ClO-)+c(HClO)
C.AgCl易溶于氨水,难溶于水,所以AgCl在氨水中的K 大于水中的K
sp sp
D.向浓度均为1×10-3 mol·L-1的KCl和KCrO 的混合溶液中滴加1×10-3 mol·L-1的
2 4
AgNO 溶液,CrO先形成沉淀
3
14.生产上用过量烧碱溶液处理某矿物(含Al O 、MgO),过滤后得到的滤液用NaHCO 溶
2 3 3
液处理,测得溶液pH、n[Al(OH) ]随加入NaHCO 溶液体积变化的曲线如图所示。下列有
3 3
关说法错误的是( )
A.NaHCO 溶液的物质的量浓度为0.8 mol·L-1
3
B.b点和c点溶液所含微粒种类相同
C.a点溶液中大量存在的离子是Na+、AlO、OH-
D.生成沉淀的离子方程式为HCO+AlO+HO===Al(OH) ↓+CO
2 3
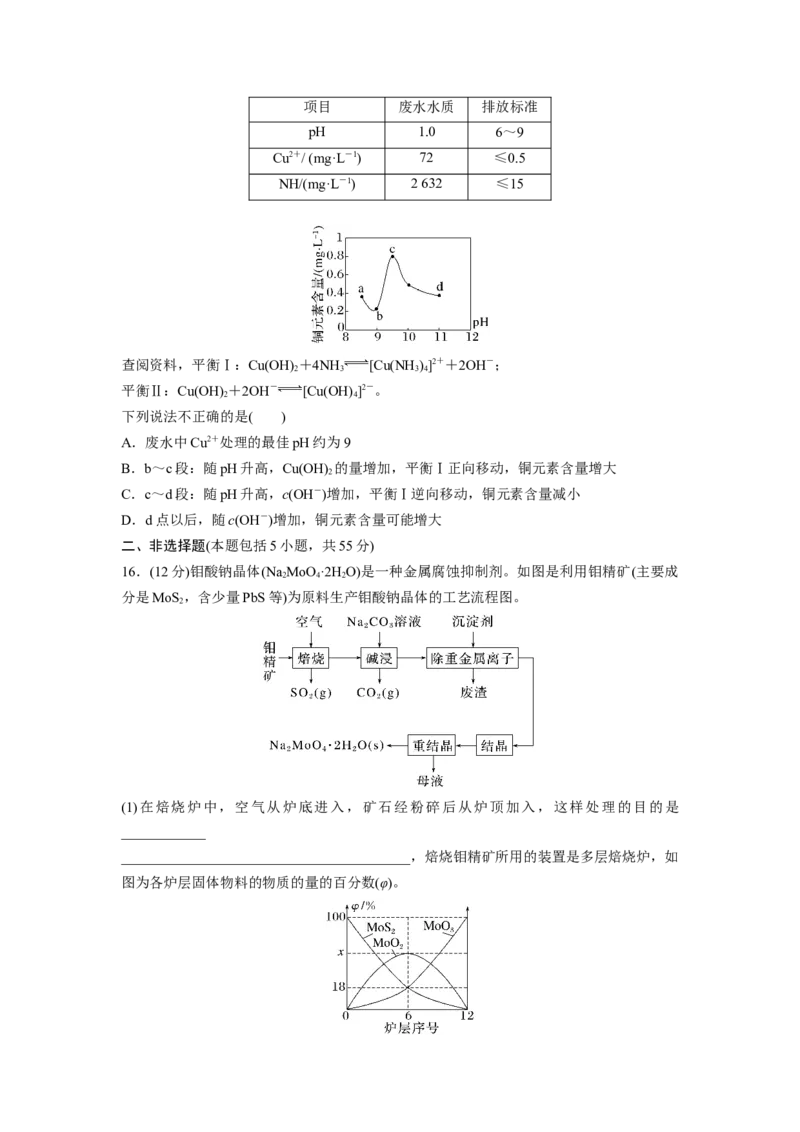
15.某电路板生产企业的水质情况及国家允许排放的污水标准如下表所示。为研究废水中
Cu2+处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、
9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如图所示。项目 废水水质 排放标准
pH 1.0 6~9
Cu2+/ (mg·L-1) 72 ≤0.5
NH/(mg·L-1) 2 632 ≤15
查阅资料,平衡Ⅰ:Cu(OH) +4NH [Cu(NH )]2++2OH-;
2 3 3 4
平衡Ⅱ:Cu(OH) +2OH- [Cu(OH) ]2-。
2 4
下列说法不正确的是( )
A.废水中Cu2+处理的最佳pH约为9
B.b~c段:随pH升高,Cu(OH) 的量增加,平衡Ⅰ正向移动,铜元素含量增大
2
C.c~d段:随pH升高,c(OH-)增加,平衡Ⅰ逆向移动,铜元素含量减小
D.d点以后,随c(OH-)增加,铜元素含量可能增大
二、非选择题(本题包括5小题,共55分)
16.(12分)钼酸钠晶体(Na MoO ·2H O)是一种金属腐蚀抑制剂。如图是利用钼精矿(主要成
2 4 2
分是MoS ,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图。
2
(1)在焙烧炉中,空气从炉底进入,矿石经粉碎后从炉顶加入,这样处理的目的是
____________
_________________________________________,焙烧钼精矿所用的装置是多层焙烧炉,如
图为各炉层固体物料的物质的量的百分数(φ)。①x=________。
② “ 焙 烧 ” 时 MoS 最 终 转 化 为 MoO , 写 出 该 反 应 的 化 学 方 程 式 :
2 3
______________________。
(2)沉淀剂通常用 NaS,使用时若溶液 pH 较小,Pb2+沉淀不完全,原因是
2
__________________。
(3)“结晶”前需向滤液中加入Ba(OH) 固体以除去CO。若滤液中c(MoO)=0.40 mol·
2
L-1,c(CO)=0.10 mol·L-1,当BaMoO 开始沉淀时,CO的去除率是________%[已知:
4
K (BaCO)=1.0×10-9,K (BaMoO )=4.0×10-8,溶液体积变化忽略不计]。
sp 3 sp 4
(4)在碱性条件下,将钼精矿加入NaClO溶液中也能制备NaMoO ,同时生成硫酸盐,该反
2 4
应的离子方程式是_______________________________________________________________。
(5)钼酸盐对碳钢的腐蚀具有缓蚀作用,其原理是在空气中钼酸盐能在钢铁表面形成
FeMoO -Fe O 保护膜。在密闭式循环冷却水系统中,为缓蚀碳钢管道,除加入钼酸盐外
4 2 3
还需加入的物质是________(填字母)。
A.NaNO B.通入适量N
2 2
C.油脂 D.盐酸
17.(8分)铜、磷及其化合物在生产、生活中有重要的用途,回答下列问题:
(1)磷的一种化合物叫亚磷酸(H PO )。已知:(i)0.1 mol·L-1 HPO 溶液的 pH=1.7;
3 3 3 3
(ii)H PO 与NaOH反应只生成NaHPO 和NaH PO ;(iii)H PO 和碘水反应,碘水棕黄色褪
3 3 2 3 2 3 3 3
去,再加AgNO 有黄色沉淀生成。
3
①关于HPO 的说法:a.强酸 b.弱酸 c.二元酸 d.三元酸 e.氧化性酸 f.还原
3 3
性酸,其中正确的是________(填字母)。
A.bdf B.ade
C.bcf D.bce
② 写 出 HPO 与 过 量 NaOH 溶 液 反 应 的 离 子 方 程 式 :
3 3
__________________________________。
③NaHPO 为__________(填“正盐”或“酸式盐”)。
2 3
(2)碘化亚铜可作催化剂、饲料添加剂等。已知:Ⅰ.铜能与氢碘酸发生置换反应得到氢气和
碘化亚铜;Ⅱ.CuSO 溶液能使淀粉-KI试纸变蓝,并产生白色固体;Ⅲ.碘化亚铜与氢氧化
4
钠作用生成氧化亚铜、碘化钠和水。
①下列关于碘化亚铜的叙述正确的是________(填字母)。
a.碘化亚铜的化学式为CuI,属于盐类
b.碘化亚铜稳定且难溶于水
c.氧化亚铜是弱酸,比碘化亚铜更难溶
d.铜能与氢碘酸反应,说明氢碘酸是强氧化性的酸
②碘化亚铜与氢氧化钠反应的离子方程式为_________________________________________。
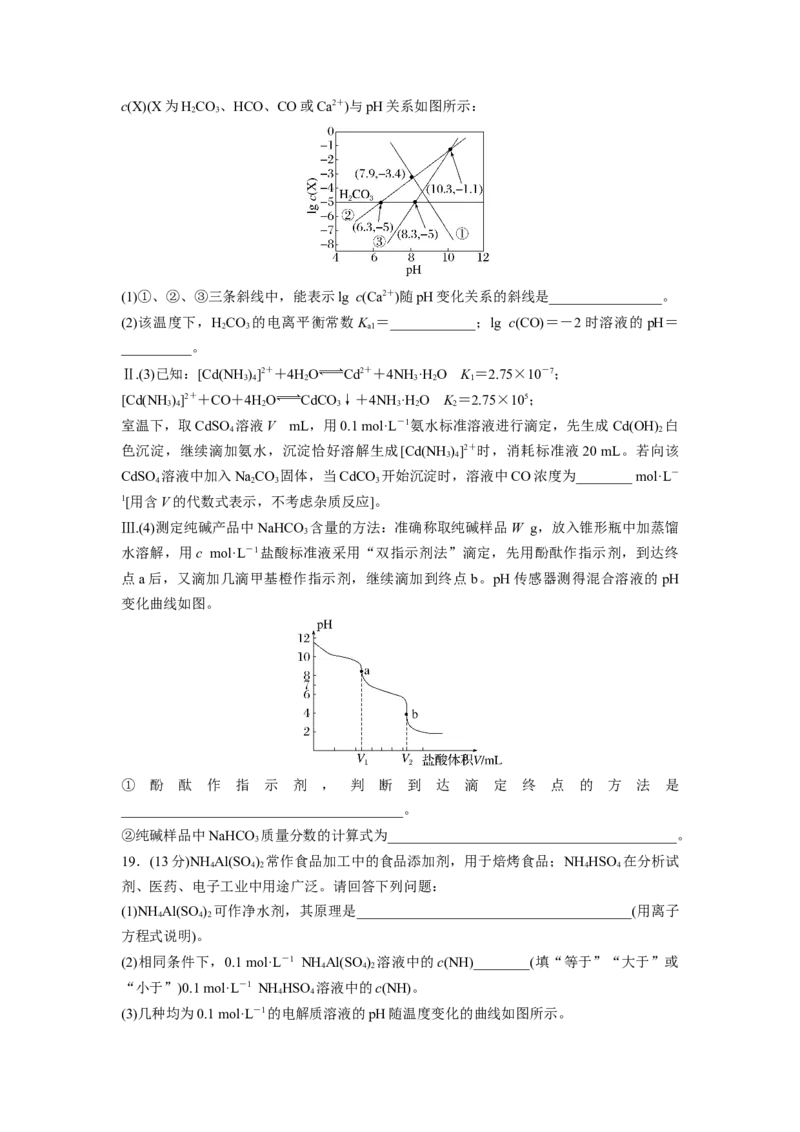
18.(12分)Ⅰ.天然水体中的HCO 与空气中的CO 保持平衡。某温度下,溶洞水体中lg
2 3 2c(X)(X为HCO、HCO、CO或Ca2+)与pH关系如图所示:
2 3
(1)①、②、③三条斜线中,能表示lg c(Ca2+)随pH变化关系的斜线是________________。
(2)该温度下,HCO 的电离平衡常数K =____________;lg c(CO)=-2时溶液的pH=
2 3 a1
__________。
Ⅱ.(3)已知:[Cd(NH )]2++4HO Cd2++4NH ·H O K =2.75×10-7;
3 4 2 3 2 1
[Cd(NH )]2++CO+4HO CdCO↓+4NH ·H O K =2.75×105;
3 4 2 3 3 2 2
室温下,取CdSO 溶液V mL,用0.1 mol·L-1氨水标准溶液进行滴定,先生成Cd(OH) 白
4 2
色沉淀,继续滴加氨水,沉淀恰好溶解生成[Cd(NH )]2+时,消耗标准液20 mL。若向该
3 4
CdSO 溶液中加入NaCO 固体,当CdCO 开始沉淀时,溶液中CO浓度为________ mol·L-
4 2 3 3
1[用含V的代数式表示,不考虑杂质反应]。
Ⅲ.(4)测定纯碱产品中NaHCO 含量的方法:准确称取纯碱样品W g,放入锥形瓶中加蒸馏
3
水溶解,用c mol·L-1盐酸标准液采用“双指示剂法”滴定,先用酚酞作指示剂,到达终
点a后,又滴加几滴甲基橙作指示剂,继续滴加到终点 b。pH传感器测得混合溶液的pH
变化曲线如图。
① 酚 酞 作 指 示 剂 , 判 断 到 达 滴 定 终 点 的 方 法 是
________________________________________。
②纯碱样品中NaHCO 质量分数的计算式为_________________________________________。
3
19.(13分)NH Al(SO ) 常作食品加工中的食品添加剂,用于焙烤食品;NH HSO 在分析试
4 4 2 4 4
剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH Al(SO ) 可作净水剂,其原理是_______________________________________(用离子
4 4 2
方程式说明)。
(2)相同条件下,0.1 mol·L-1 NH Al(SO ) 溶液中的c(NH)________(填“等于”“大于”或
4 4 2
“小于”)0.1 mol·L-1 NH HSO 溶液中的c(NH)。
4 4
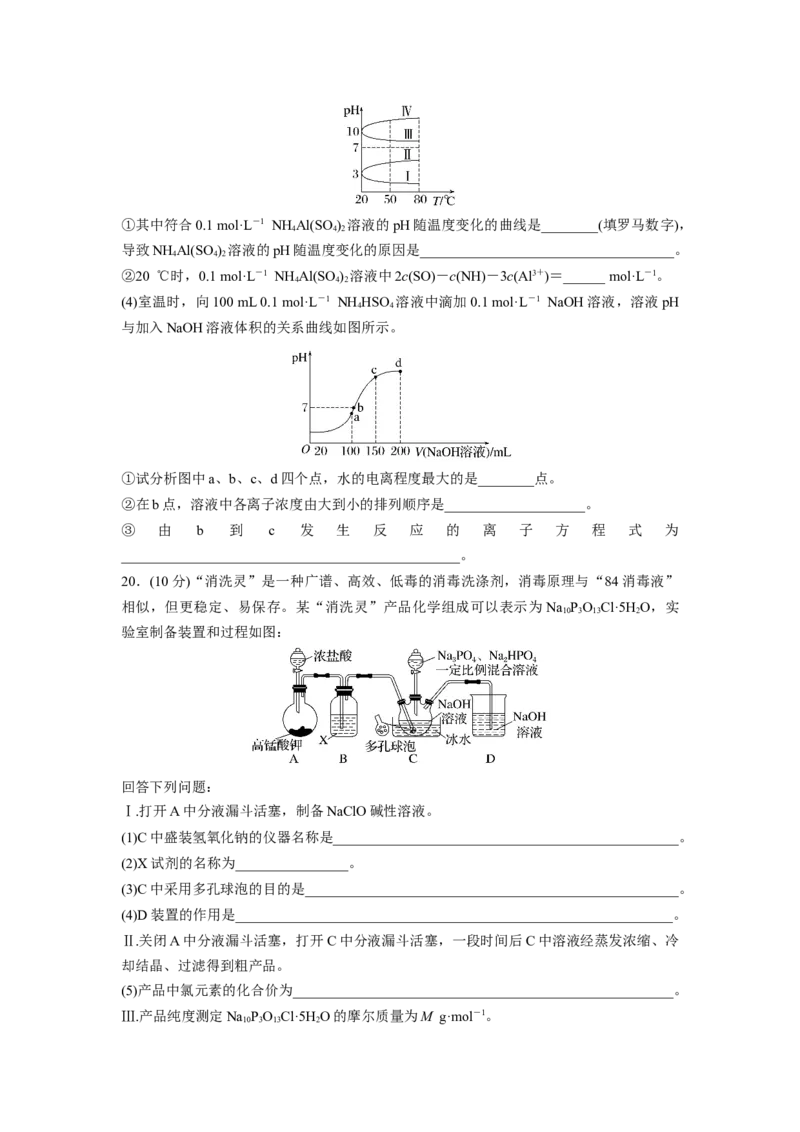
(3)几种均为0.1 mol·L-1的电解质溶液的pH随温度变化的曲线如图所示。①其中符合0.1 mol·L-1 NH Al(SO ) 溶液的pH随温度变化的曲线是________(填罗马数字),
4 4 2
导致NH Al(SO ) 溶液的pH随温度变化的原因是____________________________________。
4 4 2
②20 ℃时,0.1 mol·L-1 NH Al(SO ) 溶液中2c(SO)-c(NH)-3c(Al3+)=______ mol·L-1。
4 4 2
(4)室温时,向100 mL 0.1 mol·L-1 NH HSO 溶液中滴加0.1 mol·L-1 NaOH溶液,溶液pH
4 4
与加入NaOH溶液体积的关系曲线如图所示。
①试分析图中a、b、c、d四个点,水的电离程度最大的是________点。
②在b点,溶液中各离子浓度由大到小的排列顺序是____________________。
③ 由 b 到 c 发 生 反 应 的 离 子 方 程 式 为
________________________________________________。
20.(10分)“消洗灵”是一种广谱、高效、低毒的消毒洗涤剂,消毒原理与“84消毒液”
相似,但更稳定、易保存。某“消洗灵”产品化学组成可以表示为Na PO Cl·5H O,实
10 3 13 2
验室制备装置和过程如图:
回答下列问题:
Ⅰ.打开A中分液漏斗活塞,制备NaClO碱性溶液。
(1)C中盛装氢氧化钠的仪器名称是_________________________________________________。
(2)X试剂的名称为________________。
(3)C中采用多孔球泡的目的是_____________________________________________________。
(4)D装置的作用是______________________________________________________________。
Ⅱ.关闭A中分液漏斗活塞,打开C中分液漏斗活塞,一段时间后C中溶液经蒸发浓缩、冷
却结晶、过滤得到粗产品。
(5)产品中氯元素的化合价为______________________________________________________。
Ⅲ.产品纯度测定Na PO Cl·5H O的摩尔质量为M g·mol-1。
10 3 13 2①取a g待测试样溶于蒸馏水配成250 mL溶液;
②取25.00 mL待测液于锥形瓶中,加入10 mL 2 mol·L-1稀硫酸、25 mL 0.1 mol·L-1碘化钾
溶液(过量),此时溶液出现棕色;
③滴入3滴5%淀粉溶液,用0.05 mol·L-1硫代硫酸钠溶液滴定至终点,平行滴定三次,平
均消耗20.00 mL。
已知: 2SO+I===SO+2I-。
2 2 4
(6)产品的纯度为______________(用含a、M的代数式表示)。
答案 (1)三颈烧瓶
(2)饱和食盐水
(3)增大反应接触面积,使反应更充分
(4)除去多余的Cl,防止污染空气
2
(5)+1
(6)×100%
单元检测十 水溶液中的离子反应与平衡答案解析
1.
答案 B
解析 雨水放置一段时间后pH减小是由于HSO 被氧化为HSO ,导致溶液酸性增强。
2 3 2 4
2.
答案 D
解析 标准液被稀释,消耗标准液的体积增大,会导致测定结果偏高,A项错误;装待测
液的锥形瓶水洗后用待测液润洗2~3次,消耗标准液的体积增大,会导致测定结果偏高,
B项错误;部分热量散失,导致测定结果偏低,C项错误;硫酸钠溶液呈中性,D项正确。
3.
答案 A
解析 溶液1可加硫氰化铵溶液,若变红则能说明存在 Fe3+,故A正确;试剂X的目的是
将Fe3+还原成Fe2+,以便于在加NaOH时只有铝离子沉淀,若颠倒顺序,先加NaOH溶液
会使三价铁离子先沉淀,故B错误;操作①、②均为过滤操作,需要用到烧杯、漏斗、玻
璃棒,不需要分液漏斗,故C错误;操作③为蒸发浓缩、冷却结晶,加热到刚有晶膜生成
时就要停止加热,然后降温结晶,故D错误。
4.
答案 A
解析 pH=3的一元酸HA溶液为强酸时,与pH=11的NaOH溶液等体积混合后,溶液
pH=7,若为弱酸时,酸的浓度大于0.001 mol·L-1,反应后弱酸过量,pH<7,即25 ℃时,pH=3的一元酸HA溶液与pH=11的NaOH溶液等体积混合后,溶液的pH≤7,A错误;
Fe2+水解显酸性,NH水解也显酸性,所以(NH )Fe(SO ) 中NH抑制Fe2+的水解,故c(Fe2
4 2 4 2
+)前者大于后者,B正确;NH Cl溶液越稀释越水解,故10 mL pH=4的NH Cl溶液稀释至
4 4
1 000 mL,溶液pH<6,C正确;向NH HSO 溶液中滴加少量的NaOH溶液,c(H+)减小,
4 4
促进NH水解,故n(NH)减小;加入过量NaOH时,NaOH与NH反应,n(NH)也减小,D
正确。
5.
答案 A
解析 CHNH 、HBO 分别为一元弱碱和一元弱酸,10 mL 1 mol·L-1的CHNH 、HBO
3 2 3 3 3 2 3 3
两种溶液中酸和碱的物质的量相等,所以中和能力:CHNH =HBO ,故A正确;根据图
3 2 3 3
像可知,稀释相同倍数,CHNH 的pOH变化大,说明CHNH 的电离常数大, lg V=1
3 2 3 2
时,CHNH 和HBO 的浓度都是1 mol·L-1,CHNH 对水电离的抑制作用强,水的电离程
3 2 3 3 3 2
度:CHNH c(H AsO)>c(H AsO )>c(HAsO),A正确;HAsO 的K
2 3 3 3 4 a1
=,电离平衡常数只与温度有关,取图2的pH值为2.2计算,c(H AsO)=c(H AsO ) ,K
2 3 4 a1
=10-2.2,B错误;从图2中pH=2.2分析可知,c(H AsO )=c(H AsO),无法判断是否等于
3 4 2
c(H+),C错误;HAsO 的K 只与温度有关,把HAsO 和HAsO 的水溶液混合在一起时,
3 3 a1 3 3 3 4
HAsO 的K 不变,D错误。
3 3 a1
9.
答案 B
解 析 c 点 溶 液 中 含 有 等 浓 度 的 KA 和 NaA , K = = = ×10 - 8 , c(OH - )
2 2 h
≈ mol·L-1≈1.13×10-5 mol·L-1,pH在9~10之间,A项正确;b点溶液的pH=7,c(OH
-)=c(H+),此时溶液中所含溶质为等浓度的KA和NaA,以及少量的NaHA,根据电荷
2 2
守恒:c(Na+)+c(K+)+c(H+)=c(OH-)+c(HA-)+2c(A2-),因此c(Na+)+c(K+)=c(HA-)
+2c(A2-),在NaHA溶液中存在元素质量守恒:c(Na+)=c(HA-)+c(A2-)+c(H A),因此
2
c(K+)+c(H A)=c(A2-),B项错误;a点(加入的KOH为NaHA物质的量的一半)溶液显酸
2
性,HA-的水解常数K ===×10-11,HA-的电离常数为3.9×10-6>×10-11,则HA-的电
h
离程度大于水解程度,但其电离程度较小,所以其溶液中离子浓度关系为 c(Na+)>c(A2-)
>c(K+)>c(HA-),C项正确;a点溶液由于HA-的电离产生H+,溶液显酸性,水的电离
受到抑制,随着KOH溶液的加入,溶液中c(HA-)逐渐减小,c(A2-)逐渐增大,A2-的水解
促进水的电离,即c点水的电离程度最大,D项正确。
10.
答案 C
解析 由表可知CHCOOH和NH ·H O的电离常数相同,所以CHCOO-和NH的水解能力
3 3 2 3
相同,CHCOONH 溶液呈中性,即常温下c(OH-)=c(H+)=1×10-7 mol·L-1,故A项错
3 4
误;由题可知,c点是完全中和点,该点水的电离程度最大,故B项错误;已知d点溶液
为NH Cl和NH ·H O的混合溶液,且n(NH Cl)∶n(NH ·H O)=2∶1,NH Cl溶液中的质子
4 3 2 4 3 2 4
守恒有①c(OH-)+c(NH ·H O)=c(H+),NH ·H O溶液中的质子守恒有②c(OH-)=c(H+)+
3 2 3 2
c(NH),故 n(NH Cl)∶n(NH ·H O)=2∶1 的混合溶液中根据质子守恒得①×2+②,即
4 3 2
3c(OH-)+2c(NH ·H O) =c(NH)+3c(H+),变式可得 3c(OH-)-3c(H+)=c(NH)-
3 2
2c(NH ·H O),故C项正确;醋酸不可拆,故D项错误。
3 2
11.
答案 C
解析 A点加入2.50 mL AgNO 标准溶液,根据反应Ag++2CN-===[Ag(CN) ]-,原溶液
3 2中n(CN-)=2×0.100 0 mol·L-1×2.50×10-3 L=5×10-4 mol,生成的[Ag(CN) ]-的物质的
2
量为2.5×10-4mol,AB段发生的反应为[Ag(CN) ]-+Ag+===2AgCN↓,2.5×10-4 mol
2
[Ag(CN) ]-消耗2.5×10-4 mol Ag+转化成AgCN沉淀,所消耗标准AgNO 溶液的体积为=
2 3
2.5×10-3 L=2.50 mL,则B点的V =2.50+2.50=5.00,A正确;根据A项计算,原溶液
1
中n(CN-)=5×10-4 mol,c(KCN)==0.020 0 mol·L-1,BC段发生的反应为Ag++Cl-
===AgCl↓,BC段消耗的标准AgNO 溶液的体积为12.50 mL-5.00 mL=7.50 mL,则原溶
3
液中n(Cl-)=0.100 0 mol·L-1×7.50×10-3 L=7.5×10-4 mol,c(KCl)= =0.030 0 mol·L-
1,B 正确;① Ag++2CN-===[Ag(CN) ]-的平衡常数 K =,②[Ag(CN) ]-+Ag+
2 1 2
===2AgCN↓的平衡常数K =,K (AgCN)=c(Ag+)·
2 sp
c(CN-),则K ·K =,C错误;C点时,溶液中====106,D正确。
1 2
12.
答案 C
解析 常温下,没有加入碳酸钠时,c(Ba2+)=c(SO)=1×10-5 mol·L-1,K (BaSO)=c(Ba2
sp 4
+)·
c(SO)=1.0×10-5×1.0×10-5=1.0×10-10,A错误;BaSO 在BaCl 溶液中由于Ba2+的存在,
4 2
使沉淀溶解平衡逆向移动,因此BaSO 在BaCl 溶液中的溶解度比在水中的小,K 只随温
4 2 sp
度的改变而改变,无论在水中还是BaCl 溶液中,K 是不变的,B错误;由图像知,当
2 sp
c(CO)=2.5×10-4 mol·L-1时开始形成BaCO 沉淀,K (BaCO)=c(Ba2+)·c(CO)=1.0×10-
3 sp 3
5×2.5
×10-4=2.5×10-9,BaSO +COBaCO +SO反应的平衡常数K=====0.04,若使
4 3
0.025 mol BaSO 全部转化为BaCO ,则反应消耗0.025 mol CO、生成0.025 mol SO,反应
4 3
达到平衡时,K===0.04,解得c(CO)=0.625 mol·L-1,则至少需要NaCO 的物质的量为
2 3
0.625 mol·
L-1×1 L+0.025 mol=0.65 mol,C正确;根据C项计算,当BaSO 恰好全部转化为BaCO
4 3
时,c(CO)=0.625 mol·L-1,c(SO)=0.025 mol·L-1,c(Ba2+)= mol·L-1=4×
10-9 mol·L-1,由于CO水解溶液呈碱性,离子浓度大小关系为c(CO)>c(SO)>c(OH-)>
c(Ba2+),D错误。
13.
答案 B
解析 根据铵盐的化学式可知③中NH浓度最大,由于CHCOOH的K 大于HCO 的K ,
3 a 2 3 a1
所以HCO的水解程度大于CHCOO-,HCO对NH的水解促进作用更大,NH HCO 中NH
3 4 3
的浓度更小,故三种溶液中c(NH)由大到小的顺序为③>①>②,A错误;溶液呈中性时,根据电荷守恒有c(Na+)=c(Cl-)+c(ClO-),根据得失电子守恒有c(Cl-)=c(HClO)+c(ClO
-),所以c(Na+)=2c(ClO-)+c(HClO),B正确;温度不变,AgCl的K 不变,C错误;根
sp
据题给AgCl和Ag CrO 的K 可知当c(Cl-)和c(CrO)均为1×10-3 mol·L-1时,开始生成
2 4 sp
AgCl和Ag CrO 沉淀时需要c(Ag+)分别为1.8×10-7 mol·L-1和1.4×10-4.5 mol·L-1,所以
2 4
AgCl先沉淀,D错误。
14.
答案 A
解析 由题图可知,开始加入的8 mL NaHCO 发生反应:OH-+HCO===CO+HO,再加
3 2
入 32 mL NaHCO 溶液时,发生反应:HCO+AlO+HO===Al(OH) ↓+CO,由于
3 2 3
n[Al(OH) ]=32×10-3 mol,故c(NaHCO )==1 mol·L-1,A项说法错误;由题图可知,b
3 3
点溶液成分为NaAlO 和NaCO ,c点溶液成分也为NaAlO 和NaCO ,故溶液所含微粒的
2 2 3 2 2 3
种类相同,B项说法正确;a点溶液中溶质为NaOH、NaAlO ,溶液中大量存在的离子是
2
Na+、AlO、OH-,C项说法正确。
15.
答案 B
解析 由图像中的变化曲线可知pH约为9时铜离子浓度最小,废水中Cu2+处理的最佳pH
约为9,故A说法正确;b~c段随氢氧根离子浓度增大,铵根离子与氢氧根离子结合生成
一水合氨,氨浓度增大,平衡Ⅰ正向移动,溶液中铜元素含量增大,故B错误;c~d段,
随氢氧根离子浓度的增大,平衡Ⅰ逆向移动,溶液中铜元素含量减小,故C正确;d点以
后,随c(OH-)增加,平衡Ⅱ:Cu(OH) +2OH-[Cu(OH) ]2-正向移动,上层清液中铜元
2 4
素的含量可能增大,故D正确。
16.
答案 (1)增大固气接触面积,加快反应速率,提高原料利用率 ① 64 ② 2MoS +
2
7O=====2MoO +4SO (2)S2-与H+结合形成HS-,使PbS(s)Pb2+(aq)+S2-(aq)平衡向
2 3 2
右移动 (3)90 (4)MoS +9ClO-+6OH-===MoO+9Cl-+2SO+3HO (5)A
2 2
解析 (1)①由图可知,6层中存在的固体物质分别为 MoS 、MoO 、MoO ,且MoS 、
2 3 2 2
MoO 的物质的量百分数均为18%,根据Mo元素守恒,则MoO 的物质的量百分数为
3 2
64%,即x为64。②在“焙烧”时,氧气将MoS 氧化生成MoO 、SO ,根据得失电子守
2 3 2
恒和质量守恒,该反应的化学方程式为2MoS +7O=====2MoO +4SO 。(3)K (BaMoO )=
2 2 3 2 sp 4
4.0×10-8,c(MoO)=0.40 mol·L-1,当BaMoO 开始沉淀时,c(Ba2+)== mol·
4
L-1=10-7 mol·L-1,此时溶液中c(CO)== mol·L-1=0.01 mol·L-1,所以CO的去除率为
×100%=90%。
(4)次氯酸钠具有强氧化性,能够在碱性条件下把MoS 氧化为MoO和SO,根据得失电子
2守恒和质量守恒,发生反应的离子方程式为MoS +9ClO-+6OH-===MoO+9Cl-+2SO+
2
3HO。
2
(5)通入氮气、加入油脂,起到隔绝空气的作用,盐酸能够与钼酸钠反应,而加入NaNO 可
2
以替代空气中的氧气起氧化剂作用。
17.
答案 (1)①C ②HPO +2OH-===HPO+2HO ③正盐
3 3 2
(2)①ab ②2CuI+2OH-===Cu O+HO+2I-
2 2
解析 (1)①由0.1 mol·L-1 HPO 溶液的pH=1.7,说明亚磷酸部分电离,则亚磷酸是弱酸;
3 3
由HPO 与NaOH反应只生成NaHPO 和NaH PO 两种盐,则说明亚磷酸是二元酸;由
3 3 2 3 2 3
HPO 和碘水反应,碘水棕黄色褪去,再加AgNO 有黄色沉淀生成,说明该反应中亚磷酸
3 3 3
失电子作还原剂,所以亚磷酸有还原性,故正确的说法为bcf。②HPO 与过量NaOH反应
3 3
生成NaHPO 和HO,离子方程式为HPO +2OH-===HPO+2HO。③HPO 为二元弱酸,
2 3 2 3 3 2 3 3
则说明NaHPO 是正盐。(2)①碘化亚铜中铜元素显+1价,碘元素显-1价,化学式为
2 3
CuI,属于盐类,a正确;碘化亚铜稳定且难溶于水,b正确;氧化亚铜属于氧化物,c错误;
铜能与氢碘酸反应,是由于碘化亚铜更难溶,使反应的化学平衡正向进行,d错误。②碘
化亚铜与氢氧化钠反应生成氧化亚铜、碘化钠和水,离子方程式为2CuI+2OH-===Cu O+
2
2I-+HO。
2
18.
答案 (1)① (2)10-6.3 9.8 (3)2.0×10-12V (4)①当滴入最后半滴盐酸时,溶液由红色变
为无色,且半分钟内不恢复到原来颜色 ②×100%
解析 (1)根据图像分析,随着pH的增大,溶液的碱性增强,HCO、CO浓度都增大,而在
曲线②pH很小时也产生HCO,而随着CO浓度增大,逐渐生成CaCO 沉淀,溶液中Ca2+
3
逐渐减小,因此曲线①代表Ca2+,②代表HCO,③代表CO。(2)由点(6.3,-5)计算该温
度下HCO 的电离平衡常数K ==10-6.3;③代表CO,根据该线的数学关系式为y=ax+b
2 3 a1
分析,有8.3a+b=-5,10.3a+b=-1.1,解得a=1.95,b=-21.185,则当lg c(CO)=
-2时,即-2=1.95x-21.185,则x≈9.8。则lg c(CO)=-2时溶液的pH=9.8。(3)由题意
可知,一水合氨的物质的量为(0.1×0.02) mol=0.002 mol,根据[Cd(NH )]2++4HOCd2+
3 4 2
+4NH ·H O分析,Cd2+的物质的量为0.000 5 mol,则浓度为 mol·
3 2
L-1= mol·L-1,根据①[Cd(NH )]2++4HOCd2++4NH ·H O K =2.75×10-7,
3 4 2 3 2 1
② [Cd(NH )]2 + + CO + 4HOCdCO↓ + 4NH ·H O K = 2.75×105 , ① - ② 得
3 4 2 3 3 2 2
CdCOCO+Cd2+,K==10-12,若向该CdSO 溶液中加入NaCO 固体,当CdCO 开始
3 4 2 3 3
沉淀时,溶液中CO浓度为 mol·L-1=2×10-12V mol·L-1。(4)碳酸钠和碳酸氢钠的溶液为
碱性,加入酚酞显红色,加入盐酸,到达滴定终点时:当滴入最后半滴盐酸时,溶液由红
色变为无色,且半分钟内不恢复到原来颜色;首先碳酸钠和盐酸反应生成碳酸氢钠,碳酸钠和盐酸的物质的量相等,消耗盐酸的体积为V mL,碳酸氢钠和盐酸反应生成氯化钠、
1
水和二氧化碳,消耗盐酸的体积为(V -V) mL,碳酸氢钠和盐酸的物质的量相等,其中原
2 1
碳酸氢钠消耗的盐酸的体积为(V -2V) mL,则纯碱样品中NaHCO 质量分数的计算式为
2 1 3
×100%。
19.
答案 (1)Al3++3HOAl(OH) (胶体)+3H+ (2)小于 (3)①Ⅰ NH Al(SO ) 水解使溶液
2 3 4 4 2
呈酸性,升高温度使其水解程度增大,pH减小 ②10-3 (4)①a ②c(Na+)>c(SO)>
c(NH)>c(OH-)=c(H+) ③NH+OH-===NH ·H O
3 2
解析 (1)NH Al(SO ) 溶于水电离出Al3+,Al3+在溶液中发生水解反应:Al3++3HO
4 4 2 2
Al(OH) (胶体)+3H+,水解生成的Al(OH) 胶体具有吸附性,能吸附水中悬浮颗粒产生沉
3 3
降,从而达到净化水的目的。(2)相同条件下,氢离子和铝离子均能抑制铵根离子水解,但
等浓度的氢离子的抑制程度大于铝离子,则 0.1 mol·L-1 NH Al(SO ) 中c(NH)小于 0.1
4 4 2
mol·L-1 NH HSO 中c(NH)。(3)①由于NH Al(SO ) 溶于水电离出的NH、Al3+在溶液中水
4 4 4 4 2
解使溶液显酸性,水解反应是吸热反应,升高温度,平衡向正反应方向移动,溶液中氢离
子浓度增大,pH减小,则符合条件的曲线是 Ⅰ 。②由图可知,20 ℃时,0.1 mol·L-1
NH Al(SO ) 溶液的pH为3,由溶液中的电荷守恒关系2c(SO)+c(OH-)=c(NH)+c(H+)+
4 4 2
3c(Al3+)可得,2c(SO)-c(NH)-3c(Al3+)=c(H+)-c(OH-)≈10-3 mol·L-1。(4)①向100 mL
0.1 mol·L-1 NH HSO 溶液中滴加 0.1 mol·L-1 NaOH 溶液,发生的反应为 H++OH-
4 4
===HO、OH-+NH===NH ·H O,由方程式可知,a点时氢氧化钠溶液恰好中和溶液中的
2 3 2
氢离子,得到等浓度的硫酸铵和硫酸钠的混合溶液,溶液中的铵根离子水解促进水的电离
a点之后,铵根离子与氢氧根离子反应生成抑制水电离的一水合氨,铵根离子浓度越小,
促进水的电离程度越小,所以溶液中水的电离程度最大的是a点。②由图可知b点时,溶
液pH为7,该点为硫酸钠、硫酸铵和一水合氨的混合溶液,则溶液中各离子浓度由大到小
的排列顺序是c(Na+)>c(SO)>
c(NH)>c(OH-)=c(H+)。③由b到c发生反应的离子方程式为OH-+NH===NH ·H O。
3 2
20.
答案 (1)三颈烧瓶
(2)饱和食盐水
(3)增大反应接触面积,使反应更充分
(4)除去多余的Cl,防止污染空气
2
(5)+1
(6)×100%
解析 (2)浓盐酸易挥发,生成的氯气中含有氯化氢,需要除去,则X试剂的名称为饱和食
盐水。(4)氯气有毒,需要尾气处理,D 装置的作用是吸收尾气,防止污染大气。(5)Na PO Cl·5H O中Na、P、O、H的化合价分别是+1价、+5价、-2价,根据化合价
10 3 13 2
代数和为0可知+1×10+(+5)×3+(-2)×13+x=0,解得x=+1,氯元素的化合价是+1
价。(6)Na PO Cl·5H O能把碘离子氧化为单质碘,反应中氯元素化合价从+1价降低到-
10 3 13 2
1价,根据得失电子守恒可知 Na PO Cl·5H O~I ,又因为 2SO+I===SO+2I-,则
10 3 13 2 2 2 2 4
Na PO Cl·5H O~2SO,n(Na PO Cl·5H O)=n(S O)=×cV=×0.05×0.02 mol=5×10-4
10 3 13 2 2 10 3 13 2 2
mol,在250 mL样品溶液中物质的量n=×5×10-4 mol=5×10-3 mol,质量m=nM=
5×10-3M g,所以产品的纯度为×100%。