文档内容
第 4 讲 氧化还原反应
复习目标 1.了解氧化还原反应的概念。2.会用“单、双线桥”分析电子转移的方向和数目。
3.掌握氧化性、还原性强弱的比较及价态规律应用。
考点一 氧化还原反应及相关概念
1.氧化还原反应
(1)判断依据:反应前后有元素的化合价发生变化。
(2)本质:电子转移(得失或偏移)。
2.相关概念
概括为“升失氧、降得还,剂性一致、其他相反”。
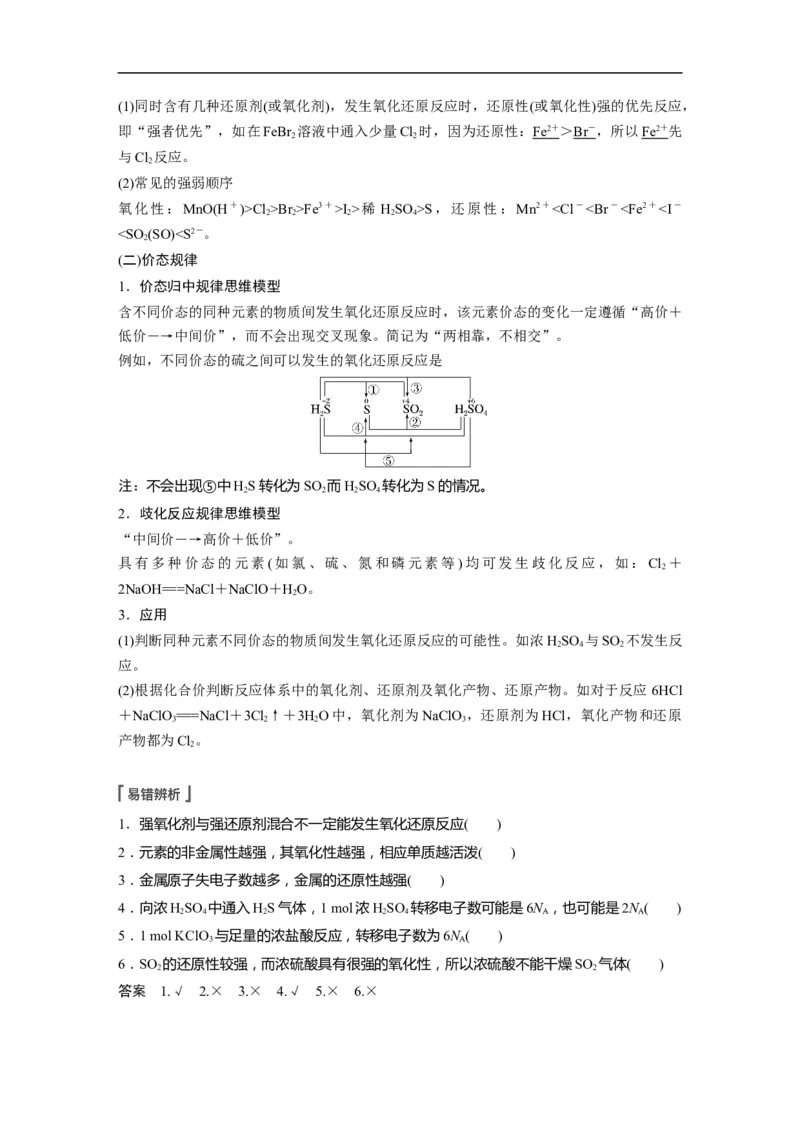
3.氧化还原反应电子转移的表示方法
(1)双线桥法:①标变价 ②画箭头(反应物指向生成物) ③算数目 ④说变化。
用双线桥法标出MnO 与浓盐酸加热反应电子转移的方向和数目:
2
。
归纳 。
(2)单线桥法:箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标
“得”“失”字样。
用单线桥法标出铜和浓硝酸反应电子转移的方向和数目:== = Cu(NO ) + 2NO ↑ + 2H O。
3 2 2 2
归纳 ===氧化产物+还原产物。
4.常见的氧化剂和还原剂
(1)常见的氧化剂
常见的氧化剂包括某些非金属单质、含有高价态元素的化合物、过氧化物等。如:
(2)常见的还原剂
常见的还原剂包括活泼的金属单质、非金属阴离子及含低价态元素的化合物、低价金属阳离
子、某些非金属单质及其氢化物等。如:
(3)元素化合价处于中间价态的物质既有氧化性,又有还原性。如:
其中:Fe2+、SO主要表现还原性,HO 主要表现氧化性。
2 2
5.氧化还原反应与四种基本反应类型间的关系图示
6.重要的还原剂——金属氢化物、NaBH
4
(1)金属氢化物
①结构特点
电子式可表示为M+[H]-(M为碱金属)。
②强还原性a.遇水强烈反应放出氢气,使溶液呈强碱性,如:NaH+HO=== NaOH + H ↑。
2 2
b.高温还原金属
如固态NaH在673 K时能将TiCl 还原为金属钛:TiCl + 4NaH ==== = T i + 4NaC l + 2H ↑。
4 4 2
(2)万能还原剂——硼氢化钠(NaBH )
4
硼氢化钠是一种无机物,化学式为NaBH ,白色至灰白色细结晶粉末或块状,吸湿性强,
4
其碱性溶液呈棕黄色,是最常用的还原剂之一。
通常用作醛类、酮类、酰氯类的还原剂,塑料工业的发泡剂,造纸漂白剂,以及医药工业制
造双氢链霉素的氢化剂。
1.在氧化还原反应中,非金属单质不一定是氧化剂( )
2.某元素从游离态变为化合态,则该元素一定被还原( )
3.有单质参加或生成的化学反应不一定是氧化还原反应( )
4.氧化还原反应中的反应物不是氧化剂就是还原剂( )
5.氧化还原反应中有一种元素被氧化时,一定有另一种元素被还原( )
答案 1.√ 2.× 3.√ 4.× 5.×
一、氧化还原反应概念的考查
1.按要求标出下列化合物中指定元素的化合价。
LiNH:N - 3,LiNH:N - 3,NH:N - 2,
2 2 2 4
NaSO:S + 2,SO:S + 6,C O:C + 3,
2 2 3 2 2
HCN:C + 2 、N - 3 ,BH:B + 3 、H - 1 ,CuH:Cu + 1 、H - 1 ,MnO(OH):Mn + 3 ,
FePO :Fe + 3,
4
CrO:Cr + 6,KFeO:Fe + 6。
2 4
2.2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO。
4 2 2 2
上述反应中,氧化剂是______,还原剂是________,氧化产物是__________,还原产物是
________,KMnO 发生__________反应,HCl 发生________反应,盐酸表现的性质是
4
________性和________性;生成1 mol Cl 时转移电子数目为________,被氧化的HCl的物
2
质的量是________ mol。
答案 KMnO HCl Cl MnCl 还原 氧化 还原 酸 2×6.02×1023(或1.204×1024)
4 2 2
2
3.工业上以石英砂为原料制取单质硅,其工艺流程图如下:
流程一:
SiO――→Si(粗)――→SiHCl ――――――→Si(纯)
2 3
流程二:有关反应分类说法不正确的是( )
A.①~⑥均属于氧化还原反应
B.只有①②③属于置换反应
C.⑥既属于氧化还原反应又属于分解反应
D.⑤中的两个化学反应均属于复分解反应
答案 A
解析 ①SiO +2C=====Si+2CO↑,②Si+3HCl=====SiHCl +H ,③SiHCl +H=====Si
2 3 2 3 2
+3HCl,④ SiO +4Mg=====MgSi+2MgO,⑤ MgSi+4HCl===2MgCl +SiH ,MgO+
2 2 2 2 4
2HCl=== MgCl +HO,⑥SiH=====Si+2H↑。
2 2 4 2
4.工业上常用以下反应炼铁和制硫酸:
①2CuFeS+7O=====CuSO +CuO+Fe O+3SO
2 2 4 2 3 2
②4FeS+11O=====2Fe O+8SO
2 2 2 3 2
已知CuFeS 中Cu为+1价。下列说法正确的是( )
2
A.反应①②中Fe均被氧化
B.反应①中CuSO 和CuO只是氧化产物
4
C.反应②中Fe O 和SO 既是氧化产物又是还原产物
2 3 2
D.反应①②生成等物质的量的SO 时,转移的电子数之比为33∶56
2
答案 C
解析 反应①生成3 mol SO 转移28 mol e-,反应②生成8 mol SO 转移44 mol e-,则反应
2 2
①②生成等物质的量的SO 时,转移的电子数之比为56∶33,D项错误。
2
二、重要的还原剂——金属氢化物、NaBH
4
5.氢化钠(NaH)是一种白色固体,能与水反应放出氢气。下列叙述正确的是( )
A.NaH为共价化合物
B.该化合物中氢为+1价
C.NaH中氢离子半径比锂离子半径小
D.NaH中氢离子被氧化为氢气
答案 D
解析 NaH由Na+和H-构成,为离子化合物,A项不正确;该化合物中,Na显+1价,则
氢显-1价,B项不正确;H-与Li+电子层结构相同,但锂的核电荷数比氢大,所以H-半
径比Li+半径大,C项不正确;NaH中H-转化为氢气时,失电子被氧化,D项正确。
6.硼氢化钠(NaBH )在有机合成、化工生产方面有广泛应用。制备硼氢化钠的化学方程式为
4
NaBO +2SiO+4Na+2HNaBH +2NaSiO。下列有关上述反应的说法错误的是( )
2 2 2 4 2 3
A.氧化产物和还原产物的物质的量之比为2∶1B.转移4 mol电子时,只需向装置中通入44.8 L H (标准状况)
2
C.装药品之前加热装置至100 ℃并持续一会儿
D.制备硼氢化钠的副产物可能有NaH
答案 B
解析 由反应可知氧化产物为NaSiO ,还原产物是NaBH ,所以氧化产物和还原产物的物
2 3 4
质的量之比为2∶1,A项正确;转移4 mol电子时,根据化学方程式可知理论上需要 2 mol
氢气,在标准状况下的体积为2 mol×22.4 L·mol-1=44.8 L,但由于是可逆反应,需要通入
氢气的体积大于44.8 L,B项错误;由于钠极易被氧化且能与水反应,所以需要排尽装置中
的空气和水蒸气,则装药品之前应加热装置至100 ℃并持续一会儿,C项正确。
7.(2022·郑州测评)LiAlH 是重要的储氢材料,可与水发生反应:LiAlH +2HO===LiAlO
4 4 2 2
+4H↑。下列说法正确的是( )
2
A.氢气既是氧化产物又是还原产物
B.LiAlH 既是氧化剂又是还原剂
4
C.若生成标准状况下4.48 L H ,则转移0.4 mol电子
2
D.还原剂与氧化剂的物质的量之比为2∶1
答案 A
解析 由反应的化学方程式可知,LiAlH 中H由-1价升高为0价,被氧化,是还原剂,
4
HO中H由+1价降为0价,被还原,是氧化剂,氢气既是氧化产物又是还原产物,A项正
2
确、B项错误;由反应的化学方程式可知,1 mol LiAlH 反应,转移4 mol电子,生成4 mol
4
H ,若生成标准状况下4.48 L(即0.2 mol)H ,则转移0.2 mol电子,C项错误;LiAlH 为还
2 2 4
原剂,水为氧化剂,还原剂与氧化剂的物质的量之比为1∶2,D项错误。
8.硼氢化钠(NaBH )中的氢元素为-1价,具有很强的还原性,被称为“万能还原剂”,
4
NaBH 在催化剂钌(Ru)表面与水反应的历程如图所示:
4
下列说法错误的是( )
A.过程②反应为BH+HO===H↑+HB(OH)
3 2 2 2
B.反应过程中硼元素的化合价发生了变化
C.若过程③和过程④均产生1 mol H ,则转移电子数目不相等
2
D.Ru可使上述反应活化分子的百分数提高,加快反应速率
答案 B
解析 各步骤中硼元素的化合价均为+3 价,B 项错误;过程③反应为 HB(OH)+
2
HO===H↑+HB(OH) ,产生1 mol H 时转移的电子数为N ,过程④反应为HB(OH) +
2 2 2 2 A 2
2HO+e-===
2H↑+B(OH),产生1 mol H 时转移的电子数为N ,两者不相等,C项正确;Ru为催化剂
2 2 A
催化剂可提高活化分子的百分数,加快反应速率,D项正确。
9.氢化钠(NaH)广泛应用于工业生产。
(1)氢化钠(NaH)中氢元素的化合价为______________________________________。
(2)NaH能与水剧烈反应:NaH+HO===NaOH+H↑,该反应中的氧化剂是________,氧
2 2
化剂与还原剂的物质的量之比是________。
(3)在高温下氢化钠(NaH)可将四氯化钛(TiCl )还原成金属钛,该反应的化学方程式为
4
________________________________________________________________________。
答案 (1)-1 (2)H O 1∶1
2
(3)2NaH+TiCl =====Ti+2NaCl+2HCl↑或4NaH+TiCl =====Ti+4NaCl+2H↑
4 4 2
考点二 氧化还原反应的强弱规律及价态规律
(一)强弱规律
1.氧化性是指得电子的性质(或能力);还原性是指失电子的性质(或能力)。
2.氧化性、还原性的强弱取决于得、失电子的难易程度,与得、失电子数目的多少无关。
如:Na-e-===Na+,Al-3e-===Al3+,但根据金属活动性顺序表,Na比Al活泼,更易失
去电子,所以Na比Al的还原性强。
3.从元素的价态考虑
最高价态——只有氧化性,如:浓HSO 、KMnO 等;
2 4 4
最低价态——只有还原性,如:金属单质、Cl-、S2-等;
中间价态——既有氧化性又有还原性,如:Fe2+、S、Cl 等。
2
4.氧化性、还原性强弱的比较方法
(1)根据化学方程式判断
氧化剂(氧化性)+还原剂(还原性)===还原产物+氧化产物
氧化性:氧化剂>氧化产物;
还原性:还原剂>还原产物。
(2)根据反应条件及反应的剧烈程度判断
反应条件要求越低,反应越剧烈,对应物质的氧化性或还原性越强。如:MnO +
2
4HCl(浓)=====MnCl +Cl↑+2HO,2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+
2 2 2 4 2 2
8HO,可判断氧化性:KMnO >MnO 。
2 4 2
(3)根据相同条件下产物的价态高低判断
如2Fe+3Cl=====2FeCl ;Fe+S=====FeS,则氧化性:Cl>S。
2 3 2
5.先后规律及应用(1)同时含有几种还原剂(或氧化剂),发生氧化还原反应时,还原性(或氧化性)强的优先反应,
即“强者优先”,如在FeBr 溶液中通入少量Cl 时,因为还原性: Fe 2 + > Br - ,所以 Fe 2 + 先
2 2
与Cl 反应。
2
(2)常见的强弱顺序
氧化性:MnO(H+)>Cl >Br >Fe3+>I >稀 HSO >S,还原性:Mn2+KX中Cl(均为正价)。假设KX中Cl元素为+a价,KZ中Cl元素的化合价为
+b价,依据得失电子守恒原理及KX―→KY+3KZ,有a+1=3(b-a),把a=1、a=3、a
=5代入上式讨论,可知a=5时,b=7符合题意。则KX中Cl元素的化合价为+5。
5.K35ClO 晶体与含有H37Cl的浓盐酸反应生成Cl,化学方程式为KClO+6HCl(浓)===KCl
3 2 3
+3Cl↑+3HO,该反应生成氯气的摩尔质量为________。
2 2
答案 73.3 g·mol-1
解析 1 mol Cl 中35Cl占 mol,37Cl占 mol,M=(×35+×37) g·mol-1≈73.3 g·mol-1。
2
6.已知G、Q、X、Y、Z均为含氯元素的化合物,在一定条件下有下列转化关系(未配平):
①G―→Q+NaCl
②Q+HO――→X+H
2 2
③Y+NaOH―→G+Q+HO
2
④Z+NaOH―→Q+X+HO
2
这五种化合物中Cl元素化合价由低到高的顺序是________。
答案 G、Y、Q、Z、X
解析 由①得出Q中Cl元素价态高于G,因为G必介于Q和-1价的氯元素之间,-1价
为氯元素的最低价;将该结论引用到③,Y介于Q与G之间,故有Q价态高于Y,Y价态
高于G;分析②:HO中的H元素化合价降低,则Q中的氯元素转变为X中的氯元素,化
2
合价必升高,则得出X价态高于Q;最后分析④:Z介于Q、X之间,则X价态高于Z,Z
价态高于Q。
1.(2020·山东,2)下列叙述不涉及氧化还原反应的是( )
A.谷物发酵酿造食醋
B.小苏打用作食品膨松剂
C.含氯消毒剂用于环境消毒
D.大气中NO 参与酸雨形成
2
答案 B
解析 谷物发酵的过程中包含淀粉水解、葡萄糖转化为乙醇、乙醇氧化为乙酸的过程;小苏
打分解的化学方程式为2NaHCO =====NaCO +CO↑+HO,不是氧化还原反应;含氯消
3 2 3 2 2
毒剂有强氧化性,可用于环境消毒;NO 与水发生反应:3NO +HO===NO+2HNO ,是氧
2 2 2 3
化还原反应。
2.(2021·浙江6月选考,8)关于反应KHIO +9HI===2KI+4I +6HO,下列说法正确的是(
2 3 6 2 2)
A.KHIO 发生氧化反应
2 3 6
B.KI是还原产物
C.生成12.7 g I 时,转移0.1 mol电子
2
D.还原剂与氧化剂的物质的量之比为7∶1
答案 D
解析 反应中KHIO 中的I元素的化合价降低,得电子发生还原反应,A错误;12.7 g I 的
2 3 6 2
物质的量为0.05 mol,根据反应的化学方程式,每生成4 mol I 转移7 mol电子,则生成
2
0.05 mol I 时转移电子的物质的量为0.087 5 mol,C错误;反应中HI为还原剂,KHIO 为
2 2 3 6
氧化剂,在反应中每消耗1 mol K HIO 就有7 mol HI失电子,则还原剂与氧化剂的物质的
2 3 6
量之比为7∶1,D正确。
3.(2020·北京,3)水与下列物质反应时,水表现出氧化性的是( )
A.Na B.Cl C.NO D.NaO
2 2 2
答案 A
解析 2Na+2HO===2NaOH+H↑,HO中H元素化合价由+1降为0,得电子被还原,
2 2 2
作氧化剂,在反应中表现出氧化性,故 A符合题意;Cl +HOHCl+HClO、3NO +
2 2 2
HO=== 2HNO +NO,HO中的元素没有发生化合价的变化,水在反应中既不是氧化剂也
2 3 2
不是还原剂,既不表现氧化性也不表现还原性,故 B、C 不符合题意;NaO +
2
HO===2NaOH,该反应没有元素化合价的变化,不是氧化还原反应,故D不符合题意。
2
4.(2019·北京,10)下列除杂试剂选用正确且除杂过程不涉及氧化还原反应的是( )
选项 物质(括号内为杂质) 除杂试剂
A FeCl 溶液(FeCl ) Fe粉
2 3
B NaCl溶液(MgCl ) NaOH溶液、稀HCl
2
C Cl(HCl) HO、浓HSO
2 2 2 4
D NO(NO ) HO、无水CaCl
2 2 2
答案 B
解析 A项,Fe粉将溶液中的Fe3+转化为Fe2+,涉及氧化还原反应;B项,Mg2+与NaOH
溶液反应生成Mg(OH) 沉淀,过滤后多余的NaOH用稀盐酸中和,两个反应均不涉及氧化
2
还原反应;C项,Cl 能溶于水并与水发生氧化还原反应,不能用水除去Cl 中的HCl;D项,
2 2
NO 与水反应生成HNO 和NO,涉及氧化还原反应。
2 3
5.(2020·海南,9改编)含有下列有害组分的尾气,常用NaOH溶液吸收以保护环境。吸收
过程中发生歧化反应的是( )A.SO B.SO C.NO D.HBr
3 2 2
答案 C
解析 三氧化硫和氢氧化钠反应生成硫酸钠和水,为非氧化还原反应,A项不符合题意;二
氧化氮与氢氧化钠反应生成亚硝酸钠、硝酸钠和水,N元素化合价既升高又降低,发生氧化
还原反应,属于歧化反应,C项符合题意;溴化氢与氢氧化钠反应生成溴化钠和水,为非氧
化还原反应,D项不符合题意。
课时精练
1.(2020·北京,2)下列物质的应用中,利用了氧化还原反应的是( )
A.用石灰乳脱除烟气中的SO
2
B.用明矾[KAl(SO)·12H O]处理污水
4 2 2
C.用盐酸去除铁锈(主要成分Fe O·xHO)
2 3 2
D.用84消毒液(有效成分NaClO)杀灭细菌
答案 D
解析 用石灰乳脱除烟气中的SO 时,SO 与氢氧化钙反应生成亚硫酸钙或亚硫酸氢钙,反
2 2
应过程中无元素化合价的变化,没有利用氧化还原反应,故 A 不符合题意;明矾
[KAl(SO)·12H O]溶于水,电离出的铝离子发生水解生成氢氧化铝胶体,利用胶体的吸附性
4 2 2
可吸附污水中的固体颗粒物,发生的反应中元素化合价没有变化,没有利用氧化还原反应,
故 B 不符合题意;用盐酸去除铁锈(主要成分 Fe O·xHO),发生的主要反应为 6HCl+
2 3 2
Fe O===2FeCl +3HO,反应中没有元素化合价的变化,没有利用氧化还原反应,故C不符
2 3 3 2
合题意;84消毒液有效成分为NaClO,具有强氧化性,能使蛋白质发生变性从而杀死细菌
病毒,杀菌消毒的过程利用了氧化还原反应,故D符合题意。
2.下列应用不涉及物质氧化性或还原性的是( )
A.用葡萄糖制镜或保温瓶胆
B.铜铸塑像上出现铜绿[Cu (OH) CO]
2 2 3
C.用NaSiO 溶液制备木材防火剂
2 3
D.用浸泡过高锰酸钾溶液的硅藻土保鲜水果
答案 C
解析 葡萄糖与银氨溶液发生氧化还原反应,生成银单质,葡萄糖作还原剂被氧化,故A
不选;高锰酸钾可氧化具有催熟作用的乙烯,从而达到保鲜水果的目的,故D不选。
3.下列实验中,颜色的变化与氧化还原反应有关的是( )
A.向紫色石蕊溶液中加入盐酸,溶液变红
B.饱和FeCl 溶液在沸水中变成红褐色胶体
3C.向FeSO 溶液中滴加NaOH溶液,生成的沉淀由白色迅速变成灰绿色,最后变成红褐色
4
D.SO 使滴有酚酞的NaOH溶液褪色
2
答案 C
解析 向FeSO 溶液中滴加NaOH溶液,得到白色沉淀Fe(OH) ,Fe(OH) 迅速与空气中的
4 2 2
O 发生氧化还原反应得到红褐色的Fe(OH) 。
2 3
4.(2020·浙江7月选考,10)反应MnO +4HCl(浓)=====MnCl +Cl↑+2HO中,氧化产物
2 2 2 2
与还原产物的物质的量之比是( )
A.1∶2 B.1∶1 C.2∶1 D.4∶1
答案 B
5.对于反应:2HS+SO ===3S↓+2HO,氧化剂与还原剂的物质的量之比为( )
2 2 2
A.1∶1 B.2∶1 C.3∶1 D.1∶2
答案 D
解析 反应2HS+SO ===3S↓+2HO中,HS中S元素化合价由-2升高为0价,HS是还
2 2 2 2 2
原剂;SO 中S元素化合价由+4价降低为0价,SO 是氧化剂,所以氧化剂与还原剂的物质
2 2
的量之比等于1∶2,D符合题意。
6.(2018·浙江11月选考,6)下列化学反应中溴元素仅被氧化的是( )
A.2NaBr+Cl===2NaCl+Br
2 2
B.Br +2NaI===2NaBr+I
2 2
C.3Br +6NaOH=====5NaBr+NaBrO +3HO
2 3 2
D.HBr+NaOH===NaBr+HO
2
答案 A
解析 溴化钠中溴元素化合价升高被氧化,选项 A符合;溴单质中溴元素化合价降低被还
原,选项B不符合;溴单质既是氧化剂又是还原剂,被氧化生成溴酸钠,被还原生成溴化
钠,选项C不符合;反应属于中和反应,各元素化合价不变,不属于氧化还原反应,选项D
不符合。
7.下列化学反应中电子转移方向、数目表示正确的是( )
A.
B.
C.D.
答案 D
解析 A项,Cl→NaCl应为得e-,Cl→NaClO应为失e-;B项中氧化产物与还原产物均
2 2
为Cl,且转移电子数目为5e-;C项中用单线桥表示电子转移时不标“得失”。
2
8.下列属于氧化还原反应,且氧化剂和还原剂为同一种物质的是( )
A.MgO+2HCl===MgCl +HO
2 2
B.C+HO(g)=====CO+H
2 2
C.8NH +6NO =====7N+12HO
3 2 2 2
D.2NaO+2HO===4NaOH+O↑
2 2 2 2
答案 D
解析 MgO+2HCl===MgCl +HO中元素化合价没有发生变化,反应不是氧化还原反应,
2 2
A不符合题意;C+HO(g)=====CO+H 中C、H两种元素的化合价都发生了变化,反应属
2 2
于氧化还原反应,其中C是还原剂,HO是氧化剂,B不符合题意;8NH +6NO =====7N
2 3 2 2
+12HO中只有N元素的化合价发生了变化,反应属于氧化还原反应,其中NH 是还原剂,
2 3
NO 是氧化剂,C不符合题意;反应2NaO+2HO===4NaOH+O↑中有O元素化合价的变
2 2 2 2 2
化,反应属于氧化还原反应,其中NaO 既是还原剂也是氧化剂,D符合题意。
2 2
9.氯元素的化合价与其形成的常见物质种类的关系如图所示。
下列说法不正确的是( )
A.b只有还原性
B.c没有漂白性,d具有漂白性
C.一定条件下,e和f均属于较强氧化剂
D.g的化学式为HClO
4
答案 A
解析 b为HCl,其中+1价的H化合价能降低,具有氧化性,A项错误。
10.已知氧化性:Fe3+>I >SO,下列说法或离子方程式正确的是( )
2
A.2Fe3++SO +2HO===2Fe2++SO+4H+
2 2B.Fe O 可写成FeO·Fe O,Fe I 可写成FeI·2FeI
3 4 2 3 3 8 2 3
C.还原性:Fe2+>SO>I-
2
D.反应HSO (浓)+2HI===I+SO ↑+2HO不能进行
2 4 2 2 2
答案 A
解析 反应2Fe3++SO +2HO===2Fe2++SO+4H+中,Fe3+是氧化剂,SO是氧化产物,该
2 2
反应的发生符合氧化性:Fe3+>SO,A正确;铁元素的化合价有+2和+3,碘元素的化合
价是-1,由于氧化性:Fe3+>I ,故I 不能将Fe2+氧化成Fe3+,只能将铁氧化到+2价,
2 2
Fe I 可表示为3FeI·I ,B错误;根据离子的氧化性顺序,得到还原性顺序是SO >I->Fe2
3 8 2 2 2
+,C错误;浓硫酸具有强氧化性,碘离子具有强还原性,反应HSO (浓)+2HI===I +
2 4 2
SO ↑+2HO能进行,D错误。
2 2
11.(2022·潍坊模拟)含元素碲(Te)的几种物质存在如图所示转化关系。下列说法错误的是(
)
A.反应①利用了HTe的还原性
2
B.反应②中HO作氧化剂
2
C.反应③利用了HO 的氧化性
2 2
D.HTeO 转化为HTeO 发生了氧化还原反应
2 2 5 2 4 9
答案 D
解析 HTe被O 氧化生成Te,HTe具有还原性,A项正确;反应②中Te与HO反应生成
2 2 2 2
HTeO ,Te元素化合价升高,是还原剂,则HO为氧化剂,应有H 生成,B项正确;反应
2 3 2 2
③中HTeO →HTeO ,Te元素化合价升高,发生氧化反应,则HO 作氧化剂,体现氧化性,
2 3 6 6 2 2
C项正确;HTeO 转化为HTeO 时不存在元素化合价的变化,未发生氧化还原反应,D项
2 2 5 2 4 9
错误。
12.已知氧化性:Br >Fe3+。FeBr 溶液中通入一定量的Cl ,发生反应的离子方程式:aFe2+
2 2 2
+bBr-+cCl===dFe3++eBr +fCl-。
2 2
下列选项中的数字与离子方程式中的 a、b、c、d、e、f一一对应,其中不符合反应实际的
是( )
A.2 4 3 2 2 6 B.0 2 1 0 1 2
C.2 0 1 2 0 2 D.2 2 2 2 1 4
答案 B
解析 氧化性:Br >Fe3+,则还原性:Fe2+>Br-,当溶液中Fe2+、Br-共存时,Cl 先和Fe2
2 2
+反应,只有Fe2+反应完后,Cl 才能和Br-反应。FeBr 溶液中n(Fe2+)∶n(Br-)=1∶2,设
2 2n(Fe2+)=2 mol,则参加反应的0≤n(Br-)≤4 mol都有可能。A、C、D项符合实际,且符合
三大守恒。而B项认为Br-先反应,违背了还原性:Fe2+>Br-,故错误。
13.HNO 是一种弱酸,且不稳定,易分解生成NO和NO ;它能被常见的强氧化剂氧化;
2 2
在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO 是一种难溶于水、易溶
2
于酸的化合物,试回答下列问题:
(1)人体正常的血红蛋白中含有Fe2+,若误食亚硝酸盐(如NaNO ),则导致血红蛋白中的Fe2+
2
转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填字母)。
A.亚硝酸盐被还原
B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+
D.亚硝酸盐是还原剂
(2)某同学把新制的氯水加到NaNO 溶液中,观察到氯水褪色,同时生成NaNO 和HCl,请
2 3
写出反应的离子方程式:_____________________________________________________。
(3)Fe与过量稀硫酸反应可以制取FeSO ,若用反应所得的酸性溶液将Fe2+转化为Fe3+,要
4
求产物纯净,可选用的最佳试剂是________(填字母)。
a.Cl b.Fe
2
c.HO d.HNO
2 2 3
(4)FeSO 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na FeO),氧化性比
4 2 4
Cl 、O 、ClO 、KMnO 更强,主要反应:2FeSO +6NaO===2NaFeO +2NaO+2NaSO
2 2 2 4 4 2 2 2 4 2 2 4
+O↑。
2
①该反应中的氧化剂是______,还原剂是______。
②简要说明NaFeO 作为水处理剂时所起的作用:
2 4
________________________________________________________________________。
答案 (1)D (2)NO+Cl +HO===NO+2H++2Cl- (3)c (4)①NaO NaO 、FeSO ②
2 2 2 2 2 2 4
高铁酸钠具有强氧化性,能杀菌消毒,消毒过程中自身被还原为 Fe3+,Fe3+水解生成
Fe(OH) 胶体,能吸附水中悬浮杂质而沉降
3
解析 (1)服用维生素C可以解毒,说明在维生素C的作用下Fe3+又转化为Fe2+,铁元素化
合价降低,被还原,则维生素C具有还原性,而亚硝酸盐会导致Fe2+转化为Fe3+,说明亚
硝酸盐具有氧化性,在反应中亚硝酸盐为氧化剂,所以维生素 C是还原剂。(3)由于Cl 、
2
HNO 都能氧化亚铁离子,但会引入新的杂质,铁不能氧化亚铁离子,双氧水作为氧化剂的
3
还原产物是水,不引入杂质,所以最佳试剂是双氧水。(4)该反应中铁元素化合价由+2变为
+6、氧元素化合价由-1变为0、-2。得电子化合价降低的反应物是氧化剂、失电子化合
价升高的反应物是还原剂,所以NaO 是氧化剂,NaO、FeSO 是还原剂。
2 2 2 2 4
14.氧化还原反应是一类重要的化学反应。
(1)已知反应:Cu+2Fe3+===Cu2++2Fe2+,反应中还原剂是__________,氧化性:Fe3+
__________(填“<”或“>”)Cu2+。(2)在2NaO +2CO===2NaCO +O 反应中,若转移3 mol电子,则所产生的氧气在标准状
2 2 2 2 3 2
况下的体积为________ L。
(3)在xR2++yH++O===mR3++nHO的离子方程式中,对系数m和R2+、R3+判断正确的是
2 2
________(填字母)。
A.m=y,R3+是还原剂 B.m=2y,R2+被氧化
C.m=2,R3+是氧化剂 D.m=4,R2+是还原剂
(4)用双线桥标出反应2KMnO +16HCl(浓)===2KCl+2MnCl +5Cl↑+8HO中电子转移的
4 2 2 2
方向和数目。
答案 (1)Cu > (2)33.6 (3)D
(4)
解析 (3)根据氧原子守恒,所以n=2,根据氢原子守恒,所以y=4,根据R原子守恒则x
=m,根据电荷守恒则2x+y=3m,所以x=y=m=4,在反应中,R的化合价升高,R2+是
还原剂,所以R3+是氧化产物,氧元素化合价降低,所以HO是还原产物。
2