文档内容
热点强化 5 钠的化合物组成成分的测定
1.测定物质组成实验数据获取的常用方法
(1)沉淀法
先将某种成分转化为沉淀,然后称量纯净、干燥的沉淀的质量,再进行相关计算。
(2)测气体体积法
对于产生气体的反应,可以通过测定气体体积的方法测定样品纯度。
(3)测气体质量法
将生成的气体通入足量的吸收剂中,通过称量实验前后吸收剂的质量,求得所吸收气体的质
量,然后进行相关计算。
(4)热重法
只要物质受热时发生质量变化,都可以用热重法来研究物质的组成。
(5)滴定法
2.测定纯碱中碳酸钠质量分数的常用方法
(1)气体法
①测定原理:NaCO+HSO ===NaSO +HO+CO↑。
2 3 2 4 2 4 2 2
依据CO 的体积确定NaCO 的物质的量,进而确定纯碱中NaCO 的含量。
2 2 3 2 3
②实验操作:向m g纯碱样品中加入足量的稀硫酸,准确测量产生 CO 气体的体积为V
2
mL(已折算为标准状况)。
③数据处理
纯碱样品中NaCO 的质量为 mol×106 g·mol-1= g,则纯碱样品中NaCO 的质量分数为
2 3 2 3
×100%=%。
(2)沉淀法
①测定原理:NaCO+BaCl ===BaCO ↓+2NaCl。
2 3 2 3
依据BaCO 沉淀的质量确定NaCO 的物质的量,进而确定纯碱中NaCO 的含量。
3 2 3 2 3
②实验操作:先将m g纯碱样品溶于水配成溶液,向溶液中加入过量的BaCl 溶液,经过滤、
2
洗涤、干燥得BaCO 沉淀的质量为n g。
3
③数据处理
纯碱样品中 NaCO 的质量为×106 g·mol-1= g,则纯碱样品中 NaCO 的质量分数为
2 3 2 3
×100%=×100%。
1.为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W g样品进行实验,
下列实验方法所对应的实验方案和测量数据合理的是( )选项 实验方法 实验方案 测量数据
将样品配成100 mL溶液,取10 mL,
A 滴定法 消耗盐酸的体积
加入酚酞,用标准盐酸滴定
将样品与盐酸反应,生成的气体全部
B 量气法 碱石灰增加的质量
被碱石灰吸收
将样品放入烧瓶中,置于电子天平
C 重量法 减少的质量
上,加入足量盐酸
将样品与盐酸反应,气体通过排水量
D 量气法 排出水的体积
气装置量气
答案 A
解析 用酚酞作指示剂时,NaCO 与盐酸发生反应 NaCO +2HCl===2NaCl+CO↑+
2 3 2 3 2
HO,依据消耗盐酸的量可以计算出样品中NaCO 的量,进而确定样品中NaCO 的质量分
2 2 3 2 3
数,A项正确;测量碱石灰增重的方法是重量法而不是量气法,B项错误;因盐酸的质量未
知,无法通过重量法测量NaCO 的质量,C项错误;因部分CO 能溶解到水里,与水反应
2 3 2
生成HCO,故排出水的体积并不是CO 的体积,D项错误。
2 3 2
2.为了测定NaCl、NaCO·10H O和NaHCO 的混合物中各组分的含量,某同学设计如下
2 3 2 3
实验:取一定质量的混合物,通过测量反应前后②和③装置质量的变化,测定该混合物中各
组分的质量分数。下列说法错误的是( )
A.①②③中可以依次盛装碱石灰、无水CaCl 、碱石灰
2
B.硬质玻璃管加热前,应关闭b,打开a,缓缓通入空气,直至a处出来的空气不再使澄清
石灰水变浑浊为止
C.若将①装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量偏大
D.实验过程中一直通入空气,停止加热后再停止通入空气
答案 C
解析 根据实验目的和装置的连接顺序可知:①装置用于吸收空气中的CO 和水蒸气,可以
2
使用碱石灰;②装置吸收 NaCO·10H O 和 NaHCO 分解生成的水蒸气,可以使用无水
2 3 2 3
CaCl ;③装置吸收碳酸氢钠分解生成的CO ,使用碱石灰,A项正确;实验前必须将装置
2 2
中的水蒸气和CO 赶净,避免影响测定结果,B项正确;若将①装置换成盛放NaOH溶液的
2
洗气瓶,则会增加水的质量,使测得NaCO·10H O和NaHCO 的含量偏高,NaCl的含量偏
2 3 2 3
低,C项错误;停止加热后继续通入空气使存留在装置中的CO 和水蒸气完全被吸收,D项
2
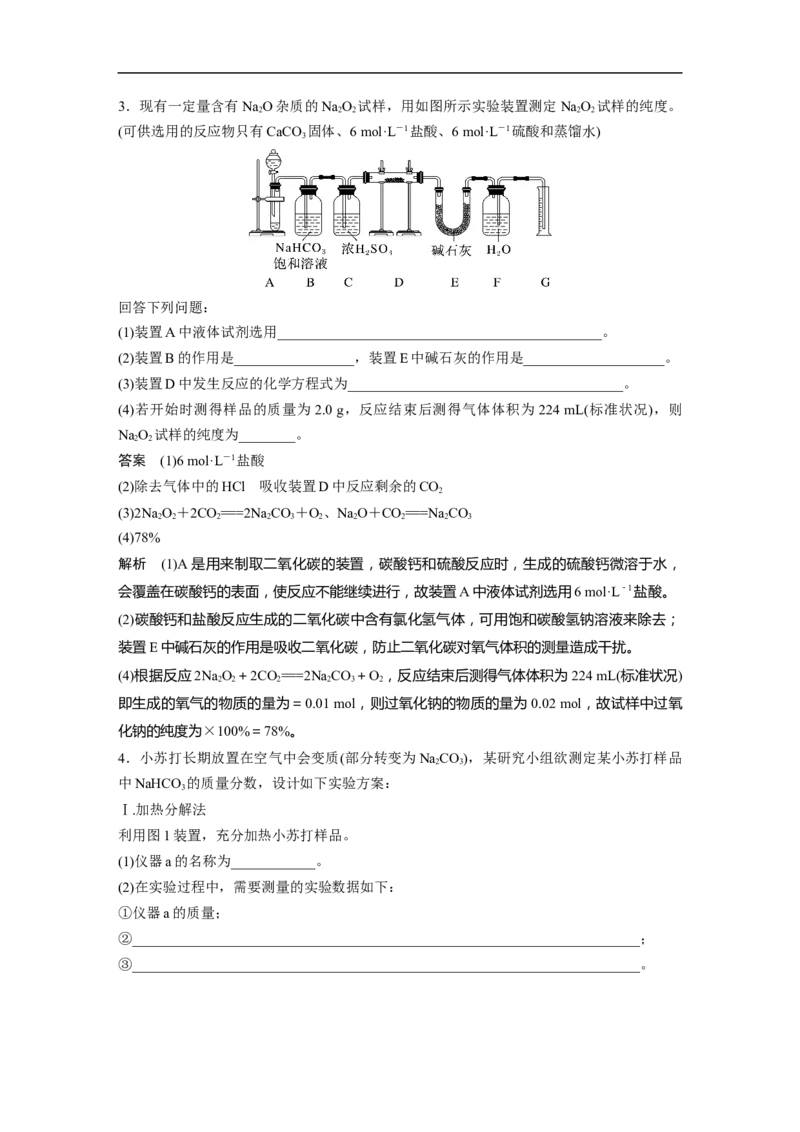
正确。3.现有一定量含有NaO杂质的NaO 试样,用如图所示实验装置测定NaO 试样的纯度。
2 2 2 2 2
(可供选用的反应物只有CaCO 固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
3
回答下列问题:
(1)装置A中液体试剂选用______________________________________________。
(2)装置B的作用是_________________,装置E中碱石灰的作用是____________________。
(3)装置D中发生反应的化学方程式为_______________________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为 224 mL(标准状况),则
NaO 试样的纯度为________。
2 2
答案 (1)6 mol·L-1盐酸
(2)除去气体中的HCl 吸收装置D中反应剩余的CO
2
(3)2Na O+2CO===2NaCO+O、NaO+CO===NaCO
2 2 2 2 3 2 2 2 2 3
(4)78%
解析 (1)A是用来制取二氧化碳的装置,碳酸钙和硫酸反应时,生成的硫酸钙微溶于水,
会覆盖在碳酸钙的表面,使反应不能继续进行,故装置A中液体试剂选用6 mol·L-1盐酸。
(2)碳酸钙和盐酸反应生成的二氧化碳中含有氯化氢气体,可用饱和碳酸氢钠溶液来除去;
装置E中碱石灰的作用是吸收二氧化碳,防止二氧化碳对氧气体积的测量造成干扰。
(4)根据反应2NaO +2CO===2NaCO +O ,反应结束后测得气体体积为224 mL(标准状况)
2 2 2 2 3 2
即生成的氧气的物质的量为=0.01 mol,则过氧化钠的物质的量为0.02 mol,故试样中过氧
化钠的纯度为×100%=78%。
4.小苏打长期放置在空气中会变质(部分转变为NaCO),某研究小组欲测定某小苏打样品
2 3
中NaHCO 的质量分数,设计如下实验方案:
3
Ⅰ.加热分解法
利用图1装置,充分加热小苏打样品。
(1)仪器a的名称为____________。
(2)在实验过程中,需要测量的实验数据如下:
①仪器a的质量;
②________________________________________________________________________;
③________________________________________________________________________。Ⅱ.测量气体体积法
利用图2装置,测定反应生成气体的体积。
(3)组装好仪器后,首先进行的操作为______________________________________。
(4)导管g的作用为_______________________________________________________。
(5)为了减小实验误差,B、C中最好用________________________________溶液代替水。
(6)待反应结束,气体冷却至室温后,利用图示装置读取气体体积时,应注意的事项如下:
①________________________________________________________________________。
②________________________________________________________________________。
(7)若所取样品的质量为m g,反应前量气管C的读数为V mL,反应结束后量气管C的读
1
数为V mL,则样品中NaHCO 和NaCO 的物质的量之和为____________(气体体积均已换
2 3 2 3
算为标准状况下的体积)。
答案 (1)坩埚 (2)②加热前,仪器a和样品的总质量 ③加热冷却后,仪器a和残留物的
总质量
(3)检查装置气密性
(4)平衡分液漏斗与锥形瓶内的气压,使液体顺利流下;滴入锥形瓶的稀硫酸的体积等于进
入分液漏斗的气体体积,从而消除因加入稀硫酸而引起的气体体积误差
(5)饱和NaHCO
3
(6)①读数时应上下移动C管,使B、C两管液面相平 ②视线与液面最低处相平
(7) mol
解析 (7)根据碳原子守恒,1 mol碳原子对应1 mol二氧化碳,二氧化碳的物质的量为
mol,所以样品中NaHCO 和NaCO 的物质的量之和为 mol。
3 2 3