文档内容
第 33 讲 新型化学电源
复习目标 1.知道常考新型化学电源的类型及考查方式。2.会分析新型化学电源的工作原理,
能正确书写新型化学电源的电极反应式。
类型一 浓差电池
1.在浓差电池中,为了限定某些离子的移动,常涉及到“离子交换膜”。
(1)常见的离子交换膜
阳离子交换膜 只允许阳离子(包括H+)通过
阴离子交换膜 只允许阴离子通过
质子交换膜 只允许H+通过
(2)离子交换膜的作用
①能将两极区隔离,阻止两极物质发生化学反应。
②能选择性地允许离子通过,起到平衡电荷、形成闭合回路的作用。
(3)离子交换膜的选择依据
离子的定向移动。
2.“浓差电池”的分析方法
浓差电池是利用物质的浓度差产生电势的一种装置。两侧半电池中的特定物质有浓度差,离
子均是由“高浓度”移向“低浓度”,阴离子移向负极区域,阳离子移向正极区域,判断电
池的正、负极,是解题的关键。
1.锌溴液流电池用溴化锌溶液作电解液,并在电池间不断循环。下列有关说法正确的是(
)
A.充电时n接电源的负极,Zn2+通过阳离子交换膜由左侧流向右侧
B.放电时每转移1 mol电子,负极区溶液质量减少65 g
C.充电时阴极的电极反应式为Br +2e-===2Br-
2
D.若将阳离子交换膜换成阴离子交换膜,放电时正、负极也随之改变
答案 A解析 充电时n接电源的负极,Zn2+通过阳离子交换膜向阴极定向迁移,故由左侧流向右侧,
A正确;放电时,负极Zn溶解生成Zn2+,Zn2+通过阳离子交换膜向正极定向迁移,故负极
区溶液质量不变,B错误;充电时阴极的电极反应式为 Zn2++2e-===Zn,C错误;若将阳
离子交换膜换成阴离子交换膜,放电时正、负极不会改变,Zn仍是负极,D错误。
2.由相同金属电极及其不同浓度的盐溶液组成的电池,称浓差电池,电子由溶液浓度较小
的一极经外电路流向浓度较大的一极。如图所示装置中,X电极与Y电极初始质量相等。
进行实验时,先闭合K ,断开K ,一段时间后,再断开K ,闭合K ,即可形成浓差电池,
2 1 2 1
电流表指针偏转。下列不正确的是( )
A.充电前,该电池两电极存在电势差
B.放电时,右池中的NO通过离子交换膜移向左池
C.充电时,当外电路通过0.1 mol电子时,两电极的质量差为21.6 g
D.放电时,电极Y为电池的正极
答案 A
解析 充电前,左右两池浓度相同,该电池两电极不存在电势差,故 A错误;放电时,电
子由溶液浓度较小的一极流向浓度较大的一极,则X是负极、Y是正极,右池中的NO通过
离子交换膜移向左池,故B正确;充电时,当外电路通过0.1 mol电子时,X电极生成0.1
mol Ag,Y电极消耗0.1 mol Ag,所以两电极的质量差为21.6 g,故C正确;电子由溶液浓
度较小的一极经外电路流向浓度较大的一极,充电后左池浓度小于右池,所以放电时,电极
Y为电池的正极,故D正确。
类型二 物质循环转化型电池
根据物质转化中,元素化合价的变化或离子的移动(阳离子移向正极区域,阴离子移向负极
区域),判断电池的正、负极,是分析该电池的关键。
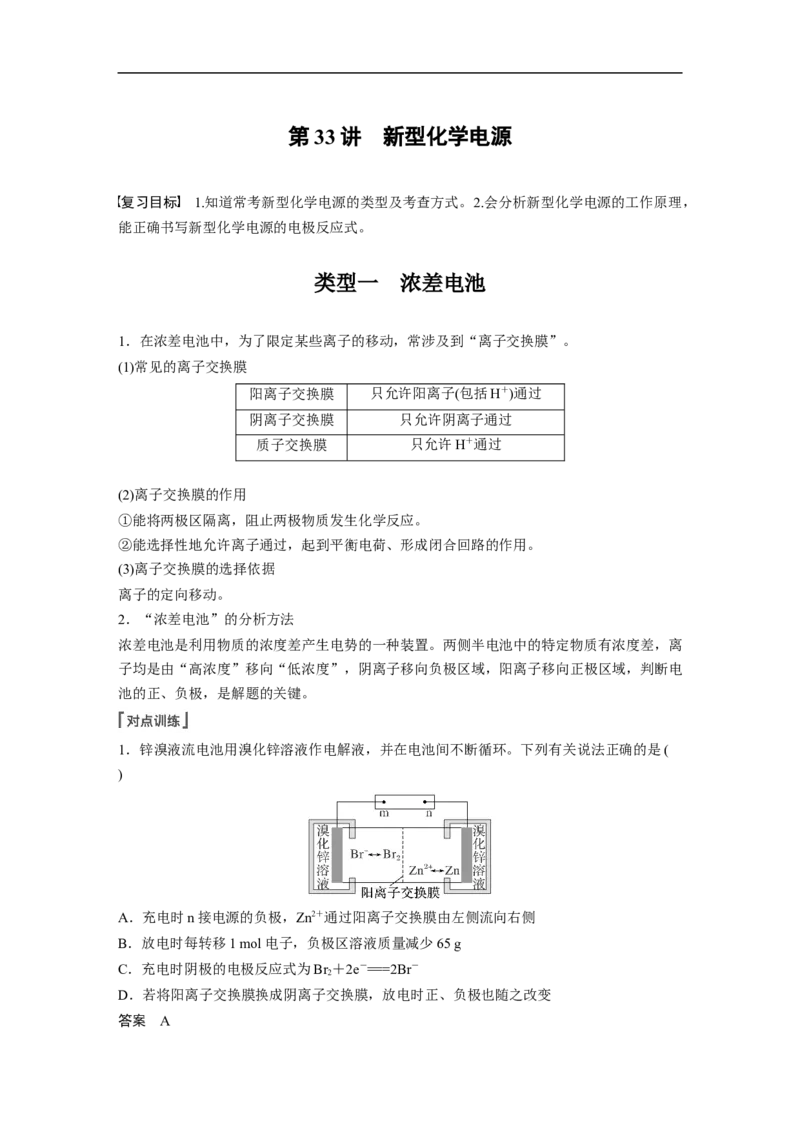
3.(2019·全国卷Ⅰ,12)利用生物燃料电池原理研究室温下氨的合成,电池工作时 MV2+/MV
+在电极与酶之间传递电子,示意图如图所示。下列说法错误的是( )A.相比现有工业合成氨,该方法条件温和,同时还可提供电能
B.阴极区,在氢化酶作用下发生反应:H+2MV2+===2H++2MV+
2
C.正极区,固氮酶为催化剂,N 发生还原反应生成NH
2 3
D.电池工作时质子通过交换膜由负极区向正极区移动
答案 B
解析 由题图和题意知,电池总反应是3H +N===2NH 。该合成氨反应在常温下进行,并
2 2 3
形成原电池产生电能,反应不需要高温、高压和催化剂,A项正确;观察题图知,左边电极
发生氧化反应:MV+-e-===MV2+,为负极,不是阴极,B项错误;正极区N 在固氮酶作
2
用下发生还原反应生成NH ,C项正确;电池工作时,H+通过交换膜,由左侧(负极区)向右
3
侧(正极区)迁移,D项正确。
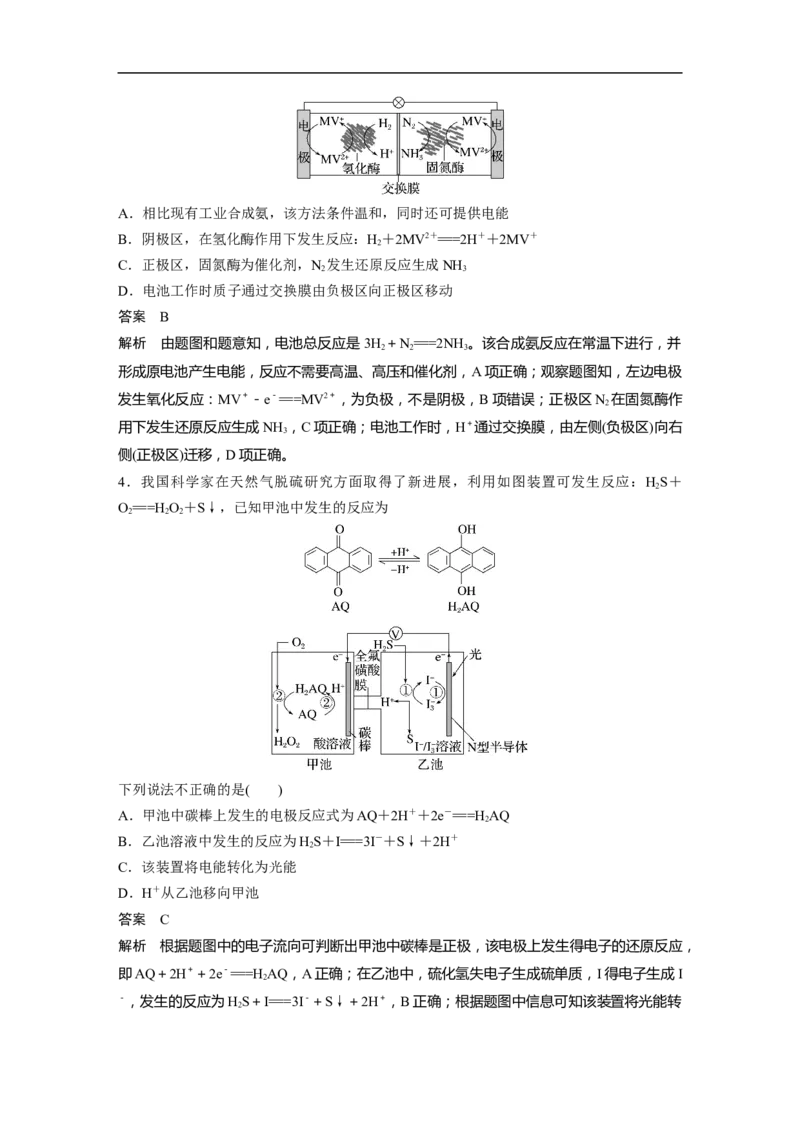
4.我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:HS+
2
O===HO+S↓,已知甲池中发生的反应为
2 2 2
下列说法不正确的是( )
A.甲池中碳棒上发生的电极反应式为AQ+2H++2e-===HAQ
2
B.乙池溶液中发生的反应为HS+I===3I-+S↓+2H+
2
C.该装置将电能转化为光能
D.H+从乙池移向甲池
答案 C
解析 根据题图中的电子流向可判断出甲池中碳棒是正极,该电极上发生得电子的还原反应,
即AQ+2H++2e-===HAQ,A正确;在乙池中,硫化氢失电子生成硫单质,I得电子生成I
2
-,发生的反应为HS+I===3I-+S↓+2H+,B正确;根据题图中信息可知该装置将光能转
2化为电能,C错误;该装置是原电池装置,阳离子移向正极,甲池中碳棒是正极,所以
H+从乙池移向甲池,D正确。
类型三 锂电池与锂离子电池
1.锂电池
锂电池是一类由金属锂或锂合金为负极材料、使用非水电解质溶液的电池。锂电池的负极材
料是金属锂或锂合金,工作时金属锂失去电子被氧化为 Li+,负极反应均为Li-e-===Li+,
负极生成的Li+经过电解质定向移动到正极。
2.锂离子二次电池
(1)锂离子电池基于电化学“嵌入/脱嵌”反应原理,替代了传统的“氧化—还原”理念;在
两极形成的电压降的驱动下,Li+可以从电极材料提供的“空间”中“嵌入”或“脱嵌”。
(2)锂离子电池充电时阴极反应式一般为6C+xLi++xe-===LiC ;放电时负极反应是充电时
x 6
阴极反应的逆过程:LiC -xe-===6C+xLi+。
x 6
(3)锂离子电池的正极材料一般为含Li+的化合物,目前已商业化的正极材料有LiFePO 、
4
LiCoO 、LiMn O 等。
2 2 4
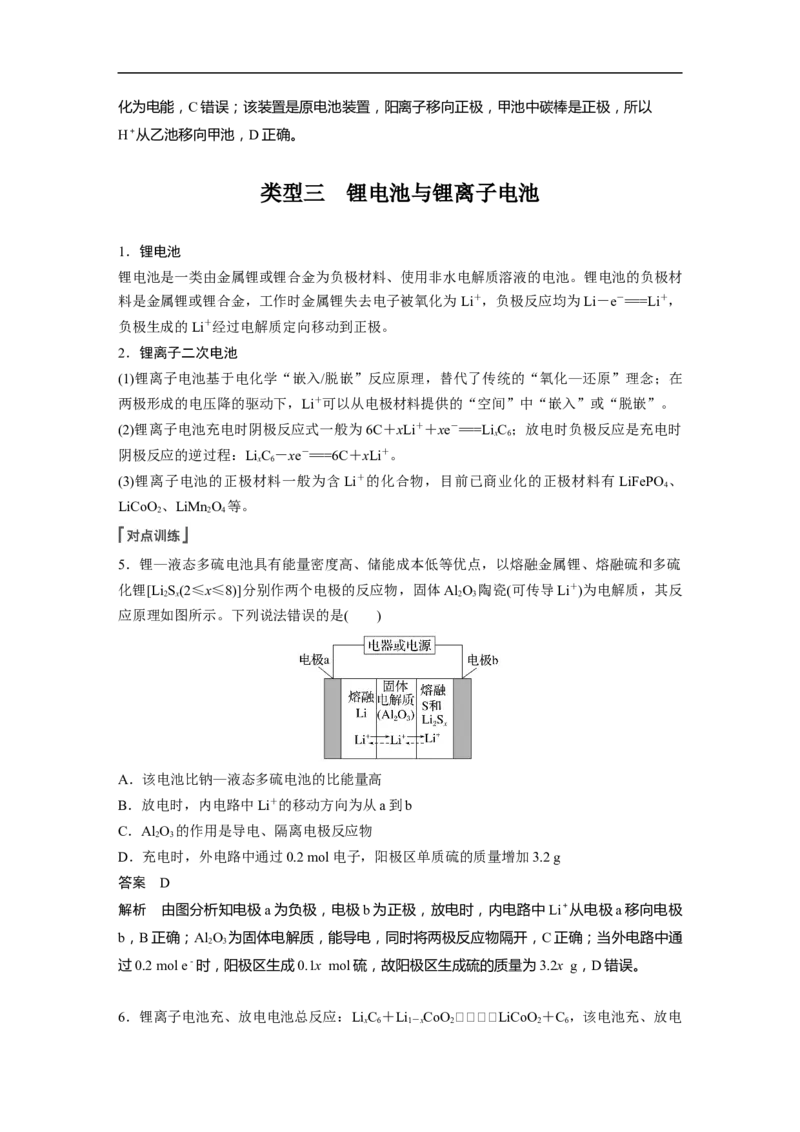
5.锂—液态多硫电池具有能量密度高、储能成本低等优点,以熔融金属锂、熔融硫和多硫
化锂[Li S(2≤x≤8)]分别作两个电极的反应物,固体Al O 陶瓷(可传导Li+)为电解质,其反
2 x 2 3
应原理如图所示。下列说法错误的是( )
A.该电池比钠—液态多硫电池的比能量高
B.放电时,内电路中Li+的移动方向为从a到b
C.Al O 的作用是导电、隔离电极反应物
2 3
D.充电时,外电路中通过0.2 mol电子,阳极区单质硫的质量增加3.2 g
答案 D
解析 由图分析知电极a为负极,电极b为正极,放电时,内电路中Li+从电极a移向电极
b,B正确;Al O 为固体电解质,能导电,同时将两极反应物隔开,C正确;当外电路中通
2 3
过0.2 mol e-时,阳极区生成0.1x mol硫,故阳极区生成硫的质量为3.2x g,D错误。
6.锂离子电池充、放电电池总反应:LiC +Li CoOLiCoO +C ,该电池充、放电
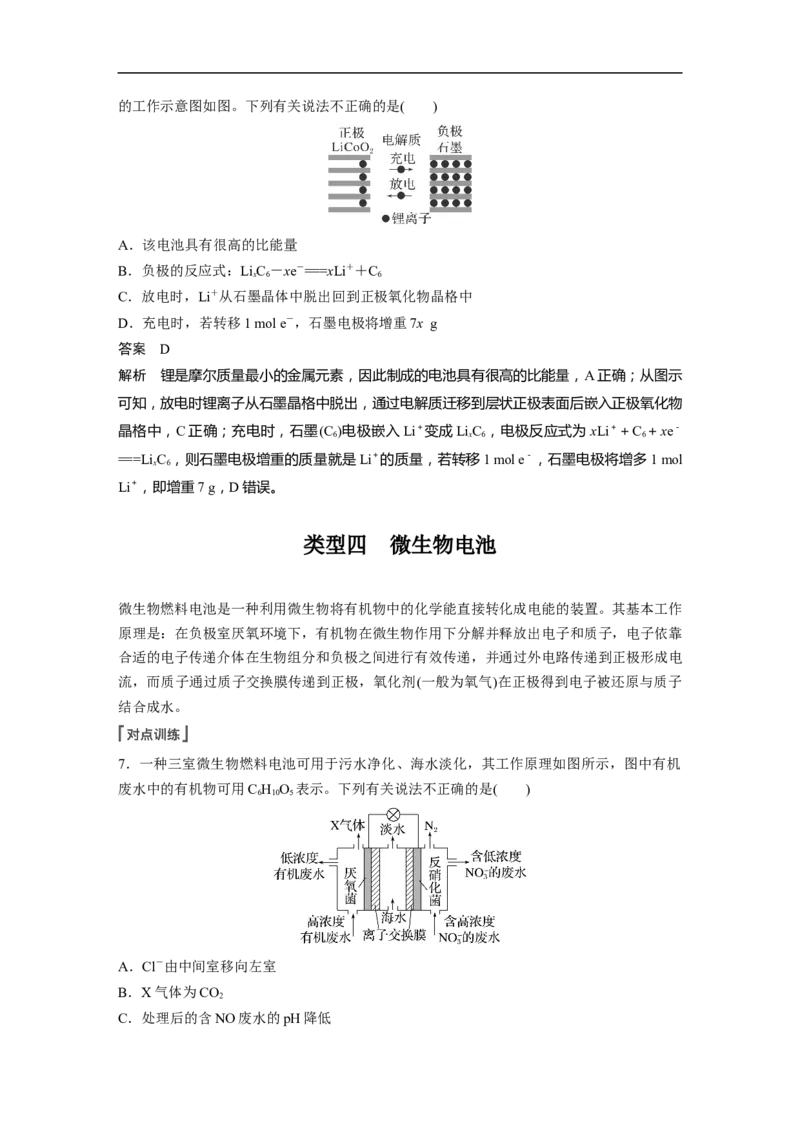
x 6 1-x 2 2 6的工作示意图如图。下列有关说法不正确的是( )
A.该电池具有很高的比能量
B.负极的反应式:LiC -xe-===xLi++C
x 6 6
C.放电时,Li+从石墨晶体中脱出回到正极氧化物晶格中
D.充电时,若转移1 mol e-,石墨电极将增重7x g
答案 D
解析 锂是摩尔质量最小的金属元素,因此制成的电池具有很高的比能量,A正确;从图示
可知,放电时锂离子从石墨晶格中脱出,通过电解质迁移到层状正极表面后嵌入正极氧化物
晶格中,C正确;充电时,石墨(C )电极嵌入Li+变成LiC ,电极反应式为xLi++C +xe-
6 x 6 6
===LiC ,则石墨电极增重的质量就是Li+的质量,若转移1 mol e-,石墨电极将增多1 mol
x 6
Li+,即增重7 g,D错误。
类型四 微生物电池
微生物燃料电池是一种利用微生物将有机物中的化学能直接转化成电能的装置。其基本工作
原理是:在负极室厌氧环境下,有机物在微生物作用下分解并释放出电子和质子,电子依靠
合适的电子传递介体在生物组分和负极之间进行有效传递,并通过外电路传递到正极形成电
流,而质子通过质子交换膜传递到正极,氧化剂(一般为氧气)在正极得到电子被还原与质子
结合成水。
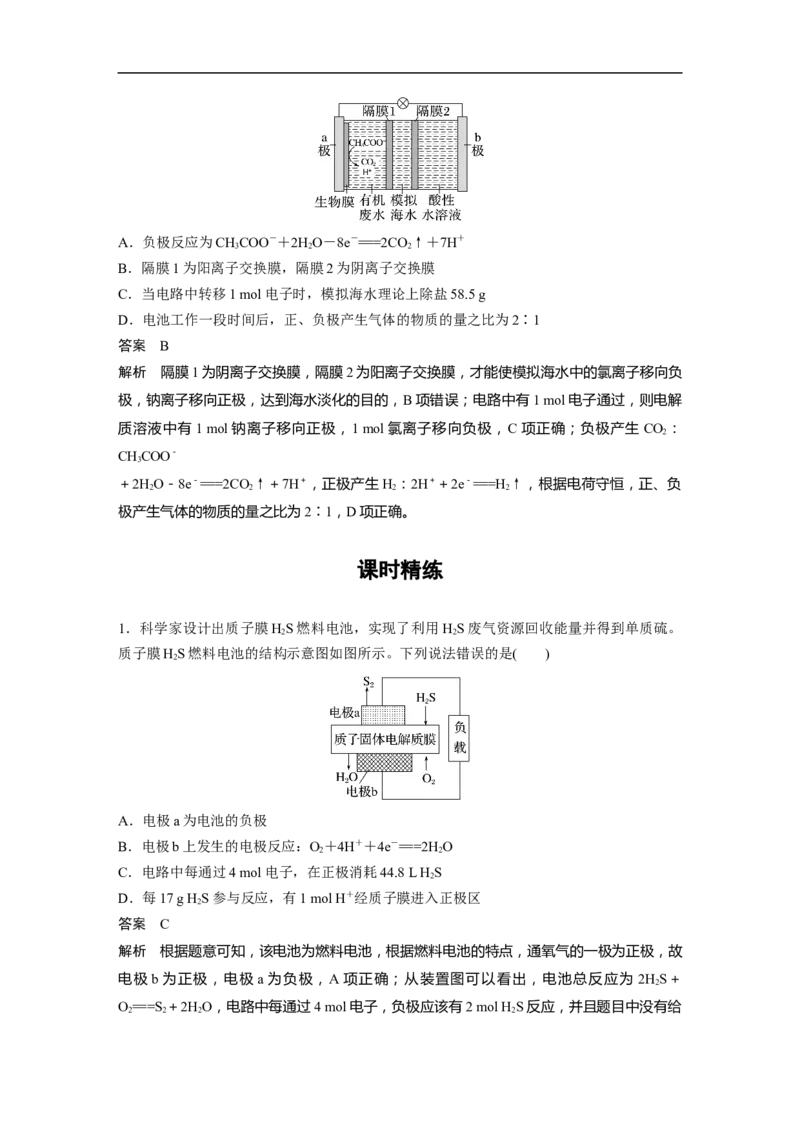
7.一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示,图中有机
废水中的有机物可用C H O 表示。下列有关说法不正确的是( )
6 10 5
A.Cl-由中间室移向左室
B.X气体为CO
2
C.处理后的含NO废水的pH降低D.电路中每通过4 mol电子,产生X气体的体积在标准状况下为22.4 L
答案 C
解析 该原电池中,NO得电子发生还原反应,则装置中右边电极是正极,电极反应为2NO
+10e-+12H+===N↑+6HO,装置左边电极是负极,负极上有机物在厌氧菌作用下生成
2 2
二氧化碳。放电时,电解质溶液中Cl-移向负极室(左室),A、B项正确;根据正极的电极反
应式可知H+参加反应导致溶液酸性减弱,溶液的pH增大,C项错误;根据负极上电极反应
为C H O -24e-+7HO===6CO↑+24H+,可知电路中每通过4 mol电子,产生标准状况
6 10 5 2 2
下X气体的体积为(×6×22.4) L=22.4 L,D项正确。
8.微生物燃料电池能将污水中的乙二胺(H NCH CHNH )氧化成环境友好的物质,示意图如
2 2 2 2
图所示,a、b均为石墨电极。下列说法错误的是( )
A.a电极的电极反应为HNCH CHNH -16e-+4HO===2CO↑+N↑+16H+
2 2 2 2 2 2 2
B.电池工作时质子通过质子交换膜由负极区向正极区移动
C.a电极上的电势比b电极上的电势低
D.电池工作时b电极附近溶液的pH保持不变
答案 D
解析 原电池中,阳离子向正极移动,阴离子向负极移动,B正确;a电极为负极,b电极
为正极,故a电极上的电势比b电极上的电势低,C正确;电池工作时,氧气在正极b上得
电子发生还原反应,电极反应式为O +4e-+4H+===2HO,H+浓度减小,故b电极附近溶
2 2
液的pH增大,D错误。
1.(2021·河北,9)K—O 电池结构如图,a和b为两个电极,其中之一为单质钾片。关于该
2
电池,下列说法错误的是( )
A.隔膜允许K+通过,不允许O 通过
2
B.放电时,电流由b电极沿导线流向a电极;充电时,b电极为阳极
C.产生1 Ah电量时,生成KO 的质量与消耗O 的质量比值约为2.22
2 2D.用此电池为铅酸蓄电池充电,消耗3.9 g钾时,铅酸蓄电池消耗0.9 g水
答案 D
解析 金属性强的钾易与氧气反应,为防止钾与氧气反应,电池所选择隔膜应允许 K+通过,
不允许O 通过,故A正确;放电时,a为负极,b为正极,电流由b电极沿导线流向a电极,
2
充电时,b电极应与直流电源的正极相连,作电解池的阳极,故 B正确;生成1 mol超氧化
钾时,消耗 1 mol 氧气,两者的质量比为(1 mol×71 g·mol-1)∶(1 mol×32 g·mol-
1)≈2.22∶1,故 C 正确;铅酸蓄电池充电时的总反应的化学方程式为 2PbSO +
4
2HO===PbO +Pb+2HSO ,反应每消耗2 mol水时,转移2 mol电子,由得失电子守恒可
2 2 2 4
知,消耗3.9 g钾时,铅酸蓄电池消耗水的质量为×18 g·mol-1=1.8 g,故D错误。
2.(2021·浙江6月选考,22)某全固态薄膜锂离子电池截面结构如图所示,电极 A为非晶硅
薄膜,充电时Li+得电子成为Li嵌入该薄膜材料中;电极B为LiCoO 薄膜;集流体起导电
2
作用。下列说法不正确的是( )
A.充电时,集流体A与外接电源的负极相连
B.放电时,外电路通过a mol电子时,LiPON薄膜电解质损失a mol Li+
C.放电时,电极B为正极,反应可表示为Li CoO+xLi++xe-===LiCoO
1-x 2 2
D.电池总反应可表示为LiSi+Li CoOSi+LiCoO
x 1-x 2 2
答案 B
解析 由图可知,集流体A与电极A相连,充电时电极A作阴极,故充电时集流体A与外
接电源的负极相连,A说法正确;放电时,外电路通过a mol电子时,内电路中有a mol Li
+通过LiPON薄膜电解质从负极迁移到正极,但是 LiPON薄膜电解质没有损失Li+,B说法
不正确;放电时,电极 B为正极,发生还原反应,反应可表示为 Li CoO +xLi++xe-
1-x 2
===LiCoO ,C说法正确;电池放电时,嵌入在非晶硅薄膜中的锂失去电子转化为 Li+,正
2
极上 Li CoO 得到电子和 Li+转化为 LiCoO ,故电池总反应可表示为 LiSi+Li
1-x 2 2 x 1-
CoOSi+LiCoO ,D说法正确。
x 2 2
3.(2020·山东,10)微生物脱盐电池是一种高效、经济的能源装置,利用微生物处理有机废
水获得电能,同时可实现海水淡化。现以NaCl溶液模拟海水,采用惰性电极,用如图装置
处理有机废水(以含CHCOO-的溶液为例)。下列说法错误的是( )
3A.负极反应为CHCOO-+2HO-8e-===2CO↑+7H+
3 2 2
B.隔膜1为阳离子交换膜,隔膜2为阴离子交换膜
C.当电路中转移1 mol电子时,模拟海水理论上除盐58.5 g
D.电池工作一段时间后,正、负极产生气体的物质的量之比为2∶1
答案 B
解析 隔膜1为阴离子交换膜,隔膜2为阳离子交换膜,才能使模拟海水中的氯离子移向负
极,钠离子移向正极,达到海水淡化的目的,B项错误;电路中有1 mol电子通过,则电解
质溶液中有 1 mol 钠离子移向正极,1 mol 氯离子移向负极,C 项正确;负极产生 CO :
2
CHCOO-
3
+2HO-8e-===2CO↑+7H+,正极产生H :2H++2e-===H↑,根据电荷守恒,正、负
2 2 2 2
极产生气体的物质的量之比为2∶1,D项正确。
课时精练
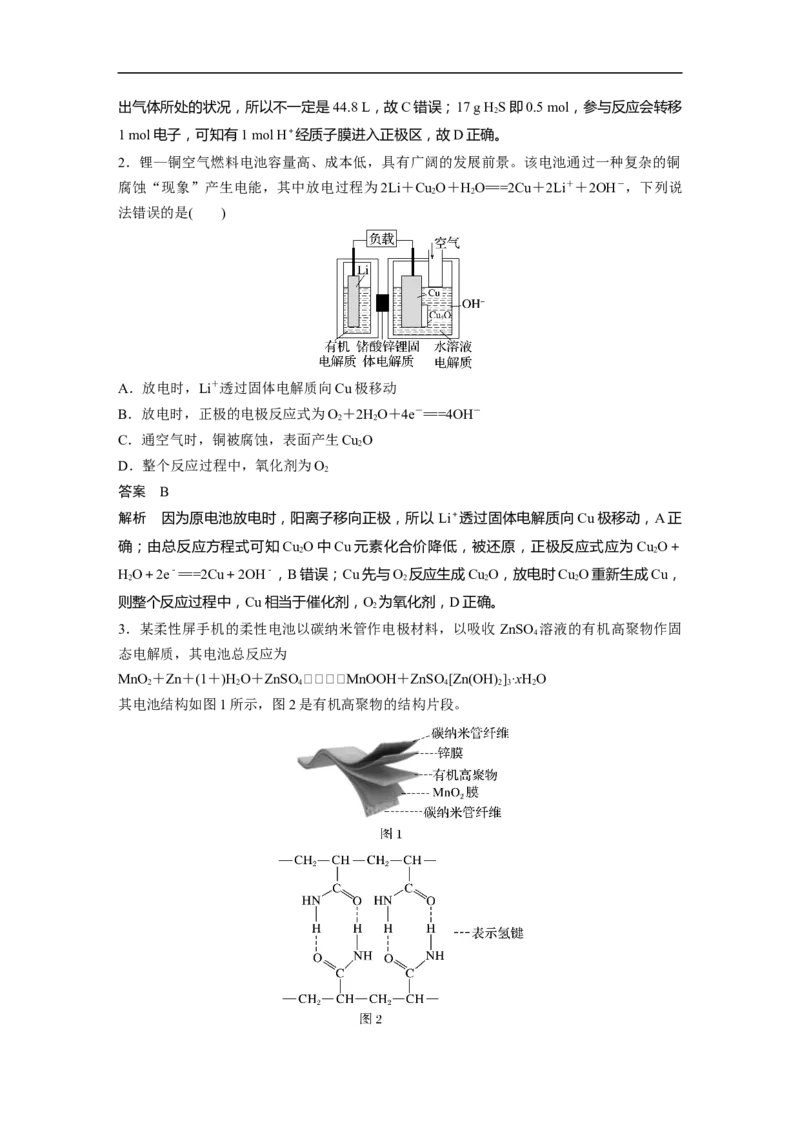
1.科学家设计出质子膜HS燃料电池,实现了利用HS废气资源回收能量并得到单质硫。
2 2
质子膜HS燃料电池的结构示意图如图所示。下列说法错误的是( )
2
A.电极a为电池的负极
B.电极b上发生的电极反应:O+4H++4e-===2HO
2 2
C.电路中每通过4 mol电子,在正极消耗44.8 L H S
2
D.每17 g HS参与反应,有1 mol H+经质子膜进入正极区
2
答案 C
解析 根据题意可知,该电池为燃料电池,根据燃料电池的特点,通氧气的一极为正极,故
电极 b为正极,电极 a为负极,A项正确;从装置图可以看出,电池总反应为 2HS+
2
O===S+2HO,电路中每通过4 mol电子,负极应该有2 mol H S反应,并且题目中没有给
2 2 2 2出气体所处的状况,所以不一定是44.8 L,故C错误;17 g H S即0.5 mol,参与反应会转移
2
1 mol电子,可知有1 mol H+经质子膜进入正极区,故D正确。
2.锂—铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜
腐蚀“现象”产生电能,其中放电过程为2Li+Cu O+HO===2Cu+2Li++2OH-,下列说
2 2
法错误的是( )
A.放电时,Li+透过固体电解质向Cu极移动
B.放电时,正极的电极反应式为O+2HO+4e-===4OH-
2 2
C.通空气时,铜被腐蚀,表面产生Cu O
2
D.整个反应过程中,氧化剂为O
2
答案 B
解析 因为原电池放电时,阳离子移向正极,所以 Li+透过固体电解质向Cu极移动,A正
确;由总反应方程式可知Cu O中Cu元素化合价降低,被还原,正极反应式应为Cu O+
2 2
HO+2e-===2Cu+2OH-,B错误;Cu先与O 反应生成Cu O,放电时Cu O重新生成Cu,
2 2 2 2
则整个反应过程中,Cu相当于催化剂,O 为氧化剂,D正确。
2
3.某柔性屏手机的柔性电池以碳纳米管作电极材料,以吸收 ZnSO 溶液的有机高聚物作固
4
态电解质,其电池总反应为
MnO +Zn+(1+)H O+ZnSOMnOOH+ZnSO[Zn(OH) ]·xHO
2 2 4 4 2 3 2
其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法不正确的是( )
A.碳纳米管具有导电性,可用作电极材料
B.放电时,电池的正极反应式为
MnO +e-+H+===MnOOH
2
C.充电时,Zn2+移向锌膜
D.合成有机高聚物的单体是CH==
2
答案 B
解析 A项,该电池以碳纳米管作电极材料,可知碳纳米管具有导电性,正确;B项,原电
池正极发生还原反应,根据放电时的总反应式,放电时 MnO 得电子发生还原反应,所以电
2
池的正极反应式为MnO +e-+HO===MnOOH+OH-,错误;C项,充电时该装置为电解
2 2
池,阳离子移向阴极,充电时锌膜充当阴极,所以Zn2+移向锌膜,正确;D项,根据高聚
物的结构单元,该高聚物为加聚产物,合成有机高聚物的单体是CH== ,正
2
确。
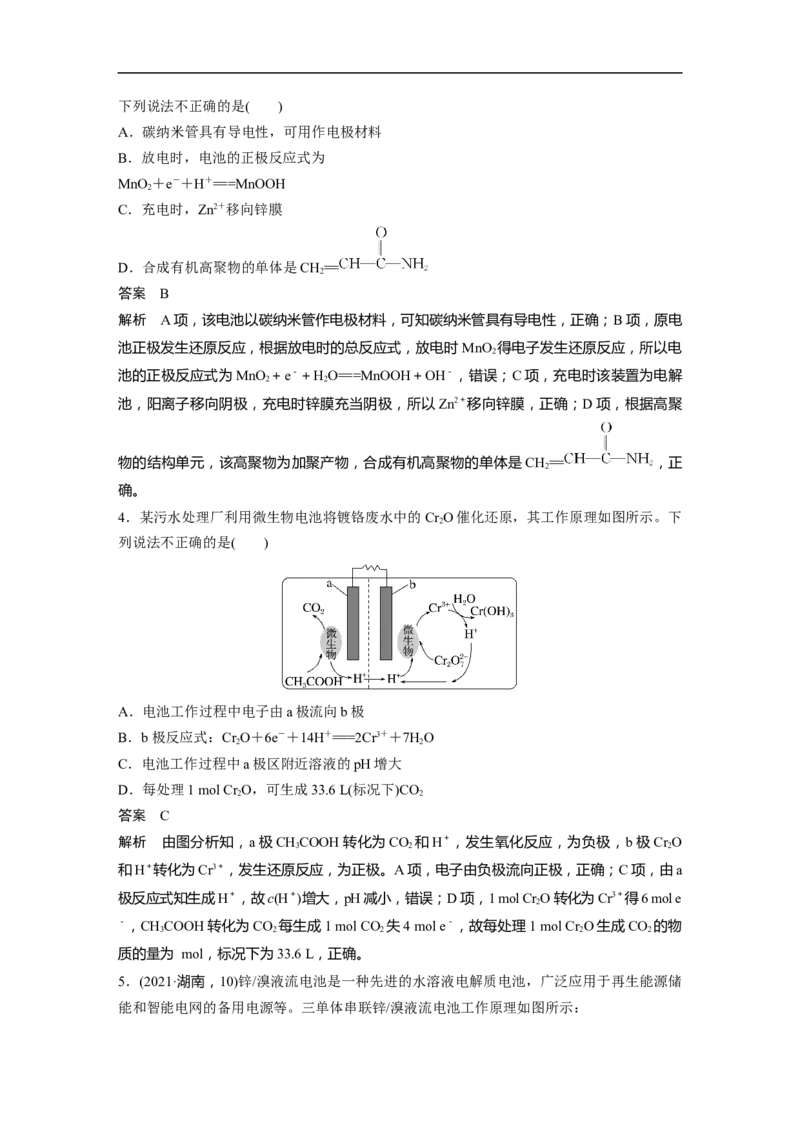
4.某污水处理厂利用微生物电池将镀铬废水中的Cr O催化还原,其工作原理如图所示。下
2
列说法不正确的是( )
A.电池工作过程中电子由a极流向b极
B.b极反应式:Cr O+6e-+14H+===2Cr3++7HO
2 2
C.电池工作过程中a极区附近溶液的pH增大
D.每处理1 mol Cr O,可生成33.6 L(标况下)CO
2 2
答案 C
解析 由图分析知,a极CHCOOH转化为CO 和H+,发生氧化反应,为负极,b极Cr O
3 2 2
和H+转化为Cr3+,发生还原反应,为正极。A项,电子由负极流向正极,正确;C项,由a
极反应式知生成H+,故c(H+)增大,pH减小,错误;D项,1 mol Cr O转化为Cr3+得6 mol e
2
-,CHCOOH转化为CO 每生成1 mol CO 失4 mol e-,故每处理1 mol Cr O生成CO 的物
3 2 2 2 2
质的量为 mol,标况下为33.6 L,正确。
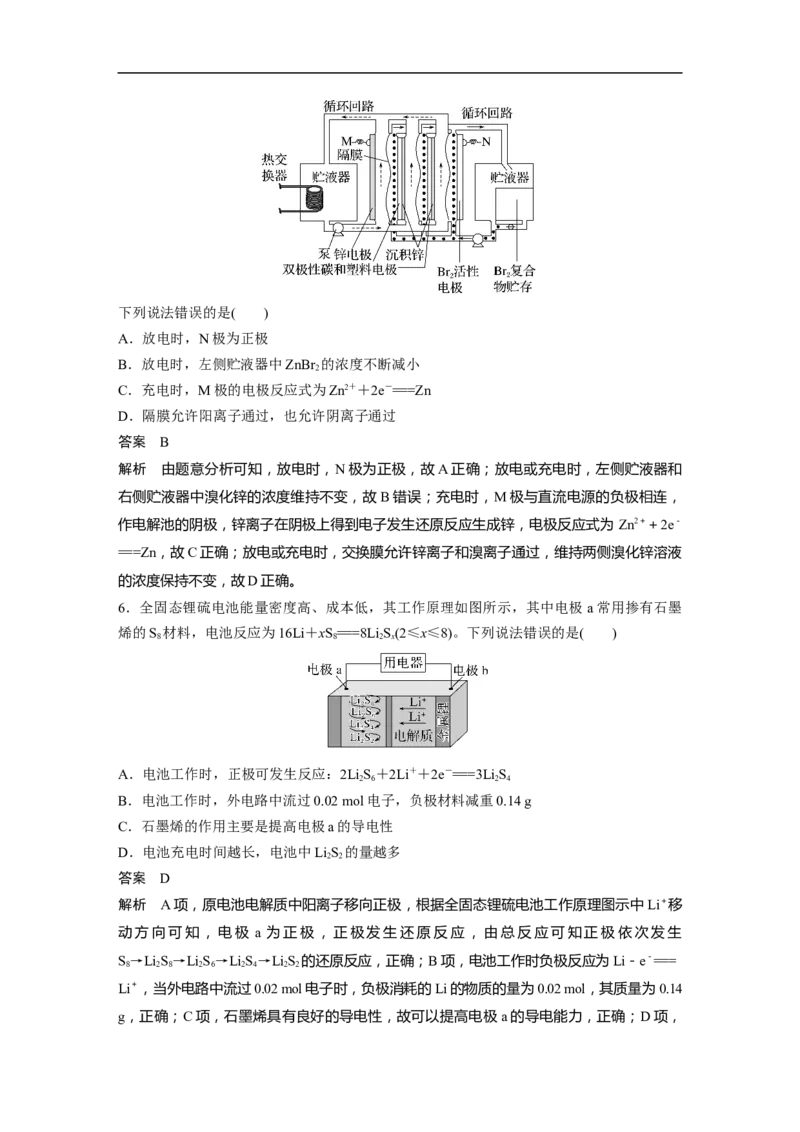
5.(2021·湖南,10)锌/溴液流电池是一种先进的水溶液电解质电池,广泛应用于再生能源储
能和智能电网的备用电源等。三单体串联锌/溴液流电池工作原理如图所示:下列说法错误的是( )
A.放电时,N极为正极
B.放电时,左侧贮液器中ZnBr 的浓度不断减小
2
C.充电时,M极的电极反应式为Zn2++2e-===Zn
D.隔膜允许阳离子通过,也允许阴离子通过
答案 B
解析 由题意分析可知,放电时,N极为正极,故A正确;放电或充电时,左侧贮液器和
右侧贮液器中溴化锌的浓度维持不变,故B错误;充电时,M极与直流电源的负极相连,
作电解池的阴极,锌离子在阴极上得到电子发生还原反应生成锌,电极反应式为 Zn2++2e-
===Zn,故C正确;放电或充电时,交换膜允许锌离子和溴离子通过,维持两侧溴化锌溶液
的浓度保持不变,故D正确。
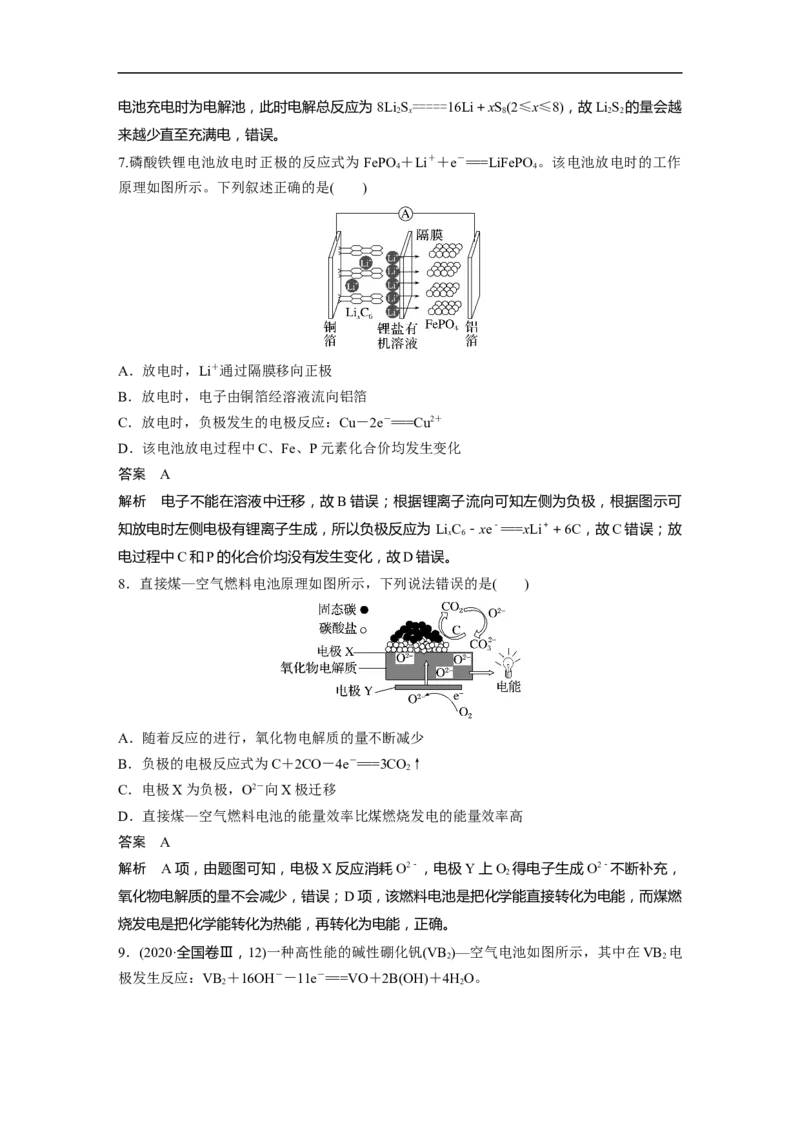
6.全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极 a常用掺有石墨
烯的S 材料,电池反应为16Li+xS===8LiS(2≤x≤8)。下列说法错误的是( )
8 8 2 x
A.电池工作时,正极可发生反应:2LiS+2Li++2e-===3LiS
2 6 2 4
B.电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g
C.石墨烯的作用主要是提高电极a的导电性
D.电池充电时间越长,电池中LiS 的量越多
2 2
答案 D
解析 A项,原电池电解质中阳离子移向正极,根据全固态锂硫电池工作原理图示中Li+移
动方向可知,电极 a 为正极,正极发生还原反应,由总反应可知正极依次发生
S→LiS→LiS→LiS→LiS 的还原反应,正确;B项,电池工作时负极反应为Li-e-===
8 2 8 2 6 2 4 2 2
Li+,当外电路中流过0.02 mol电子时,负极消耗的Li的物质的量为0.02 mol,其质量为0.14
g,正确;C项,石墨烯具有良好的导电性,故可以提高电极 a的导电能力,正确;D项,电池充电时为电解池,此时电解总反应为 8LiS=====16Li+xS(2≤x≤8),故LiS 的量会越
2 x 8 2 2
来越少直至充满电,错误。
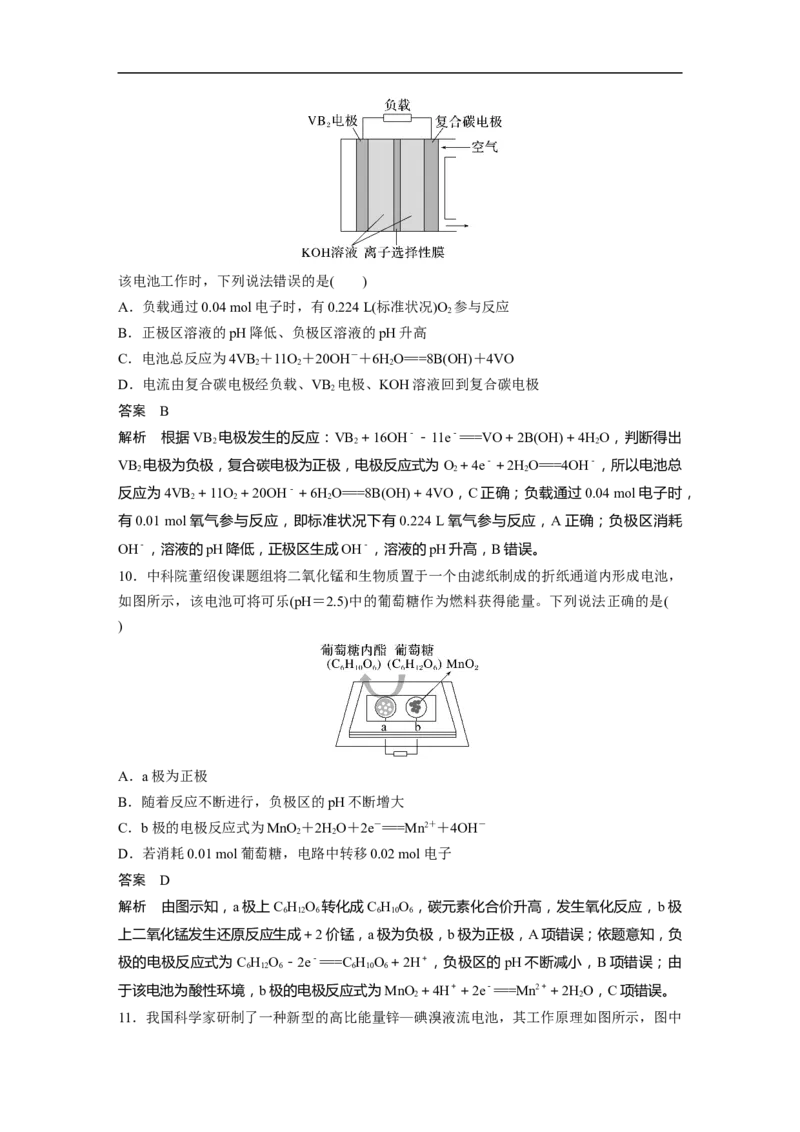
7.磷酸铁锂电池放电时正极的反应式为 FePO +Li++e-===LiFePO 。该电池放电时的工作
4 4
原理如图所示。下列叙述正确的是( )
A.放电时,Li+通过隔膜移向正极
B.放电时,电子由铜箔经溶液流向铝箔
C.放电时,负极发生的电极反应:Cu-2e-===Cu2+
D.该电池放电过程中C、Fe、P元素化合价均发生变化
答案 A
解析 电子不能在溶液中迁移,故B错误;根据锂离子流向可知左侧为负极,根据图示可
知放电时左侧电极有锂离子生成,所以负极反应为 LiC -xe-===xLi++6C,故C错误;放
x 6
电过程中C和P的化合价均没有发生变化,故D错误。
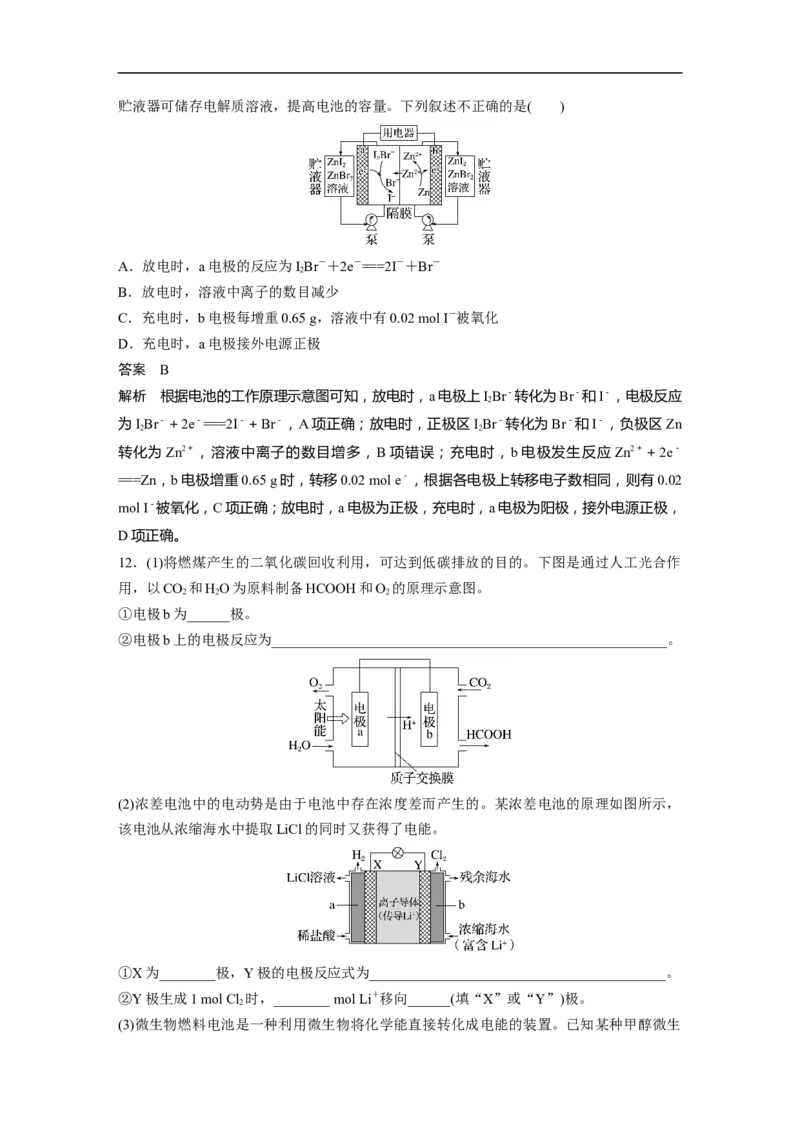
8.直接煤—空气燃料电池原理如图所示,下列说法错误的是( )
A.随着反应的进行,氧化物电解质的量不断减少
B.负极的电极反应式为C+2CO-4e-===3CO↑
2
C.电极X为负极,O2-向X极迁移
D.直接煤—空气燃料电池的能量效率比煤燃烧发电的能量效率高
答案 A
解析 A项,由题图可知,电极X反应消耗O2-,电极Y上O 得电子生成O2-不断补充,
2
氧化物电解质的量不会减少,错误;D项,该燃料电池是把化学能直接转化为电能,而煤燃
烧发电是把化学能转化为热能,再转化为电能,正确。
9.(2020·全国卷Ⅲ,12)一种高性能的碱性硼化钒(VB )—空气电池如图所示,其中在VB 电
2 2
极发生反应:VB +16OH--11e-===VO+2B(OH)+4HO。
2 2该电池工作时,下列说法错误的是( )
A.负载通过0.04 mol电子时,有0.224 L(标准状况)O 参与反应
2
B.正极区溶液的pH降低、负极区溶液的pH升高
C.电池总反应为4VB +11O+20OH-+6HO===8B(OH)+4VO
2 2 2
D.电流由复合碳电极经负载、VB 电极、KOH溶液回到复合碳电极
2
答案 B
解析 根据VB 电极发生的反应:VB +16OH--11e-===VO+2B(OH)+4HO,判断得出
2 2 2
VB 电极为负极,复合碳电极为正极,电极反应式为O+4e-+2HO===4OH-,所以电池总
2 2 2
反应为4VB +11O +20OH-+6HO===8B(OH)+4VO,C正确;负载通过0.04 mol电子时,
2 2 2
有0.01 mol氧气参与反应,即标准状况下有0.224 L氧气参与反应,A正确;负极区消耗
OH-,溶液的pH降低,正极区生成OH-,溶液的pH升高,B错误。
10.中科院董绍俊课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池,
如图所示,该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法正确的是(
)
A.a极为正极
B.随着反应不断进行,负极区的pH不断增大
C.b极的电极反应式为MnO +2HO+2e-===Mn2++4OH-
2 2
D.若消耗0.01 mol葡萄糖,电路中转移0.02 mol电子
答案 D
解析 由图示知,a极上C H O 转化成C H O ,碳元素化合价升高,发生氧化反应,b极
6 12 6 6 10 6
上二氧化锰发生还原反应生成+2价锰,a极为负极,b极为正极,A项错误;依题意知,负
极的电极反应式为C H O -2e-===C H O +2H+,负极区的pH不断减小,B项错误;由
6 12 6 6 10 6
于该电池为酸性环境,b极的电极反应式为MnO +4H++2e-===Mn2++2HO,C项错误。
2 2
11.我国科学家研制了一种新型的高比能量锌—碘溴液流电池,其工作原理如图所示,图中贮液器可储存电解质溶液,提高电池的容量。下列叙述不正确的是( )
A.放电时,a电极的反应为IBr-+2e-===2I-+Br-
2
B.放电时,溶液中离子的数目减少
C.充电时,b电极每增重0.65 g,溶液中有0.02 mol I-被氧化
D.充电时,a电极接外电源正极
答案 B
解析 根据电池的工作原理示意图可知,放电时,a电极上IBr-转化为Br-和I-,电极反应
2
为IBr-+2e-===2I-+Br-,A项正确;放电时,正极区IBr-转化为Br-和I-,负极区Zn
2 2
转化为Zn2+,溶液中离子的数目增多,B项错误;充电时,b电极发生反应Zn2++2e-
===Zn,b电极增重0.65 g时,转移0.02 mol e-,根据各电极上转移电子数相同,则有0.02
mol I-被氧化,C项正确;放电时,a电极为正极,充电时,a电极为阳极,接外电源正极,
D项正确。
12.(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作
用,以CO 和HO为原料制备HCOOH和O 的原理示意图。
2 2 2
①电极b为______极。
②电极b上的电极反应为________________________________________________________。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图所示,
该电池从浓缩海水中提取LiCl的同时又获得了电能。
①X为________极,Y极的电极反应式为__________________________________________。
②Y极生成1 mol Cl 时,________ mol Li+移向______(填“X”或“Y”)极。
2
(3)微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如下:
①该电池中外电路电子的流动方向为______________(填“从A到B”或“从B到A”)。
②A电极附近甲醇发生的电极反应为________________________________________
________________________________________________________________________。
答案 (1)①正 ②CO+2e-+2H+===HCOOH
2
(2)①正 2Cl--2e-===Cl↑ ②2 X
2
(3)①从A到B ②CHOH+HO-6e-===6H++CO↑
3 2 2
解析 (1)从图示可以看出,右侧通入的CO 转变成HCOOH,C元素被还原,电极b为正极,
2
电极反应式为CO +2e-+2H+===HCOOH。(2)根据装置可知生成H 的电极为正极,生成
2 2
Cl 的电极为负极。(3)①甲醇失去电子,作为电池的负极,所以该电池外电路电子的流动方
2
向为从A到B。②CHOH失电子生成CO 和H+,根据化合价变化和元素守恒可得电极反应
3 2
式:CHOH+HO-6e-===6H++CO↑。
3 2 2
13.[2021·河北1月选考模拟,18(1)(2)(3)(4)(5)]我国科学家最近发明了一种Zn-PbO 电池,
2
电解质为KSO 、HSO 和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个电解
2 4 2 4
质溶液区域,结构示意图如下:
回答下列问题:
(1)电池中,Zn 为________极,B 区域的电解质为________(填“KSO ”“HSO ”或
2 4 2 4
“KOH”)。
(2)电池反应的离子方程式为________________________________________________
________________________________________________________________________。
(3)阳离子交换膜为图中的______膜(填“a”或“b”)。
(4)此电池中,消耗6.5 g Zn,理论上可产生的容量(电量)为________毫安(mAh)(1 mol电子的
电量为1F,F=96 500 C·mol-1,结果保留整数)。
(5)已知E为电池电动势(电池电动势即电池的理论电压,是两个电极电位之差,E=E -
(+)
E ),ΔG为电池反应的自由能变,则该电池与传统铅酸蓄电池相比较, ________
(-); ________ (填“>”或“<”)。
答案 (1)负 KSO
2 4
(2)PbO +SO+Zn+2HO===PbSO +Zn(OH) (3)a (4)5 361 (5)> <
2 2 4
解析 (1)锌是活泼金属,Zn电极为负极;由图示可知A区域电解质为KOH,C区域电解质
为HSO ,则在B区域电解质为KSO 。
2 4 2 4
(2)负极反应为Zn-2e-+4OH-===Zn(OH),正极反应为PbO +2e-+4H++SO===PbSO +
2 4
2HO,总反应离子方程式为PbO +SO+Zn+2HO===PbSO +Zn(OH)。
2 2 2 4
(3)A区域是KOH溶液,OH-发生反应变为Zn(OH),为了维持溶液呈电中性, K+应通过交
换膜进入B区域,因此a膜为阳离子交换膜。
(4) n(Zn)==0.1 mol,则转移的电子为0.2 mol,1 mol电子的电量为96 500 C,转移0.2 mol
电子的电量Q=0.2 mol×96 500 C·mol-1=19 300 C,则理论上可产生的电量为 mAh≈5
361 mAh。
(5)由于Zn比Pb活动性强,正极材料都是PbO ,所以Zn-PbO 的电势差比Pb-PbO 的电
2 2 2
势差大,则 ;不同电池的电势差越大,电池反应的自由能变就越小,所
以 。