文档内容
第 38 讲 化学平衡状态 化学平衡的移动
复习目标 1.会用复合判据判断反应进行的方向。2.了解化学反应的可逆性及化学平衡的
建立。3.掌握化学平衡的特征。4.理解外界条件(浓度、温度、压强、催化剂等)对化学平衡
的影响,能用相关理论解释其一般规律。5.了解化学平衡的调控在生活、生产和科学研究领
域中的重要作用。
考点一 化学反应的方向
1.自发反应
在一定条件下无需外界帮助就能自发进行的反应称为自发反应。
2.熵和熵变的含义
(1)熵的含义
度量体系混乱程度的物理量,符号为S。熵值越大,体系混乱度越大。同一条件下,不同物
质有不同的熵值,同一物质在不同状态下熵值也不同,一般规律是S(g)>S(l)>S(s)。
(2)熵变的含义
ΔS=S(生成物)-S(反应物)。化学反应的ΔS越大,越有利于反应自发进行。
3.判断化学反应方向的判据
ΔG=ΔH-TΔS
ΔG<0时,反应能自发进行;
ΔG=0时,反应处于平衡状态;
ΔG>0时,反应不能自发进行。
1.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向( )
2.能自发进行的反应一定能迅速发生( )
3.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为判断反应能否
自发进行的判据( )
答案 1.× 2.× 3.×
1.下列有关说法不正确的是________(填字母)。
A.C H(g)+NH (g)+O(g)===C HN(g)+3HO(g) ΔH=-515 kJ·mol-1和 C H(g)+
3 6 3 2 3 3 2 3 6O(g)===C HO(g)+HO(g) ΔH=-353 kJ·mol-1两个反应在热力学上趋势均很大
2 3 4 2
B.Na与HO的反应是熵增的放热反应,该反应能自发进行
2
C.某吸热反应能自发进行,因此该反应是熵增反应
D.2NO(g)+2CO(g)===N(g)+2CO(g)在常温下能自发进行,则该反应的ΔH>0
2 2
E.反应SiO(s)+2C(s)===Si(s)+2CO(g)只能在高温下自发进行,则该反应的ΔH>0
2
F.反应BaSO(s)+4C(s)===BaS(s)+4CO(g)在室温下不能自发进行,说明该反应的ΔH>0
4
G.一定温度下,反应MgCl (l)===Mg(l)+Cl(g)的ΔH>0,ΔS>0
2 2
答案 D
2.已知在100 kPa、298.15 K时,石灰石发生分解反应:
CaCO (s)===CaO(s)+CO(g) ΔH=+178.3 kJ·mol-1 ΔS=+160.4 J·mol-1·K-1,则
3 2
(1)该反应____(填“能”或“不能”)正向自发进行。
(2)若温度能决定反应方向,则该反应正向自发进行的最低温度为________。
答案 (1)不能 (2)1 111.6 K
解析 (1)ΔG=ΔH-TΔS=178.3 kJ·mol-1-298.15 K×160.4×10-3 kJ·mol-1·K-1≈130.5 kJ·
mol-1>0,所以该反应不能正向自发进行。
(2)根据ΔG=ΔH-TΔS<0时,反应可正向自发进行,则有T>≈1 111.6 K。
考点二 可逆反应与化学平衡建立
1.可逆反应
2.化学平衡状态
(1)概念
一定条件下的可逆反应中,当正反应和逆反应速率相等时,反应物和生成物的浓度均保持不
变,即体系的组成不随时间而改变的状态。
(2)建立(3)平衡特点
3.判断化学平衡状态的两种方法
(1)动态标志:v正 =v逆 ≠0
①同种物质:同一物质的生成速率等于消耗速率。
②不同物质:必须标明是“异向”的反应速率关系。如aA+bBcC+dD,=时,反应达
到平衡状态。
(2)静态标志:“变量”不变
在未达到平衡时不断变化、在达到平衡时不再发生变化的各种物理量(如各物质的质量、物
质的量或浓度、百分含量、压强、密度或颜色等),如果不再发生变化,即达到平衡状态。
可简单总结为“正逆相等,变量不变”。
1.反应2NaHCO =====NaCO +CO↑+HO、NaCO +CO +HO===2NaHCO 互为可逆
3 2 3 2 2 2 3 2 2 3
反应( )
2.化学反应达到平衡后,反应物和生成物的浓度或百分含量相等( )
3.在1 L的密闭容器中发生反应:2NO(g)+O(g)2NO (g),当容器中气体的颜色保持不
2 2
变时,说明反应已达到平衡状态( )
4.对于反应H(g)+I(g)2HI(g),当压强不变时,反应达到平衡状态( )
2 2
5.恒温恒容下进行的可逆反应:2SO (g)+O(g)2SO (g),当SO 的生成速率与SO 的消
2 2 3 3 2
耗速率相等时,反应达到平衡状态( )
6.在一定条件下,向密闭容器中充入1 mol N 和3 mol H 充分反应,生成2 mol NH ( )
2 2 3
答案 1.× 2.× 3.√ 4.× 5.× 6.×1.在密闭容器中进行反应:X(g)+Y(g)2Z(g),已知X 、Y 、Z的起始浓度分别为 0.1
2 2 2 2
mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可
能是( )
A.Z为0.3 mol·L-1
B.Y 为0.4 mol·L-1
2
C.X 为0.2 mol·L-1
2
D.Z为0.4 mol·L-1
答案 A
2.在一定温度下的恒容容器中,当下列物理量不再发生变化时:①混合气体的压强;②混
合气体的密度;③混合气体的总物质的量;④混合气体的平均相对分子质量;⑤混合气体的
颜色;⑥各反应物或生成物的浓度之比等于化学计量数之比;⑦某种气体的百分含量
(1)能说明2SO (g)+O(g)2SO (g)达到平衡状态的是______________(填序号,下同)。
2 2 3
(2)能说明I(g)+H(g)2HI(g)达到平衡状态的是______________。
2 2
(3)能说明2NO (g)NO(g)达到平衡状态的是________________________。
2 2 4
(4)能说明C(s)+CO(g)2CO(g)达到平衡状态的是______________。
2
(5)能说明NH COONH(s)2NH (g)+CO(g)达到平衡状态的是______________。
2 4 3 2
(6)能说明5CO(g)+IO(s)5CO(g)+I(s)达到平衡状态的是______________。
2 5 2 2
答案 (1)①③④⑦ (2)⑤⑦ (3)①③④⑤⑦ (4)①②③④⑦ (5)①②③ (6)②④⑦
3.若上述题目中的(1)~(4)改成一定温度下的恒压密闭容器,结果又如何?
(1)__________________。(2)_______________________________________________。
(3)__________________。(4)_______________________________________________。
答案 (1)②③④⑦ (2)⑤⑦ (3)②③④⑤⑦ (4)②③④⑦
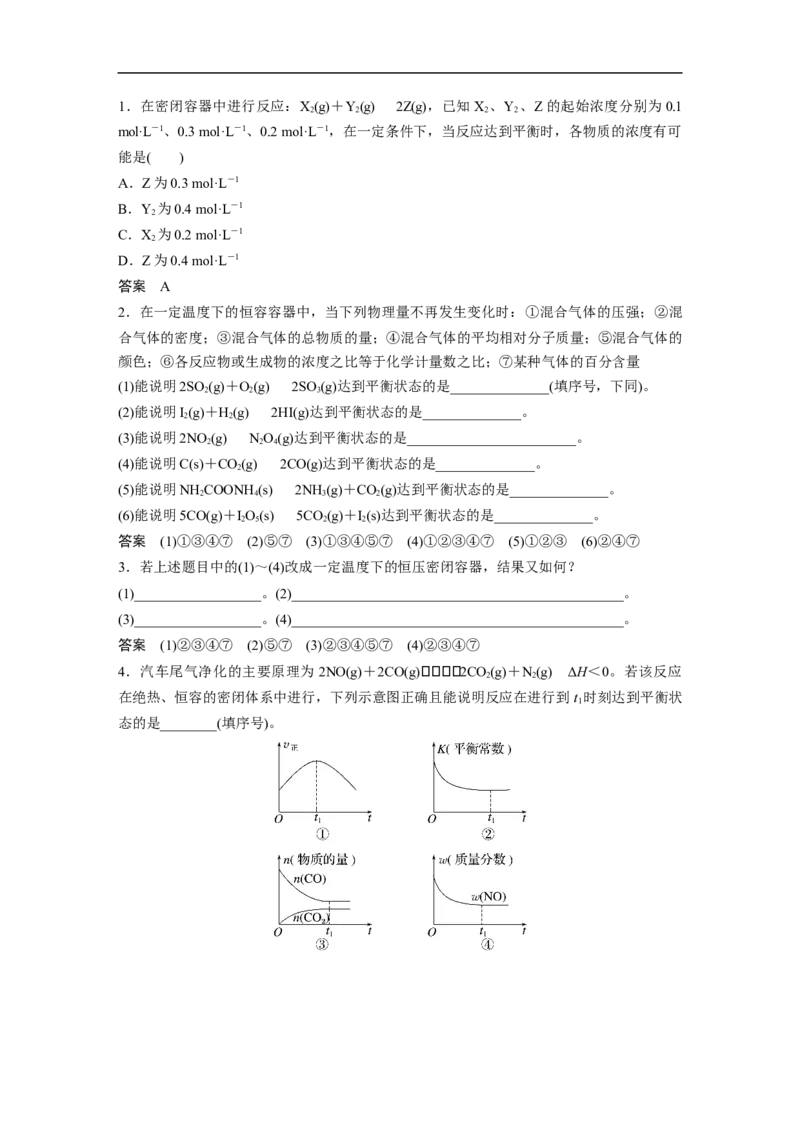
4.汽车尾气净化的主要原理为 2NO(g)+2CO(g)2CO(g)+N(g) ΔH<0。若该反应
2 2
在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到 t 时刻达到平衡状
1
态的是________(填序号)。答案 ②④⑤
解析 ①达到平衡时,v 应保持不变;②由于是放热反应,又是绝热容器,体系温度升高,
正
平衡左移,K减小,当K不变时,温度不变,达到平衡状态;③图中达到平衡时,CO、CO
2
的改变量不是1∶1;④w(NO)逐渐减小,达到平衡时保持不变;⑤因正反应放热,容器绝
热,故反应开始后体系温度升高,达到平衡状态时,体系温度不再发生变化;⑥ΔH是一个
定值,不能用于判断可逆反应是否达到平衡状态。
规避“2”个易失分点
(1)化学平衡状态判断“三关注”
关注反应条件,是恒温恒容、恒温恒压,还是绝热恒容容器;关注反应特点,是等体积反应,
还是非等体积反应;关注特殊情况,是否有固体参加或生成,或固体的分解反应。
(2)不能作为化学平衡状态“标志”的四种情况
①反应组分的物质的量之比等于化学方程式中相应物质的化学计量数之比。
②恒温恒容下的体积不变的反应,体系的压强或总物质的量不再随时间而变化,如
2HI(g)H(g)+I(g)。
2 2
③全是气体参加的体积不变的反应,体系的平均相对分子质量不再随时间而变化,如
2HI(g)H(g)+I(g)。
2 2
④全是气体参加的反应,恒容条件下体系的密度保持不变。
考点三 化学平衡的移动
1.概念
在一定条件下,当可逆反应达到平衡状态以后,若反应条件(如温度、压强、浓度等)发生了
变化,平衡混合物中各组分的浓度也会随之改变,从而在一段时间后达到新的平衡状态。这
种由原平衡状态向新平衡状态的变化过程,叫做化学平衡的移动。2.化学平衡移动的过程
3.化学平衡移动与化学反应速率的关系
(1)v正 >v逆 :平衡向正反应方向移动。
(2)v正 =v逆 :反应达到平衡状态,平衡不发生移动。
(3)v正 <v逆 :平衡向逆反应方向移动。
4.影响化学平衡的外界因素
若其他条件不变,改变下列条件对化学平衡的影响如下:
改变的条件(其他条件不变) 化学平衡移动的方向
增大反应物浓度或减小生成物浓度 向正反应方向移动
浓度
减小反应物浓度或增大生成物浓度 向逆反应方向移动
增大压强 向气体分子总数减小的方向移动
压强(对于 反应前后气体
有气体参 体积改变
减小压强 向气体分子总数增大的方向移动
加的可逆
反应前后气体
反应) 改变压强 平衡不移动
体积不变
升高温度 向吸热反应方向移动
温度
降低温度 向放热反应方向移动
催化剂 同等程度地改变v正 、v逆 ,平衡不移动
5.化学平衡中的特殊情况
(1)当反应混合物中存在与其他物质不相混溶的固体或液体物质时,由于其“浓度”是恒定
的,不随其量的增减而变化,故改变这些固体或液体的量,对化学平衡没影响。
(2)同等程度地改变反应混合物中各物质的浓度时,应视为压强的影响。
(3)充入惰性气体与平衡移动的关系
①恒温、恒容条件
原平衡体系―――――→体系总压强增大―→体系中各组分的浓度不变―→平衡不移动
②恒温、恒压条件
原平衡体系―――――→容器容积增大,各反应气体的分压减小―→体系中各组分的浓度同倍数
减小(等效于减压)6.勒夏特列原理及应用
1.升高温度,平衡向吸热反应方向移动,此时v 减小,v 增大( )
放 吸
2.化学平衡正向移动,反应物的转化率一定增大( )
3.向平衡体系FeCl +3KSCNFe(SCN) +3KCl中加入适量KCl固体,平衡逆向移动,溶
3 3
液的颜色变浅( )
4.对于2NO (g)NO(g)的平衡体系,压缩体积,增大压强,平衡正向移动,混合气体的
2 2 4
颜色变浅( )
5.C(s)+CO(g)2CO(g) ΔH>0,其他条件不变时,升高温度,反应速率 v(CO)和CO
2 2 2
的平衡转化率均增大( )
6.只要v 增大,平衡一定正向移动( )
正
答案 1.× 2.× 3.× 4.× 5.√ 6.×
一、化学平衡移动原理的理解
1.对于一定条件下的可逆反应
甲:A(g)+B(g)C(g) ΔH<0
乙:A(s)+B(g)C(g) ΔH<0
丙:A(g)+B(g)2C(g) ΔH>0
达到化学平衡后,只改变一种条件,按要求回答下列问题:
(1)升温,平衡移动的方向分别为甲____________(填“向左”“向右”或“不移动”,下同);
乙________;丙________。此时反应体系的温度均比原来____(填“高”或“低”)。混合气
体的平均相对分子质量变化分别为甲________(填“增大”“减小”或“不变”,下同);乙
________;丙________。
答案 向左 向左 向右 高 减小 减小 不变
(2)加压,使体系体积缩小为原来的
①平衡移动的方向分别为甲________(填“向左”“向右”或“不移动”,下同);乙
________;丙______________________________________________________。
②设压缩之前压强分别为p 、p 、p ,压缩后压强分别为p′ 、p′ 、p′ ,则p 与
甲 乙 丙 甲 乙 丙 甲
p′ ,p 与p′ ,p 与p′ 的关系分别为
甲 乙 乙 丙 丙甲________;乙________;丙________。
③混合气体的平均相对分子质量变化分别为甲________(填“增大”“减小”或“不变”,
下同);乙________;丙________。
答案 ①向右 不移动 不移动 ②p <p ′<2p p ′=2p p ′=2p ③增大
甲 甲 甲 乙 乙 丙 丙
不变 不变
二、调控化学反应的应用
2.在压强为0.1 MPa、温度为300 ℃条件下,a mol CO与3a mol H 的混合气体在催化剂
2
作用下发生反应生成甲醇:CO(g)+2H(g)CHOH(g) ΔH<0。
2 3
(1)平衡后将容器的容积压缩到原来的一半,其他条件不变,对平衡体系产生的影响是
__________(填字母,下同)。
A.c(H )减小
2
B.正反应速率加快,逆反应速率减慢
C.反应物转化率增大
D.重新平衡时减小
(2)若容器容积不变,下列措施可增大甲醇产率的是________。
A.升高温度
B.将CHOH从体系中分离
3
C.充入He,使体系总压强增大
(3)达到平衡后,为提高H 的转化率和该反应的速率,可采取的措施是________(填序号)。
2
①加催化剂同时升高温度 ②加催化剂同时增大压强 ③升高温度同时充入N ④降低温
2
度同时增大压强 ⑤增大CO的浓度
答案 (1)CD (2)B (3)②⑤
解析 (1)该反应为正向气体分子数减小的可逆反应,缩小容器体积,平衡正向移动,c(H )
2
增大,正、逆反应速率均增大,因而A、B均不正确。(2)由于该反应正向是放热反应,升高
温度平衡逆向移动,CHOH的产率降低;容器容积不变,充入He,平衡不移动。
3
1.(2021·辽宁1月适应性测试,7)某温度下,在一恒容密闭容器中进行如下两个反应并达到
平衡:
①2X(g)+Y(g)Z(s)+2Q(g) ΔH<0
1
②M(g)+N(g)R(g)+Q(g) ΔH>0
2
下列叙述错误的是( )
A.加入适量Z,①和②平衡均不移动
B.通入稀有气体Ar,①平衡正向移动C.降温时无法判断Q浓度的增减
D.通入Y,则N的浓度增大
答案 B
解析 Z为固体,加入适量Z不影响反应①的平衡移动,而反应②与Z无关,故加入Z也不
影响反应②的平衡移动,A正确;通入稀有气体Ar,由于容器体积不变,故气体浓度不发
生改变,反应①的平衡不移动,B错误;温度降低,反应①正向进行,反应②逆向进行,但
两个反应中反应物的起始浓度未知,故无法判断Q浓度的增减,C正确;通入气体Y,反应
①平衡正向移动,Q的浓度增大,导致反应②平衡逆向移动,则N的浓度增大,D正确。
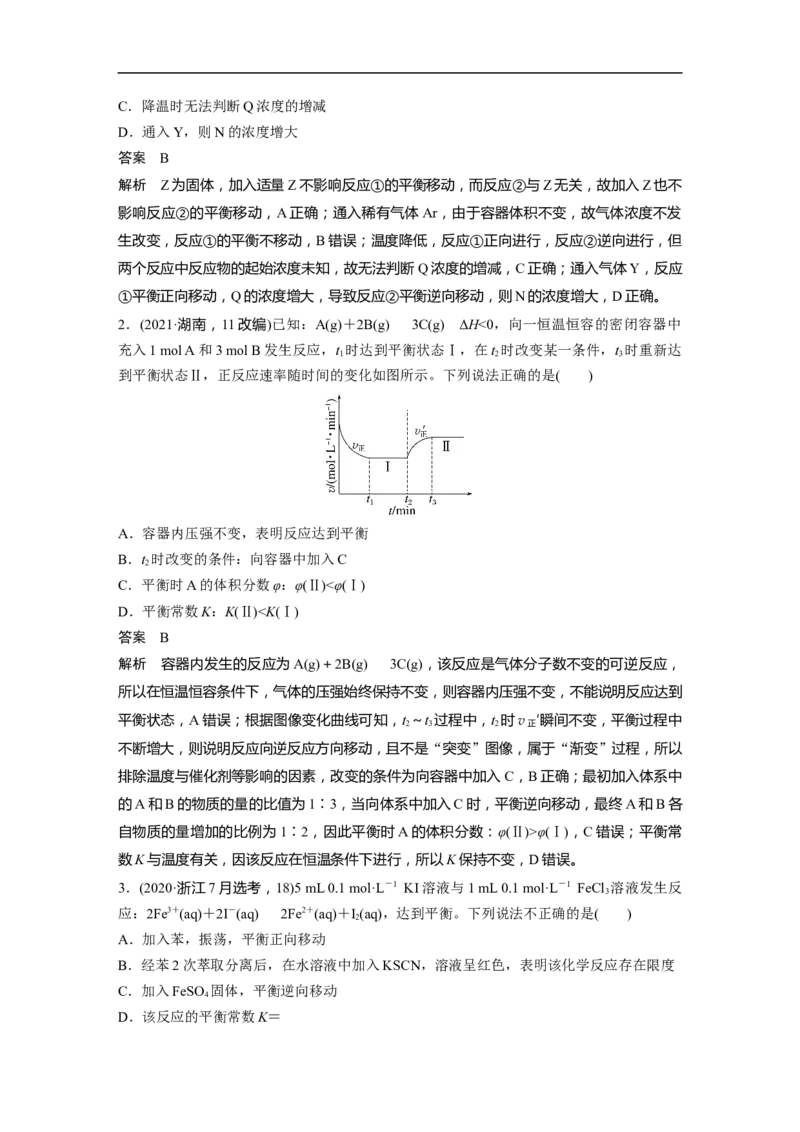
2.(2021·湖南,11改编)已知:A(g)+2B(g)3C(g) ΔH<0,向一恒温恒容的密闭容器中
充入1 mol A和3 mol B发生反应,t 时达到平衡状态Ⅰ,在t 时改变某一条件,t 时重新达
1 2 3
到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是( )
A.容器内压强不变,表明反应达到平衡
B.t 时改变的条件:向容器中加入C
2
C.平衡时A的体积分数φ:φ(Ⅱ)<φ(Ⅰ)
D.平衡常数K:K(Ⅱ)φ(Ⅰ),C错误;平衡常
数K与温度有关,因该反应在恒温条件下进行,所以K保持不变,D错误。
3.(2020·浙江7月选考,18)5 mL 0.1 mol·L-1 KI溶液与1 mL 0.1 mol·L-1 FeCl 溶液发生反
3
应:2Fe3+(aq)+2I-(aq)2Fe2+(aq)+I(aq),达到平衡。下列说法不正确的是( )
2
A.加入苯,振荡,平衡正向移动
B.经苯2次萃取分离后,在水溶液中加入KSCN,溶液呈红色,表明该化学反应存在限度
C.加入FeSO 固体,平衡逆向移动
4
D.该反应的平衡常数K=答案 D
解析 加入苯,振荡,苯萃取了I ,水溶液中的c(I)减小,平衡正向移动,A正确;反应开
2 2
始时n(KI)>n(FeCl ),反应中KI过量,经苯两次萃取分离后,水溶液中 c(I)很小,加入
3 2
KSCN,溶液呈红色,说明水溶液中仍含有Fe3+,证明该反应是可逆反应,存在一定限度,
B正确;加入FeSO 固体,c(Fe2+)增大,平衡逆向移动,C正确;该反应在溶液中进行,平
4
衡常数K=,D错误。
4.(2020·浙江7月选考,20)一定条件下:2NO (g)NO(g) ΔH<0。在测定NO 的相对
2 2 4 2
分子质量时,下列条件中,测定结果误差最小的是( )
A.温度0 ℃、压强50 kPa
B.温度130 ℃、压强300 kPa
C.温度25 ℃、压强100 kPa
D.温度130 ℃、压强50 kPa
答案 D
解析 测定NO 的相对分子质量时,要使平衡逆向移动,且逆向移动的程度越大,测定结
2
果的误差越小。该反应的正反应是气体分子数减少的放热反应,因此温度越高、压强越小时,
平衡逆向移动的程度越大,故选D。
5.[2021·湖南,16(1)(2)]氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,
可通过下面两种方法由氨气得到氢气。
方法Ⅰ.氨热分解法制氢气
相关化学键的键能数据
化学键 N≡N H—H N—H
键能E/(kJ·mol-1) 946 436.0 390.8
在一定温度下,利用催化剂将NH 分解为N 和H。回答下列问题:
3 2 2
(1)反应2NH (g)N(g)+3H(g) ΔH=________ kJ·mol-1。
3 2 2
(2)已知该反应的 ΔS=198.9 J·mol-1·K-1,在下列哪些温度下反应能自发进行?
______________(填字母)。
A.25 ℃ B.125 ℃ C.225 ℃ D.325 ℃
答案 (1)+90.8 (2)CD
解析 (1) 根据反应热=反应物的总键能-生成物的总键能,2NH (g)N(g)+3H(g) ΔH
3 2 2
=390.8 kJ·mol-1×3×2-(946 kJ·mol-1+436.0 kJ·mol-1×3)=+90.8 kJ·mol-1。
(2)若反应自发进行,则需ΔH-TΔS<0,T>=≈456.5 K,即温度应高于(456.5-273)℃=
183.5 ℃。
6.[2017·全国卷Ⅲ,28(4)]298 K时,将20 mL 3x mol·L-1 Na AsO 、20 mL 3x mol·L-1 I
3 3 2
和20 mL NaOH溶液混合,发生反应:AsO(aq)+I(aq)+2OH-(aq)AsO(aq)+2I-(aq)+
2
HO(l)。溶液中c(AsO)与反应时间(t)的关系如图所示。
2①下列可判断反应达到平衡的是______(填字母)。
a.溶液的pH不再变化
b.v(I-)=2v(AsO)
c.c(AsO)/c(AsO)不再变化
d.c(I-)=y mol·L-1
②t
m
时,v正 ______v逆 (填“大于”“小于”或“等于”)。
③t
m
时v逆 ________t
n
时v逆 (填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K为________。
答案 ①ac ②大于 ③小于 t 时生成物浓度较低 ④
m
课时精练
1.已知①碳酸钙的分解CaCO (s)===CaO(s)+CO(g) ΔH 仅在高温下自发进行;②氯酸钾
3 2 1
的分解2KClO(s)===2KCl(s)+3O(g) ΔH 在任何温度下都自发进行,下面有几组焓变数据,
3 2 2
其中可能正确的是( )
A.ΔH=-178.32 kJ·mol-1 ΔH=-78.3 kJ·mol-1
1 2
B.ΔH=+178.32 kJ·mol-1 ΔH=-78.3 kJ·mol-1
1 2
C.ΔH=-178.32 kJ·mol-1 ΔH=+78.3 kJ·mol-1
1 2
D.ΔH=+178.32 kJ·mol-1 ΔH=+78.3 kJ·mol-1
1 2
答案 B
2.一定条件下,对于可逆反应X(g)+3Y(g)2Z(g),若X、Y、Z的起始浓度分别为c 、
1
c 、c(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.08
2 3
mol·L-1,则下列判断正确的是( )
A.c∶c=3∶1
1 2
B.平衡时,Y和Z的生成速率之比为2∶3
C.X、Y的转化率不相等
D.c 的取值范围为0<c<0.14 mol·L-1
1 1
答案 D
解析 平衡浓度之比为1∶3,转化浓度之比亦为1∶3,故c∶c =1∶3,A、C不正确;平
1 2
衡时Y生成表示逆反应速率,Z生成表示正反应速率且v (Y)∶v (Z)=3∶2,B不正确;
生成 生成由可逆反应的特点可知0<c<0.14 mol·L-1,D正确。
1
3.反应NH HS(s)NH (g)+HS(g)在某温度下达到平衡,下列各种情况不会使平衡发生移
4 3 2
动的是( )
A.温度、容积不变时,通入SO 气体
2
B.移走一部分NH HS固体
4
C.容器体积不变,充入HCl气体
D.保持压强不变,充入氮气
答案 B
解析 A项,2HS+SO ===3S+2HO,通入SO 气体使反应正向移动;B项,增减固体的
2 2 2 2
量不影响平衡;C项,NH (g)+HCl(g)===NH Cl(s),充入HCl气体使反应正向移动;D项,
3 4
保持压强不变,充入氮气,平衡向正反应方向移动。
4.在一定温度下,向2 L固定容积的密闭容器中通入1 mol CO 、3 mol H ,发生反应:
2 2
CO(g)+3H(g)CHOH(g)+HO(g) ΔH<0。能说明该反应已达到平衡状态的是( )
2 2 3 2
A.混合气体的平均相对分子质量不变
B.体系中=,且保持不变
C.混合气体的密度不随时间变化
D.单位时间内有n mol H—H断裂,同时有n mol O—H生成
答案 A
5.下列事实不能用勒夏特列原理解释的是( )
A.溴水中有下列平衡:Br +HOHBr+HBrO,当加入少量AgNO 溶液后,溶液的颜色
2 2 3
变浅
B.对于反应:2HI(g)H(g)+I(g),缩小容器的容积可使平衡体系的颜色变深
2 2
C.反应:CO(g)+NO (g)CO(g)+NO(g) ΔH<0,升高温度可使平衡向逆反应方向移动
2 2
D.对于合成NH 的反应,为提高NH 的产率,理论上应采取低温措施
3 3
答案 B
解析 加入少量AgNO 溶液,HBr与AgNO 反应生成AgBr沉淀,c(HBr)减小,平衡正向移
3 3
动,溶液的颜色变浅,A可以用勒夏特列原理解释;2HI(g)H(g)+I(g)是反应前后气体
2 2
分子总数不变的反应,缩小容器的容积,压强增大,平衡不移动,但c(I)增大,导致平衡体
2
系的颜色变深,故B不能用勒夏特列原理解释;反应 CO(g)+NO (g)CO(g)+NO(g)的
2 2
ΔH<0,升高温度,平衡逆向移动,C可以用勒夏特列原理解释;合成氨的反应是放热反应,
降低温度,平衡正向移动,有利于生成NH ,D可以用勒夏特列原理解释。
3
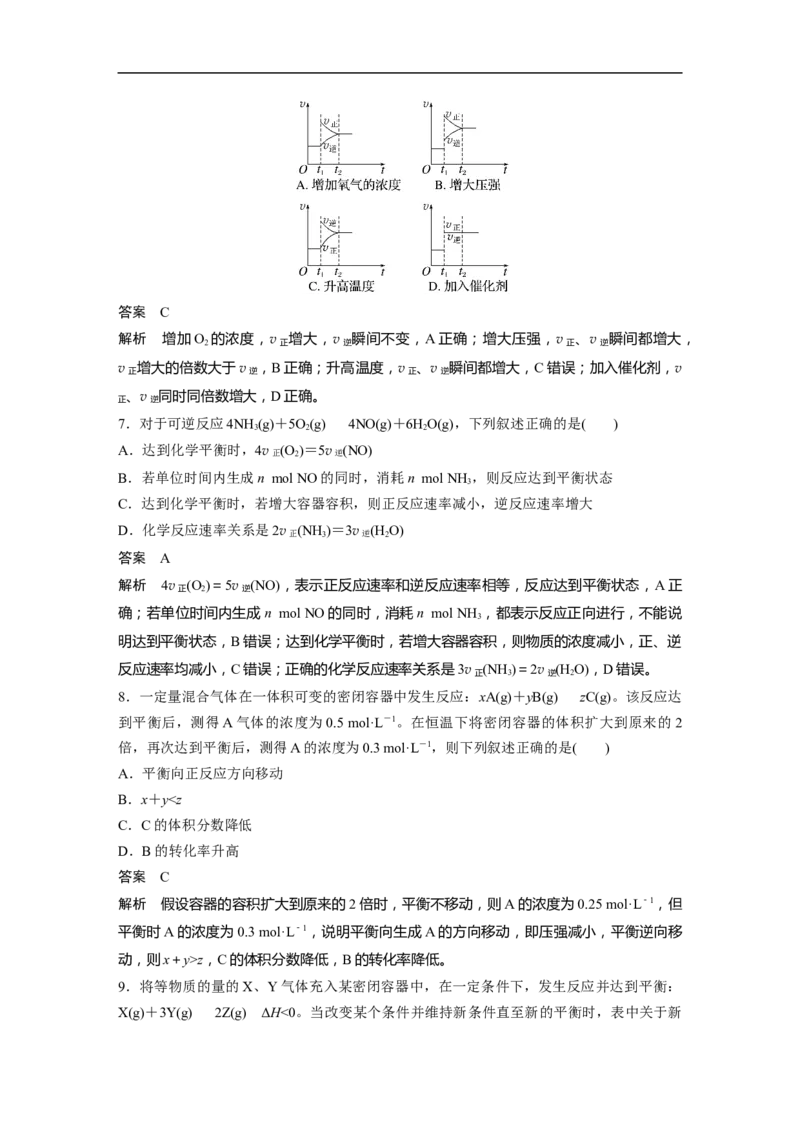
6.反应2SO (g)+O(g)2SO (g) ΔH<0已达平衡,如果其他条件不变时,分别改变下列
2 2 3
条件,对化学反应速率和化学平衡产生影响,下列条件与图像不相符的是(O~t
1
:v正 =v逆 ;
t 时改变条件,t 时重新建立平衡)( )
1 2答案 C
解析 增加O 的浓度,v 增大,v 瞬间不变,A正确;增大压强,v 、v 瞬间都增大,
2 正 逆 正 逆
v 增大的倍数大于v ,B正确;升高温度,v 、v 瞬间都增大,C错误;加入催化剂,v
正 逆 正 逆
、v 同时同倍数增大,D正确。
正 逆
7.对于可逆反应4NH (g)+5O(g)4NO(g)+6HO(g),下列叙述正确的是( )
3 2 2
A.达到化学平衡时,4v正 (O
2
)=5v逆 (NO)
B.若单位时间内生成n mol NO的同时,消耗n mol NH ,则反应达到平衡状态
3
C.达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是2v正 (NH
3
)=3v逆 (H
2
O)
答案 A
解析 4v (O )=5v (NO),表示正反应速率和逆反应速率相等,反应达到平衡状态,A正
正 2 逆
确;若单位时间内生成n mol NO的同时,消耗n mol NH ,都表示反应正向进行,不能说
3
明达到平衡状态,B错误;达到化学平衡时,若增大容器容积,则物质的浓度减小,正、逆
反应速率均减小,C错误;正确的化学反应速率关系是3v (NH )=2v (H O),D错误。
正 3 逆 2
8.一定量混合气体在一体积可变的密闭容器中发生反应:xA(g)+yB(g)zC(g)。该反应达
到平衡后,测得A气体的浓度为0.5 mol·L-1。在恒温下将密闭容器的体积扩大到原来的2
倍,再次达到平衡后,测得A的浓度为0.3 mol·L-1,则下列叙述正确的是( )
A.平衡向正反应方向移动
B.x+yz,C的体积分数降低,B的转化率降低。
9.将等物质的量的X、Y气体充入某密闭容器中,在一定条件下,发生反应并达到平衡:
X(g)+3Y(g)2Z(g) ΔH<0。当改变某个条件并维持新条件直至新的平衡时,表中关于新平衡与原平衡的比较正确的是( )
选项 改变条件 新平衡与原平衡比较
A 升高温度 X的转化率变小
B 增大压强 X的浓度变小
C 充入一定量Y Y的转化率增大
D 使用适当的催化剂 X的体积分数变小
答案 A
解析 升高温度,平衡逆向移动,X的转化率变小,A项正确;增大压强,平衡正向移动,
但容器的体积减小,X的浓度变大,B项错误;充入一定量Y,X的转化率增大,而Y的转
化率减小,C项错误;使用适当的催化剂,只能加快反应速率,不能改变平衡,X的体积分
数不变,D项错误。
10.在容积一定的密闭容器中发生可逆反应A(g)+B(g)C(g) ΔH>0,平衡移动关系如
图所示。下列说法正确的是( )
选项 压强 纵坐标
A p<p C的物质的量浓度
1 2
B p>p B的转化率
1 2
C p<p 混合气体的平均摩尔质量
1 2
D p>p A的质量分数
1 2
答案 B
解析 p <p ,压强增大,平衡正向移动,C的物质的量浓度增大,故A选项错误;p >
1 2 1
p ,随压强的增大,平衡正向移动,B的转化率增大,故B选项正确;p <p ,压强增大,
2 1 2
平衡正向移动,混合气体平均摩尔质量增大,故 C选项错误;p >p ,随压强的增大,平衡
1 2
正向移动,A的质量分数减小,故D选项错误。
11.下列关于可逆反应A(?)+2B(s)C(g) ΔH<0,叙述正确的是( )
A.当反应达到平衡之后,气体摩尔质量不变,则反应达到平衡状态
B.平衡后,恒温下扩大容器体积,再次平衡后气体密度一定减小
C.平衡后,恒容下降低温度,再次平衡后气体中C的体积分数可能减小
D.平衡后,恒温恒容下,通入气体C,气体C的浓度可能不变
答案 D解析 若A不是气体,气体摩尔质量一直不变,不能判断是否是平衡状态,故A错误;若
A不是气体,温度不变,平衡常数不变,气体 C的浓度不变,密度也不变,若A是气体,
气体化学计量数相等,平衡不移动,密度减小,故B错误;若A不是气体,C的体积分数
可能一直是100%,若A是气体,降低温度,平衡正向移动,C的体积分数增加,故C错误;
若A不是气体,恒温恒容下,平衡常数不变,气体C的浓度不变,故D正确。
12.已知某密闭容器中发生反应:X(g)+Y(g)mZ(g) ΔH<0。反应过程中,X、Y、Z的
物质的量随时间的变化如图所示,则t 时刻改变的条件可能是( )
1
A.升高温度 B.加入更高效的催化剂
C.增大压强 D.加入一定量的Z
答案 A
解析 正反应是放热反应,升高温度,平衡向逆反应方向移动,Z的物质的量减少,X或Y
的物质的量增大,符合图像,A正确;使用催化剂不影响化学平衡的移动,不符合图像,B
错误;由题图知,反应达到平衡时,Δn(X或Y)=a mol,Δn(Z)=2a mol,即m=2,反应
前后气体物质的化学计量数之和相等,增大压强,化学平衡不移动,不符合图像,C错误;
加入一定量的Z,t 时,Z的物质的量应增大,不符合图像,D错误。
1
13.某实验小组研究温度对化学反应H(g)+I(g)2HI(g)的影响,在其他条件相同时,将
2 2
1 mol H (g)和1 mol I (g)充入体积为2 L的恒容密闭容器中,测得HI(g)的物质的量分数随时
2 2
间(min)变化的实验数据如下:
时间 0 20 40 60 80 100
HI(g)的物 T 0 0.50 0.68 0.76 0.80 0.80
1
质的量分数 T 0 0.60 0.72 0.75 0.75 0.75
2
下列说法正确的是( )
A.T 温度下,0~20 min内,H 的平均反应速率为0.012 5 mol·L-1·min-1
1 2
B.在T 温度下,该反应有可能在70 min时已达到平衡状态
1
C.由表中数据推测,T>T
1 2
D.由表中数据可知,温度越高,H(g)与I(g)的反应限度越大
2 2
答案 A
解析 T 温度下,0~20 min内,HI的物质的量分数为0.50,反应前后气体的物质的量不变,
1
则说明生成1 mol HI,消耗了0.5 mol氢气,H 的平均反应速率为=0.012 5 mol·
2
L-1·min-1,选项A正确;由表中数据分析可知,在T 温度下,该反应在70 min时没有达到
1平衡状态,选项B错误;T 温度下,反应更快达到平衡,其他条件不变的情况下,这是受
2
温度影响,从而可推断T>T ,选项C错误;T>T ,温度越大H(g)与I(g)的反应限度越小,
2 1 2 1 2 2
选项D错误。
14.燃煤会产生CO、CO、SO 等大气污染物。燃煤脱硫的相关反应的热化学方程式如下:
2 2
Ⅰ.CaSO (s)+CO(g)CaO(s)+SO (g)+CO(g) ΔH=+281.4 kJ·mol-1
4 2 2 1
Ⅱ.CaSO(s)+CO(g)CaS(s)+CO(g) ΔH=-43.6 kJ·mol-1
4 2 2
(1)一定温度下,向某恒容密闭容器中加入CaSO(s)和1 mol CO,若只发生反应Ⅰ,下列能
4
说明该反应已达到平衡状态的是______(填字母)。
a.容器内的压强不发生变化
b.v正 (CO)=v正 (CO
2
)
c.容器内气体的密度不发生变化
d.n(CO)+n(CO)=1 mol
2
(2)一定温度下,体积为1 L的容器中加入CaSO(s)和1 mol CO,若只发生反应Ⅱ,测得CO
4 2
的物质的量随时间变化如图中曲线A所示:
①在0~2 min内的平均反应速率v(CO)=______________________________________。
②曲线B表示过程与曲线A相比,改变的反应条件可能为________(答出一条即可)。
③若要提高反应体系中CO 的体积分数,可采取的措施为__________________________。
2
(3)一定温度下,向恒容密闭容器中加入CaSO(s)和1 mol CO,下列能说明反应Ⅰ和反应Ⅱ
4
同时发生的是________(填字母)。
a.反应后气体能使品红褪色
b.反应过程中,CO的体积分数逐渐减小
c.反应体系达到平衡之前,SO 和CO 两种气体的浓度之比随时间发生变化
2 2
d.体系压强逐渐增大
答案 (1)ac (2)①0.45 mol·L-1·min-1 ②加入催化剂(或增大压强) ③降低温度 (3)c
解析 (1)反应Ⅰ反应前后气体体积不相等,则容器内的压强不发生变化,可说明达到平衡
状态,故a正确;v (CO)、v (CO)都表示正反应速率,两者相等不能说明反应达到平衡状
正 正 2
态,故b错误;有固体参加反应,则容器内气体的密度不发生变化,可说明达到平衡状态,
故c正确;由碳原子守恒可知,始终有n(CO)+n(CO)=1 mol,不能说明反应达到平衡状态,
2
故d错误。
(2)①一定温度下,体积为1 L的容器中加入CaSO(s)和1 mol CO,若只发生反应Ⅱ,图中2
4
min时达到平衡状态,二氧化碳的物质的量为 0.9 mol,达到平衡状态消耗一氧化碳的物质的量为0.9 mol,在0~2 min内的平均反应速率v(CO)==0.45 mol·L-1·min-1。②曲线B表
示过程与曲线A相比,曲线斜率增大,反应速率增大,改变的反应条件可能为加入催化剂
或增大压强。③反应Ⅱ是体积不变的放热反应,若要提高反应体系中CO 的体积分数,需要
2
使平衡正向移动,降低温度反应正向进行。(3)反应后气体能使品红褪色,只能说明生成了
SO ,可能只发生反应Ⅰ,故a错误;CO的体积分数逐渐减小,也可能只发生反应Ⅰ,故b
2
错误;压强逐渐增大,说明气体物质的量增多,反应Ⅰ一定发生,不能确定反应Ⅱ是否发生,
故d错误。
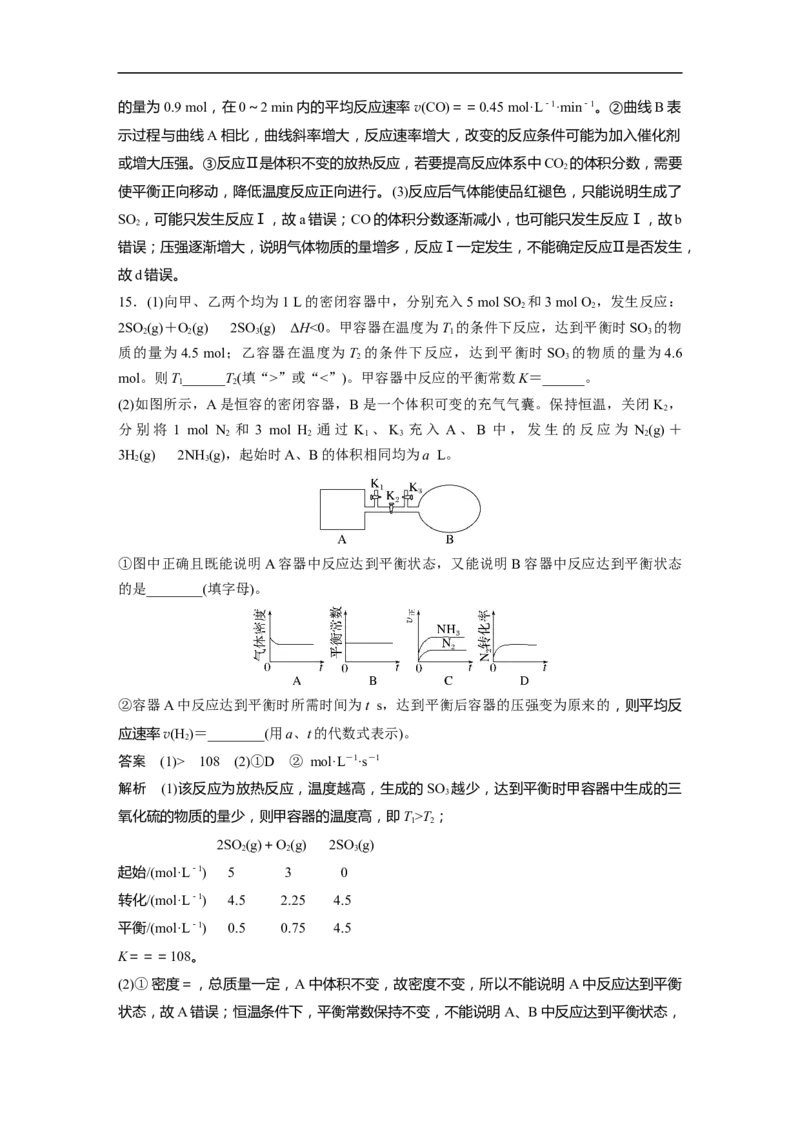
15.(1)向甲、乙两个均为1 L的密闭容器中,分别充入5 mol SO 和3 mol O ,发生反应:
2 2
2SO (g)+O(g)2SO (g) ΔH<0。甲容器在温度为T 的条件下反应,达到平衡时SO 的物
2 2 3 1 3
质的量为4.5 mol;乙容器在温度为T 的条件下反应,达到平衡时SO 的物质的量为4.6
2 3
mol。则T______T(填“>”或“<”)。甲容器中反应的平衡常数K=______。
1 2
(2)如图所示,A是恒容的密闭容器,B是一个体积可变的充气气囊。保持恒温,关闭 K ,
2
分别将 1 mol N 和 3 mol H 通过 K 、K 充入 A、B 中,发生的反应为 N(g)+
2 2 1 3 2
3H(g)2NH (g),起始时A、B的体积相同均为a L。
2 3
①图中正确且既能说明A容器中反应达到平衡状态,又能说明B容器中反应达到平衡状态
的是________(填字母)。
②容器A中反应达到平衡时所需时间为t s,达到平衡后容器的压强变为原来的,则平均反
应速率v(H )=________(用a、t的代数式表示)。
2
答案 (1)> 108 (2)①D ② mol·L-1·s-1
解析 (1)该反应为放热反应,温度越高,生成的SO 越少,达到平衡时甲容器中生成的三
3
氧化硫的物质的量少,则甲容器的温度高,即T>T;
1 2
2SO (g)+O(g)2SO (g)
2 2 3
起始/(mol·L-1) 5 3 0
转化/(mol·L-1) 4.5 2.25 4.5
平衡/(mol·L-1) 0.5 0.75 4.5
K===108。
(2)①密度=,总质量一定,A中体积不变,故密度不变,所以不能说明A中反应达到平衡
状态,故A错误;恒温条件下,平衡常数保持不变,不能说明A、B中反应达到平衡状态,故B错误;都是正反应速率,不能说明A、B中反应达到平衡状态,故C错误;N 的转化
2
率先增大,后保持不变,说明A、B中反应达到平衡状态,与图像相符,故D正确。
②根据反应:N(g)+3H(g)2NH (g)
2 2 3
起始/mol 1 3 0
转化/mol x 3x 2x
平衡/mol 1-x 3-3x 2x
达到平衡后容器的压强变为原来的,则=,
解得x=,v(H )== mol·L-1·s-1。
2