文档内容
第 53 讲 常见的烃 化石燃料的综合利用
复习目标 1.了解甲烷、乙烯、苯等有机化合物的主要性质及应用。2.了解煤、石油、天
然气的综合利用。3.了解常见高分子材料的合成及重要应用。
考点一 甲烷、乙烯、苯的结构与性质
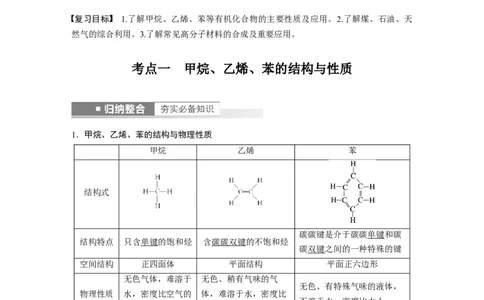
1.甲烷、乙烯、苯的结构与物理性质
甲烷 乙烯 苯
结构式
碳碳键是介于碳碳单键和碳
结构特点 只含单键的饱和烃 含碳碳双键的不饱和烃
碳双键之间的一种特殊的键
空间结构 正四面体 平面结构 平面正六边形
无色气体,难溶于 无色、稍有气味的气
无色、有特殊气味的液体,
物理性质 水,密度比空气的 体,难溶于水,密度比
不溶于水,密度比水小
小 空气的略小
2.甲烷、乙烯、苯的化学性质
在横线上填写化学方程式、物质或现象。3.烷烃
(1)结构与性质
通式 C H (链状烷烃,n≥1)
n 2n+2
链状(可带支链)分子中碳原子呈锯齿状排列;碳原子间以单键相连,其余
结构
价键均被氢原子饱和
一个碳原子与相邻四个原子构成四面体结构;1 mol C H 含共价键的数
n 2n+2
特点
目是 (3 n + 1) N
A
密度:随着分子中碳原子数的增加而增大,但都小于水的密度;
物理性质 熔、沸点:随分子中碳原子数的增加而升高;
状态:气态→液态→固态,碳原子数小于5的烷烃常温下呈气态
化学性质 取代反应;氧化反应(燃烧);分解反应(高温裂解)
(2)习惯命名法①当碳原子数n≤10时,用甲、乙、丙、丁、戊、己、庚、辛、壬、癸表示;当n>10时,
用汉字数字表示。
②当碳原子数n相同时,用正、异、新来区分。
如:CHCHCHCHCH 称为正戊烷,(CH)CHCH CH 称为异戊烷,C(CH) 称为新戊烷。
3 2 2 2 3 3 2 2 3 3 4
1.碳原子数小于5的烷烃常温下都为气体( )
2.正丁烷的四个碳原子在同一条直线上( )
3.1 mol CH 与1 mol Cl 在光照条件下反应,生成1 mol CH Cl气体( )
4 2 3
4.苯不能使酸性高锰酸钾溶液褪色,说明苯不能发生氧化反应( )
5.乙烯和苯都能使溴水褪色,褪色的原理相同( )
6.甲烷中混有乙烯气体,可通过酸性高锰酸钾溶液除去( )
答案 1.√ 2.× 3.× 4.× 5.× 6.×
一、几种重要烃的性质及应用
1.下列关于常见烃的认识正确的是( )
A.C H 与氯气发生取代反应、C H 与HCl发生加成反应均可得到纯净的C HCl
2 6 2 4 2 5
B.将甲烷和乙烯的混合气体通过盛有浓溴水的洗气瓶,即可提纯甲烷
C.乙烯结构中含有碳碳双键,苯中不含有碳碳双键,但两者均可以发生加成反应
D.甲烷和苯都是常见的燃料,燃烧时甲烷的火焰更明亮
答案 C
解析 C H 与氯气发生取代反应得到的取代产物不唯一,无法得到纯净的 C HCl,A项错
2 6 2 5
误;浓溴水易挥发,气体通过他时会带出溴蒸气,B项错误;苯环中的碳碳键是一种介于碳
碳单键和碳碳双键之间的独特的键,也能够发生加成反应,C项正确;苯是重要的有机溶剂,
含碳量高,燃烧时火焰比甲烷明亮,不易充分燃烧,一般不用作燃料,D项错误。
2.下列反应中前者属于取代反应,后者属于加成反应的是( )
A.甲烷与氯气混合后在光照条件下反应;乙烯使酸性高锰酸钾溶液褪色
B.乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷
C.将苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成;乙烯与水生成乙醇
D.在苯中滴入溴水,溴水褪色;乙烯自身生成聚乙烯的反应
答案 C
解析 A项,分别属于取代反应、氧化反应;B项,都属于加成反应;C项,分别属于取代
反应、加成反应;D项,分别属于物理变化(萃取)、加聚反应。
轻松突破加成反应、取代反应(1)加成反应的特点是:“断一,加二,都进来”。“断一”是指不饱和键中的一个不稳定
键断裂;“加二”是指加上两个其他原子或原子团,一定分别加在两个不饱和原子上,此反
应类似无机反应中的化合反应,理论上原子利用率为100%。
(2)取代反应的特点是“上一下一,有进有出”,类似无机反应中的复分解反应,注意在书
写化学方程式时,防止漏写产物中的小分子,如苯的硝化反应中生成的水。
二、重要烃的性质实验
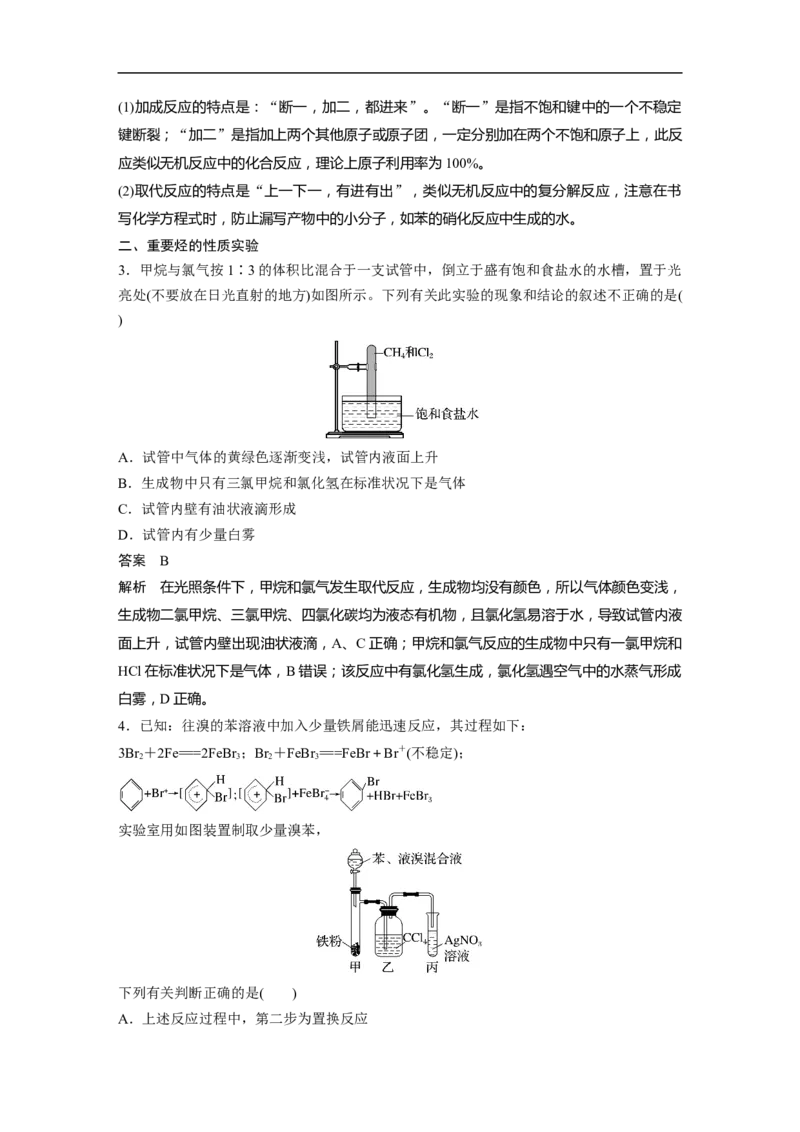
3.甲烷与氯气按1∶3的体积比混合于一支试管中,倒立于盛有饱和食盐水的水槽,置于光
亮处(不要放在日光直射的地方)如图所示。下列有关此实验的现象和结论的叙述不正确的是(
)
A.试管中气体的黄绿色逐渐变浅,试管内液面上升
B.生成物中只有三氯甲烷和氯化氢在标准状况下是气体
C.试管内壁有油状液滴形成
D.试管内有少量白雾
答案 B
解析 在光照条件下,甲烷和氯气发生取代反应,生成物均没有颜色,所以气体颜色变浅,
生成物二氯甲烷、三氯甲烷、四氯化碳均为液态有机物,且氯化氢易溶于水,导致试管内液
面上升,试管内壁出现油状液滴,A、C正确;甲烷和氯气反应的生成物中只有一氯甲烷和
HCl在标准状况下是气体,B错误;该反应中有氯化氢生成,氯化氢遇空气中的水蒸气形成
白雾,D正确。
4.已知:往溴的苯溶液中加入少量铁屑能迅速反应,其过程如下:
3Br +2Fe===2FeBr ;Br +FeBr ===FeBr+Br+(不稳定);
2 3 2 3
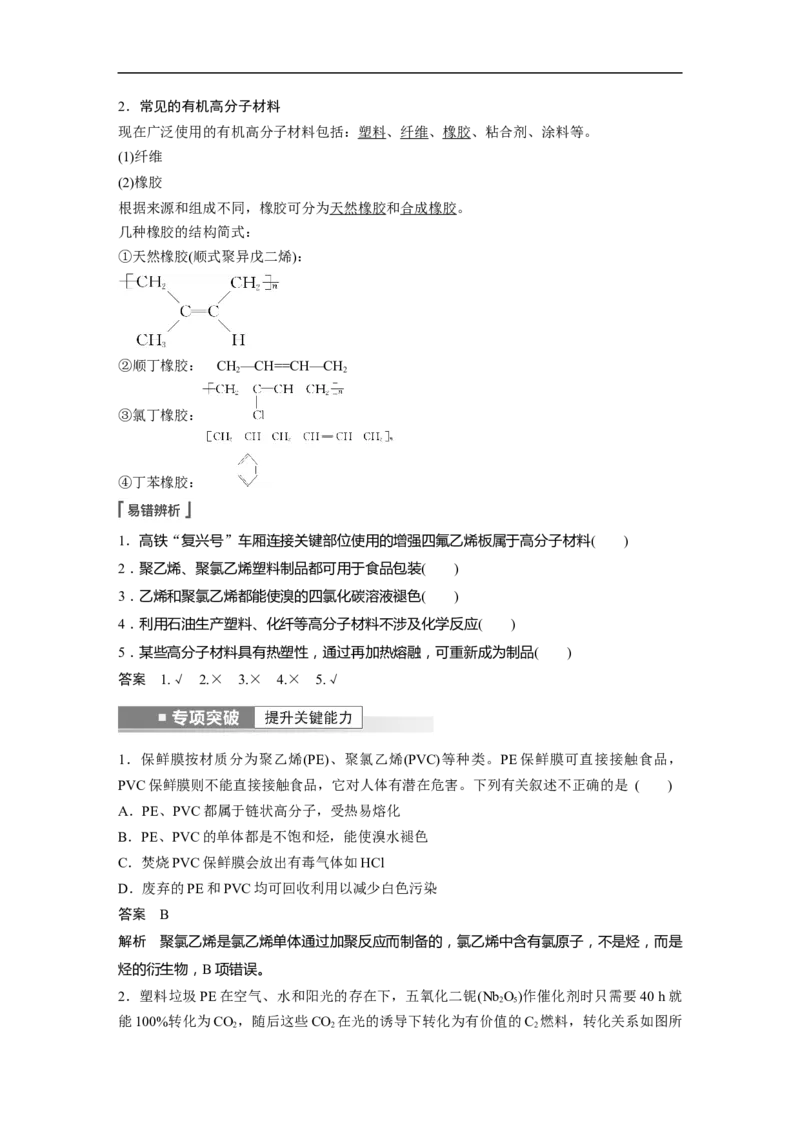
实验室用如图装置制取少量溴苯,
下列有关判断正确的是( )
A.上述反应过程中,第二步为置换反应B.装置乙能吸收反应过程中挥发出来的溴蒸气
C.装置甲中生成溴苯的化学方程式为 +Br ――→
2
D.装置丙中导管口有白雾生成,溶液中有白色沉淀生成
答案 B
解析 化学反应Br +FeBr ===FeBr+Br+产物中没有新的单质生成,故 A错误;单质溴易
2 3
溶于四氯化碳,因此装置乙能吸收反应过程中挥发出来的溴蒸气,故B正确;装置甲中生
成溴苯的化学方程式为 +Br ――→ +HBr,故C错误;装置丙中导管口有白雾生
2
成,溶液中有淡黄色沉淀生成,故D错误。
考点二 煤 石油 天然气
1.煤的综合利用
(1)煤的干馏
将煤隔绝空气加强热使其分解的过程。煤的干馏是一个复杂的物理、化学变化过程。
(2)煤的气化
将煤转化为可燃性气体的过程,主要反应是碳和水蒸气反应生成水煤气等。化学方程式为 C
+ H O(g) ===== CO + H 。
2 2
(3)煤的液化
①直接液化:煤+氢气――――→液体燃料。
②间接液化:煤+水――→水煤气――→甲醇等。
2.石油的综合利用
(1)石油的成分:由多种碳氢化合物组成的混合物,主要成分是烷烃、环烷烃和芳香烃。所
含元素以 C 、 H 为主,还含有少量N、S、P、O等。
(2)石油的加工
方法 过程 目的
分馏 把原油中沸点不同的各组分进行分离的过程 获得各种燃料用油
催化裂化 把相对分子质量大的烃断裂成相对分子质量 得到更多、更好的汽油小的烃
得到乙烯、丙烯、甲烷等
裂解 深度裂化,产物呈气态
重要的化工原料
3.天然气的综合利用
(1)天然气的主要成分是甲烷,它是一种清洁的化石燃料,更是一种重要的化工原料。
(2)天然气与水蒸气反应制取H
2
原理:CH+HO(g)――→CO+3H。
4 2 2
1.石油是混合物,其分馏产品汽油为纯净物( )
2.裂化的目的是得到轻质油,裂解的目的是得到乙烯、丙烯等化工原料( )
3.煤的气化和液化都是化学变化( )
4.天然气作为燃料的优点,不仅是热值高,还易充分燃烧( )
5.大量燃烧化石燃料是造成雾霾天气的一个重要因素( )
答案 1.× 2.√ 3.√ 4.√ 5.√
1.《天工开物》记载了古代四川“井火取盐”的过程,“临邛(地名)火井(废井,废气遇明
火可燃)一所,纵广五尺,深二三丈”“取井火还煮井水”“一水得四五斗盐”,“井火”
燃烧的物质是( )
A.天然气 B.煤炭
C.石油 D.石蜡
答案 A
解析 根据题给信息可知井中废气遇明火可燃,“井火”燃烧的物质是可燃性气体天然气。
2.有关煤的综合利用如图所示。下列说法正确的是( )
A.煤和水煤气均是二次能源
B.煤中含有苯、甲苯、二甲苯等有机物
C.①是将煤在空气中加强热使其分解的过程
D.B为甲醇或乙酸时,原子利用率均可达到100%
答案 D
解析 煤属于一次能源,A项错误;苯、甲苯等是煤干馏过程中生成的物质,B项错误;干
馏是在隔绝空气的条件下进行的,否则,煤就会在空气中燃烧,C项错误;水煤气的成分是CO、H,当二者按物质的量之比为1∶2反应时可得到甲醇,当二者按物质的量之比为1∶1
2
反应时可得到乙酸,D项正确。
3.石油是由多种碳氢化合物组成的混合物,石油精炼可以获得多种化工原料。
(1)写出下列石油加工的方法:①_____________________,②____________,③__________。
其中属于化学变化的是__________(填序号)。
(2)下列物质中沸点最高的是________。
a.汽油 b.煤油 c.柴油 d.重油
(3)裂化汽油可以使溴的四氯化碳溶液褪色,其原因是_______________________________。
答案 (1)分馏 裂化 裂解 ②③ (2)d (3)裂化汽油中含有烯烃等不饱和烃,能与Br 发
2
生加成反应,使溴的四氯化碳溶液褪色
考点三 有机高分子材料与 STSE
1.高分子
(1)高分子的相对分子质量比一般有机化合物大得多,通常在104以上。
注意:①没有特殊说明时,高分子特指有机高分子,②所有高分子均为混合物。
(2)聚合反应与加聚反应
①由相对分子质量较小的化合物分子互相结合成相对分子质量大的聚合物的反应叫做聚合反
应。
②含有不饱和键的有机物分子间通过碳原子彼此加成相互结合,聚合成很长的碳链,生成有
机高分子的聚合反应叫做加成聚合反应,简称加聚反应。
(3)有机高分子的通性
高分子通常难溶于水,即使在适当的有机溶剂中溶解得也很缓慢,或者只有一
溶解性
定程度的溶胀
热塑 有些高分子(如聚乙烯)具有热塑性,即受热时会变软、流动,受冷时又硬化,
性、热 可通过加热、受冷反复塑造;有些高分子(如酚醛塑料,俗称“电木”)则具有
固性 热固性,即受热时不会变软而只能被裂解,因此不能通过加热、受冷反复塑造
高分子中的原子之间一般是以共价键结合的,因此高分子通常不导电,是很好
绝缘性
的绝缘材料2.常见的有机高分子材料
现在广泛使用的有机高分子材料包括:塑料、纤维、橡胶、粘合剂、涂料等。
(1)纤维
(2)橡胶
根据来源和组成不同,橡胶可分为天然橡胶和合成橡胶。
几种橡胶的结构简式:
①天然橡胶(顺式聚异戊二烯):
②顺丁橡胶:CH—CH==CH—CH
2 2
③氯丁橡胶:
④丁苯橡胶:
1.高铁“复兴号”车厢连接关键部位使用的增强四氟乙烯板属于高分子材料( )
2.聚乙烯、聚氯乙烯塑料制品都可用于食品包装( )
3.乙烯和聚氯乙烯都能使溴的四氯化碳溶液褪色( )
4.利用石油生产塑料、化纤等高分子材料不涉及化学反应( )
5.某些高分子材料具有热塑性,通过再加热熔融,可重新成为制品( )
答案 1.√ 2.× 3.× 4.× 5.√
1.保鲜膜按材质分为聚乙烯(PE)、聚氯乙烯(PVC)等种类。PE保鲜膜可直接接触食品,
PVC保鲜膜则不能直接接触食品,它对人体有潜在危害。下列有关叙述不正确的是 ( )
A.PE、PVC都属于链状高分子,受热易熔化
B.PE、PVC的单体都是不饱和烃,能使溴水褪色
C.焚烧PVC保鲜膜会放出有毒气体如HCl
D.废弃的PE和PVC均可回收利用以减少白色污染
答案 B
解析 聚氯乙烯是氯乙烯单体通过加聚反应而制备的,氯乙烯中含有氯原子,不是烃,而是
烃的衍生物,B项错误。
2.塑料垃圾PE在空气、水和阳光的存在下,五氧化二铌(Nb O)作催化剂时只需要40 h就
2 5
能100%转化为CO ,随后这些CO 在光的诱导下转化为有价值的C 燃料,转化关系如图所
2 2 2示。下列叙述错误的是( )
A.工业生产PE的加聚反应为nCH==CH――→CH—CH
2 2 2 2
B.该转化的总反应为CH—CH+nO―――→nCHCOOH
2 2 2 3
C.“C 燃料”可以分别与H、C HOH发生加成反应、酯化反应
2 2 2 5
D.“C 燃料”与甲酸甲酯、羟基乙醛互为同分异构体
2
答案 C
解析 由题中“C 燃料”的球棍模型知,“C 燃料”分子中有1个甲基和1个羧基,为乙酸,
2 2
根据分析知该转化的反应物有聚乙烯、氧气,在阳光、水和催化剂作用下,反应生成乙酸,
总反应的化学方程式为CH—CH+nO―――→nCHCOOH,B 项正确;CHCOOH、
2 2 2 3 3
HCOOCH 、HOCH CHO的分子式均为C HO,三者互为同分异构体,D项正确。
3 2 2 4 2
3.ABS合成树脂的结构简式如图所示:
则合成这种树脂的单体为 ______________、
______________、__________,反应类型为____________。
答案 CH==CH—CN CH==CH—CH==CH 加聚反应
2 2 2
判断加聚反应产物单体的方法
加聚产物 方法 单体
CH—CH CH==CH
2 2 2 2
1.(2020·浙江1月选考,10改编)下列说法不正确的是( )
A.天然气的主要成分甲烷是高效、较洁净的燃料
B.石油的分馏、煤的气化和液化都是物理变化
C.石油的裂化主要是为了得到更多的轻质油
D.己烷属于烷烃,在一定条件下能与Cl 发生取代反应
2答案 B
解析 石油的分馏是物理变化,煤的气化和液化都是化学变化,B项错误。
2.(2021·河北,2)高分子材料在生产生活中应用广泛。下列说法错误的是( )
A.芦苇可用于制造黏胶纤维,其主要成分为纤维素
B.聚氯乙烯通过加聚反应制得,可用于制作不粘锅的耐热涂层
C.淀粉是相对分子质量可达几十万的天然高分子物质
D.大豆蛋白纤维是一种可降解材料
答案 B
解析 芦苇中含有天然纤维素,可用于制造黏胶纤维,故 A正确;聚氯乙烯在高温条件下
会分解生成有毒气体,因此不能用于制作不粘锅的耐热涂层,故B错误;淀粉为多糖,属
于天然高分子物质,其相对分子质量可达几十万,故C正确;大豆蛋白纤维的主要成分为
蛋白质,能够被微生物分解,因此大豆蛋白纤维是一种可降解材料,故D正确。
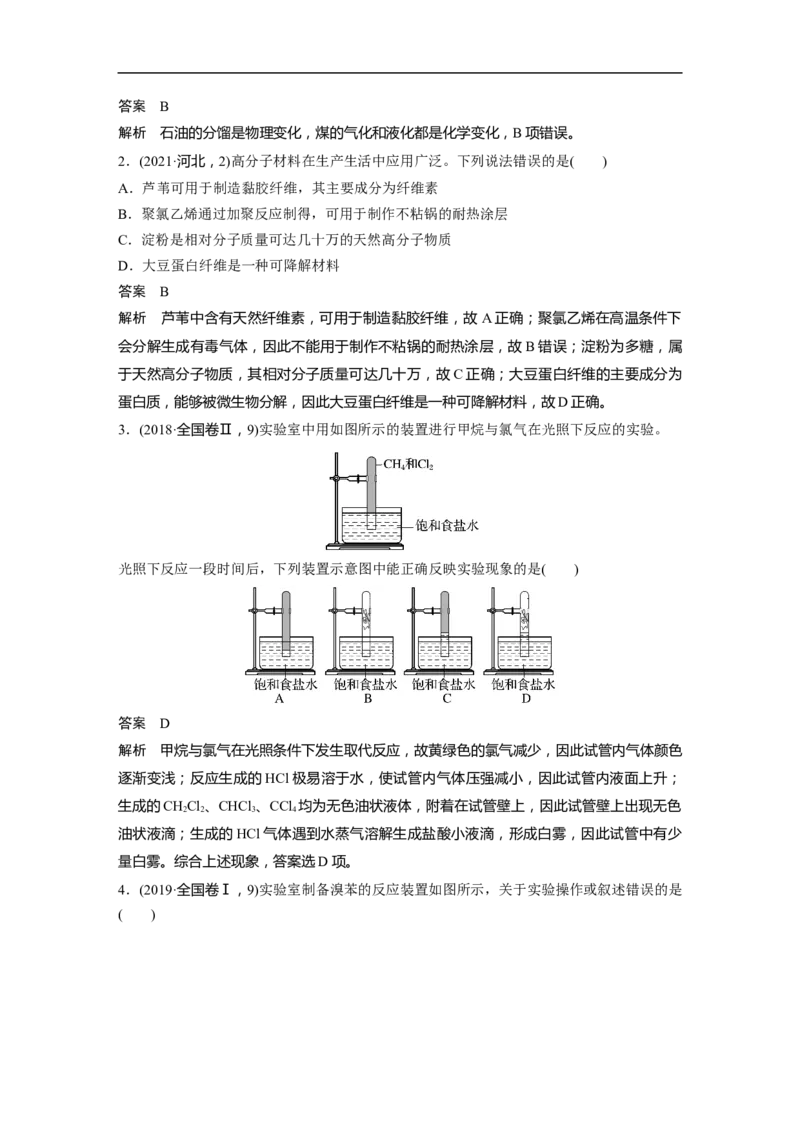
3.(2018·全国卷Ⅱ,9)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。
光照下反应一段时间后,下列装置示意图中能正确反映实验现象的是( )
答案 D
解析 甲烷与氯气在光照条件下发生取代反应,故黄绿色的氯气减少,因此试管内气体颜色
逐渐变浅;反应生成的HCl极易溶于水,使试管内气体压强减小,因此试管内液面上升;
生成的CHCl 、CHCl 、CCl 均为无色油状液体,附着在试管壁上,因此试管壁上出现无色
2 2 3 4
油状液滴;生成的HCl气体遇到水蒸气溶解生成盐酸小液滴,形成白雾,因此试管中有少
量白雾。综合上述现象,答案选D项。
4.(2019·全国卷Ⅰ,9)实验室制备溴苯的反应装置如图所示,关于实验操作或叙述错误的是
( )A.向圆底烧瓶中滴加苯和溴的混合液前需先打开K
B.实验中装置b中的液体逐渐变为浅红色
C.装置c中碳酸钠溶液的作用是吸收溴化氢
D.反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
答案 D
解析 苯和溴均易挥发,苯与液溴在溴化铁作用下发生剧烈的放热反应,释放出溴化氢气体
(含少量苯和溴蒸气),先打开K,后加入苯和液溴,避免因装置内气体压强过大而发生危险,
A项正确;四氯化碳用于吸收溴化氢气体中混有的溴单质,防止溴单质与碳酸钠溶液反应,
纯净的四氯化碳呈无色,吸收红棕色溴蒸气后,液体呈浅红色,B项正确;溴化氢极易溶于
水,倒置漏斗可防倒吸,碳酸钠溶液呈碱性,易吸收溴化氢,C项正确;反应后的混合液中
混有苯、液溴、溴化铁和少量溴化氢等,提纯溴苯的正确操作是①用大量水洗涤,除去可溶
性的溴化铁、溴化氢和少量溴;②用氢氧化钠溶液洗涤,除去剩余的溴等物质;③用水洗涤,
除去残留的氢氧化钠;④加入干燥剂除去水,过滤;⑤对有机物进行蒸馏,除去杂质苯,从
而提纯、分离溴苯,不能用“结晶”的方法,D项错误。
课时精练
1.化学与生活密切相关。下列说法错误的是( )
A.PM 是指颗粒直径不大于2.5 μm的可吸入悬浮颗粒物
2.5
B.绿色化学要求从源头上消除或减少生产活动对环境的污染
C.燃煤中加入CaO可以减少酸雨的形成及温室气体的排放
D.天然气和液化石油气是我国目前推广使用的清洁燃料
答案 C
解析 燃煤中加入CaO是为了除去煤燃烧生成的SO ,可减少酸雨的形成,但不能减少温室
2
气体的排放,C项错误;天然气和液化石油气完全燃烧的产物是CO 和HO,属于清洁燃料,
2 2
D项正确。
2.如图所示是四种常见有机物的空间填充模型示意图。下列说法正确的是( )A.甲能使酸性KMnO 溶液褪色
4
B.乙可与溴水发生取代反应使溴水褪色
C.丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键
D.丁在稀硫酸作用下可与乙酸发生取代反应
答案 C
解析 甲是甲烷、乙是乙烯、丙是苯、丁是乙醇。甲烷不能使酸性 KMnO 溶液褪色,A项
4
错误;乙烯能与Br 发生加成反应使溴水褪色,B项错误;苯分子中碳碳键是一种介于碳碳
2
单键和碳碳双键之间的独特的键,C项正确;乙醇在浓HSO 作用下可与乙酸发生酯化反应
2 4
(取代反应),D项错误。
3.(2022·西安八校联考)化学与科学、技术、社会、环境等密切相关,下列说法不正确的是(
)
A.乙烯可作为水果的催熟剂
B.煤中含有苯、甲苯和粗氨水,可通过干馏得到上述产品
C.石油裂解可以得到甲烷、乙烯、丙烯等重要化工原料
D.海底可燃冰开发不当释放出的甲烷会使温室效应加剧
答案 B
解析 乙烯可以调节植物生长,可以作为水果的催熟剂,A项正确;煤中不含苯、甲苯和粗
氨水,可通过煤的干馏得到苯、甲苯和粗氨水等,B项错误;可燃冰的主要成分为甲烷,甲
烷为温室气体,D项正确。
4.除去乙烷中混有的少量乙烯,应采用的简便方法是( )
A.将混合气体通过氢氧化钠溶液
B.将混合气体通过溴水
C.将混合气体在催化剂条件下跟氢气反应
D.使混合气体中的乙烯气体发生加聚反应
答案 B
解析 乙烯和乙烷均不与氢氧化钠溶液反应,不能除去乙烷中混有的少量乙烯,A错误;乙
烯能和溴水发生加成反应,而乙烷不能,可以除去乙烷中混有的少量乙烯,B正确;将混合
气体在催化剂条件下跟氢气反应会使乙烯转化为乙烷,但操作复杂,且易引入新杂质 H,C
2
错误;乙烯能发生加聚反应,但条件复杂,D错误。
5.下列说法正确的是( )
A.所有的烷烃在光照条件下都能与氯气发生取代反应
B.丙烯分子中所有的原子一定在同一平面上
C.分子式为C H 的烃一定能使酸性KMnO 溶液褪色
4 8 4
D.丁烯只能发生加成反应不能发生取代反应
答案 A解析 烷烃在光照条件下都能与氯气发生取代反应,这是烷烃化学性质的主要特征之一,A
项正确;烯烃分子中,与双键碳原子相连的4个原子及双键碳原子处于同一平面上,而其他
的原子则不一定处于该平面上,丙烯(CH==CH—CH )分子中—CH 上的氢原子最多只有一
2 3 3
个处于其他6个原子所在的平面上,B项错误;分子式为C H 的烃可以是烯烃,也可以是
4 8
环烷烃,而环烷烃不能使酸性KMnO 溶液褪色,C项错误;加成反应是不饱和键的特征反
4
应,烯烃在一定条件下也可以发生取代反应,D项错误。
6.对下列有机反应类型的认识中,错误的是( )
A. +HNO――→ +HO;取代反应
3 2
B.CH==CH+Br ―→CHBr—CHBr;加成反应
2 2 2 2 2
C.2CHCHOH+O――→2CHCHO+2HO;取代反应
3 2 2 3 2
D.CHCOOH+CHCHOHCHCOOCH CH+HO;取代反应
3 3 2 3 2 3 2
答案 C
7.下列各项物质使用一种试剂就能鉴别出来的是( )
A.苯、甲苯、己烯 B.甲苯、己烯、四氯化碳
C.己烯、汽油、苯 D.苯、甲苯、二甲苯
答案 B
解析 B项可用溴水鉴别,甲苯萃取溴后分层,上层为橙红色;己烯使溴水褪色;四氯化碳
萃取溴后分层,下层为橙红色。
8.生活中使用的塑料食品盒、水杯等通常由聚苯乙烯制成,其结构简式为 。
根据所学知识,下列说法正确的是( )
A.聚苯乙烯能使溴水褪色
B.聚苯乙烯是一种天然高分子材料
C.聚苯乙烯可由苯乙烯通过化合反应制得
D.聚苯乙烯单体的分子式为C H
8 8
答案 D
解析 聚苯乙烯为苯乙烯发生加聚反应生成的高分子,属于合成高分子材料,故B、C错误;
聚苯乙烯的单体为苯乙烯,分子式为C H,故D正确。
8 8
9.工业上可由乙苯制苯乙烯:
―――→ +H↑
2
下列说法错误的是( )
A.乙苯不能与溴水反应,而苯乙烯能B.苯乙烯在一定条件下能发生加聚反应
C.苯乙烯和乙苯在一定条件下都能和氢气发生加成反应
D.可用酸性高锰酸钾溶液鉴别乙苯和苯乙烯
答案 D
10.中科院研究所首次实现了CO 催化加氢制取汽油。CO 转化过程示意图如图所示:
2 2
下列说法不正确的是( )
A.多功能催化剂可提高H 的转化率
2
B.汽油主要是C ~C 的烃类混合物
5 11
C.a的一氯代物有4种
D.图中a和b互为同系物
答案 A
解析 多功能催化剂只能影响化学反应的速率,不能提高H 的转化率,A项错误。
2
11.下列说法不正确的是( )
――→――→――→
A.石油是由烃组成的混合物
B.①主要发生物理变化
C.②是石油的裂化、裂解
D.③属于取代反应
答案 D
解析 ①为石油的分馏,发生物理变化,B项正确;由石油分馏产品获得乙烯需经过石油的
裂 化 和 裂 解 , C 项 正 确 ; 由 乙 烯 制 得 1,2- 二 溴 乙 烷 的 反 应 为 CH==CH +
2 2
Br ―→CHBrCHBr,属于加成反应,D项错误。
2 2 2
12.从柑橘中可提炼得1,8-萜二烯( )。下列有关他的说法正确的是( )
A.分子式为C H
10 14
B.属于烃,难溶于水,可用某些有机溶剂提取1,8-萜二烯
C.与酸性高锰酸钾溶液、氧气、溴水等均可发生氧化反应
D.它的一种同分异构体的结构中可能含有苯环
答案 B
解析 A项,根据结构简式可确定分子式为C H ,错误;B项,该物质中只含C、H元素,
10 16
所以属于烃,难溶于水,易溶于有机溶剂,因此可用某些有机溶剂提取1,8-萜二烯,正确;
C项,该物质中含有碳碳双键,能和溴水发生加成反应,错误;D项,该物质的不饱和度是3,苯的不饱和度是4,该物质的同分异构体中不可能含有苯环,错误。
13.(2022·衡水中学模拟)150 ℃时,将1 L混合烃与9 L氧气混合,在密闭容器内充分燃烧,
当恢复至150 ℃,体积恒定时,容器内压强增大8%,则该混合烃的组成是( )
A.甲烷与乙烷体积比是1∶4 B.丙炔与乙炔体积比是1∶4
C.乙烯与丁烷体积比是1∶4 D.乙烯与丁烯体积比是1∶4
答案 D
解析 根据烃燃烧的化学方程式:
CH+(x+)O ―→xCO+HO(g) ΔV
x y 2 2 2
1 mol (x+)mol x mol mol -1
1 L 0.8 L
可得y=7.2,若是乙烯与丁烷,则乙烯与丁烷体积比是7∶8;若是乙烯与丁烯,则乙烯与
丁烯体积比是1∶4,故选D。
14.如图是两种烃的球棍模型,下列说法正确的是( )
A.二者互为同系物
B.二者互为同分异构体
C.都不能使酸性高锰酸钾溶液褪色
D.都不能发生加成反应
答案 B
解析 A为乙苯,B为间二甲苯,二者分子式相同,结构不同,互为同分异构体,A错误、
B正确;乙苯、间二甲苯中的侧链都能被酸性高锰酸钾溶液氧化为羧基,使酸性高锰酸钾溶
液褪色,C错误;苯环能够与氢气发生加成反应,乙苯、间二甲苯均含苯环结构,所以都能
与氢气发生加成反应,D错误。
15.豪猪烯形状宛如伏地伸刺的动物,其键线式如图。下列有关豪猪烯的说法正确的是( )
A.豪猪烯与乙烯互为同系物 B.豪猪烯分子中所有的碳原子可能在同一平面上
C.豪猪烯的分子式为C H D.1 mol豪猪烯能与6 mol H 发生加成反应
14 20 2
答案 D
解析 豪猪烯与乙烯结构上不相似,组成上不相差若干个“CH”原子团,二者不互为同系
2物,A错误;分子中含有类似甲烷中碳原子的空间结构,碳原子连有四条单键,为空间四面
体结构,所有碳原子不可能共平面,B错误;由题中键线式可知,豪猪烯分子式为C H ,
14 14
C错误;1 mol豪猪烯含有6 mol ,能与6 mol H 发生加成反应,D正确。
2
16.某兴趣小组在实验室中模拟利用甲烷和氯气发生取代反应制取副产品盐酸,设计如图装
置,下列说法错误的是( )
A.实验时先点燃A处酒精灯再通甲烷
B.装置B有均匀混合气体、控制气体流速、干燥混合气体等作用
C.装置C经过一段时间的强光照射后,生成的有机物有4种
D.从装置D中分离出盐酸的方法为过滤
答案 D
解析 B项,生成的氯气中含有水,B装置除了具有控制气体流速、均匀混合气体的作用,
因浓硫酸具有吸水性,还具有干燥混合气体的作用,正确;C项,装置C经过一段时间的强
光照射后,甲烷和氯气发生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳 4种有
机物,正确;D项,D装置中除了有盐酸存在外,还含有二氯甲烷、三氯甲烷和四氯化碳,
二氯甲烷、三氯甲烷和四氯化碳不溶于水,能分层,可用分液的方法分离,错误。
17.现有CH、C H、C H 三种有机物:
4 2 4 2 6
(1)等质量的以上三种物质完全燃烧时消耗O 的量最多的是________。
2
(2)同状况、同体积的以上三种物质完全燃烧时消耗O 的量最多的是________。
2
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是________,生成水最多的是
________。
(4)在120 ℃、1.01×105 Pa时,上述三种有机物中两种气态烃和足量的氧气混合点燃,相
同条件下测得反应前后气体体积都没有发生变化,这两种气体是________。
答案 (1)CH (2)C H (3)C H CH (4)CH 、C H
4 2 6 2 4 4 4 2 4
解析 (1)等质量的烃CH 完全燃烧时,氢元素的质量分数越大,耗氧量越大,CH、C H、
x y 4 2 4
C H 中的的值依次为4、2、3,CH 中H元素的质量分数最大,故甲烷消耗O 最多。
2 6 4 2
(2)同状况、同体积的三种气体,其物质的量相等,等物质的量的烃 CH 完全燃烧时,(x+)
x y
的值越大,耗氧量越大,CH、C H、C H 的(x+)的值依次为2、3、3.5,故C H 消耗O 最
4 2 4 2 6 2 6 2
多。(4)在120 ℃、1.01×105 Pa时,烃燃烧生成的水是气态,设烃的平均组成为 CH ,则:
x y
CH+(x+)O ――→xCO +HO,燃烧反应前后气体体积没有变化,则反应前后气体的化学计
x y 2 2 2
量数之和相等,故1+(x+)=x+,解得y=4,即满足H原子数目为4即可,故这两种气体
为CH、C H。
4 2 4