文档内容
(一)共价键
1.下表是两者的键能(单位:kJ·mol-1)数据:
A-B A==B A≡B
CO 351 745 1 071.9
N 139 418 946
2
结合数据说明CO比N 活泼的原因:___________________________________________。
2
答案 CO中第一个π键的键能是326.9 kJ·mol-1,N 中第一个π键的键能是528 kJ·mol-1,
2
所以CO的第一个π键比N 中第一个π键更容易断裂,所以CO比N 活泼
2 2
2.两种三角锥形气态氢化物PH 和NH 的键角分别为93°6′和107°,试分析PH 的键角小
3 3 3
于NH 的原因:____________________________________________________________。
3
答案 电负性:N>P,中心原子的电负性越大,成键电子对离中心原子越近,成键电子对
之间的距离越小,成键电子对之间的排斥力增大,键角变大
3.NF 的键角______NH 的键角(填“>”“<”或“=”),理由是_____________________
3 3
_______________________________________________________________________________
。
答案 < F的电负性比H大,NF 中N原子周围电子云的密度减小,成键电子对之间的排
3
斥力较小,因而键角较小
4 . HO + 中 H—O—H 的 键 角 比 HO 中 H—O—H 的 键 角 大 , 原 因 是
3 2
_______________________
_______________________________________________________________________________
。
答案 HO中的氧原子有2个孤电子对,HO+中的氧原子有1个孤电子对,排斥力较小
2 3
5.CH 、NH 、HO 的 VSEPR 模型都是______,键角分别是________、________、
4 3 2
__________ ; 分 析 它 们 键 角 差 异 的 原 因 :
______________________________________________________。
答案 四面体形 109°28′ 107° 105° CH 中键与键之间的排斥力一样,是正四面体形,
4
键角为109°28′;而其他两个分子均有未成键的孤电子对,孤电子对间的排斥力>孤电子对
与σ键电子对间的排斥力>σ键电子对间的排斥力。由于孤电子对对成键电子的排斥作用,
使得成键电子间夹角变小,HO中有两个孤电子对,NH 中有一个孤电子对,故HO中键角
2 3 2
比NH 更小
3
6.HS键角比HSe大的原因:__________________________________________。
2 2
答案 电负性:S>Se,共用电子对离S近,共用电子对间的排斥力大7.SO的键角小于SO的原因是_________________________________________________。
答案 SO中无孤电子对,SO中有一个孤电子对,孤电子对与成键电子对间的斥力更大,导
致SO的键角小于SO
8.CHNH中H—N—H的键角比NH 中H—N—H的键角________(填“大”或“小”),理
3 3
由是__________________________________________________________________________。
答案 大 CHNH中N形成4个σ键,而NH 分子中N有1个孤电子对,孤电子对对H—N
3 3
的排斥力更大,H—N—H的键角变小
(二)氢键
9.HS的熔点为-85.5 ℃,而与其具有类似结构的HO的熔点为0 ℃,极易结冰成固体,
2 2
二者物理性质出现差异的原因是_________________________________________________。
答案 HO分子间极易形成氢键,而HS分子间只存在较弱的范德华力
2 2
10.NH 常用作制冷剂,原因是___________________________________________。
3
答案 NH 分子间能形成氢键,沸点高,易液化,汽化时吸收大量的热
3
11.硝酸和尿素的相对分子质量接近,但常温下硝酸为挥发性液体,尿素为固体,请解释原
因:_________________________________________________________________________。
答案 尿素分子间存在氢键,使其熔、沸点升高,而硝酸分子内存在氢键,使其熔、沸点降
低
12.氨气极易溶于水的原因为___________________________________________________。
答案 氨气和水都是极性分子,依据“相似相溶”规律,且氨气分子与水分子间能形成氢键
13.NH 与O 的相对分子质量相近,但NH 的熔点(2 ℃)、沸点(114 ℃)分别远远高于O
2 4 2 2 4 2
的 熔 点 ( - 218 ℃) 、 沸 点 ( - 183 ℃) , 原 因 是
___________________________________________。
答案 NH 分子之间存在氢键,O 分子之间为范德华力,氢键比范德华力更强
2 4 2
14.HO、PH 、KH 按熔点由高到低的顺序排列为________,熔点差异的原因是
2 3
______________
_______________________________________________________________________________
。
答案 KH>H O>PH KH为离子晶体,HO、PH 均为分子晶体,HO分子间存在氢键
2 3 2 3 2
15.硼酸分子的结构简式可写为B(OH) ,其晶体为层型片状结构,容易在层与层之间裂解,
3
这是因为在平面层内硼酸分子之间通过______结合,而层与层之间通过________结合。
答案 氢键 范德华力
16. 的分子内部存在氢键,画出氢键结构:______________________。
答案
17.HSCN的结构有两种,其中硫氰酸(H—S—C≡N)的沸点低于异硫氰酸(H—N==C==S),原因是_________________________________________________________________________。
答案 异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键
(三)配位键、配合物
18.CO为配合物中常见的配体。CO作配体时,提供孤电子对的通常是C原子而不是O原
子,其原因是____________________________________________________________。
答案 C元素的电负性比O元素小,C原子提供孤电子对的倾向更大,更易形成配位键
19.镍的氨合离子[Ni(NH )]2+中存在的化学键有________(填字母)。
3 6
A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
答案 BCE
20.Cu O与NH ·H O反应能形成较稳定的[Cu(NH )]+的原因是______________________。
2 3 2 3 2
答案 NH ·H O中的N原子提供孤电子对,与Cu+形成配位键
3 2
21 . Co3 + 在 水 中 易 被 还 原 成 Co2 + , 而 在 氨 水 中 可 稳 定 存 在 , 其 原 因 为
___________________。
答案 Co3+可与 NH 形成较稳定的配合物
3
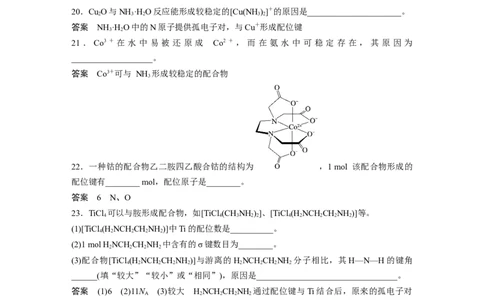
22.一种钴的配合物乙二胺四乙酸合钴的结构为 ,1 mol 该配合物形成的
配位键有________ mol,配位原子是________。
答案 6 N、O
23.TiCl 可以与胺形成配合物,如[TiCl (CHNH )]、[TiCl (H NCH CHNH )]等。
4 4 3 2 2 4 2 2 2 2
(1)[TiCl (H NCH CHNH )]中Ti的配位数是__________。
4 2 2 2 2
(2)1 mol H NCH CHNH 中含有的σ键数目为________。
2 2 2 2
(3)配合物[TiCl (H NCH CHNH )]与游离的HNCH CHNH 分子相比,其H—N—H的键角
4 2 2 2 2 2 2 2 2
______(填“较大”“较小”或“相同”),原因是_________________________________。
答案 (1)6 (2)11N (3)较大 HNCH CHNH 通过配位键与Ti结合后,原来的孤电子对
A 2 2 2 2
变为成键电子对,对N—H成键电子对的排斥力减小,N—H之间的键角增大
24.邻二氮菲( )中N原子可与Fe2+通过配位键形成橙红色邻二氮菲亚铁离子,利
用该反应可测定Fe2+浓度,该反应的适宜pH范围为2~9,试解释选择该pH范围的原因:
_____________________________________________________________________________。
答案 当H+浓度较高时,邻二氮菲中的N优先与H+形成配位键,导致与Fe2+配位的能力
减弱;若OH-浓度较高时,OH-与Fe2+反应,也会影响与邻二氮菲配位
25.含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Ni2+与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形
成的配位键有________个,其中提供孤电子对的原子为________(写元素符号)。
答案 6 N、O