文档内容
特色练 8 电化学基础
1.水溶液中电解催化还原CO 制甲酸是实现“碳中和”的途径之一。下列说法正确的是(
2
)
A.该过程将化学能转化为电能
B.生成甲酸的电极反应为CO+2e-+2H+===HCOOH
2
C.阳离子由阴极移向阳极
D.电路中通过4 mol e-,阳极生成22.4 L O
2
答案 B
解析 该实验装置是电解池,将电能转化为化学能,A错误;电解过程中二氧化碳得电子生
成甲酸,故电极反应为CO +2e-+2H+===HCOOH,B正确;电解池中阳离子由阳极移向
2
阴极,C错误;电路中通过4 mol e-,阳极生成1 mol O ,但没有说明是否标准状况,无法
2
确定气体的体积,D错误。
2.知识源于实践。学习原电池知识后,某学习小组以Zn和Cu为电极材料,制作了如图所
示的水果电池(水果果汁中含游离的H+)。该组电池放电时,下列说法正确的是( )
A.铜a为电池正极,发生氧化反应
B.锌a、b发生的电极反应是2H++2e-===H↑
2
C.四个水果电池串联,则电极d为铜片
D.每个水果果汁中的H+移向正极
答案 D
解析 铜a为电池正极,氢离子得电子生成氢气,发生还原反应,A错误;锌a、b为电池
负极,发生的电极反应是Zn-2e-===Zn2+,B错误;四个水果电池串联,根据图中各电极
分布可知,电极d为锌片,C错误;原电池中阳离子移向正极,则每个水果果汁中的H+移
向正极,D正确。
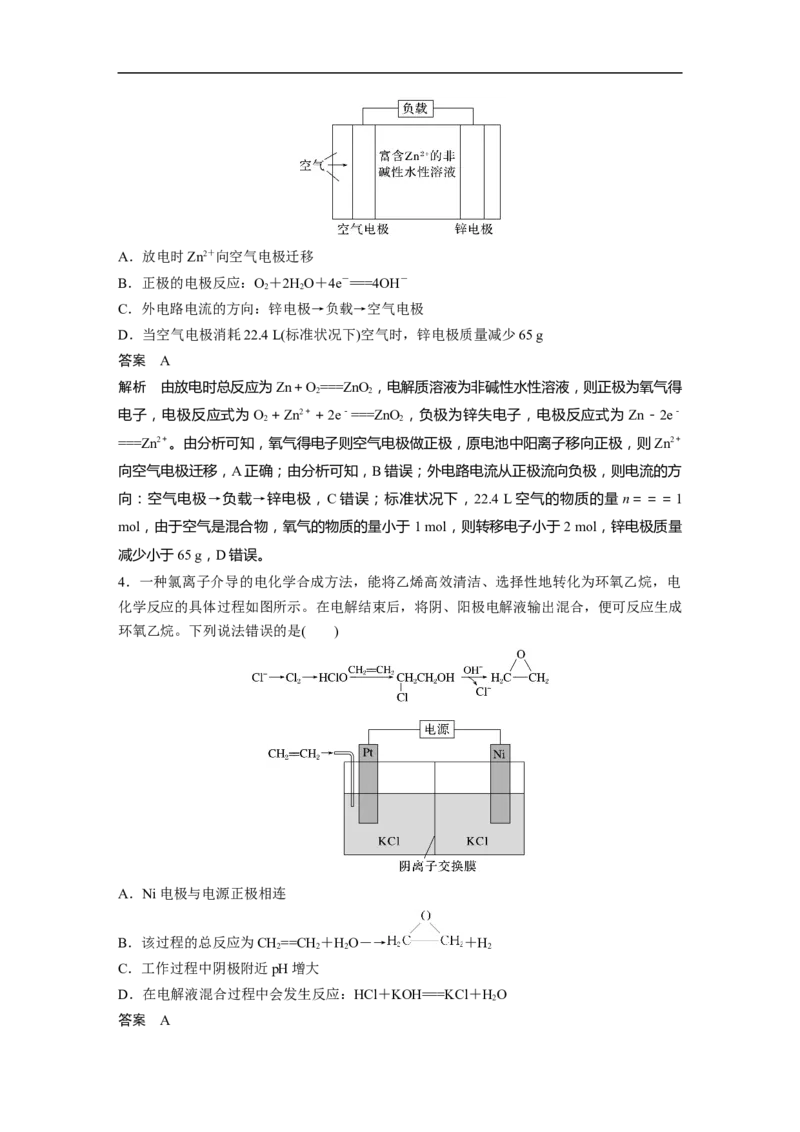
3.我国报道了一种新型的锌-空气电池,如图所示。该电池以一种富含Zn2+的非碱性水性溶
液为电解质溶液,放电时总反应为 Zn+O===ZnO 。下列有关该电池放电时的说法正确的
2 2
是( )A.放电时Zn2+向空气电极迁移
B.正极的电极反应:O+2HO+4e-===4OH-
2 2
C.外电路电流的方向:锌电极→负载→空气电极
D.当空气电极消耗22.4 L(标准状况下)空气时,锌电极质量减少65 g
答案 A
解析 由放电时总反应为Zn+O===ZnO ,电解质溶液为非碱性水性溶液,则正极为氧气得
2 2
电子,电极反应式为O +Zn2++2e-===ZnO ,负极为锌失电子,电极反应式为 Zn-2e-
2 2
===Zn2+。由分析可知,氧气得电子则空气电极做正极,原电池中阳离子移向正极,则Zn2+
向空气电极迁移,A正确;由分析可知,B错误;外电路电流从正极流向负极,则电流的方
向:空气电极→负载→锌电极,C错误;标准状况下,22.4 L空气的物质的量n===1
mol,由于空气是混合物,氧气的物质的量小于1 mol,则转移电子小于2 mol,锌电极质量
减少小于65 g,D错误。
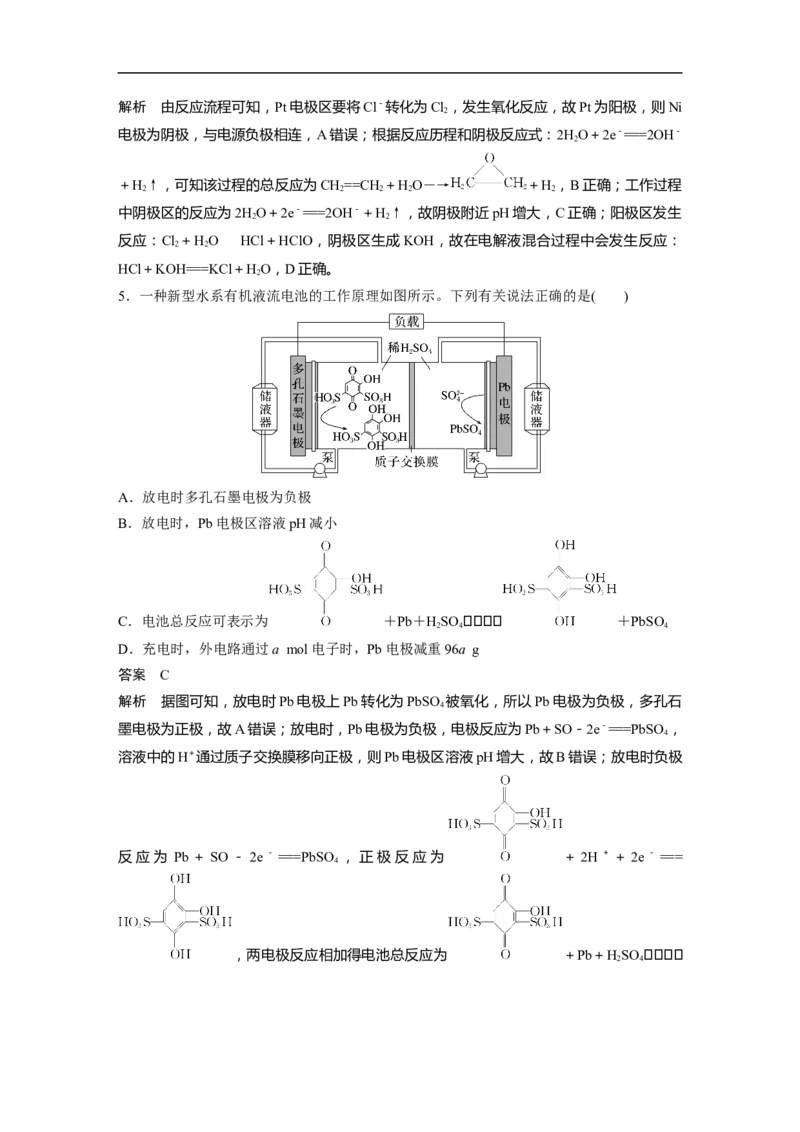
4.一种氯离子介导的电化学合成方法,能将乙烯高效清洁、选择性地转化为环氧乙烷,电
化学反应的具体过程如图所示。在电解结束后,将阴、阳极电解液输出混合,便可反应生成
环氧乙烷。下列说法错误的是( )
A.Ni电极与电源正极相连
B.该过程的总反应为CH==CH+HO―→ +H
2 2 2 2
C.工作过程中阴极附近pH增大
D.在电解液混合过程中会发生反应:HCl+KOH===KCl+HO
2
答案 A解析 由反应流程可知,Pt电极区要将Cl-转化为Cl ,发生氧化反应,故Pt为阳极,则Ni
2
电极为阴极,与电源负极相连,A错误;根据反应历程和阴极反应式:2HO+2e-===2OH-
2
+H↑,可知该过程的总反应为CH==CH +HO―→ +H ,B正确;工作过程
2 2 2 2 2
中阴极区的反应为2HO+2e-===2OH-+H↑,故阴极附近pH增大,C正确;阳极区发生
2 2
反应:Cl +HOHCl+HClO,阴极区生成KOH,故在电解液混合过程中会发生反应:
2 2
HCl+KOH===KCl+HO,D正确。
2
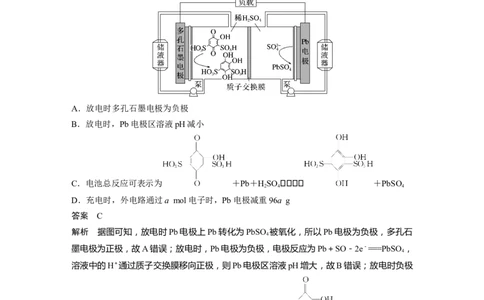
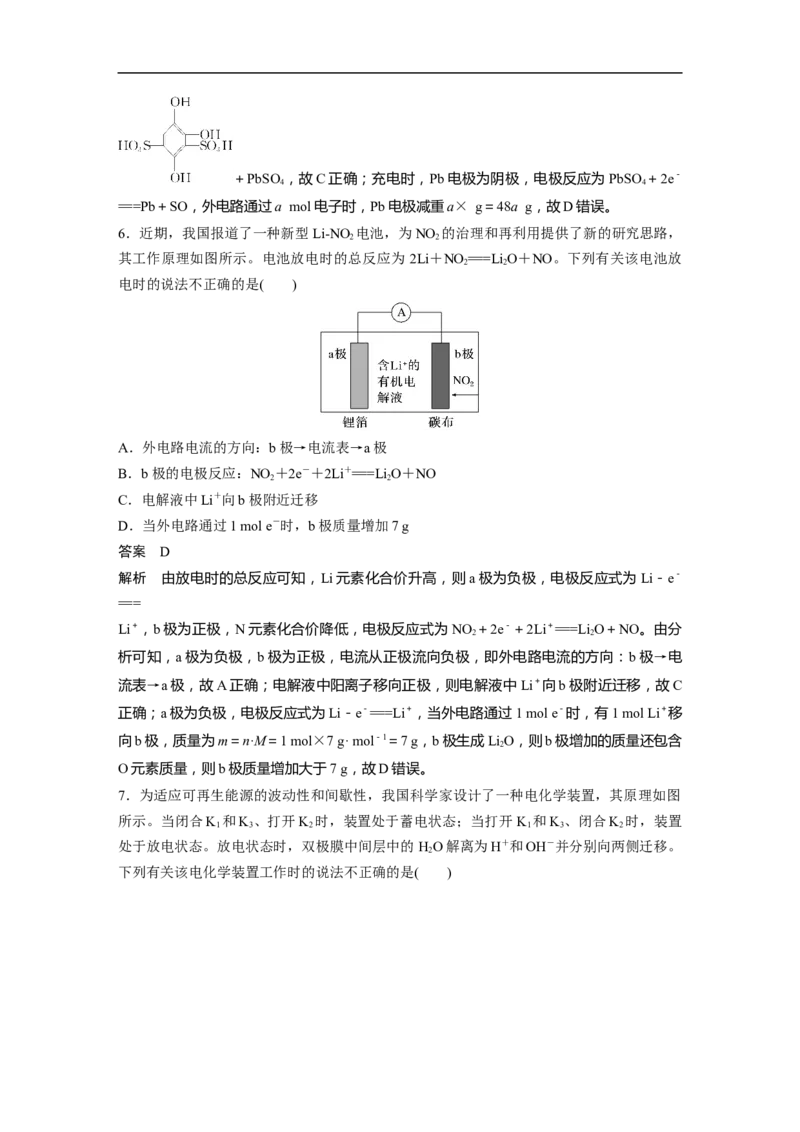
5.一种新型水系有机液流电池的工作原理如图所示。下列有关说法正确的是( )
A.放电时多孔石墨电极为负极
B.放电时,Pb电极区溶液pH减小
C.电池总反应可表示为 +Pb+HSO +PbSO
2 4 4
D.充电时,外电路通过a mol电子时,Pb电极减重96a g
答案 C
解析 据图可知,放电时Pb电极上Pb转化为PbSO 被氧化,所以Pb电极为负极,多孔石
4
墨电极为正极,故A错误;放电时,Pb电极为负极,电极反应为Pb+SO-2e-===PbSO ,
4
溶液中的H+通过质子交换膜移向正极,则Pb电极区溶液pH增大,故B错误;放电时负极
反应为 Pb+SO-2e-===PbSO ,正极反应为 +2H++2e-===
4
,两电极反应相加得电池总反应为 +Pb+HSO
2 4+PbSO ,故C正确;充电时,Pb电极为阴极,电极反应为PbSO +2e-
4 4
===Pb+SO,外电路通过a mol电子时,Pb电极减重a× g=48a g,故D错误。
6.近期,我国报道了一种新型Li-NO 电池,为NO 的治理和再利用提供了新的研究思路,
2 2
其工作原理如图所示。电池放电时的总反应为 2Li+NO ===LiO+NO。下列有关该电池放
2 2
电时的说法不正确的是( )
A.外电路电流的方向:b极→电流表→a极
B.b极的电极反应:NO +2e-+2Li+===LiO+NO
2 2
C.电解液中Li+向b极附近迁移
D.当外电路通过1 mol e-时,b极质量增加7 g
答案 D
解析 由放电时的总反应可知,Li元素化合价升高,则a极为负极,电极反应式为Li-e-
===
Li+,b极为正极,N元素化合价降低,电极反应式为NO +2e-+2Li+===LiO+NO。由分
2 2
析可知,a极为负极,b极为正极,电流从正极流向负极,即外电路电流的方向:b极→电
流表→a极,故A正确;电解液中阳离子移向正极,则电解液中Li+向b极附近迁移,故C
正确;a极为负极,电极反应式为Li-e-===Li+,当外电路通过1 mol e-时,有1 mol Li+移
向b极,质量为m=n·M=1 mol×7 g· mol-1=7 g,b极生成LiO,则b极增加的质量还包含
2
O元素质量,则b极质量增加大于7 g,故D错误。
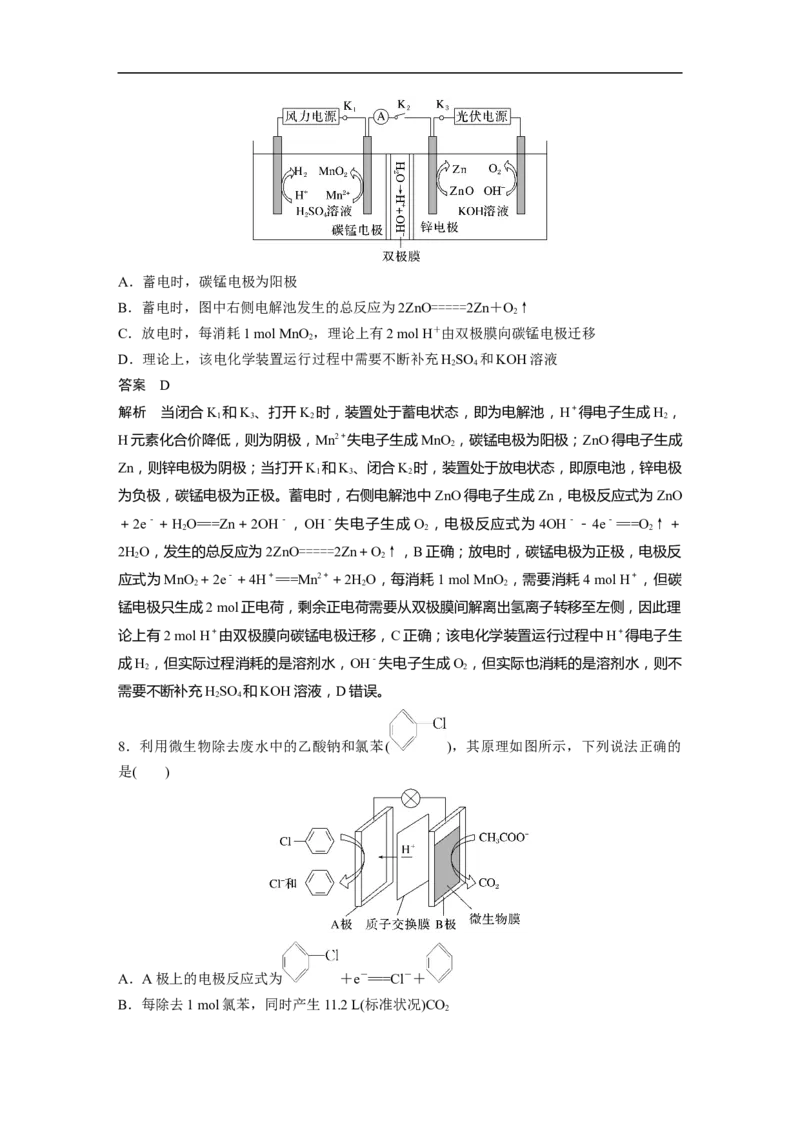
7.为适应可再生能源的波动性和间歇性,我国科学家设计了一种电化学装置,其原理如图
所示。当闭合K 和K 、打开K 时,装置处于蓄电状态;当打开K 和K 、闭合K 时,装置
1 3 2 1 3 2
处于放电状态。放电状态时,双极膜中间层中的 HO解离为H+和OH-并分别向两侧迁移。
2
下列有关该电化学装置工作时的说法不正确的是( )A.蓄电时,碳锰电极为阳极
B.蓄电时,图中右侧电解池发生的总反应为2ZnO=====2Zn+O↑
2
C.放电时,每消耗1 mol MnO ,理论上有2 mol H+由双极膜向碳锰电极迁移
2
D.理论上,该电化学装置运行过程中需要不断补充HSO 和KOH溶液
2 4
答案 D
解析 当闭合K 和K 、打开K 时,装置处于蓄电状态,即为电解池,H+得电子生成H ,
1 3 2 2
H元素化合价降低,则为阴极,Mn2+失电子生成MnO ,碳锰电极为阳极;ZnO得电子生成
2
Zn,则锌电极为阴极;当打开K 和K、闭合K 时,装置处于放电状态,即原电池,锌电极
1 3 2
为负极,碳锰电极为正极。蓄电时,右侧电解池中ZnO得电子生成Zn,电极反应式为ZnO
+2e-+HO===Zn+2OH-,OH-失电子生成O ,电极反应式为 4OH--4e-===O↑+
2 2 2
2HO,发生的总反应为2ZnO=====2Zn+O↑,B正确;放电时,碳锰电极为正极,电极反
2 2
应式为MnO +2e-+4H+===Mn2++2HO,每消耗1 mol MnO ,需要消耗4 mol H+,但碳
2 2 2
锰电极只生成2 mol正电荷,剩余正电荷需要从双极膜间解离出氢离子转移至左侧,因此理
论上有2 mol H+由双极膜向碳锰电极迁移,C正确;该电化学装置运行过程中H+得电子生
成H ,但实际过程消耗的是溶剂水,OH-失电子生成O ,但实际也消耗的是溶剂水,则不
2 2
需要不断补充HSO 和KOH溶液,D错误。
2 4
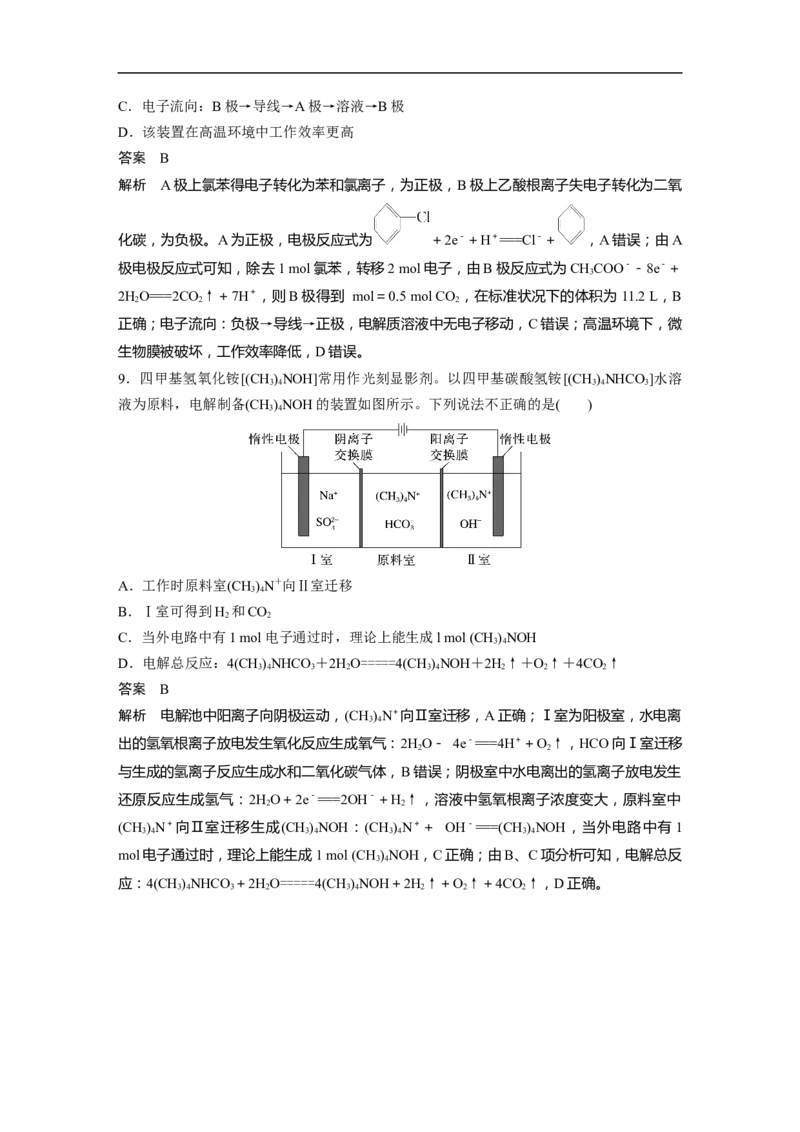
8.利用微生物除去废水中的乙酸钠和氯苯( ),其原理如图所示,下列说法正确的
是( )
A.A极上的电极反应式为 +e-===Cl-+
B.每除去1 mol氯苯,同时产生11.2 L(标准状况)CO
2C.电子流向:B极→导线→A极→溶液→B极
D.该装置在高温环境中工作效率更高
答案 B
解析 A极上氯苯得电子转化为苯和氯离子,为正极,B极上乙酸根离子失电子转化为二氧
化碳,为负极。A为正极,电极反应式为 +2e-+H+===Cl-+ ,A错误;由A
极电极反应式可知,除去1 mol氯苯,转移2 mol电子,由B极反应式为CHCOO--8e-+
3
2HO===2CO↑+7H+,则B极得到 mol=0.5 mol CO ,在标准状况下的体积为11.2 L,B
2 2 2
正确;电子流向:负极→导线→正极,电解质溶液中无电子移动,C错误;高温环境下,微
生物膜被破坏,工作效率降低,D错误。
9.四甲基氢氧化铵[(CH )NOH]常用作光刻显影剂。以四甲基碳酸氢铵[(CH )NHCO ]水溶
3 4 3 4 3
液为原料,电解制备(CH)NOH的装置如图所示。下列说法不正确的是( )
3 4
A.工作时原料室(CH)N+向Ⅱ室迁移
3 4
B.Ⅰ室可得到H 和CO
2 2
C.当外电路中有1 mol电子通过时,理论上能生成l mol (CH )NOH
3 4
D.电解总反应:4(CH)NHCO +2HO=====4(CH)NOH+2H↑+O↑+4CO↑
3 4 3 2 3 4 2 2 2
答案 B
解析 电解池中阳离子向阴极运动,(CH)N+向Ⅱ室迁移,A正确;Ⅰ室为阳极室,水电离
3 4
出的氢氧根离子放电发生氧化反应生成氧气:2HO- 4e-===4H++O↑,HCO向Ⅰ室迁移
2 2
与生成的氢离子反应生成水和二氧化碳气体,B错误;阴极室中水电离出的氢离子放电发生
还原反应生成氢气:2HO+2e-===2OH-+H↑,溶液中氢氧根离子浓度变大,原料室中
2 2
(CH)N+向Ⅱ室迁移生成(CH)NOH:(CH)N++ OH-===(CH)NOH,当外电路中有1
3 4 3 4 3 4 3 4
mol电子通过时,理论上能生成1 mol (CH )NOH,C正确;由B、C项分析可知,电解总反
3 4
应:4(CH)NHCO +2HO=====4(CH)NOH+2H↑+O↑+4CO↑,D正确。
3 4 3 2 3 4 2 2 2