文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题18
1.下列指定反应的离子方程式正确的是
A.用氨水吸收足量的SO 气体: 2NH ·H O + SO = 2NH+SO O
2 3 2 2 + H2
B.将Cl 通入石灰乳中制漂白粉: Cl+ 2OH- = ClO- + Cl-+ H O
2 2 2
C.ZnCO 溶于稀盐酸:CO += H O + CO ↑
3 + 2H 2 2
D.向AgBr悬浊液中滴加足量NaS溶液,出现黑色沉淀:2AgBr(s)+S2-(aq)=Ag S(s) +2Br-(aq)
2 2
答案:D
解析:A.用氨水吸收足量的SO 气体,反应生成亚硫酸氢铵:NH ·H O + SO =NH+HSO A
2 3 2 2 ,
错误;
B.将Cl 通入石灰乳中制漂白粉,反应生成氯化钙、次氯酸钙和水,反应的离子方程式为:
2
2Cl+ 2Ca(OH) =2Ca2++2ClO- +2Cl-+ 2H O, B错误;
2 2 2
C.ZnCO 溶于稀盐酸生成氯化锌、二氧化碳和水,反应的离子方程式为:ZnCO + 2H+=
3 3
Zn2++HO+CO↑,C错误;
2 2
D.向AgBr悬浊液中滴加足量NaS溶液,出现黑色沉淀,转化为更难溶的硫化银,反应的离
2
子方程式为:2AgBr(s)+S2- (aq)=Ag S(s) +2Br-(aq), D正确;
2
2.下列离子方程式不正确的是
A. 碳酸钠溶液中滴加过量澄清石灰水:Ca2++CO ↓
=CaCO3
B. 用过量的热烧碱溶液检验NH HCO 中的NH:NH+OH-===NH ↑+H O
4 3 3 2
C. 金属铝溶于NaOH溶液:2Al+2OH-+2H O=2AlO+3H↑
2 2
D. 使用含氟牙膏预防龋齿的原理:Ca (PO )OH(s)+F-(aq) Ca (PO )F(s)+OH-(aq)
5 4 3 5 4 3
答案:B
解析:A.澄清石灰水是氢氧化钙溶液,碳酸钠和澄清石灰水反应,其离子方程式为Ca2++CO
=
CaCO ↓;故A正确;
3
B.所加烧碱为过量,OH-应先与HCO CO OH-再与NH在加热条件下生成氨气和
反应生成 和水,过量
水,即离子方程式为NH+2OH-+HCO NH ↑+2H O+ CO B说法错误;
=== 3 2 ,故
C.金属铝能与氢氧化钠溶液反应生成氢气和偏铝酸钠,其离子方程式为2Al+2OH-
+2H O=2AlO+3H↑,故C说法正确;
2 2
D.使用含氟牙膏预防龋齿的原理:Ca (PO )OH(s)+F-(aq) Ca (PO )F(s)+OH-(aq),使用含
5 4 3 5 4 3
氟牙膏,F-浓度增大,平衡右移,故D说法正确;
3.废旧电器中电路板主要含有Fe、Cu、SnO 、PbO 、塑料等物质,研究小组从废旧电路板中
2 2
回收金属锡( Sn)的流程如图。下列说法正确的是
50已知:SnO 、PbO 可与强碱共热反应生成易溶于水的NaSnO 和NaPbO 。
2 2 2 3 2 3
A. Sn元素的核外电子排布式为[Kr]5s25p2
B. 焙烧的主要目的是将Fe和Cu变成氧化物
C. 若过滤后得到干燥的PbS和S的固体混合物27.1g,则反应①有N 个电子转移
A
D. 焦炭和SnO 反应的方程式为2C+SnO=====Sn+2CO↑
2 2
答案:D
解析:由题给流程可知,废旧电路板粉碎后在空气中焙烧可将塑料转化为气体除去,铁、铜转
化为氧化铁、氧化铜,向焙烧渣中加入过量的氢氧化钠溶液碱浸,将SnO 、PbO 转化为NaSnO
2 2 2 3
和NaPbO ,过滤得到含有氧化铁、氧化铜的滤渣和含有NaSnO 和NaPbO 的滤液a;向滤液中加
2 3 2 3 2 3
入硫化钠溶液将NaPbO 还原为PbS,过滤得到含有PbS 、S的固体混合物和含有NaSnO 的滤液
2 3 2 3
b;滤液b用水热法将NaSnO 转化为二氧化锡,二氧化锡与焦炭在高温下反应制得锡。
2 3
A.锡元素的原子序数为50,基态原子的的核外电子排布式为[Kr]4p65s25p2,故A错误;
B.由分析可知,焙烧的主要目的是将塑料转化为气体除去,故B错误;
C.设混合物中PbS和S的物质的量分别为xmol和ymol,由质量可得:239x+32y=27.1,由得
失电子数目守恒可得:x=y,解联立方程可得x=y=0.1,则反应①转移电子数目为0.1mol×2×N mol—
A
1=0.2N ,故C错误;
A
D.由分析可知,二氧化锡与焦炭在高温下反应生成锡和一氧化碳,反应的化学方程式为
2C+SnO=====Sn+2CO↑,故D正确;
2
4.湖南省有众多国家级非物质文化遗产,如湘绣、醴陵彩瓷、苗银锻造工艺、安化黑茶等。下
列说法错误的是
A. 技艺精湛的湘绣,绣线分为丝线、线线、织花线、金银线等,其中丝线的主要成分是蛋白
质
B. 陶瓷的生产以黏土和石灰石为主要原料
C. 苗族银饰锻制工艺需要使用较多的银质材料,银质材料在常温下化学性质比较稳定
D. 安化黑茶制作中的发酵工序涉及了氧化还原反应
答案:B
解析:A.丝线是一种用蚕丝制成的线,主要成分是蛋白质,A正确;
B.生产陶瓷的主要原料是黏土,不需要使用石灰石,B错误;
C.银的金属活动性顺序在氢后面,所以银质材料在常温下化学性质比较稳定,C正确;
D.黑茶制作的基本工艺流程是杀青、初揉、渥堆、复揉、烘焙,其中渥堆是发酵工序,涉及氧化还原反应,D正确;
5.下列各组离子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式正
确的是
选项 离子组 加入试剂 加入试剂后发生的离子反应
A Fe2+、NO NH NaHSO 3Fe2++NO 4H+=3Fe3++NO↑+2HO
、 4 + 2
Ca2++2HCO 2OH-=2HO+CaCO ↓
B Ca2+、HCO Cl- 少量NaOH(aq) + 2 3
、 +CO
C K+、HCO AlO 通入少量CO 2AlO+3HO+CO=2Al(OH) ↓+CO
、 2 2 2 3
2NH+SO+Ba2++2OH-=2NH ∙HO+
D NH、Al3+、SO 少量Ba(OH) 3 2
2 BaSO↓
4
答案:A
解析:A.NO ,Fe2+能被硝酸氧化成Fe3+,其反应为3Fe2++NO +=3Fe3++
在酸性条件下具有强氧化性 +4H
NO↑+2HO,A项正确;
2
B.根据以少定多原则,向碳酸氢钙溶液中加入少量NaOH溶液,离子方程式为Ca2++HCO
+
OH-=HO+CaCO ↓,B项错误;
2 3
C.AlO和HCO +HO+HCO Al(OH) ↓+CO
不能共存,AlO 2 = 3 ,C项错误;
D.向含有NH、Al3+的溶液中加入少量Ba(OH) ,Al3+结合OH-能力比NH强,所以Al3+先反应,
2
离子方程式为:3Al3++3SO+3Ba2++6OH-=3BaSO+2Al(OH) ↓,D项错误;
4 3
6. 下列离子方程式正确的是
A. 磁性氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++H O
2
B. 四氯化钛的浓溶液制备水合二氧化钛:Ti4++(x+2)H O=TiO·xH O↓+4H+
2 2 2
C. 水玻璃中通入少量CO:NaSiO+CO +H O=CO SiO↓+2Na+
2 2 3 2 2 +H2 3
D. 酸性KMnO 溶液滴定双氧水:2MnO O+6H+=2Mn2++3O ↑+4H O
4 +H2 2 2 2
答案:B
解析:A.氧化亚铁有还原性,稀硝酸有氧化性,两者发生氧化还原反应,反应的离子方程式
为:3FeO+10H++NO Fe3++NO↑+5HO,A错误;
=3 2
B.四氯化钛的浓溶液制备水合二氧化钛利用其水解:Ti4++(x+2)H O=TiO·xH O↓+4H+,B正
2 2 2
确;
C.硅酸钠为可溶性盐,离子方程式中应拆成离子形式,正确的离子方程式为:SiO +H O=
+CO2 2
CO SiO↓,C错误;
+H2 3
D.酸性KMnO 溶液滴定双氧水,双氧水被氧化得到氧气,反应的离子方程式为
4
2MnO O+6H+=2Mn2++5O ↑+8H O,D错误;
+5H2 2 2 2
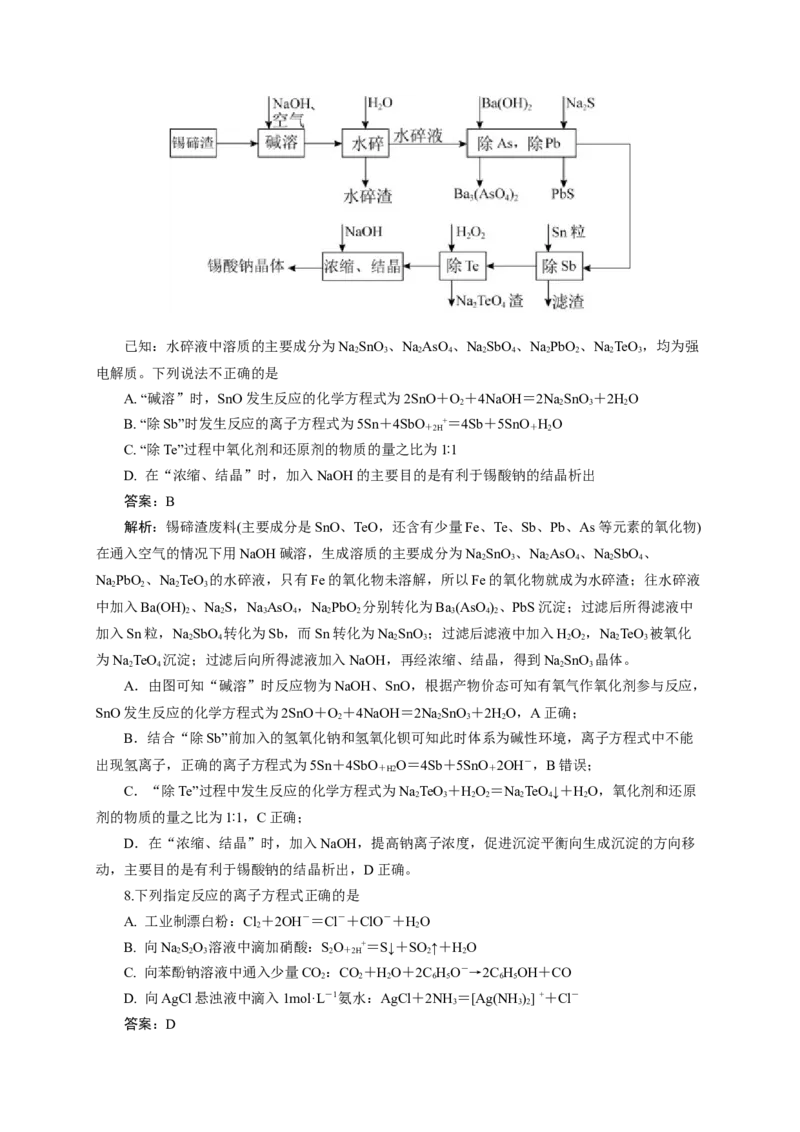
7.锡酸钠晶体(Na SnO ∙3HO)在染料工业上用作媒染剂。以锡碲渣废料(主要成分是SnO、
2 3 2
TeO,还含有少量Fe、Te、Sb、Pb、As等元素的氧化物)为原料,制备锡酸钠晶体的工艺流程如图:已知:水碎液中溶质的主要成分为NaSnO 、NaAsO 、NaSbO 、NaPbO 、NaTeO ,均为强
2 3 2 4 2 4 2 2 2 3
电解质。下列说法不正确的是
A. “碱溶”时,SnO发生反应的化学方程式为2SnO+O+4NaOH=2NaSnO +2HO
2 2 3 2
B. “除Sb”时发生反应的离子方程式为5Sn+4SbO +=4Sb+5SnO HO
+2H + 2
C. “除Te”过程中氧化剂和还原剂的物质的量之比为1∶1
D. 在“浓缩、结晶”时,加入NaOH的主要目的是有利于锡酸钠的结晶析出
答案:B
解析:锡碲渣废料(主要成分是SnO、TeO,还含有少量Fe、Te、Sb、Pb、As等元素的氧化物)
在通入空气的情况下用NaOH碱溶,生成溶质的主要成分为NaSnO 、NaAsO 、NaSbO 、
2 3 2 4 2 4
NaPbO 、NaTeO 的水碎液,只有Fe的氧化物未溶解,所以Fe的氧化物就成为水碎渣;往水碎液
2 2 2 3
中加入Ba(OH) 、NaS,NaAsO ,NaPbO 分别转化为Ba (AsO)、PbS沉淀;过滤后所得滤液中
2 2 3 4 2 2 3 4 2
加入Sn粒,NaSbO 转化为Sb,而Sn转化为NaSnO ;过滤后滤液中加入HO,NaTeO 被氧化
2 4 2 3 2 2 2 3
为NaTeO 沉淀;过滤后向所得滤液加入NaOH,再经浓缩、结晶,得到NaSnO 晶体。
2 4 2 3
A.由图可知“碱溶”时反应物为NaOH、SnO,根据产物价态可知有氧气作氧化剂参与反应,
SnO发生反应的化学方程式为2SnO+O+4NaOH=2NaSnO +2HO,A正确;
2 2 3 2
B.结合“除Sb”前加入的氢氧化钠和氢氧化钡可知此时体系为碱性环境,离子方程式中不能
出现氢离子,正确的离子方程式为5Sn+4SbO O=4Sb+5SnO 2OH-,B错误;
+H2 +
C.“除Te”过程中发生反应的化学方程式为NaTeO +HO=NaTeO ↓+HO,氧化剂和还原
2 3 2 2 2 4 2
剂的物质的量之比为1∶1,C正确;
D.在“浓缩、结晶”时,加入NaOH,提高钠离子浓度,促进沉淀平衡向生成沉淀的方向移
动,主要目的是有利于锡酸钠的结晶析出,D正确。
8.下列指定反应的离子方程式正确的是
A. 工业制漂白粉:Cl+2OH-=Cl-+ClO-+HO
2 2
B. 向NaSO 溶液中滴加硝酸:SO +=S↓+SO ↑+HO
2 2 3 2 +2H 2 2
C. 向苯酚钠溶液中通入少量CO:CO+HO+2C HO-→2C HOH+CO
2 2 2 6 5 6 5
D. 向AgCl悬浊液中滴入1mol·L-1氨水:AgCl+2NH =[Ag(NH)] ++Cl-
3 3 2
答案:D解析:A.工业上向石灰乳中通氯气制漂白粉,离子反应式为Cl+Ca(OH) =Ca2++ClO-+Cl-
2 2
+HO,A错误;
2
B.稀硝酸有氧化性,SO 和S单质会被继续氧化,不能稳定存在,B错误;
2
C.苯酚的酸性强于碳酸氢根,弱于碳酸,则向苯酚钠溶液中通入少量二氧化碳,离子反应式
为CO+HO+C HO-→C HOH+HCO
2 2 6 5 6 5 ,C错误;
D.氨气可与难溶于水的氯化银结合生成可溶于水的络合物[Ag(NH)] Cl,D正确;
3 2
9.下列离子方程式正确的是
A.用稀盐酸处理铜器表面的铜锈:CuO+2H+=Cu2++HO
2
B.用醋酸和淀粉-KI溶液检验加碘盐中的IO IO -+6H+=3I+3HO
: +5I 2 2
C.金属铜溶于氨水和过氧化氢混合溶液:Cu+HO+4NH ∙HO=[Cu(NH )]2++2OH-+4HO
2 2 3 2 3 4 2
D.用银作阴极电解稀盐酸:2Ag+2H+=====H↑+2Ag+
2
答案:C
解析:A.铜锈的主要成分是Cu (OH) CO 而不是CuO,A错误;
2 2 3
B.醋酸属于弱酸,在离子方程式中不能拆开,B错误;
C.金属铜溶于氨水和过氧化氢混合溶液的离子方程式为Cu+HO+4NH ∙HO=
2 2 3 2
[Cu(NH )]2++2OH-+4HO,C正确;
3 4 2
D.电解池属于外加电流的阴极保护法,阴极本身不参与电极反应,D错误;
10.某水溶液中只可能含有下列离子中的若干种:K+、Mg2+、Ca2+、Ba2+、NH、Cl−、NO SO
、
和CO
。现每次取10mL进行实验:
①第一份加入足量NaOH后加热,收集到气体1.12L(标准状况下)
②第二份加入足量BaCl 溶液后得干燥沉淀6.27g,沉淀经足量盐酸洗涤,干燥后剩余2.33g
2
下列说法错误的是
A.原溶液中一定不含有Mg2+、Ba2+、Ca2+
B.无法确定原溶液中是否含有Cl−和NO
C.原溶液中一定含有SO和CO
,且浓度分别为1mol/L、2mol/L
D.要判断原溶液中是否含有K+,需再做焰色试验确定
答案:D
解析:根据实验①现象可知气体为氨气,则含有NH,且铵根的物质的量=气体物质的量==
=0.05mol,且溶液中不含Mg2+;
根据实验②现象判断,该溶液中含有SO和CO 质量,计算出硫酸
,经足量盐酸洗涤,干燥后剩余2.33g为BaSO4
根的物质的量为= =0.01mol,碳酸根的物质的量==0.02mol;由于SO和CO 2+、Ba2+不共存,
与Ca
则溶液中一定不含有Ca2+、Ba2+;由溶液呈电中性,已知一定存在的阳离子K+的物质的量为
0.05×1=0.05mol,阴离子为0.01mol×2+0.02mol×2=0.06mol,则一定存在K+,Cl−、NO
不能确定;
A.依据以上分析可知,原溶液中一定不含有Mg2+、Ba2+、Ca2+,故A正确;
B.依据以上分析可知,无法确定原溶液中是否含有Cl−和NO
,故B正确;
C.原溶液中一定含有SO和CO c===1mol/L、c===2mol/L,故C正确;
,且浓度分别为D.由溶液呈电中性,已知一定存在阳离子K+,故D错误;
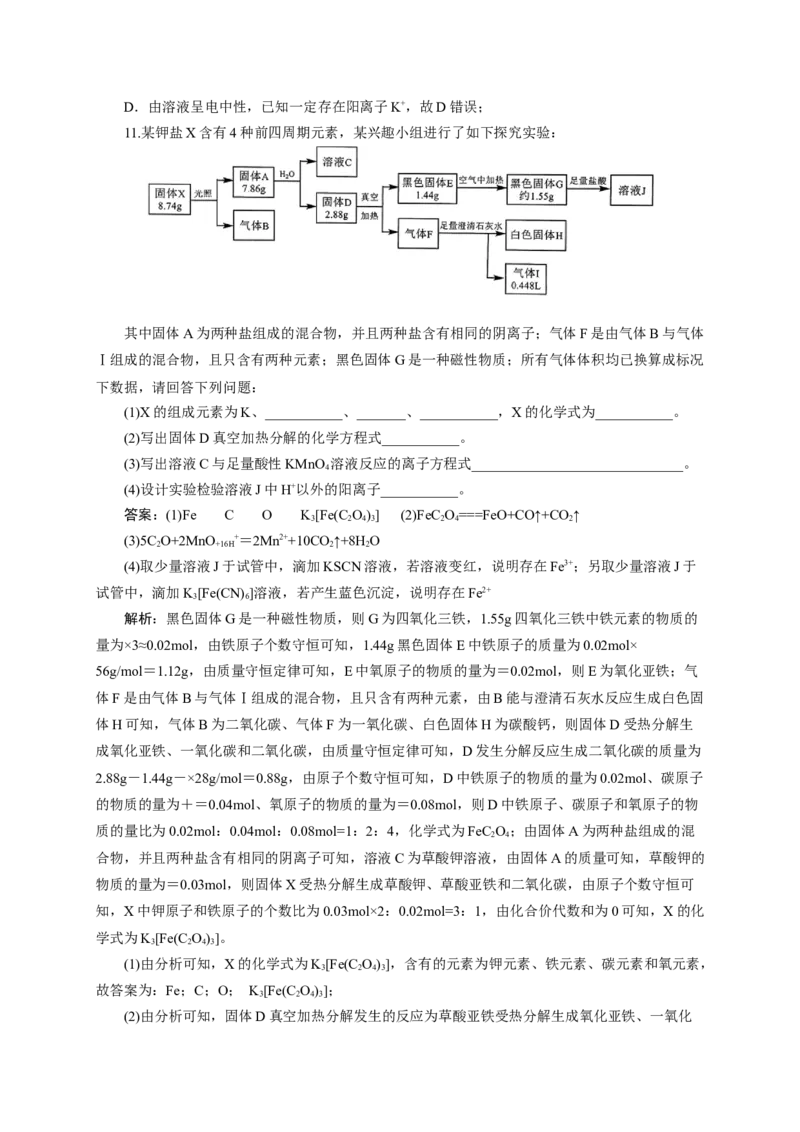
11.某钾盐X含有4种前四周期元素,某兴趣小组进行了如下探究实验:
其中固体A为两种盐组成的混合物,并且两种盐含有相同的阴离子;气体F是由气体B与气体
Ⅰ组成的混合物,且只含有两种元素;黑色固体G是一种磁性物质;所有气体体积均已换算成标况
下数据,请回答下列问题:
(1)X的组成元素为K、___________、_______、___________,X的化学式为___________。
(2)写出固体D真空加热分解的化学方程式___________。
(3)写出溶液C与足量酸性KMnO 溶液反应的离子方程式______________________________。
4
(4)设计实验检验溶液J中H+以外的阳离子___________。
答案:(1)Fe C O K [Fe(C O)] (2)FeC O===FeO+CO↑+CO ↑
3 2 4 3 2 4 2
(3)5C O+2MnO +=2Mn2++10CO ↑+8H O
2 +16H 2 2
(4)取少量溶液J于试管中,滴加KSCN溶液,若溶液变红,说明存在Fe3+;另取少量溶液J于
试管中,滴加K[Fe(CN) ]溶液,若产生蓝色沉淀,说明存在Fe2+
3 6
解析:黑色固体G是一种磁性物质,则G为四氧化三铁,1.55g四氧化三铁中铁元素的物质的
量为×3≈0.02mol,由铁原子个数守恒可知,1.44g黑色固体E中铁原子的质量为0.02mol×
56g/mol=1.12g,由质量守恒定律可知,E中氧原子的物质的量为=0.02mol,则E为氧化亚铁;气
体F是由气体B与气体Ⅰ组成的混合物,且只含有两种元素,由B能与澄清石灰水反应生成白色固
体H可知,气体B为二氧化碳、气体F为一氧化碳、白色固体H为碳酸钙,则固体D受热分解生
成氧化亚铁、一氧化碳和二氧化碳,由质量守恒定律可知,D发生分解反应生成二氧化碳的质量为
2.88g-1.44g-×28g/mol=0.88g,由原子个数守恒可知,D中铁原子的物质的量为0.02mol、碳原子
的物质的量为+=0.04mol、氧原子的物质的量为=0.08mol,则D中铁原子、碳原子和氧原子的物
质的量比为0.02mol:0.04mol:0.08mol=1:2:4,化学式为FeC O;由固体A为两种盐组成的混
2 4
合物,并且两种盐含有相同的阴离子可知,溶液C为草酸钾溶液,由固体A的质量可知,草酸钾的
物质的量为=0.03mol,则固体X受热分解生成草酸钾、草酸亚铁和二氧化碳,由原子个数守恒可
知,X中钾原子和铁原子的个数比为0.03mol×2:0.02mol=3:1,由化合价代数和为0可知,X的化
学式为K[Fe(C O)]。
3 2 4 3
(1)由分析可知,X的化学式为K[Fe(C O)],含有的元素为钾元素、铁元素、碳元素和氧元素,
3 2 4 3
故答案为:Fe;C;O; K[Fe(C O)];
3 2 4 3
(2)由分析可知,固体D真空加热分解发生的反应为草酸亚铁受热分解生成氧化亚铁、一氧化碳和二氧化碳,反应的化学方程式为FeC O===FeO+CO↑+CO ↑,故答案为:
2 4 2
FeC O===FeO+CO↑+CO ↑;
2 4 2
(3)由分析可知,溶液C为草酸钾溶液,草酸钾溶液与足量酸性高锰酸钾溶液反应生成硫酸钾、
硫酸锰、二氧化碳和水,反应的离子方程式为5C O+2MnO +=2Mn2++10CO ↑+8H O,故答案为:
2 +16H 2 2
5C O+2MnO +=2Mn2++10CO ↑+8H O;
2 +16H 2 2
(4)由分析可知,黑色固体D为四氧化三铁,四氧化三铁与足量盐酸反应生成氯化铁、氯化亚
铁和水,则溶液J为盐酸、氯化铁和氯化亚铁的混合溶液,检验溶液中铁离子和亚铁离子的操作为
取少量溶液J于试管中,滴加KSCN溶液,若溶液变红,说明存在Fe3+;另取少量溶液J于试管中,
滴加K[Fe(CN) ]溶液,若产生蓝色沉淀,说明存在Fe2+,故答案为:取少量溶液J于试管中,滴加
3 6
KSCN溶液,若溶液变红,说明存在Fe3+;另取少量溶液J于试管中,滴加K[Fe(CN) ]溶液,若产
3 6
生蓝色沉淀,说明存在Fe2+。
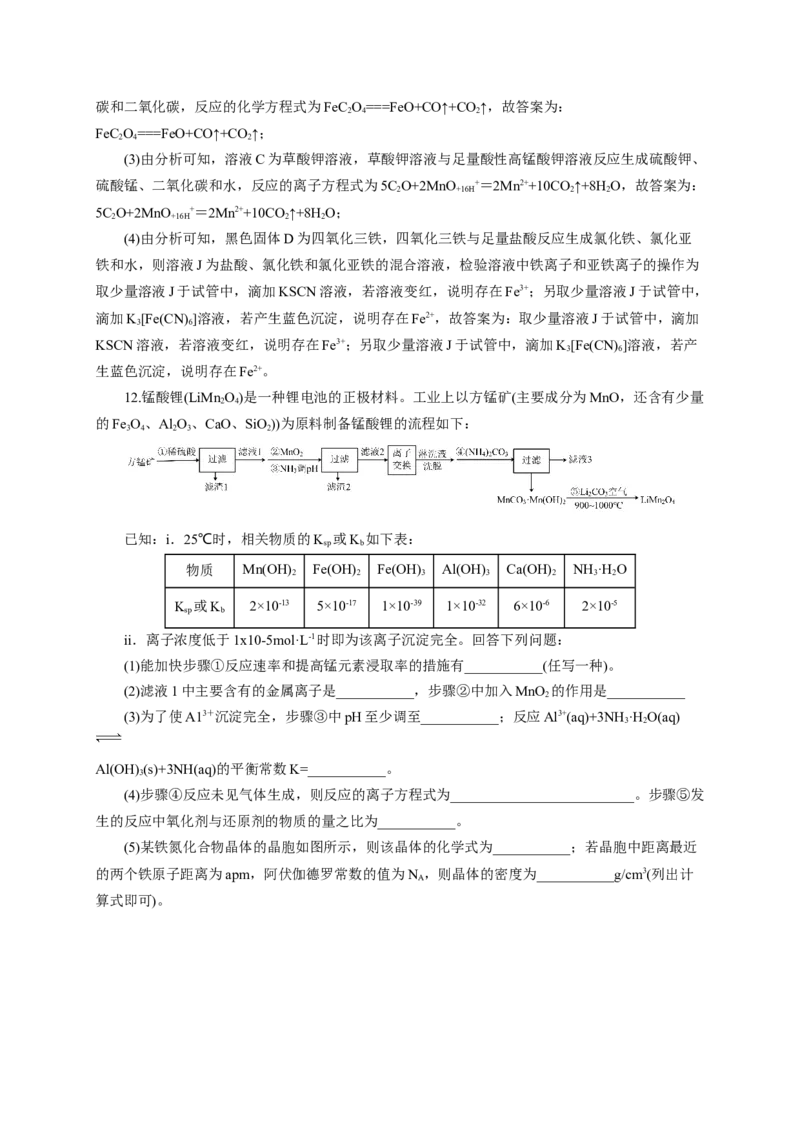
12.锰酸锂(LiMn O)是一种锂电池的正极材料。工业上以方锰矿(主要成分为MnO,还含有少量
2 4
的Fe O、Al O、CaO、SiO))为原料制备锰酸锂的流程如下:
3 4 2 3 2
已知:i.25℃时,相关物质的K 或K 如下表:
sp b
物质 Mn(OH) Fe(OH) Fe(OH) Al(OH) Ca(OH) NH ·H O
2 2 3 3 2 3 2
K 或K 2×10-13 5×10-17 1×10-39 1×10-32 6×10-6 2×10-5
sp b
ii.离子浓度低于1x10-5mol·L-1时即为该离子沉淀完全。回答下列问题:
(1)能加快步骤①反应速率和提高锰元素浸取率的措施有___________(任写一种)。
(2)滤液1中主要含有的金属离子是___________,步骤②中加入MnO 的作用是___________
2
(3)为了使A13+沉淀完全,步骤③中pH至少调至___________;反应Al3+(aq)+3NH·H O(aq)
3 2
Al(OH) (s)+3NH(aq)的平衡常数K=___________。
3
(4)步骤④反应未见气体生成,则反应的离子方程式为__________________________。步骤⑤发
生的反应中氧化剂与还原剂的物质的量之比为___________。
(5)某铁氮化合物晶体的晶胞如图所示,则该晶体的化学式为___________;若晶胞中距离最近
的两个铁原子距离为apm,阿伏伽德罗常数的值为N ,则晶体的密度为___________g/cm3(列出计
A
算式即可)。答案:(1)粉碎方锰矿(或升温、适当提高硫酸浓度等)
(2)Fe2+、Fe3+、Al3+、Mn2+ 将Fe2+氧化成Fe3+ (3)5 8×1017
(4)2Mn2++3CO O=MnCO ·Mn(OH) ↓+2HCO ∶4 (5) Fe N
+2H2 3 2 3 4
解析:由题给流程可知,方锰矿用稀硫酸酸溶时,金属氧化物与稀硫酸反应转化为硫酸盐,二
氧化硅不与稀硫酸反应,过滤得到含有硫酸钙、二氧化硅的滤渣1和含有可溶性硫酸盐的滤液1;
向滤液1中加入二氧化锰将溶液中亚铁离子氧化为铁离子后,加入氨水调节溶液的pH,将溶液中
铁离子、铝离子转化为氢氧化铁、氢氧化铝沉淀,过滤得到含有氢氧化铁、氢氧化铝的滤渣2和含
有硫酸锰的滤液2,滤液2经离子交换、淋洗涤液洗脱后,加入碳酸铵溶液将溶液中的锰离子转化
为碱式碳酸锰沉淀,过滤得到碱式碳酸锰和滤液3,碱式碳酸锰和碳酸锂在高温条件下在空气中煅
烧制得锰酸锂,据此分析解答。
(1)能加快步骤①反应速率和提高锰元素浸取率的措施有:粉碎方锰矿(或升温、适当提高硫酸
浓度等);
(2)由以上分析可知滤液1中含相应金属的硫酸盐,主要含有的金属离子Fe2+、Fe3+、Al3+、
Mn2+,步骤②中加入MnO 将溶液中亚铁离子氧化为铁离子;
2
(3)由分析可知,加入氨水调节溶液pH的目的是将溶液中铁离子、铝离子转化为氢氧化铁、氢
氧化铝沉淀,而锰离子不转化为氢氧化锰沉淀,由氢氧化铝的溶度积可知,溶液中氢氧根离子不小
于=1×10-9mol/L,由氢氧化锰的溶度积可知溶液中氢氧根离子浓度不大于=1×10-6mol/L,则溶液的
nH范围为5~8,pH至少调至5;由方程式可知,反应的平衡常数K====8×1017;
(4)步骤④中加入碳酸铵溶液将溶液中的锰离子转化为碱式碳酸锰沉淀,反应未见气体生成,可
知生成碳酸氢根离子,反应离子方程式为:2Mn2++3CO O=MnCO ·Mn(OH) ↓+2HCO ⑤发生
+2H2 3 2 ;步骤
的反应2LiCO+4MnCO ∙Mn(OH) +3O===========4LiMn O+6CO↑+4HO ,反应中氧化剂
2 3 3 2 2 2 4 2 2
为氧气,还原剂为MnCO ·Mn(OH) ,两者物质的量之比为3∶4;
3 2
(5)由晶胞结构可知Fe位于顶点和面心,个数为:8×+6×=4;N位于体心个数为1,则Fe:
N=4∶1,化学式为:Fe N;晶胞中距离最近的两个铁原子距离为面对角线的一半,为a pm,则晶胞
4
边长apm,晶胞的质量==g,晶胞体积=(a×10-10)3cm3,则晶胞密度=。