文档内容
2024届高考化学一轮复习限时训练:《化学物质及其变化》专题19
1.下列所加物质的作用与其还原性有关的是
A. 腌咸菜加氯化钠 B. 红酒中添加SO
2
C 食用盐中加碘酸钾 D. 泡打粉加碳酸氢钠
2.工业生产中,主要反应原理不涉及氧化还原反应的是
A. 海水提溴 B. 纯碱工业 C. 硫酸工业 D. 合成氨工业
3.有一澄清透明的溶液,只可能含有大量的Fe3+、Fe2+、H+、AlO、Al3+、CO NO
、 七种离子中的几种,向
1mol·L-1NaOH溶液一定体积后才产生沉淀。则下列判断正确的是
该溶液中逐滴滴入
A. 溶液中可能含有AlO B. 溶液中可能含有CO
C. 溶液中一定不含Al3+ D. 溶液中一定含有NO
4.常温下,下列各组离子在指定溶液中一定能大量共存的是
A. =1×10-14的溶液:Ca2+、Na+、HCO NO
、
B. 0.1 mol·L-1 KOH溶液:AlO、Na+、I-、SO
C. 能使pH试纸显深红色的溶液:Fe3+、Cl-、Ba2+、SCN-
D. 0.1 mol·L-1NaClO溶液:HS-、Na+、Cl-、CO
5.下列实验所涉及反应的离子方程式错误的是
A. 过氧化钠与水反应:2Na2O +2HO=4Na++4OH-+O↑
2 2 2
B. 向海带灰浸出液中滴加几滴硫酸酸化的过氧化氢溶液:2I-+HO+2H+=I+2HO
2 2 2 2
C. 向硫酸铜溶液中通入HS:Cu2++HS=CuS↓+2H+
2 2
D. 用酸性高锰酸钾标准溶液滴定草酸:2MnO ++C O=2Mn2++10CO↑+8HO
+16H 2 2 2
6.下列离子方程式书写正确的是
A. 将过量Cl 通入到FeBr 溶液中:2Fe2++Cl=2Fe3++2Cl-
2 2 2
B. Fe O 溶于HI溶液:Fe O+8H+=Fe2++2Fe3++4HO
3 4 3 4 2
C. 澄清石灰水与过量的小苏打溶液混合:Ca2++2OH-+2HCO CaCO ↓+CO 2HO
= 3 + 2
D. 向氯化铝溶液中滴入过量的氨水Al3++4NH ∙HO=AlO+4NH+2HO
3 2 2
7.下列指定反应的离子方程式错误的是
A.酸化NaIO 和NaI的混合溶液:5I-+IO +=3I+3HO
3 +6H 2 2
B.Al (SO ) 与过量氨水反应:Al3++3NH ∙HO=Al(OH) ↓+3NH
2 4 3 3 2 3
C.室温下用稀HNO 溶解铜:3Cu+8H++2NO 3Cu2++NO↑+4HO
3 = 2
D.向沸水中滴加饱和FeCl 溶液得Fe(OH) 胶体:Fe3++3HO= Fe(OH) ↓+3H+
3 3 2 3
8.下列化学反应的离子方程式不正确的是
A.将少量SO 气体通入足量的NaClO溶液中:SO +ClO-+ H O=SO
2 2 2 +2HClO
B.向偏铝酸钠溶液中加入小苏打溶液:HCO +H O=Al(OH) ↓ +CO
+AlO 2 3
C.向Ba(OH) 溶液中滴加NH HSO 溶液至刚好沉淀完全:Ba2++ 2OH-+ NH+ H++ SO=
2 4 4
BaSO↓+ NH ·H O+ H O
4 3 2 2D.稀硝酸中加入过量的铁屑:3Fe+ 8H+ +2NO 2+ 2NO↑+ 4H O
= 3Fe 2
9.某溶液中可能存在Br-、CO 3+、I-、Mg2+、Na+等7种离子中的某几种,现取该溶液进
、SO、Al
行实验,得到如下现象:①向溶液中滴加足量氯水后,溶液变橙黄色,且有无色气泡冒出,②向所
得色溶液中加入足量BaCl 溶液,无沉淀生成,③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色,
2
据此可以推断:该溶液中肯定不存在的离子组是
A. Al3+、Mg2+、I-、SO 2+、Na+、CO -
B. Mg 、I
C. Al3+、Na+、SO - D. Na+、CO Br-、I-
、I 、
10.(双选)下列物质的用途是基于其氧化性的是
A.氨用作制冷剂 B.次氯酸钙用于生活用水的消毒
C.用铝槽车运输浓硝酸 D.生石灰用于废气的脱硫
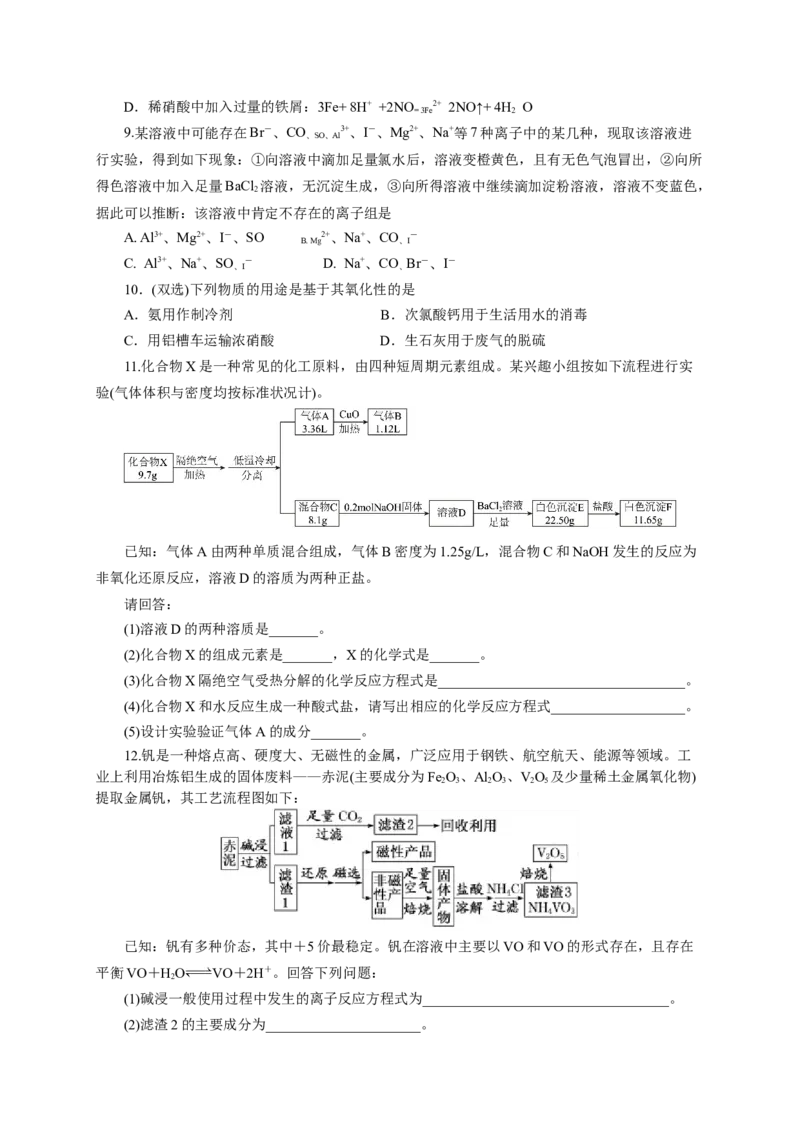
11.化合物X是一种常见的化工原料,由四种短周期元素组成。某兴趣小组按如下流程进行实
验(气体体积与密度均按标准状况计)。
已知:气体A由两种单质混合组成,气体B密度为1.25g/L,混合物C和NaOH发生的反应为
非氧化还原反应,溶液D的溶质为两种正盐。
请回答:
(1)溶液D的两种溶质是_______。
(2)化合物X的组成元素是_______,X的化学式是_______。
(3)化合物X隔绝空气受热分解的化学反应方程式是___________________________________。
(4)化合物X和水反应生成一种酸式盐,请写出相应的化学反应方程式___________________。
(5)设计实验验证气体A的成分_______。
12.钒是一种熔点高、硬度大、无磁性的金属,广泛应用于钢铁、航空航天、能源等领域。工
业上利用冶炼铝生成的固体废料——赤泥(主要成分为Fe O、Al O、VO 及少量稀土金属氧化物)
2 3 2 3 2 5
提取金属钒,其工艺流程图如下:
已知:钒有多种价态,其中+5价最稳定。钒在溶液中主要以VO和VO的形式存在,且存在
平衡VO+HO VO+2H+。回答下列问题:
2
(1)碱浸一般使用过程中发生的离子反应方程式为___________________________________。
(2)滤渣2的主要成分为______________________。(3)非磁选产品焙烧后的产物加入盐酸溶解时能否过量_________;理由是________________。
(4)对滤渣3进行焙烧时的化学反应方程式为_____________________________________。
(5)设计实验验证磁性产品的主要成分_______________。