文档内容
2025届高三化学一轮专题复习讲义(08)
专题三 基本理论
3-1 反应热(1课时)
【复习目标】
1.通过生活中实例,辨识化学反应中的能量变化,解释化学反应中能量变化的本质。
2.能进行反应焓变的简单计算,能用热化学方程式表示反应中的能量变化。
3.能运用反应焓变来选择和利用化学反应。
【重点突破】
1.能辨识常见吸热、放热反应及产生能量变化的原因。
2.正确书写热化学方程式,掌握盖斯定律的应用。
【真题再现】
例1.(2023·江苏高考)合成尿素[CO(NH)]是利用CO 的途径之一。尿素合成主要通过下列反应
2 2 2
实现:
反应I:2NH (g)+CO (g)=== NH COONH(l)
3 2 2 4
反应Ⅱ:NH COONH(l)=== CO(NH)(l)+H O(l)
2 4 2 2 2
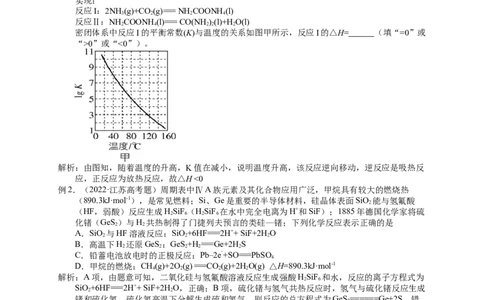
密闭体系中反应I的平衡常数(K)与温度的关系如图甲所示,反应I的△H= (填“=0”或
“>0”或“<0”)。
解析:由图知,随着温度的升高,K值在减小,说明温度升高,该反应逆向移动,逆反应是吸热反
应,正反应为放热反应,故△H <0
例2.(2022·江苏高考题)周期表中ⅣA族元素及其化合物应用广泛,甲烷具有较大的燃烧热
(890.3kJ·mol-1),是常见燃料;Si、Ge是重要的半导体材料,硅晶体表面SiO 能与氢氟酸
2
(HF,弱酸)反应生成HSiF(HSiF 在水中完全电离为H+和SiF);1885年德国化学家将硫
2 6 2 6
化锗(GeS )与H 共热制得了门捷列夫预言的类硅—锗;下列化学反应表示正确的是
2 2
A.SiO 与HF溶液反应:SiO+6HF===2H++ SiF+2HO
2 2 2
B.高温下H 还原GeS :GeS +H ===Ge+2HS
2 2 2 2 2
C.铅蓄电池放电时的正极反应:Pb–2eˉ+SO===PbSO
4
D.甲烷的燃烧:CH(g)+2O(g) ===CO(g)+2HO(g) △H=890.3kJ·mol-1
4 2 2 2
解析:A项,由题意可知,二氧化硅与氢氟酸溶液反应生成强酸HSiF 和水,反应的离子方程式为
2 6
SiO+6HF===2H++ SiF+2HO,正确;B项,硫化锗与氢气共热反应时,氢气与硫化锗反应生成
2 2
锗和硫化氢,硫化氢高温下分解生成硫和氢气,则反应的总方程式为GeS======Ge+2S,错
2
误;C项,铅蓄电池放电时,二氧化铅为正极,酸性条件下在硫酸根离子作用下二氧化铅得到
电子发生还原反应生成硫酸铅和水,电极反应式为正极反应Pb+2eˉ+SO+4H+===PbSO +2H O,
4 2
错误;D项,由题意可知,1mol甲烷完全燃烧生成二氧化碳和液态水放出热量为890.3kJ,反
应的热化学方程式为CH(g)+2O(g) ===CO(g)+2HO(g) △H=-890.3kJ·mol-1,错误。
4 2 2 2
答案:A
例3.(2021·江苏高考)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生
2 3
产HNO ;HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件
3 3
下 , N 与 O 反 应 生 成 NO , NO 进 一 步 氧 化 生 成 NO 。 2NO(g)+O (g)===2NO (g)
2 2 2 2 2
ΔH=-116.4kJ·mol-1。大气中过量的NO 和水体中过量的NH +、NO -均是污染物。通过催化还原
x 4 3
的方法,可将烟气和机动车尾气中的NO转化为N ,也可将水体中的NO -转化为N 。对于反
2 3 2
应2NO(g)+O (g) 2NO (g),下列说法正确的是
2 2
A.该反应的ΔH<0,ΔS<0B.反应的平衡常数可表示为K=
C.使用高效催化剂能降低反应的焓变
D.其他条件相同,增大 ,NO的转化率下降
解析:A项,2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1,反应气体物质的量减少,ΔS<0,正确;
2 2
B项,2NO(g)+O (g) 2NO(g)反应的平衡常数可表示为K= ,错误;C项,使用
2 2
高效催化剂,反应的焓变不变,错误;D项,其他条件相同,增大 ,NO的转化率增大,
错误。
答案:A
例4.(2020·江苏卷)反应 可用于纯硅的制备。下列有关该
反应的说法正确的是
A.该反应△H>0、△S>0
B.该反应的平衡常数K=
C.高温下反应每生成1 mol Si需消耗
D.用E表示键能,该反应
解析:A项,SiCl 、H 、HCl为气体,且反应前气体系数之和小于反应后气体系数之和,因此该反
4 2
应为熵增,即△S>0,错误;B 项,根据化学平衡常数的定义,该反应的平衡常数 K=
,正确;C项,题中说的是高温,不是标准状况下,因此不能直接用22.4L·mol-1
计算,错误;D项,△H=反应物键能总和-生成物键能总和,即△H=4E(Si-Cl)+2E(H-H)
-4E(H-Cl)-2E(Si-Si),错误。
答案:B
例5.(2019·江苏卷)“硫碘循环法”是分解水制备氢气的研究热点,涉及下列两个反应:
反应Ⅰ:SO (g)+I (aq)+2H O(l)=2HI(aq)+H SO (aq) △H
2 2 2 2 4 1
反应Ⅱ:HI(aq)=1/2H (g)+1/2I (aq) △H
2 2 2
①反应:SO (g)+2HO(l)=HSO (aq)+H (g)的△H=_________(用△H、△H 表示)。
2 2 2 4 2 1 2
解析:运用盖斯定律进行计算,将反应Ⅰ和反应Ⅱ进行叠加即可。
答案:ΔH+2ΔH
1 2
小结:主要涉及反应热的判断、热化学方程式的书写和盖斯定律的应用。
【知能整合】
1.热化学方程式书写
(1)步骤(2)注意事项
2.有关反应热的计算
(1)根据物质具有的能量来计算:ΔH=E(总生成物)-E(总反应物)
(2)根据化学键的断裂与形成计算:ΔH=反应物的键能总和-生成物的键能总和
利用键能计算反应热的关键,就是要算清物质中化学键的数目,清楚中学阶段常见单质、
化合物中所含共价键的种类和数目。
物质 CO CH P SiO 石墨 金刚石 S Si
2 4 4 2 8
(化学键) (C=O) (C—H) (P—P) (Si—O) (C—C) (C—C) (S—S) (Si—Si)
每个微粒所含
2 4 6 4 1.5 2 8 2
化学键数目
(3)根据化学反应过程中的能量变化来计算
图示
意义 a表示正反应的活化能;b表示逆反应的活化能;c表示该反应的反应热
图1:ΔH=(a-b) kJ·mol-1=-c kJ·mol-1,表示放热反应
ΔH
图2:ΔH=(a-b) kJ·mol-1=c kJ·mol-1,表示吸热反应
3.盖斯定律
(1)内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应热是相同的。即:
化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。
(2)意义:间接计算某些反应的反应热。
(3)应用:
转化关系 反应热间的关系aA——→B、A——→B ΔH=aΔH
1 2
A B ΔH=-ΔH
1 2
ΔH=ΔH+ΔH
1 2
【体系再构】
【随堂反馈】
基础训练
1.碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:
①H(g)+I(?)===2HI(g) ΔH=+9.48 kJ·mol-1
2 2
②H(g)+I(?)===2HI(g) ΔH=-26.48 kJ·mol-1
2 2
下列判断正确的是
A.①中的I 为气态,②中的I 为固态
2 2
B.①的反应物总能量比②的反应物总能量低
C.①的产物比②的产物热稳定性好
D.1 mol 固态碘升华时将吸热17 kJ
2.用CH 催化还原NO 可以消除氮氧化物的污染。如:
4 x
①CH(g)+4NO (g)===4NO(g)+CO(g)+2HO(g) ΔH=-574 kJ·mol-1
4 2 2 2
②CH(g)+4NO(g)===2N (g)+CO(g)+2HO(g) ΔH=-1 160 kJ·mol-1
4 2 2 2
下列说法中错误的是
A.等物质的量的CH 在反应①、②中转移电子数相同
4
B.由反应①可推知:CH(g)+4NO (g)===4NO(g)+CO(g)+2HO(l) ΔH>-574 kJ·mol-1
4 2 2 2
C.4NO (g)+2N(g)===8NO(g) ΔH=+586 kJ·mol-1
2 2
D.若用标准状况下4.48 L CH 把NO 还原为N,整个过程中转移的电子总数为1.6N
4 2 2 A
3.研究表明,化学反应中能量变化的本质是化学键的形成和断裂过程中会释放和吸收能量。下图
表示反应2H(g)+O(g)===2H O(g)的能量变化,下列有关说法中错误的是
2 2 2
A.图中的①是指吸收能量,②是指放出能量
B.图示说明反应2H(g)+O(g)===2H O(g)是一个吸热反应
2 2 2
C.图示说明化学键的形成与断裂是化学反应中发生能量变化的主要原因
D.③中a为484
4.下列有关热化学方程式的叙述中,正确的是
A.含20.0gNaOH的稀溶液与足量的稀硫酸完全中和,放出28.7kJ的热量,则表示中和热的热
化学方程式为:2NaOH(aq)+HSO (aq)=Na SO (aq)+2H O(l) ∆H=-114.6 kJ·mol-1
2 4 2 4 2
B.已知热化学方程式: SO (g)+ O(g) SO(g) ∆H=-98.32 kJ·mol-1,在容器中充入
2 2 3
2mol SO 和1mol O 充分反应,最终放出的热量为196.64kJ
2 2
C.已知2H(g)+O(g) =2H O(g) ∆H=-483.6 kJ·mol-1,则H 的燃烧热为241.8 kJ·mol-1
2 2 2 2
D.用稀氨水与稀盐酸进行中和热的测定实验,计算得到的中和热的∆H偏大拓展训练
5.多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为
气态),甲醇与水在钢基催化剂上的反应机理相能量图如下:
下列说法正确的是
A.反应II的热化学方程式为:CO(g)+HO(g)→H (g)+CO (g) ∆H=-Q kJ·mol-1 (Q>0)
2 2 2
B.1 mol CHOH(g)和l mol HO(g)的总能量大于l mol CO(g)和3 mol H(g)的总能量
3 2 2 2
C.选择优良的催化剂降低反应I和II的活化能,有利于减少过程中的能耗
D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂
6.CO 与CH 经催化重整,制得合成气:CH(g)+CO (g) 2CO(g)+2H(g)
2 4 4 2 2
已知上述反应中相关的化学键键能数据如下:
化学键 C—H H—H C ←O(CO)
键能/(kJ·mol-1) 413 745 436 1 075
则该反应的ΔH= 。
分别在v L恒温密闭容器A(恒容)、B(恒压,容积可变)中,加入CH 和CO 各1 mol的混合气体
4 2
两容器中反应达平衡后放出或吸收的热量较多的是 (填“A”或“B”)。
【随堂反馈】答案:
1.B 2.B 3.B 4.D 5.C 6.+120 kJ·mol-1 B
【课后作业】
1.炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成对环境有不良影响的活化氧。
反应过程的能量变化如下图。下列说法不正确的是
A.生成活化氧的总反应是吸热反应
B.反应前后氧元素的化合价发生改变
C.生成活化氧的反应在有水条件下更容易发生
D.反应过程中存在氧氧键的断裂和碳氧键的生成
2.H 与ICl的反应分①、②两步进行,其能量曲线如图所示,下列有关说法错误的是
2
A.反应①、反应②均为放热反应
B.反应①、反应②均为氧化还原反应
C.反应①比反应②的速率慢,与相应正反应的活化能无关
D.反应①、反应②的焓变之和为ΔH=-218kJ·mol-13.苯乙烯的制备
已知下列反应的热化学方程式:
①
②
③
计算反应④C HC H(g)=== C HCH=CH(g)+H(g)的ΔH= 。
6 5 2 5 6 5 2 2 4
4.(1)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下:
反应Ⅰ:2HSO (l)=2SO (g)+2HO(g)+O (g) ΔH=+551 kJ·mol-1
2 4 2 2 2 1
反应Ⅲ:S(s)+O (g)=SO(g) ΔH=-297 kJ·mol-1
2 2 3
反应Ⅱ的热化学方程式: 。
(2)用O 将HCl转化为Cl,可提高效益,减少污染。
2 2
传统上该转化通过如下图所示的催化循环过程实现。
其中,反应①为2HCl(g)+CuO(s) HO(g)+CuCl (s) ΔH;反应②生成1 mol Cl(g)的反应
2 2 1 2
热为ΔH,则总反应的热化学方程式为 (反应热用ΔH 和ΔH 表示)。
2 1 2
5. (1)硝酸厂的尾气直接排放将污染空气,目前科学家探索利用燃料气体中的甲烷等将氮氧化
物还原为氮气和水,其反应机理为
CH(g)+4NO (g)===4NO(g)+CO(g)+2HO(g) ΔH=-574 kJ·mol-1
4 2 2 2
CH(g)+4NO(g)===2N (g)+CO(g)+2HO(g) ΔH=-1160 kJ·mol-1
4 2 2 2
则甲烷直接将NO 还原为N 的热化学方程式为 。
2 2
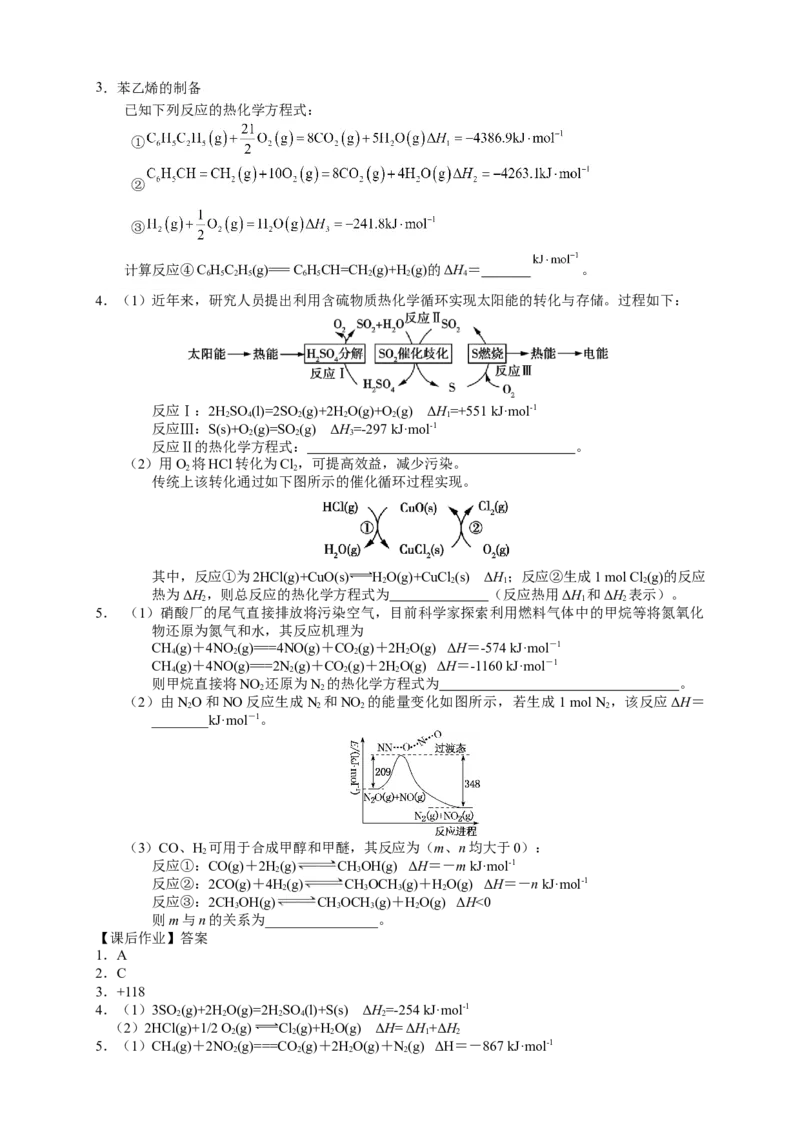
(2)由NO和NO反应生成N 和NO 的能量变化如图所示,若生成1 mol N ,该反应ΔH=
2 2 2 2
________kJ·mol-1。
(3)CO、H 可用于合成甲醇和甲醚,其反应为(m、n均大于0):
2
反应①:CO(g)+2H(g) CHOH(g) ΔH=-m kJ·mol-1
2 3
反应②:2CO(g)+4H(g) CHOCH (g)+HO(g) ΔH=-n kJ·mol-1
2 3 3 2
反应③:2CHOH(g) CHOCH (g)+HO(g) ΔH<0
3 3 3 2
则m与n的关系为________________。
【课后作业】答案
1.A
2.C
3.+118
4.(1)3SO (g)+2HO(g)=2H SO (l)+S(s) ΔH=-254 kJ·mol-1
2 2 2 4 2
(2)2HCl(g)+1/2 O (g) Cl(g)+HO(g) ΔH= ΔH+ΔH
2 2 2 1 2
5.(1)CH(g)+2NO (g)===CO(g)+2HO(g)+N(g) ΔH=-867 kJ·mol-1
4 2 2 2 2(2)-139
(3)n>2m