文档内容
2025届高三化学一轮专题复习讲义(24)
专题六 化学实验和化学计算
6-1 化学实验基础(1课时)
【复习目标】
1.了解化学实验室常用仪器的使用方法和主要用途;掌握必需实验操作技能;
2.熟悉常见离子的检验方法以及常见物质的分离提纯手段;
3.掌握常见气体和简单有机物实验室制备和注意事项。
【重点突破】实验操作或装置规范要求
【真题再现】
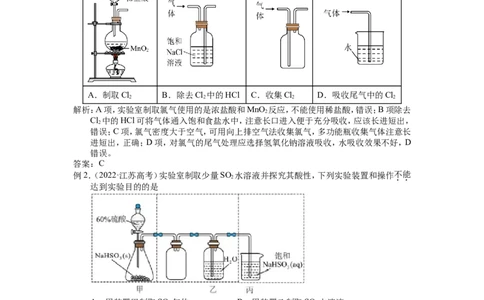
例1.(2023·江苏高考)实验室制取 的实验原理及装置均正确的是
Cl2
A.制取Cl B.除去Cl 中的HCl C.收集Cl D.吸收尾气中的Cl
2 2 2 2
解析:A项,实验室制取氯气使用的是浓盐酸和MnO 反应,不能使用稀盐酸,错误;B项除去
2
Cl 中的HCl可将气体通入饱和食盐水中,注意长口进入便于充分吸收,应该长进短出,
2
错误;C项,氯气密度大于空气,可用向上排空气法收集氯气,多功能瓶收集气体注意长
进短出,正确;D项,对氯气的尾气处理应选择氢氧化钠溶液吸收,水吸收效果不好,D
错误。
答案:C
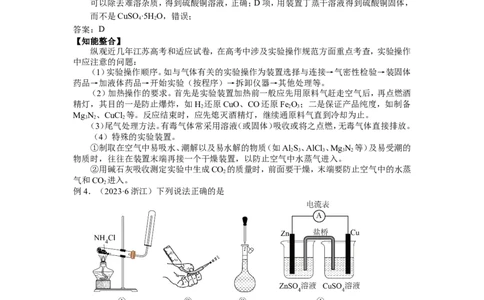
例2.(2022·江苏高考)实验室制取少量SO 水溶液并探究其酸性,下列实验装置和操作不能
2
达到实验目的的是
A.用装置甲制取SO 气体 B.用装置乙制取SO 水溶液
2 2
C.用装置丙吸收尾气中的SO D.用干燥pH试纸检验SO 水溶液的酸性
2 2
解析:A项,60%硫酸和NaHSO(s)可发生反应:HSO +2NaHSO ===NaSO +2SO↑+2H O,因
3 2 4 3 2 4 2 2
此装置甲可以制取SO 气体,正确;B项,气体通入液体时“长进短处”,装置乙可以制
2
取SO 水溶液,正确;C项,SO 不会与饱和NaHSO 溶液发生反应,因此装置丙不能吸收
2 2 3
尾气中的SO ,错误;D项,SO 水溶液显酸性,可用干燥的pH试纸检验其酸性,正确。
2 2
答案:C
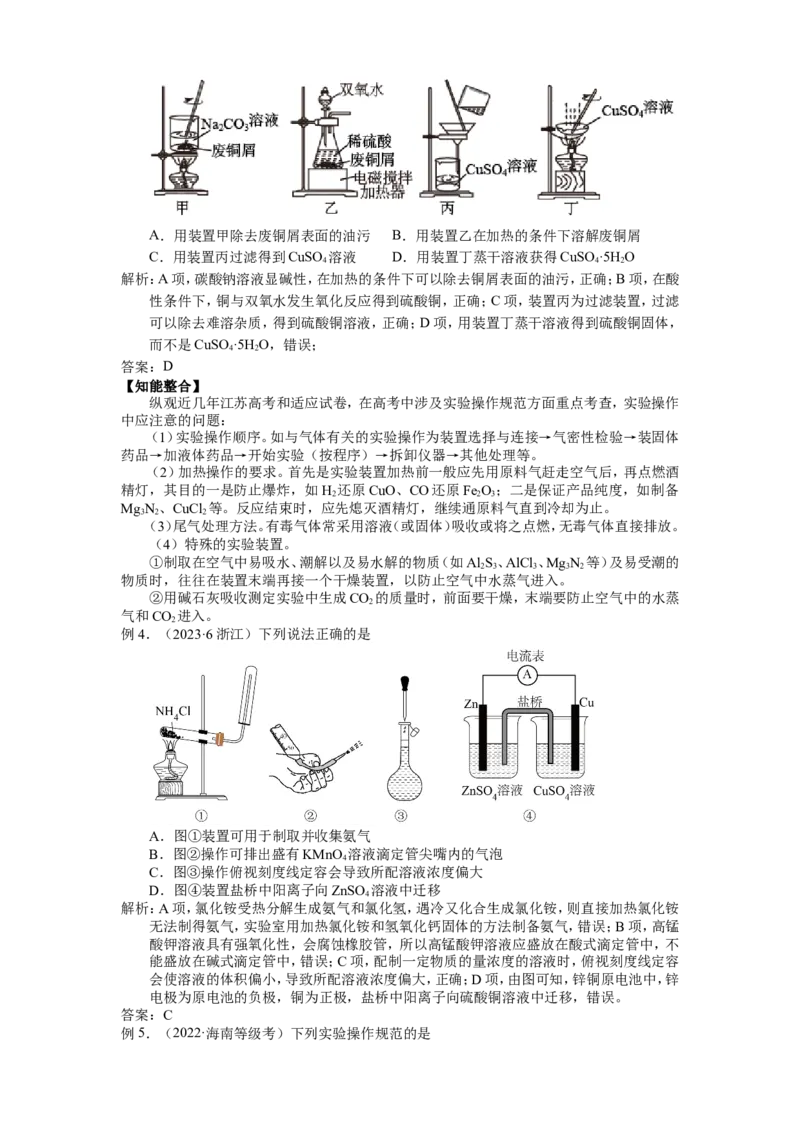
例3.下列由废铜屑制取CuSO ·5H O的实验原理与装置不能达到实验目的的是
4 2A.用装置甲除去废铜屑表面的油污 B.用装置乙在加热的条件下溶解废铜屑
C.用装置丙过滤得到CuSO 溶液 D.用装置丁蒸干溶液获得CuSO ·5H O
4 4 2
解析:A项,碳酸钠溶液显碱性,在加热的条件下可以除去铜屑表面的油污,正确;B项,在酸
性条件下,铜与双氧水发生氧化反应得到硫酸铜,正确;C项,装置丙为过滤装置,过滤
可以除去难溶杂质,得到硫酸铜溶液,正确;D项,用装置丁蒸干溶液得到硫酸铜固体,
而不是CuSO ·5H O,错误;
4 2
答案:D
【知能整合】
纵观近几年江苏高考和适应试卷,在高考中涉及实验操作规范方面重点考查,实验操作
中应注意的问题:
(1)实验操作顺序。如与气体有关的实验操作为装置选择与连接→气密性检验→装固体
药品→加液体药品→开始实验(按程序)→拆卸仪器→其他处理等。
(2)加热操作的要求。首先是实验装置加热前一般应先用原料气赶走空气后,再点燃酒
精灯,其目的一是防止爆炸,如H 还原CuO、CO还原Fe O;二是保证产品纯度,如制备
2 2 3
MgN、CuCl 等。反应结束时,应先熄灭酒精灯,继续通原料气直到冷却为止。
3 2 2
(3)尾气处理方法。有毒气体常采用溶液(或固体)吸收或将之点燃,无毒气体直接排放。
(4)特殊的实验装置。
①制取在空气中易吸水、潮解以及易水解的物质(如Al S、AlCl 、MgN 等)及易受潮的
2 3 3 3 2
物质时,往往在装置末端再接一个干燥装置,以防止空气中水蒸气进入。
②用碱石灰吸收测定实验中生成CO 的质量时,前面要干燥,末端要防止空气中的水蒸
2
气和CO 进入。
2
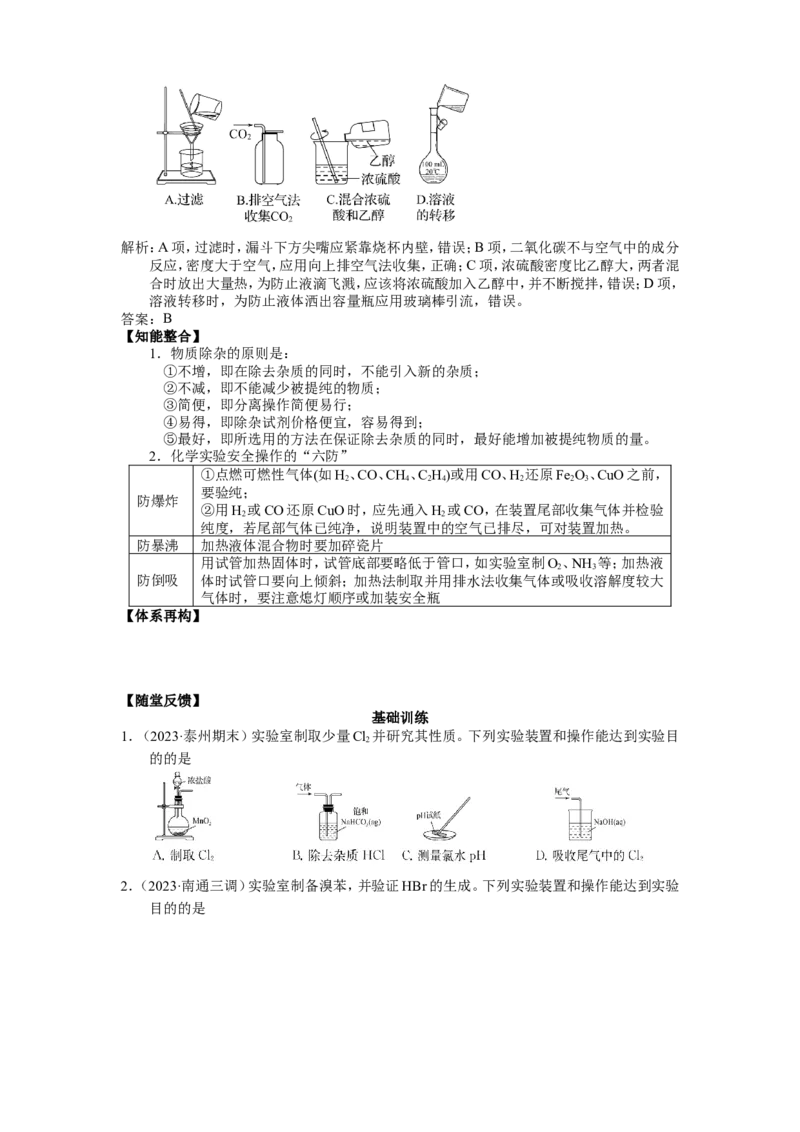
例4.(2023·6浙江)下列说法正确的是
A.图①装置可用于制取并收集氨气
B.图②操作可排出盛有KMnO 溶液滴定管尖嘴内的气泡
4
C.图③操作俯视刻度线定容会导致所配溶液浓度偏大
D.图④装置盐桥中阳离子向ZnSO 溶液中迁移
4
解析:A项,氯化铵受热分解生成氨气和氯化氢,遇冷又化合生成氯化铵,则直接加热氯化铵
无法制得氨气,实验室用加热氯化铵和氢氧化钙固体的方法制备氨气,错误;B项,高锰
酸钾溶液具有强氧化性,会腐蚀橡胶管,所以高锰酸钾溶液应盛放在酸式滴定管中,不
能盛放在碱式滴定管中,错误;C项,配制一定物质的量浓度的溶液时,俯视刻度线定容
会使溶液的体积偏小,导致所配溶液浓度偏大,正确;D项,由图可知,锌铜原电池中,锌
电极为原电池的负极,铜为正极,盐桥中阳离子向硫酸铜溶液中迁移,错误。
答案:C
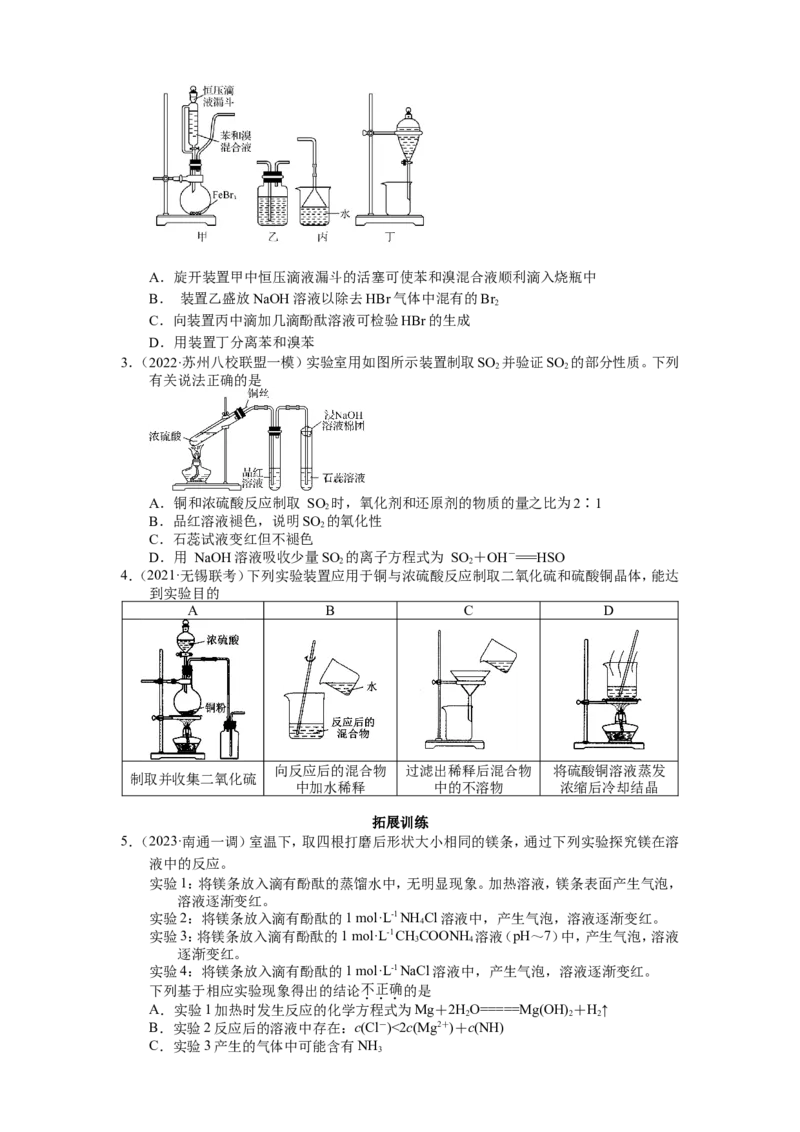
例5.(2022·海南等级考)下列实验操作规范的是解析:A项,过滤时,漏斗下方尖嘴应紧靠烧杯内壁,错误;B项,二氧化碳不与空气中的成分
反应,密度大于空气,应用向上排空气法收集,正确;C项,浓硫酸密度比乙醇大,两者混
合时放出大量热,为防止液滴飞溅,应该将浓硫酸加入乙醇中,并不断搅拌,错误;D项,
溶液转移时,为防止液体洒出容量瓶应用玻璃棒引流,错误。
答案:B
【知能整合】
1.物质除杂的原则是:
①不增,即在除去杂质的同时,不能引入新的杂质;
②不减,即不能减少被提纯的物质;
③简便,即分离操作简便易行;
④易得,即除杂试剂价格便宜,容易得到;
⑤最好,即所选用的方法在保证除去杂质的同时,最好能增加被提纯物质的量。
2.化学实验安全操作的“六防”
①点燃可燃性气体(如H、CO、CH、C H)或用CO、H 还原Fe O、CuO之前,
2 4 2 4 2 2 3
要验纯;
防爆炸
②用H 或CO还原CuO时,应先通入H 或CO,在装置尾部收集气体并检验
2 2
纯度,若尾部气体已纯净,说明装置中的空气已排尽,可对装置加热。
防暴沸 加热液体混合物时要加碎瓷片
用试管加热固体时,试管底部要略低于管口,如实验室制O、NH 等;加热液
2 3
防倒吸 体时试管口要向上倾斜;加热法制取并用排水法收集气体或吸收溶解度较大
气体时,要注意熄灯顺序或加装安全瓶
【体系再构】
【随堂反馈】
基础训练
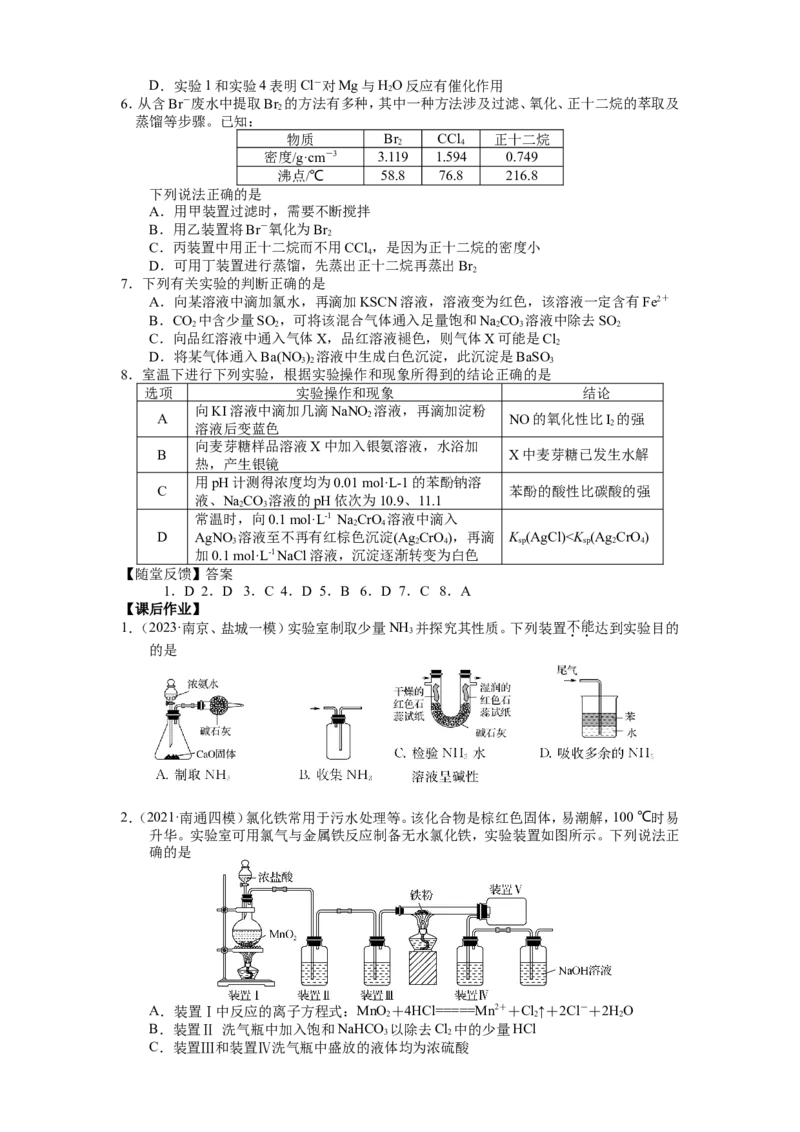
1.(2023·泰州期末)实验室制取少量Cl 并研究其性质。下列实验装置和操作能达到实验目
2
的的是
2.(2023·南通三调)实验室制备溴苯,并验证HBr的生成。下列实验装置和操作能达到实验
目的的是A.旋开装置甲中恒压滴液漏斗的活塞可使苯和溴混合液顺利滴入烧瓶中
B. 装置乙盛放NaOH溶液以除去HBr气体中混有的Br
2
C.向装置丙中滴加几滴酚酞溶液可检验HBr的生成
D.用装置丁分离苯和溴苯
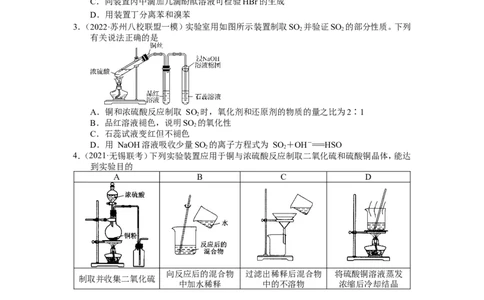
3.(2022·苏州八校联盟一模)实验室用如图所示装置制取SO 并验证SO 的部分性质。下列
2 2
有关说法正确的是
A.铜和浓硫酸反应制取 SO 时,氧化剂和还原剂的物质的量之比为2∶1
2
B.品红溶液褪色,说明SO 的氧化性
2
C.石蕊试液变红但不褪色
D.用 NaOH溶液吸收少量SO 的离子方程式为 SO +OH-===HSO
2 2
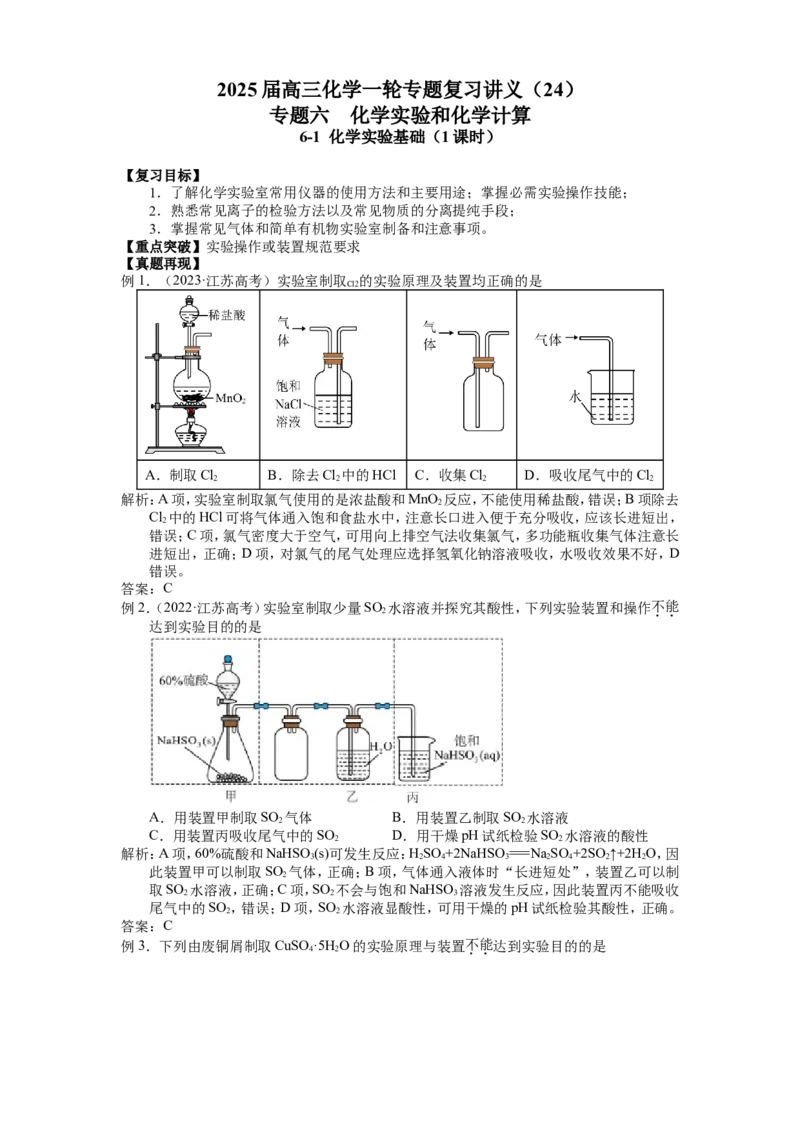
4.(2021·无锡联考)下列实验装置应用于铜与浓硫酸反应制取二氧化硫和硫酸铜晶体,能达
到实验目的
A B C D
向反应后的混合物 过滤出稀释后混合物 将硫酸铜溶液蒸发
制取并收集二氧化硫
中加水稀释 中的不溶物 浓缩后冷却结晶
拓展训练
5.(2023·南通一调)室温下,取四根打磨后形状大小相同的镁条,通过下列实验探究镁在溶
液中的反应。
实验1:将镁条放入滴有酚酞的蒸馏水中,无明显现象。加热溶液,镁条表面产生气泡,
溶液逐渐变红。
实验2:将镁条放入滴有酚酞的1 mol·L-1 NH Cl溶液中,产生气泡,溶液逐渐变红。
4
实验3:将镁条放入滴有酚酞的1 mol·L-1 CHCOONH 溶液(pH~7)中,产生气泡,溶液
3 4
逐渐变红。
实验4:将镁条放入滴有酚酞的1 mol·L-1 NaCl溶液中,产生气泡,溶液逐渐变红。
下列基于相应实验现象得出的结论不正确的是
A.实验1加热时发生反应的化学方程式为Mg+2HO=====Mg(OH) +H↑
2 2 2
B.实验2反应后的溶液中存在:c(Cl-)<2c(Mg2+)+c(NH)
C.实验3产生的气体中可能含有NH
3D.实验1和实验4表明Cl-对Mg与HO反应有催化作用
2
6.从含Br-废水中提取Br 的方法有多种,其中一种方法涉及过滤、氧化、正十二烷的萃取及
2
蒸馏等步骤。已知:
物质 Br CCl 正十二烷
2 4
密度/g·cm-3 3.119 1.594 0.749
沸点/℃ 58.8 76.8 216.8
下列说法正确的是
A.用甲装置过滤时,需要不断搅拌
B.用乙装置将Br-氧化为Br
2
C.丙装置中用正十二烷而不用CCl ,是因为正十二烷的密度小
4
D.可用丁装置进行蒸馏,先蒸出正十二烷再蒸出Br
2
7.下列有关实验的判断正确的是
A.向某溶液中滴加氯水,再滴加KSCN溶液,溶液变为红色,该溶液一定含有Fe2+
B.CO 中含少量SO ,可将该混合气体通入足量饱和NaCO 溶液中除去SO
2 2 2 3 2
C.向品红溶液中通入气体X,品红溶液褪色,则气体X可能是Cl
2
D.将某气体通入Ba(NO ) 溶液中生成白色沉淀,此沉淀是BaSO
3 2 3
8.室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
向KI溶液中滴加几滴NaNO 溶液,再滴加淀粉
A 2 NO的氧化性比I 的强
溶液后变蓝色 2
向麦芽糖样品溶液X中加入银氨溶液,水浴加
B X中麦芽糖已发生水解
热,产生银镜
用pH计测得浓度均为0.01 mol·L-1的苯酚钠溶
C 苯酚的酸性比碳酸的强
液、NaCO 溶液的pH依次为10.9、11.1
2 3
常温时,向0.1 mol·L-1 Na CrO 溶液中滴入
2 4
D AgNO 溶液至不再有红棕色沉淀(Ag CrO),再滴 K (AgCl)