文档内容
2025届高三化学一轮专题复习讲义(26)
专题六 化学实验和化学计算
6-3 化学计算(1课时)
【复习目标】
1.掌握把物质性质、实验原理与化学计算有机融合,突出了化学计算综合能力;
2.强化基本计算思想和方法,提高数学计算方法的运用能力。
【重点突破】 关系式法和守恒法。
【真题再现】
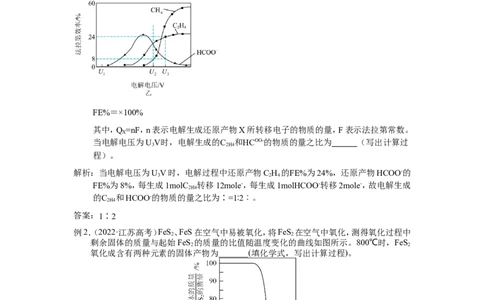
例1.(2023·江苏高考)催化电解吸收 的KOH溶液可将 转化为有机物。在相同条件下,恒
CO2 CO2
定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化
如图乙所示。
FE%=×100%
其中,Q =nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
X
当电解电压为UV时,电解生成的C 和HCOO-的物质的量之比为______(写出计算过
3 2H4
程)。
解析:当电解电压为UV时,电解过程中还原产物C H 的FE%为24%,还原产物HCOO-的
3 2 4
FE%为8%,每生成1molC 转移12mole-,每生成1molHCOO-转移2mole-,故电解生成
2H4
的C 和HCOO-的物质的量之比为∶=1∶2︰。
2H4
答案:1∶2
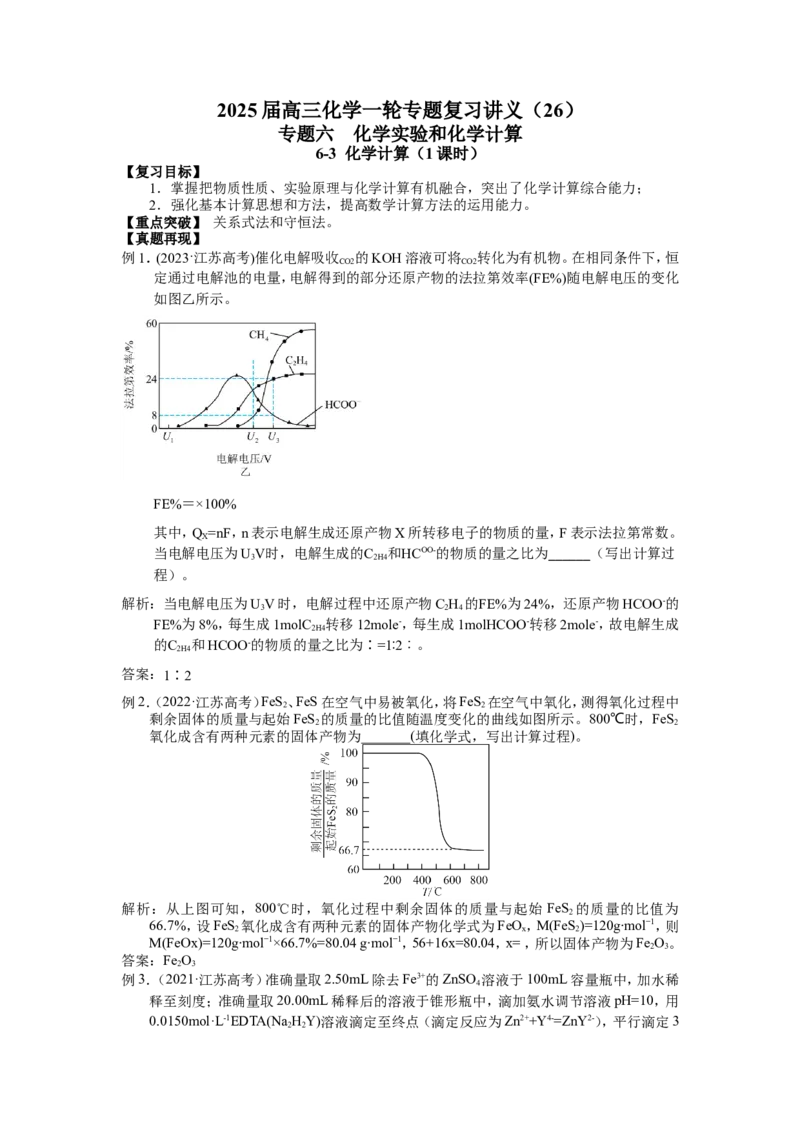
例2.(2022·江苏高考)FeS、FeS在空气中易被氧化,将FeS 在空气中氧化,测得氧化过程中
2 2
剩余固体的质量与起始FeS 的质量的比值随温度变化的曲线如图所示。800℃时,FeS
2 2
氧化成含有两种元素的固体产物为_______(填化学式,写出计算过程)。
解析:从上图可知,800℃时,氧化过程中剩余固体的质量与起始 FeS 的质量的比值为
2
66.7%,设FeS 氧化成含有两种元素的固体产物化学式为FeO,M(FeS)=120g∙mol−1,则
2 x 2
M(FeOx)=120g∙mol−1×66.7%=80.04 g∙mol−1,56+16x=80.04,x= ,所以固体产物为Fe O。
2 3
答案:Fe O
2 3
例3.(2021·江苏高考)准确量取2.50mL除去Fe3+的ZnSO 溶液于100mL容量瓶中,加水稀
4
释至刻度;准确量取20.00mL稀释后的溶液于锥形瓶中,滴加氨水调节溶液pH=10,用
0.0150mol·L-1EDTA(Na HY)溶液滴定至终点(滴定反应为Zn2++Y4-=ZnY2-),平行滴定3
2 2次,平均消耗EDTA溶液25.00mL。计算ZnSO 溶液的物质的量浓度 (写出
4
计算过程)。
解析:根据 Zn2++Y4-=ZnY2-,可知 20.00mL 稀释后的溶液中含 ZnSO 的物质的量为
4
0.025L×0.015mol·L-1=3.75×10-4mol;ZnSO 溶液的物质的量浓度为
4
;
答案:0.75 mol·L-1
例4.(2021·江苏适应卷)(3)通过下列方法测定产品纯度:准确称取0.5000g CuSO ·5H O样
4 2
品,加适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀HSO 酸化,以淀粉溶液为
2 4
指示剂,用0.1000 mol∙L−1 NaSO 标准溶液滴定至终点,消耗NaSO 的溶液19.80mL。
2 2 3 2 2 3
测定过程中发生下列反应:2Cu2++4I-=2CuI↓+I 、2 +I =SO2-+2I-。计算
2 2 4 6
CuSO ·5H O样品的纯度(写出计算过程):_______。
4 2
解析:根据题意得到关系式CuSO ·5H O~NaSO,样品中CuSO ·5H O物质的量为0.1000
4 2 2 2 3 4 2
mol∙L−1×0.0198L=0.00198mol,则CuSO ·5H O样品的纯度的纯度
4 2
。
答案:根据关系式CuSO ·5H O~NaSO
4 2 2 2 3
样品中CuSO ·5H O物质的量为0.1000 mol∙L−1×0.0198L=0.00198mol,则CuSO ·5H O
4 2 4 2
样品的纯度的纯度 99.00%。
小结:基本的氧化还原关系式的计算要提高正确率。
例5.硫酸镍铵[(NH )Ni (SO ) ·nH O]可用于电镀、印刷等领域。某同学为测定硫酸镍铵的组
4 x y 4 m 2
成,进行如下实验:
①准确称取2.335 0 g样品,配制成100.00 mL溶液A;
②准确量取25.00 mL溶液A,用0.040 00 mol·L-1 EDTA(Na HY)标准溶液滴定其中的
2 2
Ni2+(离子方程式为Ni2++H Y2- NiY2-+2H+),消耗EDTA标准溶液31.25 mL;
2
③另取25.00 mL溶液A,加足量的NaOH溶液并充分加热,生成NH 56.00 mL(标准状
3
况)。
(1)25.00 mL溶液A中n(Ni2+)= 、n(NH)= 。
(2)25.00 mL溶液A中n(SO)= 。
(3)0.58375 g(原样品质量的1/4)硫酸镍铵中结晶水n(H O)= 。
2
(4)硫酸镍铵的化学式为 。
解析:(1)n(Ni2+)=n(EDTA)=0.04000mol·L-1×31.25×10-3L=1.250×10-3mol,
n(NH)=n(NH )= =2.500×10-3 mol。
3
(2)根据电荷守恒,n(SO)==2.500×10-3 mol。
(3)m(Ni2+)=59 g·mol-1×1.250×10-3 mol=0.07375 g
m(NH) )=18 g·mol-1×2.500×10-3 mol=0.045 00 g
m(SO)=96 g·mol-1×2.500×10-3 mol=0.240 0 g
n(H O)= 1.250×10-2 mol。
2
(4)x∶y∶m∶n= n(NH)∶n(Ni2+)∶m(SO)∶n(H O)=2∶1∶2∶10,
2
硫酸镍铵的化学式为(NH )Ni(SO )·10H O。
4 2 4 2 2
答案:(1)1.250×10-3 mol 2.500×10-3 mol
(2)2.500×10-3 mol
(3)1.250×10-2 mol
(4)(NH )Ni(SO )·10H O
4 2 4 2 2
小结:综合运用电荷和质量守恒进行计算。
【知能整合】
解化学计算题的关键是要能应用化学知识,从定量的角度分析、解决化学实际问题。以
考查计算能力为主的第16题,基本上是以中和滴定、氧化还原滴定、热重分析等原理,利用
电子守恒、质量守恒、电荷守恒等方法对特定物质的质量、浓度、质量分数、转化率、化学式、混合物成分、化学平衡常数、Ksp、pH等进行相关计算。计算题的情景一般符合客观事实,具
有真实性和一定的应用价值,出现纯计算的大题已经很少了,一般穿插于实验题、工业设计
题中,均以小题的形式呈现。把物质性质、实验操作与化学计算有机融合,突出了学科知识的
综合和化学计算的本质,体现了化学学科对化学计算的要求,首先是化学问题,其次才是考
计算能力,计算具有应用意义。解计算题目时要注意分析题中信息,弄清变化实质,然后从量
的角度,发现、找寻物质之间的转变和联系。化学计算不一再是全卷中的最难试题,化学计算
实用性更明显。
1.多步进行的连续反应运用关系式法。关系式的建立:
(1)利用化学方程式之间的化学计量数间的关系建立关系式
(2)利用化学方程式的加合建立关系式
(3)利用微粒守恒建立关系式
2.化学反应前后质量守恒、元素守恒、得失电子守恒、能量守恒、电荷守恒。建立守恒关
系,运用守恒解题是常用方法。关键在于建立守恒关系:
质量守恒定律、微粒守恒
氧化还原反应:得失电子守恒
化合物的化学式存在的-----正、负化合价总数相等
电解质溶液中存在的-----阴、阳离子电荷守恒
3.化学反应前后物质的某些物理量发生的变化,如质量、气体物质的体积、压强、物质的
量、反应过程中热量的变化,它们的变化参与反应的物质的量也成正比。利用这个规律来行
计算。
4.解计算题要注意规范,不规范的主要表现:
(1)不按照要求写解题过程
(2)未注意溶液体积的变化,未注意溶液的部分取用等
(3)化学方程式写错(系数)
(4)相对分子质量计算错
(5)关系式看错或数据引用看错
(6)不注意有效数字的要求
(7)若无巧妙的解法,题给的所有数据基本都应被用到。
【体系再构】
【巩固练习】
基础训练
1.通过下列方法测定产品纯度:准确称取2.000 g NaHSO ·HCHO·2H O样品,完全溶于水配
2 2
成100.00mL溶液,取20.00mL于碘量瓶中,加入50.00 mL 0.09000 mol·L-1 I 标准溶液,
2
振荡,于暗处充分反应。以淀粉溶液为指示剂,用0.1000 mol·L-1NaSO 标准溶液滴定
2 2 3
至终点,消耗NaSO 溶液10.00mL.测定过程中发生下列反应:
2 2 3
NaHSO·HCHO·2H O+2I ===NaHSO+4HI+HCHO 2SO2-+I ===SO2-+2I-
2 2 2 4 2 3 2 4 6
计算NaHSO·HCHO·2H O样品的纯度 (写出计算过程)。
2 2
2.三草酸合铁(Ⅲ)酸钾晶体[K Fe(C O)·xH O]是一种光敏材料。为测定其纯度(杂质不参加
3 2 4 3 2
反应)进行如下实验:
步骤一:称取5.000 g三草酸合铁酸钾晶体,配制成250.00 mL溶液。
步骤二:取25.00 mL溶液用酸性KMnO 溶液将C O恰好全部氧化为二氧化碳,向反应
4 2
后的溶液中加入锌粉至黄色消失,过滤,洗涤,将滤液和洗涤液合并。
步骤三:用0.010 00 mol·L-1酸性KMnO 溶液滴定合并后的溶液至终点,消耗KMnO 溶
4 4
液20.00 mL。
步骤四:另取5.000 g三草酸合铁酸钾晶体,在110 ℃下加热至完全失去结晶水,剩余固
体质量为4.460 g。
已知:酸性条件下MnO被还原成Mn2+。
(1)加入锌粉的目的是 。
(2)步骤二中C O发生反应的离子方程式为 ,在步骤二中,若加入的
2
KMnO 溶液的量不足,则测得的铁含量 (填“偏低”“偏高”或“不变”)。
4(3)步骤三滴定终点的现象为 。
(4)计算该三草酸合铁(Ⅲ)酸钾晶体的纯度,写出计算过程。
拓展训练
3.用硫酸亚铁铵[(NH )SO ·FeSO ·6H O]为原料通过下列流程可以制备晶体A。
4 2 4 4 2
已知:25 ℃时,[Fe(C O)]3-(aq)+SCN-(aq) [Fe(SCN)]2+(aq)+3C O(aq),K=10-16
2 4 3 2
(1)写出步骤Ⅰ生成黄色沉淀(FeC O·2H O)的化学方程式: 。
2 4 2
(2)步骤Ⅱ水浴加热需控制40 ℃的理由是 。
(3)某研究小组同学欲检验晶体A中含有三价铁,取少量晶体放入试管中,用蒸馏水充
分溶解,向试管中滴入几滴0.1mol·L-1KSCN溶液。请判断上述实验方案是否可行并
说明理由: 。
(4)某研究小组通过如下实验步骤测定晶体A的化学式:
步骤1:准确称取A样品4.9100 g,干燥脱水至恒重,残留物质量为4.3700 g。
步骤2:准确称取A样品4.9100 g置于锥形瓶中,加入足量的3.000 mol·L-1 H SO 溶
2 4
液和适量蒸馏水,用0.5000 mol·L-1 KMnO 溶液滴定,当MnO恰好完全被还
4
原为Mn2+时,消耗KMnO 溶液的体积为24.00 mL。
4
步骤3:将步骤1所得固体溶于水,加入铁粉0.2800 g,恰好完全反应。
通过计算确定晶体A的化学式(写出计算过程)。
4.以软锰矿(主要成分为MnO )和硫锰矿(主要成分为MnS)为原料制备硫酸锰晶体的工艺
2
流程如下:
(1)滤渣中存在一种非金属单质,则酸浸过程中的化学方程式为 。
(2)实验室常用氧化还原法测定MnSO ·H O晶体的纯度,原理如下:
4 2
2Mn2++NO+4PO+2H+===2[Mn(PO )]3-+NO+H O NH+ NO===N↑+2H O
4 2 2 2 2
[Mn(PO )]3-+Fe2+===Mn2++[Fe(PO)]3-
4 2 4 2
称取MnSO ·H O样品1.0000 g,溶于适量水,以磷酸作配位剂,加入过量硝酸铵,在
4 2
220~240℃下充分反应。然后以N—苯代邻氨基苯甲酸作指示剂,用0.1000 mol·L-1
硫酸亚铁铵标准溶液滴定生成的[Mn(PO )]3-至终点。重复操作3次,记录数据如下
4 2
表:
0.100 0 mol·L-1(NH )Fe(SO )
4 2 4 2
滴定次数 标准溶液读数/mL
滴定前 滴定后
1 0.10 20.20
2 1.32 21.32
3 1.05 20.95
①已知:Fe2++ NO+2H+===Fe3++NO↑+HO。测定过程中,加入过量硝酸铵的作用是
2
和 。
② 若滴定过程中标准溶液硫酸亚铁铵不是新配制的,所测定的MnSO ·H O晶体的
4 2
纯度将会 (填“偏低”“偏高”或“不变”)。
③ 计算样品中MnSO ·H O的质量分数(写出计算过程)。
4 2
【巩固练习】答案
1.77.00%
2.(1)将Fe3+还原为Fe2+(2)2 MnO+5 C O+16H+===2Mn2++10CO ↑+8H O 偏高
2 2 2
(3)锥形瓶内溶液变浅红色且半分钟内不消失
(4)5Fe2++ MnO+8H+===5Fe3++Mn2++4H O
2
n(Fe2+)=5n(MnO)=5×20.00×10-3 L×0.010 00 mol·L-1×10=1.000×10-2 mol
n(H O)==3.000×10-2 mol
2
1∶x=1.000×10-2 mol∶3.000×10-2 mol x=3
晶体化学式为KFe(C O)·3H O
3 2 4 3 2
晶体纯度=×100%=98.20%
3.(1)(NH )SO ·FeSO ·6H O+HC O===HSO +FeC O·2H O↓+(NH )SO +4H O
4 2 4 4 2 2 2 4 2 4 2 4 2 4 2 4 2
(2)温度太高,HO 分解;温度太低,Fe2+氧化速度太慢
2 2
(3)不可行,因为[Fe(C O)]3-转化为[Fe(SCN)]2+反应的平衡常数较小,离子浓度太小,观察
2 4 3
不到明显现象,所以无法检验
(4)n(HO)= =0.0300 mol
2
2Fe3++Fe===3Fe2+
n(Fe3+)=2n(Fe)= mol=0.0100 mol
由方程式2KMnO +5H C O+3H SO ===2MnSO +K SO +10CO ↑+8H O可知:
4 2 2 4 2 4 4 2 4 2 2
n(C O)=2.5n(KMnO)=2.5×0.5000 mol·L-1×0.024 L=0.0300 mol
2 4
根据离子电荷守恒:n(K+)+3n(Fe3+)=2n(C O),n(K+)=0.0300 mol,
2
n(K+)∶n(Fe3+)∶n(C O)∶n(H O)
2 2
=0.0300mol∶0.0100mol∶0.0300mol∶0.0300 mol=3∶1∶3∶3
所以A为KFe(C O)·3H O
3 2 4 3 2
4.(1)MnO +MnS+2H SO ===2MnSO +S+2H O
2 2 4 4 2
(2) ①将试样中的二价锰定量氧化成三价锰 与产生的亚硝酸盐反应消除对滴定的影响
②偏高 ③消耗(NH )Fe(SO ) 标准溶液平均值为20.00 mL
4 2 4 2
2MnSO ·H O-2[Mn(PO )]3--2Fe2+
4 2 4 2
n(MnSO ·H O)=n(Fe2+)=20.00×10-3 L×0.1000 mol·L-1=2×10-3 mol
4 2
样品中MnSO ·H O的质量分数为×100%=33.8%
4 2
【课后作业】
1.高锰酸钾纯度的测定:称取1.0800 g样品,溶解后定容于100 mL容量瓶中,摇匀。取浓度
为0.2000 mol·L-1的HC O 标准溶液20.00 mL,加入稀硫酸酸化,用KMnO 溶液平行滴
2 2 4 4
定三次,平均消耗的体积为24.48mL,该样品的纯度为________(列出计算式即可,已知
2MnO+5HC O+6H+===2Mn2++10CO↑+8HO)。
2 2 4 2 2
2.“灼烧”时,Sc (C O)·6H O[摩尔质量为462 g·mol-1]在空气中分解得到Sc O,实验测得
2 2 4 3 2 2 3
灼烧过程中固体残留率随温度的变化如图 3 所示,500 K 时,固体的主要成分是
________(写出计算过程)。
3.聚合硫酸铁[Fe (OH) (SO )] 广泛用于水的净化。以FeSO ·7H O为原料,经溶解、氧化、
2 6-2n 4 n m 4 2
水解聚合等步骤,可制备聚合硫酸铁。
(1)将一定量的FeSO ·7H O溶于稀硫酸,在约70 ℃下边搅拌边缓慢加入一定量的HO
4 2 2 2
溶液,继续反应一段时间,得到红棕色黏稠液体。HO氧化Fe2+的离子方程式为
2 2
;水解聚合反应会导致溶液的pH 。
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000 g,置于250 mL锥形
瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl 溶液(Sn2+将Fe3+还原为Fe2+),充
2
分反应后,除去过量的Sn2+。用5.000×10−2 mol·L-1 KCr O溶液滴定至终点(滴定过程
2 2 7
中Cr O与Fe2+反应生成Cr3+和Fe3+),消耗KCr O溶液22.00 mL。
2 2 2 7
①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将 (填“偏大”“偏小”或“无影响”)。
②计算该样品中铁的质量分数。
4.工厂化验员检验某含有KBrO 、KBr及惰性物的样品。化验员称取了该固体样品1.000 g,
3
加水溶解后配成100 mL溶液X。
Ⅰ. 取25.00 mL溶液X,加入稀硫酸,然后用NaSO 将BrO还原为Br-;
2 3
Ⅱ. 去除过量的SO后调至中性;
Ⅲ. 加入KCrO 作指示剂,用0.100 0 mol·L-1AgNO 标准溶液滴定Br-至终点,消耗
2 4 3
AgNO 标准溶液11.25 mL;
3
Ⅳ. 另取25.00 mL溶液X,酸化后加热,再用碱液调至中性,测定过剩Br-,消耗上述
AgNO 标准溶液3.75 mL。
3
已知:①25 ℃时,Ag CrO(砖红色)K =1.12×10-12,AgBr(浅黄色)的K =5.0×10-
2 4 sp sp
15;②Ⅳ中酸化时发生反应:BrO+5Br-+6H+=== 3Br+3HO
2 2
请回答:
(1)步骤Ⅰ中,反应的离子方程式为________________________________。
(2)步骤Ⅲ中,滴定终点的现象为__________________________________________。
(3)步骤Ⅳ中,加热的目的是________________________。
(4)计算试样中KBrO 质量分数。(写出计算过程,结果保留3位有效数字)
3
【课后作业】答案
1.根据新信息反应式或得失电子守恒计算高锰酸钾产品纯度,注意配制溶液体积与取用量
之间的转化问题。草酸中碳元素为+3价,氧化产物为CO,高锰酸钾被还原为+2价锰
2
离子,根据得失电子守恒知,5n(KMnO)=2n(H C O),
4 2 2 4
w(KMnO)=×100%
4
2.设初始时为1 mol Sc (C O)·6H O,m[Sc (C O)·6H O]=1 mol×462 g·mol-1=462 g。500 K
2 2 4 3 2 2 2 4 3 2
时,剩余固体质量=1 mol×462 g·mol-1×76.62%≈354 g,固体质量减少Δm=462 g-354 g=
108 g,减少的质量为6 mol H O的质量,故500 K时固体成分为Sc (C O)。
2 2 2 4 3
3.(1)2Fe2++ H O+2H+===2Fe3++2H O 减小
2 2 2
(2)①偏大
②n(Cr O)=5.000×10−2 mol·L−1×22.00 mL×10−3 L·mL−1=1.100×10−3 mol
2
由滴定时Cr O→Cr3+和Fe2+→Fe3+,根据电子得失守恒可得微粒的关系式:
2
Cr O~6Fe2+
2
(或Cr O+14H++6Fe2+===6Fe3++2Cr3++7H O)
2 2
则n(Fe2+)=6n(Cr O)=6×1.100×10−3 mol=6.600×10−3 mol
2
样品中铁元素的质量:
m(Fe)=6.600×10−3 mol×56 g·mol−1=0.3696 g
样品中铁元素的质量分数:w(Fe)= ×100%=12.32%
4.(1) 3SO+BrO===Br-+3SO
(2)当滴入最后一滴AgNO 溶液时,产生砖红色沉淀
3
(3)除去溶解在溶液中的Br (或使Br 挥发)
2 2
(4) w(KBrO )=8.35%
3
第一次所取25.00 mL溶液中:
n(Br-) =n(AgBr)=0.1000 mol·L-1×11.25×10-3 L=1.125×10-3 mol
总
所以,n(BrO)+n(Br-)=n(Br-) =1.125×10-3 mol
总
第二次所取25.00 mL溶液,加酸反应后:
n(Br-) =0.1000mol·L-1× 3.75×10-3L=3.75×10-4 mol
余
由步骤Ⅳ可知:BrO~5Br-
所以,n(BrO)=×[n(Br-) -n(Br-) ]
总 余
=×(1.125×10-3 mol-3.75×10-4 mol)=1.25×10-4 mol
由1 g样品配成100 mL溶液,且每次实验取的是25 mL
所以,w(KBrO )=×100%=8.35%。
3